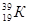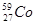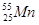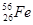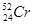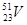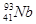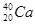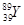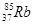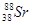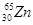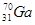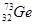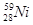Семейства элементов



Структура периодической системы (ПС)
Основным числом для характеристики химического элемента является его порядковый номер Z.
Пример. Порядковый номер элемента марганца равен 25. Отсюда следует, что заряд ядра атома марганца равен +25, число протонов в ядре – 25 и число электронов в атоме – 25.
В периодической системе выделяют периоды и группы.
Ряд элементов, расположенных в порядке возрастания их порядковых номеров, начинающийся щелочным металлом и заканчивающийся инертным элементом, называется периодом.
В периодах расположены элементы, имеющие одинаковое число энергетических уровней, которое совпадает с номером периода.
Первый, второй и третий периоды называются малыми, остальные – большими.
Различают короткопериодный и длиннопериодный варианты периодической таблицы.
Элементы, расположенные в одном и том же вертикальном столбце периодической таблицы, составляют группу элементов.
В группах расположены элементы, имеющие одинаковое число валентных электронов, которое совпадает с номером группы.
Группы делятся на главную и побочную подгруппы.
В подгруппах расположены элементы с аналогичным строением валентного уровня.
Тип элемента (s, p, d или f) определяется тем, какой подуровень у атома заполняется последним.
s-элементы расположены в главных подгруппах первой и второй групп периодической системы, у них заполняется s-подуровень (красный цвет). У s-элементов валентными являются s-электроны последнего энергетического уровня.
p-элементы расположены в главных подгруппах третьей – восьмой групп периодической системы, у них заполняется p-подуровень (желтый цвет). Валентными являются s- и p-электроны последнего энергетического уровня.
d-элементы образуют побочные подгруппы с четвертого по седьмой периоды периодической системы. У них заполняется d- подуровень (синий цвет). Валентные электроны находятся на s-подуровне последнего энергетического уровня и d-подуровне предпоследнего энергетического уровня.
f- элементы «вклиниваются» в побочную подгруппу третьей группы шестого и седьмого периодов. У них происходит заполнение второго снаружи f-подуровня (черный или зеленый цвет).
Ввиду сходства лантаноидов и актиноидов их помещают вне общей таблицы.
Пример. Рассмотрим два элемента, находящиеся в одной и той же группе и в одном и том же периоде, например, марганец и бром:
Как марганец, так и бром имеют по четыре энергетических уровня, что совпадает с номером четвертого периода, в котором они находятся. Число валентных электронов у каждого атома – семь – совпадает с номером седьмой группы, в которой они расположены.
Электронные семейства элементов
В зависимости от того, какой подуровень последним заполняется электронами, все элементы делятся на четыре типа – электронные семейства:
1. s – элементы; заполняется электронами s – подуровень внешнего уровня. К ним относятся первые два элемента каждого периода. Валентными1 являются электроны внешнего уровня.
2. p – элементы; заполняется электронами р – подуровень внешнего уровня. Это последние шесть элементов каждого периода (кроме I и VII). Валентными являются s- и p- электроны внешнего уровня.
3. d – элементы; заполняется электронами d – подуровень второго снаружи уровня, а на внешнем уровне – один или два электрона (y 46Pd – нуль). К ним относятся элементы вставных декад больших периодов, расположенных между s – и p – элементами (их также называют переходными элементами). Валентными являются s – электроны внешнего уровня и d – электроны предвнешнего уровня (второго снаружи).
4. f – элементы; заполняется электронами f – подуровень третьего снаружи уровня, а на внешнем уровне остается два электрона. Они расположены в 6 – м (4f – элементы) и 7 – м (5f – элементы) периодах периодической системы. 4f – элементы объединяют в семейство лантаноидов, а 5f – элементы – семейство актиноидов.
В периодической системе s – элементов 14, p – элементов 30, d – элементов 38, f – элементов 28.
Атомы элементов с одинаковым заполнением внешнего энергетического уровня носят название электронных аналогов. Например:
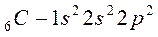

Элементы с одинаковым строением внешнего и предвнешнего энергетических уровней называют полными электронными аналогами. Например:


116 Вертикальное, горизонтальное и диагональное сходство элементов в периодической системе.
В результате объединения вертикальной, горизонтальной и диагональной периодичности появляется так называемая звездная периодичность. Так, свойства германия напоминают свойства окружающих его галлия, кремния, мышьяка и олова. На основании таких «геохимических звезд» можно предсказать присутствие элемента в минералах и рудах.
Аналогичное явление наблюдается и для платиновых металлов. Триады рутений, родий, палладий и осмий, иридий, платина являются горизонтальными аналогами. В то же время пары рутений-осмий, родий-иридий, палладий-платина относятся к шринк-аналогам. В результате все платиновые металлы близки по свойствам.
В ряду лантаноидов элементы подсемейства церия (Ce-Gd) сильнее отличаются друг от друга по свойствам, чем элементы подсемейства тербия (Tb-Lu); это явление также связано с горизонтальной аналогией.
Дата добавления: 2015-01-29 ; просмотров: 183 ; Нарушение авторских прав
Химия. Подскажите что такое Электронные семейства элементов.
Это связь между положением элемента в периодической системе и электронным строением его атомов. От того, какой энергетический подуровень заполняется последним, различают 4 электронных семейства элементов: s, p, d и f:
1. s-Элементы – семейство элементов, у которых при заполнении электронных уровней электронами, последний электрон идет на внешний s-подуровень. Это первая и вторая группа главной подгруппы. На внешнем энергетическом уровне у них 1 или 2 электрона.
Например, Na: 14s2 2s2 p6 3s1, валентным является один s-электрон.
3. У d-элементов сначала заполняется s-подуровень внешнего уровня, а последний электрон идет на d-подуровень предвнешнего уровня. d-Элементы находятся в побочных подгруппах п. с. (У d-элементов возможен проскок электронов с s-подуровня внешнего уровня на свободную d-орбиталь предвнешнего уровня, если это энергетически выгодно. )
4. У f-Элементов последний электрон идет на f-подуровень предпредвнешнего уровня. К ним относятся лантаноиды и актиноиды.
Это связь между положением элемента в периодической системе и электронным строением его атомов. От того, какой энергетический подуровень заполняется последним, различают 4 электронных семейства элементов: s, p, d и f:
1. s-Элементы – семейство элементов, у которых при заполнении электронных уровней электронами, последний электрон идет на внешний s-подуровень. Это первая и вторая группа главной подгруппы. На внешнем энергетическом уровне у них 1 или 2 электрона.
Например, Na: 14s2 2s2 p6 3s1, валентным является один s-электрон.
3. У d-элементов сначала заполняется s-подуровень внешнего уровня, а последний электрон идет на d-подуровень предвнешнего уровня. d-Элементы находятся в побочных подгруппах п. с. (У d-элементов возможен проскок электронов с s-подуровня внешнего уровня на свободную d-орбиталь предвнешнего уровня, если это энергетически выгодно. )
4. У f-Элементов последний электрон идет на f-подуровень предпредвнешнего уровня. К ним относятся лантаноиды и актиноиды.
Электронные семейства элементов
Принадлежность элемента к электронному семейству определяется характером заполнения энергетических подуровней:
s-элементы являются активными металлами, характерные степени окисления которых численно равны количеству электронов на последнем уровне:
+1 для щелочных металлов и +2 для элементов второй группы
р- элементы – заполнение внешнего p- подуровня, например:
Элементы от В до Ne включительно образуют первую серию p-элементов (элементы главных подгрупп), в атомах которых наиболее удаленные от ядра электроны располагаются на втором подуровне внешнего энергетического уровня.
d- элементы – заполнение предвнешнего d- подуровня, например:
V 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 3
d- элементы относятся к металлам.
f- элементы – заполнение f- подуровня второго снаружи уровня, например:

f- элементы – это элементы семейств актиноидов и лантаноидов.
Квантовая механика, сравнивая электронные конфигурации атомов приходит к следующим теоретическим выводам:
1. Строение внешней оболочки атома является периодической функцией зарядового числа атома Z.
2. Поскольку химические свойства атома определяются строением внешней оболочки, из предыдущего пункта следует: химические свойства элементов находятся в периодической зависимости от заряда ядра.
Контрольные вопросы
3. Квантовые числа (главное, орбитальное, магнитное, спиновое).
4. Строение электронных оболочек атомов. Принцип Паули. Принцип наименьшей энергии. Правило Гунда.
5. Электронно-структурные формулы атомов. Гибридизация атомных орбиталей.
6. Характеристики атома. Атомный радиус. Электроотрицательность. Сродство к электрону. Энергия ионизации. S, p, d, f – электронные семейтсва атомов.
Типовые задачи
Задача № 1.Радиусы ионов Na + и Cu + одинаковы (0,098 нм). Объяснить различие температур плавления хлорида натрия (801°С) и хлорида меди(I) (430°С).
Задача №2. Как обозначается состояние электрона а) с n=4,L=2; б) с n=5,L=3.
Задача № 3. Сколько всего орбиталей соответствует третьему энергетическому уровню? Сколько электронов на этом уровне? На сколько подуровней расщепляется этот уровень?
Решение: Для третьего энергетического уровня n=3, количество атомных орбиталей 9(3 2 ), что
является суммой 1(s) +3(p) +5(d)=9. По принципу Паули количество электронов на этом уровне 18. Третий энергетический уровень расщепляется на три подуровня: s,p,d (количество подуровней совпадает с числом значений главного квантового числа).
Задача №4. На какие электронные семейства классифицируются химические элементы?
Решение: Все химические элементы можно классифицировать в зависимости от характера заполняемых подуровней на 4 типа:
s-элементы-заполняют электронами ns подуровень;
d-элементы-заполняют электронами (n-1)d подуровень;
f-элементы –заполняют электронами (n-2)f подуровень;
Задача № 5. Какой подуровень заполняется в атоме электронами после заполнения подуровня: а) 4р; б)4s
Решение: А) подуровню 4р отвечает сумма (n+1), равная 4+1=5. Такой же суммой характеризуются подуровни 3d (3+2=5) и 5s (5+0=5). Однако состоянию 3d отвечает меньшее значение n (n=3), чем состоянию 4р, поэтому подуровень 3d будет заполняться раньше, чем подуровень 4р. Следовательно, после заполнения подуровня 4р будет заполняться подуровень 5s, которому отвечает на единицу большее значение n(n=5).
Б) подуровню 4s соответствует сумма n+1=4+0=4. Такой же суммой n+1 характеризуется подуровень 3р, но заполнение этого подуровня предшествует заполнению подуровня 4s, т.к. последнему отвечает большее значение главного квантового числа. Следовательно, после подуровня 4s будет заполняться подуровень с суммой (n+1)=5,причем из всех возможных комбинаций n+l, соответствующих этой сумме(n=3, l=2; n=4; l=1; n=5; l=0), первой будет реализоваться комбинация с наименьшим значением главного квантового числа, то есть вслед за подуровнем 4s будет заполняться подуровень 3d.
Вывод: таким образом, заполнение подуровня d отстает на один квантовый уровень, заполнение подуровня f отстает на два квантовых уровня.
Для написания электронной формулы элемента необходимо: арабской цифрой указать номер энергетического уровня, написать буквенное значение подуровня, количество электронов записать в виде показателя степени.
Например: 26Fe 4 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6
Задача № 6. Электронная структура атома описывается формулой 1s22s22p63s23d74s2. Какой это элемент?
Тестовые задания
Выберите правильный вариант ответа
02. МОГУТ ЛИ СУЩЕСТВОВАТЬ В АТОМЕ ДВА ЭЛЕКТРОНА С ОДИНАКОВЫМ НАБОРОМ ВСЕХ ЧЕТЫРЕХ КВАНТОВЫХ ЧИСЕЛ?
Могут
3) могут только в возбужденном состоянии
4) могут только в нормальном (невозбужденном) состоянии
03. КАКОЙ ПОДУРОВЕНЬ ЗАПОЛНЯЕТСЯ ПОСЛЕ ПОДУРОВНЯ 4D?
1)
2)
3)
4)
06. КАКОЙ ПОДУРОВЕНЬ ЗАПОЛНЯЕТСЯ ПЕРЕД 4D-ПОДУРОВНЕМ?
07. СРЕДИ ПРИВЕДЕННЫХ НИЖЕ ЭЛЕКТРОННЫХ КОНФИГУРАЦИЙ УКАЗАТЬ НЕВОЗМОЖНУЮ
1)
2)
3)
4)
09. У КАКОГО ЭЛЕМЕНТА НАЧИНАЕТСЯ ЗАПОЛНЕНИЕ ПОДУРОВНЯ 4D?
1)
2)
3)
4)
10. У КАКОГО ЭЛЕМЕНТА ЗАКАНЧИВАЕТСЯ ЗАПОЛНЕНИЕ ПОДУРОВНЯ 3D?
1)
2)
3)
4)
11. ОПРЕДЕЛИТЕ ЭЛЕКТРОННУЮ ЕМКОСТЬ (ВМЕСТИМОСТЬ) ТРЕТЬЕГО ЭНЕРГЕТИЧЕСКОГО УРОВНЯ
12. СКОЛЬКО ЗНАЧЕНИЙ ПРИНИМАЕТ ML ПРИ L =3?
13. СКОЛЬКО НЕСПАРЕННЫХ ЭЛЕКТРОНОВ В НЕВОЗБУЖДЕННОМ СОСТОЯНИИ ИМЕЕТ АТОМ ФОСФОРА?
14. КАКИЕ ЗНАЧЕНИЯ ПРИНИМАЕТ ПОБОЧНОЕ КВАНТОВОЕ ЧИСЛО (L), ЕСЛИ ЗНАЧЕНИЕ ГЛАВНОГО КВАНТОВОГО ЧИСЛА (N) РАВНО 3?
15. ПРИЗНАКОМ СХОДСТВА ХИМИЧЕСКИХ БИОГЕННЫХ ЭЛЕМЕНТОВ НАТРИЯ И КАЛИЯ ЯВЛЯЕТСЯ ОДИНАКОВОЕ ЧИСЛО
1) электронов внешнего слоя
3) электронных слоев
4) нейтронов в ядре
Дата добавления: 2015-11-20 ; просмотров: 5340 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Классификация химических элементов. Естественные семейства элементов и их характеристика.
Урок предназначен для учащихся 8 класса. Урок комбинированный. На уроке используется дифференцированная работа, работа с составлением таблицы.
Просмотр содержимого документа
«Классификация химических элементов. Естественные семейства элементов и их характеристика.»
Урок по теме «Классификация химических элементов. Естественные семейства элементов и их характеристика»
Фахриева Эльмира Тиллабековна, учитель химии КГУ «общеобразовательная школа №155», г.Алматы
Цель урока: Организация деятельности учащихся по восприятию, осмыслению и первичному запоминанию новых знаний и способов деятельности.
1 Образовательная: ознакомить с первыми попытками классификации химических элементов; рассмотреть семейства химических элементов; дать понятие об амфотерных элементах
2.Развивающая: развивать умения приводить примеры металлов, неметаллов, амфотерных элементов; доказывать, объяснять, по каким признакам химические элементы объединены в семейства.
Тип урока: Изучение и первичное запоминание новых знаний и способов деятельности.
Форма организации урока: Лекция
Дидактическое обеспечение урока: ПСХЭ Д.И.Менделеева, коллекция «Металлы и сплавы», схема «Классификация химических элементов», таблица «Естественные семейства химических элементов».
2.Планетарная модель строения атома.
3.В чем заключается физический смысл порядкового номера?
4.Состав атомного ядра. Протоны, нейтроны.
5.Что такое изотопы?
Задание1. Пользуясь ПСХЭ Д.И.Менделеева, определите число протонов и нейтронов в ядрах атомов натрия, фосфора. (1 уровень)
Задание 2. Определите число протонов и нейтронов в ядрах следующих изотопов: а) 12 С и 13 С; б) 20 Ne и 23 Ne. (2 уровень)
Задание3.В ядре изотопа одного из элементов отсутствуют нейтроны. Назовите этот элемент. (3 уровень)
3.Формирование новых понятий и способов деятельности.
1. Деление химических элементов на металлы и неметаллы.

твердые, ковкие, пластичные, имеют различное агрегатное состояние,
проводят эл.ток. тепло непластичны, не проводят тепло и эл.ток
Амфотерными называются элементы, проявляющие двойственную природу, их нельзя отнести ни к типичным металлам, ни к типичным неметаллам. Например: Ве, Zn, Al, Cr. Амфотерные элементы могу проявлять в химических реакциях как металлические, так и неметаллические свойства, т.е. обладают двойственными свойствами.
3.Естественные семейства химических элементов.
1.Понятие о естественном семействе.
2.Виды естественных семейств.
Естественные семейства химических элементов
Щелочные Галогены Щелочноземельные Семейство Благородные
металлы металлы кислорода газы
3.Характеристика естественных семейств химических элементов.
Естественные семейства химических элементов
Элементы данного семейства
Особенности данного семейства
1.При взаимодействии с водой образуют щёлочи.
2.Мягкие, быстро окисляются кислородом, поэтому хранятся под слоем керосина,
3.В соединениях одновалентны.
4.Из всех металлов самые активные.
1.Образуют простые вещества, молекулы которых состоят из 2х атомов:
2.Высшая валентность в соединениях с кислородом YII.
3.С водородом образуют летучие соединения, в которых проявляют валентность I, например: НF.
4.С металлами образуют соли: NaF.
6. Из всех неметаллов самые активные.
Благородные (инертные) газы
2.Не образуют соединений с водородом и металлами, т.е. проявляют валентность 0.
1.Оксиды этих Ме при взаимодействии с водой образуют щёлочи.
2.Все они в соединениях двухвалентные.
3.Образуют оксиды с общей формулой RO, которым соответствуют гидроксиды с общей формулой R(OH)2.
Элементы подгруппы кислорода
1.Образуют кислотные оксиды с общей формулой RO3, где проявляют валентность YI. Этим оксидам соответствуют кислоты состава H2RO4.
2.Химические элементы S, Se, Te называют халькогенами-«рождающие медные руды»
3.С водородом образуют соединения состава H2R.
Примечание: Первое семейство учитель показывает учащимся, остальные они составляют самостоятельно, используя учебник.
4.Применение. Формирование умений и навыков.
Работа с учебником, п.20: закончить таблицу, дать характеристику остальным семействам химических элементов.
5.Этап информации о домашнем задании.
п.19, 20 (учебник), выучить таблицу «Естественные семейства химических элементов»
6.Подведение итогов урока.
Качественная оценка работе класса и отдельных учащихся