Диагностика патологии эндометрия в постменопаузе: применение 2D и 3D технологий
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Трехмерное УЗИ в последние годы чаще используется в работе как врачей ультразвуковой диагностики, так и врачей акушеров-гинекологов, несмотря на то, что остается ряд дискуссионных вопросов, роль которых в диагностике гинекологической патологии еще предстоит определить 3.
В большей мере освещены вопросы патологии эндометрия в постменопаузальном возрасте. Так, S. Kupesic и соавт. определили, что трехмерная энергетическая допплерография может использоваться для раннего выявления рака эндометрия, особенно у женщин в постменопаузальном возрасте без клинической симптоматики заболевания, а также для уточнения инвазии опухоли в миометрий [4].
При обследовании пациенток постменопаузального возраста с аденокарциномой, гиперплазией, атрофией эндометрия и субмукозной миомой матки, J.L. Alcazar и R. Galv n установили, что 3D энергетическая допплерография может быть полезна в диагностике рака эндометрия, так как у этих пациенток статистически значимо повышены индекс васкуляризации (ИВ) и васкуляризационно-потоковый индекс (ВПИ) эндометрия в сравнении с пациентками других групп [5].
В свою очередь R. Galv n и соавт. при изучении стадийности эндометриального рака у пациенток в постменопаузе определили, что ИВ в малигнизированном эндометрии коррелирует с некоторыми гистологическими характеристиками опухоли [6].
G. Opolskiene и соавт. определили, что у женщин с кровотечением в постменопаузальном возрасте ИВ и ВПИ не отличались как при доброкачественных, так и при злокачественных изменениях в эндометрии [7]. К противоположным выводам пришли A.K. Makled и соавт., которые в своих исследованиях доказали, что значение ИВ является достоверным диагностическим критерием рака эндометрия в постменопаузе [8].
Как видно из изложенного выше, в последние годы увеличивается интерес к проблемам постменопаузы, что связано в первую очередь с тенденцией населения развитых стран к старению. Поэтому так актуальны вопросы патологии эндометрия в постменопаузальном периоде [9].
Кроме того, заболеваемость раком эндометрия увеличилась во всех экономически развитых странах [10, 11].
В постменопаузальном возрасте у ряда пациенток происходит полная облитерация цервикального канала, и показанием для проведения раздельного диагностического выскабливания становится расширение полости матки за счет жидкости, выявленное при УЗИ в 2D режиме. Между тем у врачей ультразвуковой диагностики нет четких критериев, позволяющих исключить злокачественную трансформацию эндометрия у таких пациенток. Следовательно, поиск путей улучшения диагностики патологических состояний эндометрия у пациенток в постменопаузальном возрасте с использованием трехмерной эхографии с опцией энергетического допплера побудил нас к исследованиям в этой области.
Целью настоящего исследования стало проведение анализа совпадений результатов рутинного двухмерного трансвагинального УЗИ у пациенток постменопаузального возраста с окончательным патоморфологическим заключением исследования биоптата эндометрия, определение возможности использования трехмерной энергетической допплерографии у пациенток с облитерацией цервикального канала в постменопаузе.
Материал и методы
Для достижения поставленной цели нами ретроспективно оценено 50 историй болезни женщин постменопаузального возраста, госпитализированных в гинекологическое отделение для проведения раздельного диагностического выскабливания и гистероскопии в плановом порядке. Показанием для госпитализации явились данные рутинного трансвагинального УЗИ (ультразвуковое заключение: патология эндометрия). Данные ультразвуковых заключений, послужившие поводом для госпитализации в стационар, были оценены ретроспективно и сопоставлены с данными гистологических заключений после раздельного диагностического выскабливания.
Пациентке с атрезией цервикального канала и скоплением жидкости в полости матки проведено трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison в режиме 3D реконструкции с опцией энергетического допплера по методике И.А. Озерской [12], с последующим автоматическим получением ИВ, индекса потока (кровотока) (ИП), ВПИ реконструированной матки в программе Virtual Organ Computeraided AnaLysis (VOCAL).
Статистическая обработка данных осуществлялась с применением прикладного программного пакета «Statistica 6.0», адаптированного для медико-биологических исследований. Производилось вычисление относительных частот признака (%) в группе.
Результаты и обсуждение
Анализ приведенных результатов побуждает к поиску дополнительных ультразвуковых методик, которые можно применить в постменопаузальном возрасте, особенно в ситуации с атрезией цервикального канала и последующим скоплением жидкости в полости матки. Именно это состояние занимает высокий удельный вес в постменопаузальном возрасте и, не представляя трудностей в диагностике при рутинном трансвагинальном УЗИ, ведет к проведению раздельного диагностического выскабливания.
Мы попытались применить у такой категории пациенток 3D энергетическую допплерографию и приводим клинический пример.
Пациентка К., 60 лет, поступила в гинекологическое отделение для проведения раздельного диагностического выскабливания под контролем гистероскопии с диагнозом: подозрение на рак тела матки. Данные трансвагинального УЗИ, проведенного амбулаторно: тело матки нормальных размеров, контур матки ровный, миометрий однородный, полость матки расширена до 6 мм, заполнена анэхогенным содержимым. Яичники обычных размеров и эхоструктуры, свободная жидкость в позадиматочном пространстве не визуализируется. Ультразвуковое заключение: серозометра.
Анамнестические данные: постменопауз 5 лет, из гинекологических заболеваний в анамнезе пациентка отмечает эктопию шейки матки, по поводу чего была произведена диатермоэлектрокоагуляция шейки матки. В анамнезе 2 родов, в срок, без осложнений и один медицинский аборт в срок 8-9 нед, без осложнений.
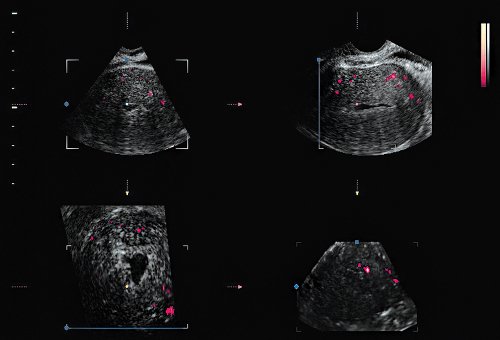
До проведения раздельного диагностического выскабливания, на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison после опорожнения мочевого пузыря мы провели трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц в режиме 3D реконструкции с опцией энергетического допплера и получили объемное изображение (рис. 1).
Рис. 1. Объемное изображение в режиме энергетического допплера.
Cерозометра: термин врача ультразвуковой диагностики или диагноз гинеколога?
Волгоградский государственный медицинский университет
В настоящее время одной из наиболее часто выполняемых внутриматочных операций является гистероскопия, с помощью, которой возможны не только визуализация различных видов внутриматочной патологии, но и осуществление хирургических вмешательств и контроля за эффективностью лечения [1]. Вместе с тем, это инвазивная манипуляция, имеющая определенный риск инфекционных осложнений, которые по данным разных авторов составляют от 0,7 до 12% (Баев О.Р., Стрижаков А.Н., Давыдов А.И. 2010) [2,3]. Вследствие возможности риска развития осложнений в послеоперационном периоде, необходимо иметь чёткие показания к выполнению данной операции [4]. Тем не менее, на современном этапе развития медицины неинвазивные методы диагностики внутриматочной патологии, такое как УЗИ органов малого таза, являются одним из начальных этапов постановки диагноза, а также определяющим фактором для определений показаний к выполнению гистероскопии [5,6]. Особенно важен метод УЗИ гениталий в период постменопаузы. Период постменопаузы является наиболее опасным в плане развития онкологических процессов гениталий, диагностика которых имеет большое практическое значение [7,8]. Негативные последствия имеют как несвоевременно проведенная диагностика, так и гипердиагностика, которая ведет к необоснованным внутриматочным вмешательствам.
Последние годы все чаще гинекологи встречаются с диагнозом «серозометра», на основании чего пациентка направляется в стационар для выполнения гистероскопии. Анализ литературы демонстрирует противоречивые мнения, как в отношении природы появления жидкости в полости матки, так и о прогностической значимости этого явления. Ряд авторов указывают на повышение риска злокачественных процессов в малом тазу при обнаружении жидкости в полости матки [9]. Некоторые исследователи, связывают скопление внутриматочной жидкости с доброкачественной внутриматочной патологией [10]. Другие исследователи расценивают появление жидкости в полости матки в период постменопаузы как вариант нормы, связывая ее с окклюзией цервикального канала [10].
Цель исследования: оценить прогностическую значимость определения при ультразвуковом исследовании жидкости в полости матки в постменопаузальном периоде.
Материалы и методы исследования. Для достижения поставленной цели были обследованы 27 пациенток, направленных для выполнения гистероскопии в плановом порядке с диагнозом «Серозометра» в гинекологические отделения ВОКБ №1 и КБСМП №7 г. Волгограда за период 2013-2015 гг. Оценивались факторы риска развития заболеваний гениталий с учетом длительности менопаузы, технические особенности гистероскопии в постменопаузальном возрасте, риск осложнений после манипуляции, фармакологическая нагрузка. Всем пациенткам после выполнения гистероскопий проводилось гистологическое исследование полученного материала.
Результаты исследования. Результаты исследования свидетельствуют, что возраст больных колебался от 53 до 73 лет и в среднем составил 62,8±1,8. Все пациентки человек были в периоде менопаузы. Причём длительность менопаузы составила от 2 до 19 лет в среднем 11,9±2,7. Таким образом, среди пациенток, которым выставлялся диагноз «серозометра» и выполнялась гистероскопия не было ни одной женщины репродуктивного или перименопаузального возраста. Минимальный срок менопаузы составил 2 года.
Подавляющее большинство обследованных (58,8%) были пенсионерами. В тоже время, обращает на себя внимание, что несмотря на средний возраст обследованных более шестидесяти лет более 40% из них продолжают работать.
Анализ менструальной функции обследованных пациенток в репродуктивном возрасте показал, что ее нарушения были выявлены у 52,9%. Возможно, одним из факторов нарушений менструального цикла была высокая частота прерываний беременности по желанию у пациенток исследуемой группы, 82,4% пациенток имели в анамнезе медицинские аборты. Причём у каждой третьей (30%) пациентки было более 2-х абортов. Среднее количество абортов на одну пациентку составило 2,1±0,3 (от 1 до 10). Количество родов в анамнезе у пациенток колебалось от 1 до 4 и в среднем составило 1,8±0,2.
Самопроизвольное прерывание беременности, в том числе замершие, имели в анамнезе 23,52% обследуемых женщин. Данные по соотношению родов, прервавшихся беременностей и медицинских абортов представлены на рис. 1.
Рис. 1. Соотношение доли родов, абортов и самопроизвольных выкидышей у пациенток исследуемой группы.
Всем пациенткам диагноз серозометра был поставлен на основании данных УЗИ малого таза, которое проводилось с профилактической целью. Данный диагноз был выявлен впервые, при этом какие-либо жалобы у пациенток отсутствовали. У большинства (81,8%) пациенток гистероскопия выполнялась впервые, повторное внутриматочное вмешательство в виде гистероскопии было у 18,2%.
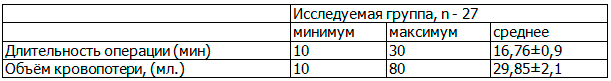
Данные по продолжительности операции и объеме кровопотери в исследуемой группе приведены в табл. 1.
Таблица 1. Продолжительность гистероскопии и объём кровопотери
Учитывая возраст и длительность менопаузы более 10 лет у большинства пациенток выполнение гистероскопии было сопряжено с определенными техническими трудностями в связи с инволютивными процессами в матке. Так, перфорация матки является крайне редким осложнением при выполнении гистероскопии в репродуктивном возрасте, однако у одной пациентки (3,70%) данной исследуемой группы операция была осложнена перфорацией матки.
По данным историй болезней у 88,2% пациенток послеоперационный период протекал без осложнений. Длительность пребывания в стационаре была от 2 до 7 дней, средний койко-день составил 4,18±0,1 койко-дня.
Результаты гистологических исследований представлены в табл. 2.
Таблица 2. Результаты гистологического исследования у пациенток с диагнозом «серозометра»
Данные гистологического исследования подтвердили диагноз полип, из двух пациенток с гиперплазией у 1 пациентки диагностирована атрофия эндометрия, а у второй пациентки с гиперплазией эндометрия выявлена аденокарцинома. Ни у одной из пациенток с изолированной серозометрой злокачественного процесса эндометрия не было выявлено.
Диагноза «Серозометры» по международной классификации болезней МКБ-10 не существует. Результаты проведенного исследования свидетельствуют,что большинство женщин с серозометрой не имеют никаких жалоб. Все они поступали в стационар для выполнения гистероскопии с раздельным диагностическим выскабливанием только на основании данных УЗИ малого таза (жидкость в полости матки). Данные гистологического исследования указывают на низкую диагностическую ценность ультразвуковых признаков серозометры для своевременного выявления патологии эндометрия в постменопаузальном периоде. Ни в одном случае изолированной серозометры заболеваний выявлено не было. В тоже время, выполнение внутриматочного вмешательства на фоне атрофичного эндометрия следует признать нецелесообразным, так как несет ряд негативных последствий для пациентки. Кроме того, это сопряжено с неоправданной госпитализацией и необоснованной фармакологической нагрузкой.
Патологии эндометрия, полости матки и цервикального канала
1. Паталогии эндометрия
Полость матки выстлана эндометрием – пронизанной кровеносными сосудами слизистой оболочкой (мукозный слой), ткань которой постоянно меняется и обновляется в зависимости от фазы менструального цикла.
Природное предназначение эндометрия – обеспечить надежное прикрепление и кровоснабжение (питание) оплодотворенной яйцеклетки. В эндометрии, как и в любом другом структурно сложном образовании живого организма, обнаруживаются многочисленные заболевания, функциональные расстройства и аномалии развития. К наиболее распространенным относятся следующие.
2. Гиперплазия и полипы
Гиперплазия
Увеличение, разрастание эндометрия, зачастую неравномерное, очаговое, полипообразное, железисто-кистовое и т.д. Согласно статистическим данным, гиперплазия эндометрия наблюдается примерно у 40% всех гинекологических пациенток, причем частота встречаемости не зависит от возраста. Основными этиопатогенетическими факторами считаются эндокринные нарушения, инфекционные заболевания, генетические сбои; однако, пусковые механизмы остаются неясными. Как правило, больные жалуются на патологически обильные менструации, выделения или маточные кровотечения, не связанные с циклом. Основными диагностическими методами являются УЗИ (трансвагинальный вариант наиболее информативен), гистероскопия (при необходимости отбирается материал для гистологического исследования). Терапия гиперплазии эндометрия включает гормональные препараты и/или малоинвазивное вмешательство: хирургическую гистероскопию, аблацию, гистерорезектоскопию.
Полипы
Очаговая доброкачественная пролиферация (разрастание) клеток эндометрия матки и/или цервикального канала (участка между маткой и влагалищем). Обнаруживаются более чем у половины пациенток после менопаузы; проявляются, в основном, кровянистыми выделениями. К главным причинам образования полипов относят неоднократные и неполные выскабливания. Различают несколько видов полипов (аденоматозные, железистые и пр.). Диагностика и лечение (удаление) полипов осуществляется, как правило, гистероскопическим методом.
3. Перегородка полости матки
4. Синехии и серозометра
Синехии
Внутриматочные синехии (спайки, сращения – синдром Ашермана) могут быть обусловлены рядом причин: травмы (в т.ч. хирургические), инфекции, нарушения нейровисцеральной регуляции. По охвату внутриматочного пространства выделяют три степени синехий. Основным клиническим симптомом является неспособность забеременеть либо выносить беременность. Диагностируется аппаратными методами. Единственным лечением является хирургическая коррекция (в настоящее время подавляющее большинство вмешательств производится малоинвазивными методами).
Серозометра
Скопление серозной жидкости (т.е. секрета слизистой оболочки) в полости матки. Серозометра не является самостоятельным диагнозом – это всегда симптом иного заболевания или состояния (в частности, послеродовое скопление носит название лохиометра, наличие жидкой крови – гематометра). Часто встречается в раннем климактерическом периоде на фоне гормональной перестройки. Провоцирующими факторами считают также вредные привычки и гиподинамический образ жизни. Проявляется ноющей болью, при большом объеме жидкости – видимым увеличением живота, водянистыми выделениями, при инфицировании – симптоматикой острого воспаления. Терапией выбора обычно является расширение цервикального канала с отводом жидкости; обязательно проводится гистологическое исследование, при необходимости – бактериальный посев и лечение инфекции.
Заболевания 
Жалобы и симптомы 
Диагностика 
Наши цены 
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Как бороться с субсерозной миомой матки
Доброкачественные опухоли, к числу которых относится и субсерозная миома матки, требуют внимательного к себе отношения, точной диагностики и квалифицированной помощи грамотных специалистов. Только при таком подходе возможен положительный исход в борьбе с проблемой.
Суть заболевания
Субсерозная миома матки – что это? Это доброкачественное образование, являющееся одной из разновидностей гинекологической болезни. При данном заболевании появляются узелковые опухоли разного размера, которые располагаются как внутри, так и снаружи полости матки, затрагивая мышечные ткани, связки.
Миома матки, ее субсерозный тип характеризуется локализацией узелков на внешней стороне полости этого органа. Все образования носят доброкачественный характер и распространяются в сторону малого таза, захватывая на своем пути новые площади.
Субсерозный узел миомы матки выглядеть может по-разному: и как образование с широким основанием, и как узелок на тоненькой ножке, примыкающие к серозной маточной оболочке. Количество узлов может варьироваться от одного до нескольких, размеры – от миллиметровых «крошек» до значительных десятисантиметровых опухолей.
Чтобы не задаваться вопросами «субсерозная миома матки что это такое», насколько это опасно и какой возраст женщин подвержен ее нападкам, нужно запомнить, что это доброкачественная опухоль у дам репродуктивного возраста.
Субсерозная миома тела матки может длительное время никак не проявлять себя. Только в случае ее разрастания и увеличения размеров представительницы слабого пола могут испытывать некоторый дискомфорт.
Но и в этом случае не стоит опасаться увеличения матки или влияния опухоли на изменения в менструальном цикле, следовательно, и зачатие, вынашивание плода, роды могут протекать нормально. Не исключаются случаи самопроизвольного выкидыша в результате влияния субсерозной миомы матки. Все очень индивидуально и зависит от места расположения и размера опухоли.
Основная причина такого новообразования – изменения или сбои гормонального характера.
Характерные признаки
Узловая субсерозная миома матки дает о себе знать лишь в случае увеличения размеров опухоли и давлении на ткани и органические системы, расположенные рядом с этим образованием.
Симптомы субсерозной миомы матки:
Длительное нахождение на ногах, значительные физические нагрузки могут привести к тому, что при диагнозе субсерозная миома матки, ее симптомы начинают проявляться более явно, например, усилением или видоизменением болей. Неприятные ощущения могут стать схваткообразыми, изнуряющими, это может свидетельствовать о росте опухоли, перекруте ножки или изменении места расположения.
Обнаружив у себя признаки субсерозной миомы матки, стоит обратиться к специалисту-гинекологу для уточнения диагноза и ни в коем случае не заниматься самолечением.
Стоит насторожиться
Если не начать своевременное лечение субсерозной миомы матки, то можно получить устрашающую цепочку фактов, следующих и вытекающих один из другого:
О таких осложнениях организм подаст сигнал в виде острой боли, повышения температуры, головокружения, усиления потливости, слабости. Все это – повод для скорейшего обращения в клинику.
Диагностические методы
Для подтверждения диагноза субсерозной миомы матки недостаточно пройти лишь осмотр у гинеколога, необходимы более точные методики. К таким способам относятся:
Только пройдя все необходимое обследование можно приступать к лечению субсерозного узла миомы матки.
Лечение
Для эффективной борьбы с доброкачественной опухолью лечащий врач должен учесть все моменты: темпы роста узелковых образований, их место дислокации, возраст пациентки, ее состояние здоровья.
Наблюдение за миомой – один из главных моментов в проведении лечебных мероприятий. В случае отсутствия роста и угрозы для жизненно важных органов опухоль могут оставить на уровне контроля (проведение УЗИ через три месяца).
Лечение субсерозной миомы матки при средних и медленных скоростях возникновения новых опухолей заключается в приеме препаратов гормонального свойства и проведении симптоматических терапевтических мер.
Назначение гормонов может стать сдерживающим фактором и приостановить (в некоторых случаях уменьшить размер опухоли) процесс.
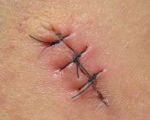
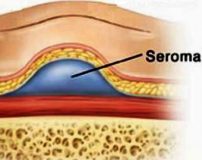
Послеоперационная серома ( Серома шва )
Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
МКБ-10
Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.
Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.