Что такое сократимость мышц
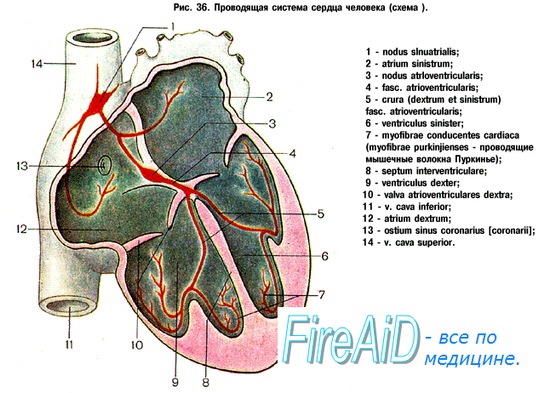
Сократимость, т. е. способность сокращаться, характерная для всех разновидностей мышечной ткани, реализуется в миокарде благодаря трем специфическим свойствам сердечной мышцы: автоматизм — способность клеток водителей ритма генерировать импульсы без каких-либо внешних воздействий; проводимость — способность элементов проводящей системы к электротонической передаче возбуждения; возбудимость — способность кардиомиоцитов возбуждаться в естественных условиях под влиянием импульсов, передаваемых по волокнам Пуркинье (рис. 9.5). Важной особенностью возбудимости сердечной мышцы является длительный рефракторный период (полное исчезновение или резкое снижение возбудимости кардиомиоцитов после их предыдущего сокращения), гарантирующий ритмический характер последующего сокращения.
Автоматизм и проводимость миокарда
В области правого предсердия, а также на границе предсердий и желудочков располагаются участки, ответственные за возбуждение сердечной мышцы. Автоматизм сердца имеет миогенную природу и обусловлен спонтанной активностью части клеток его атипической ткани.
Указанные клетки образуют скопления в определенных участках миокарда. Наиболее важным в функциональном отношении из них является синусный, или синоатриалъный, узел, расположенный между местом впадения верхней полой вены и ушком правого предсердия. В нижней части межпредсердной перегородки, непосредственно над местом прикрепления септальной створки трехстворчатого клапана, располагается атриовентри-кулярный узел. От него отходит пучок атипических мышечных волокон, который пронизывает фиброзную перегородку между предсердиями и переходит в узкий длинный мышечный тяж, заключенный в межжелудочковую перегородку. Он называется атриовентрикулярным пучком, или пучком Гиса. Пучок Гиса разветвляется, образуя две ножки, от которых приблизительно на уровне середины перегородки отходят волокна Пуркинье, также образованные атипической тканью и формирующие субэндокардиальную сеть в стенках обоих желудочков (см. рис. 9.5).
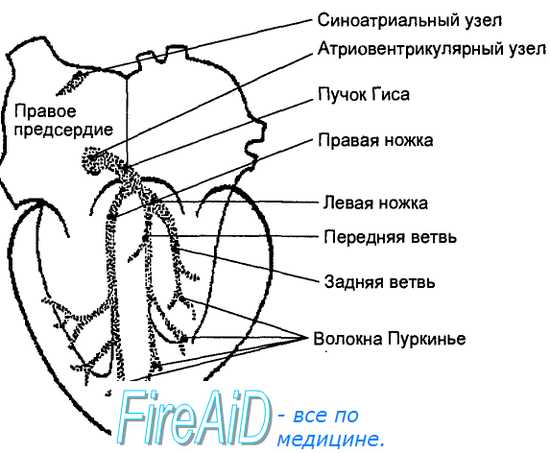
Функция проводимости в сердце имеет электротоническую природу. Она обеспечивается низким электрическим сопротивлением щелевидных контактов (нексусов) между элементами атипического и рабочего миокарда, а также в области вставочных пластинок, разделяющих кардиомиоциты. В результате сверхпороговое раздражение любого участка вызывает генерализованное возбуждение всего миокарда. Это позволяет считать ткань сердечной мышцы, морфологически разделенную на отдельные клетки, функциональным синцитием.
Возбуждение миокарда зарождается в синоатриальном узле, который называют водителем ритма, или пейсмекером первого порядка, и далее распространяется на мускулатуру предсердий с последующим возбуждением атриовентрикулярного узла, который является водителем ритма второго порядка. Скорость распространения возбуждения в предсердиях составляет 1 м/с. При переходе возбуждения на атриовентрикулярный узел имеет место так называемая атриовентрикулярная задержка, составляющая 0,04— 0,06 с. Механизм атриовентрикулярной задержки состоит в том, что проводящие ткани синоатриального и атриовентрикулярного узлов контактируют не непосредственно, а через волокна рабочего миокарда, для которых характерна более низкая скорость проведения возбуждения. Последнее распространяется далее по ножкам пучка Гиса и волокнам Пуркинье, передаваясь на мускулатуру желудочков, которую оно охватывает со скоростью 0,75—4,0 м/с. В силу особенностей расположения волокон Пуркинье возбуждение сосочковых мышц происходит несколько раньше, чем оно охватывает стенки желудочков. Благодаря этому нити, удерживающие трехстворчатый и митральный клапаны, оказываются натянутыми раньше, чем на них начинает действовать сила сокращения желудочков. По той же причине наружная часть стенки желудочков у верхушки сердца возбуждается несколько раньше участков стенки, прилежащих к ее основанию. Таким образом, волна возбуждения последовательно охватывает различные отделы сердца в направлении от правого предсердия к верхушке. Однако указанные сдвиги во времени крайне невелики и обычно принимается, что весь миокард желудочков охватывается возбуждением одновременно.
Что такое сократимость мышц
Выделяют несколько последовательных этапов запуска и осуществления мышечного сокращения.
1. Потенциал действия распространяется вдоль двигательного нервного волокна до его окончаний на мышечных волокнах.
2. Каждое нервное окончание секретирует небольшое количество нейромедиатора ацетилхолина.
3. Ацетилхолин действует на ограниченную область мембраны мышечного волокна, открывая многочисленные управляемые ацетилхолином каналы, проходящие сквозь белковые молекулы, встроенные в мембрану.
4. Открытие управляемых ацетилхолином каналов позволяет большому количеству ионов натрия диффундировать внутрь мышечного волокна, что ведет к возникновению на мембране потенциала действия.
5. Потенциал действия проводится вдоль мембраны мышечного волокна так же, как и по мембране нервного волокна.
6. Потенциал действия деполяризует мышечную мембрану, и большая часть возникающего при этом электричества течет через центр мышечного волокна. Это ведет к выделению из саркоплазматического ретикулума большого количества ионов кальция, которые в нем хранятся.
7. Ионы кальция инициируют силы сцепления между актиновыми и миозиновыми нитями, вызывающие скольжение их относительно друг друга, что и составляет основу процесса сокращения мыщц.
8. Спустя долю секунды с помощью кальциевого насоса в мембране саркоплазматического ретикулума ионы кальция закачиваются обратно и сохраняются в ретикулуме до прихода нового потенциала действия. Удаление ионов кальция от миофибрилл ведет к прекращению мышечного сокращения.
Далее мы обсудим молекулярные механизмы этого процесса.
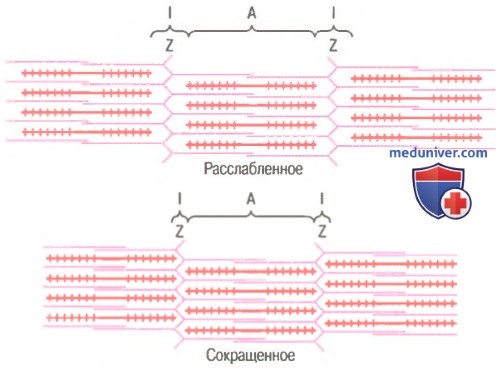
Молекулярные механизмы мышечного сокращения
Механизм скольжения нитей для мышечного сокращения. На рисунке показан основной механизм мышечного сокращения. Показано расслабленное состояние саркомера (вверху) и сокращенное состояние (внизу). В расслабленном состоянии концы актиновых нитей, отходящие от двух последовательных Z-дисков, лишь незначительно перекрываются. Наоборот, в сокращенном состоянии актиновые нити втягиваются внутрь между миозиновыми так сильно, что их концы максимально перекрывают друг друга. При этом Z-диски притягиваются актиновыми нитями к концам миозиновых. Таким образом, мышечное сокращение осуществляется путем механизма скольжения нитей.
Что заставляет нити актина скользить внутрь среди нитей миозина? Это связано с действием сил, генерируемых при взаимодействии поперечных мостиков, исходящих от нитей миозина, с нитями актина. В условиях покоя эти силы не проявляются, однако распространение потенциала действия вдоль мышечного волокна приводит к выделению из саркоплазматическо-го ретикулума большого количества ионов кальция, которые быстро окружают миофи-бриллы. В свою очередь, ионы кальция активируют силы взаимодействия между нитями актина и миозина, в результате начинается сокращение. Для осуществления процесса сокращения необходима энергия. Ее источником являются высокоэнергетические связи молекулы АТФ, которая разрушается до АДФ с высвобождением энергии. В следующих разделах мы приведем известные детали молекулярных процессов сокращения.
Молекулярные особенности сократительных нитей
Миозиновая нить. Она состоит из множества молекул миозина, молекулярная масса каждой составляет около 480000. На рисунке показана отдельная молекула; и также — объединение многих молекул миозина в миозиновую нить, а также взаимодействие одной стороны этой нити с концами двух актиновых нитей.
В состав молекулы миозина входят 6 полипептидных цепей: 2 тяжелые цепи с молекулярной массой около 200000 каждая и 4 легкие цепи с молекулярной массой около 20000 каждая. Две тяжелые цепи спирально закручиваются вокруг друг друга, формируя двойную спираль, которую называют миозиновым хвостом. С одного конца обе цепи изгибаются в противоположных направлениях, формируя глобулярную полипептидную структуру, называемую миозиновой головкой. Таким образом, на одном конце двойной спирали молекулы миозина образуются 2 свободные головки; 4 легкие цепи также включены в состав миозиновой головки (по 2 в каждой). Они помогают регулировать функцию головки во время мышечного сокращения.
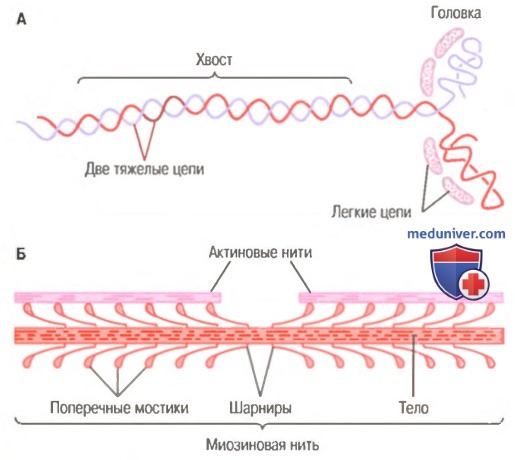
Б. Объединение многих молекул миозина в одну миозиновую нить.
Показаны также тысячи миозиновых поперечных мостиков и взаимодействие их головок с прилежащими актиновыми нитями.
Миозиновая нить состоит из 200 или более отдельных молекул миозина. Видно, что хвосты молекул миозина объединяются, формируя тело нити, а многочисленные головки молекул выдаются наружу по сторонам тела. Кроме того, наряду с головкой в сторону выступает часть хвоста каждой миозиновой молекулы, образуя плечОу которое выдвигает головку наружу от тела, как показано на рисунке. Выступающие плечи и головки вместе называют поперечными мостиками. Каждый поперечный мостик может сгибаться в двух точках, называемых шарнирами. Один из них расположен в месте, где плечо отходит от тела миозиновой нити, а другой — где головка крепится к плечу. Движение плеча позволяет головке или выдвигаться далеко наружу от тела миозиновой нити, или приближаться к телу. В свою очередь, повороты головки участвуют в процессе сокращения, что обсуждается в следующих разделах.
Общая длина каждой миозиновой нити остается постоянной и равна почти 1,6 мкм. В самом центре миозиновой нити на протяжении 0,2 мкм поперечных мостиков нет, поскольку снабженные шарнирами плечи отходят в стороны от центра.
Сама миозиновая нить сплетена таким образом, что каждая последующая пара поперечных мостиков смещена в продольном направлении относительно предыдущей на 120°, что обеспечивает распределение поперечных мостиков во всех направлениях вокруг нити.
АТФ-азная активность миозиновой головки. Есть и другая особенность миозиновой головки, необходимая для мышечного сокращения: миозиновая головка функционирует как фермент АТФ-аза. Как объясняется далее, это свойство позволяет головке расщеплять АТФ и использовать энергию расщепления высокоэнергетической связи для процесса сокращения.
Актиновая нить. Актиновая нить состоит из трех белковых компонентов: актина, тропомиозина и тропонина.
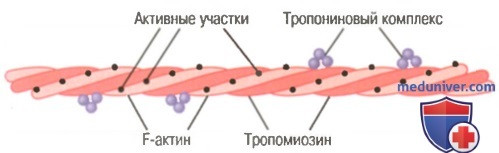
К одному концу каждой молекулы тропомиозина прикреплен тропониновый комплекс, который запускает сокращение.
Основой актиновой нити являются две цепи белковой молекулы F-актина. Обе цепи закручиваются в спираль так же, как и молекула миозина.
Каждая цепь двойной спирали F-актина состоит из полимеризованных молекул G-актина с молекулярной массой около 42000. К каждой молекуле G-актина прикреплена 1 молекула АДФ. Полагают, что эти молекулы АДФ являются активными участками на актиновых нитях, с которыми взаимодействуют поперечные мостики миозиновых нитей, обеспечивая мышечное сокращение. Активные участки на обеих цепях F-актина двойной спирали расположены со смещением таким образом, что вдоль всей поверхности актиновой нити встречается один активный участок примерно через каждые 2,7 нм.
Длина каждой актиновой нити — около 1 мкм. Основания актиновых нитей прочно встроены в Z-диски; концы этих нитей выступают в обоих направлениях, располагаясь в пространствах между миозиновыми молекулами.
Молекулы тропомиозина. Актиновая нить также содержит другой белок — тропомиозин. Каждая молекула тропомиозина имеет молекулярную массу 70000 и длину 40 нм. Эти молекулы спирально оплетают спираль из F-актина. В состоянии покоя молекулы тропомиозина располагаются поверх активных участков актиновых нитей, препятствуя их взаимодействию с миозиновыми нитями, лежащему в основе сокращения.
Тропонин и его роль в мышечном сокращении. По ходу молекул тропомиозина к ним периодически прикреплены другие белковые молекулы, называемые тропонином. Они представляют собой комплексы трех слабосвязанных белковых субъединиц, каждая из которых играет специфическую роль в регуляции мышечного сокращения. Одна из субъединиц (тропонин I) имеет высокое сродство к актину, другая (тропонин Т) — к тропомиозину, третья (тропонин С) — к ионам кальция. Считают, что этот комплекс прикрепляет тропомиозин к актину. Высокое сродство тропонина к ионам кальция, как полагают, инициирует процесс сокращения, о чем говорится в следующей статье.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Биомеханические свойства скелетных мышц человека
В третьей лекции по дисциплине «Биомеханика мышц» для студентов НГУ им. П.Ф.Лесгафта рассматриваются биомеханические свойства скелетных мышц человека: сократимость, жесткость, вязкость, прочность, релаксация. Рассмотрена трехкомпонентная модель мышцы.
Лекция 3
Биомеханические свойства скелетных мышц человека
Анализируя предмет биомеханики, А.А. Ухтомский (1927) указывал: «Биомеханика изучает ту же систему нервно-мышечных приборов как рабочую машину, то есть задается вопросом, каким образом полученная механическая энергия движения и напряжения может приобрести определенное рабочее применение» (С. 141). Начиная с этой лекции, мы будем рассматривать именно этот аспект деятельности мышц.
3.1. Биомеханические свойства мышц
Биомеханические свойства скелетных мышц – это характеристики, которые регистрируют при механическом воздействии на мышцу.
Следует отметить, что в условиях живого организма изучение биомеханических свойств мышц крайне затруднено. В этой лекции, кроме биомеханических свойств мышц, приводятся данные о свойствах сухожилий и связок.
К биомеханическим свойствам мышц относятся:
Сократимость
Сократимость – способность мышцы укорачиваться при возбуждении, в результате чего возникает сила тяги.
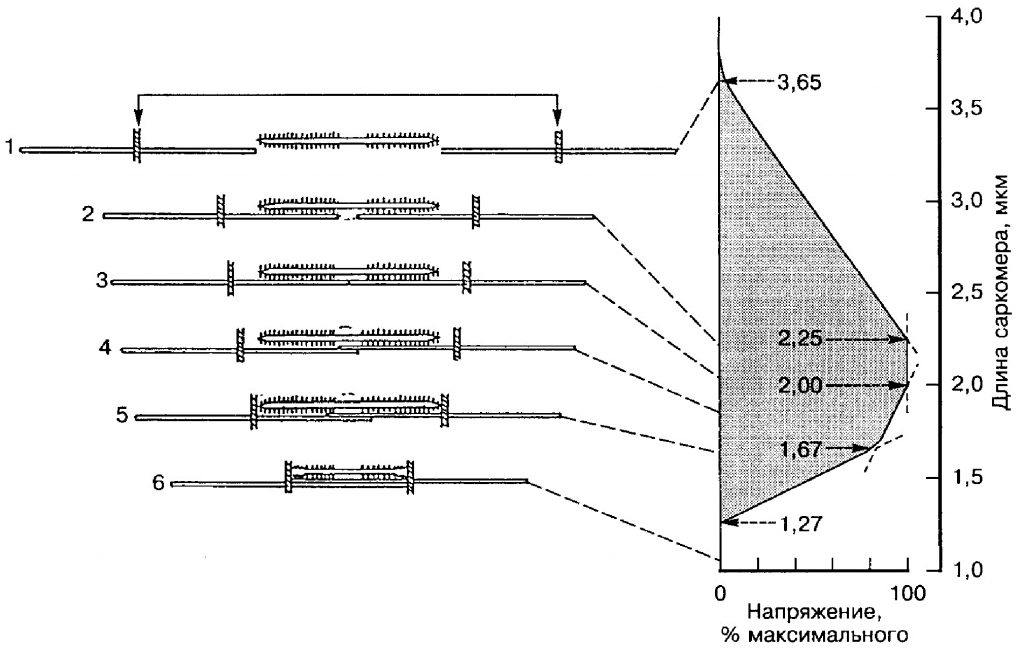
В первой лекции было подробно рассмотрено строение первичного сократительного элемента мышцы – саркомера. В 1966 году А. Гордон, А. Хаксли и Ф. Джулиан провели специальные исследования, позволившие установить зависимость силы, развиваемой саркомером, от его длины. Одно из предположений, касающихся механизма скольжения филаментов, заключалось в том, что каждый поперечный мостик (миозиновая головка) действует подобно независимому генератору силы. Поэтому уровень силы, развиваемой во время сокращения, должен зависеть от количества одновременных взаимодействий между толстыми и тонкими филаментами. Это предположение подтвердилось. Действительно, существуют критические значения длины саркомера, при которых развиваемая им сила падает до нуля (рис.3.1).
Рис. 3.1. Схема, иллюстрирующая зависимость между степенью перекрытия толстых и тонких филаментов и силой, развиваемой саркомером (по: A.M. Gordon, A.F. Huxley. F.J. Julian, 1966)
Первое критическое значение длины саркомера равно 1,27 мкм. Оно соответствует максимальному укорочению мышцы. В этом состоянии мышцы регулярность расположения толстого и тонкого филаментов нарушается, они искривляются. Поэтому количество одновременных взаимодействий между филаментами резко уменьшается. Сила падает до нуля. Второе критическое значение длины саркомера равно 3,65 мкм. Оно соответствует максимальному удлинению мышцы. При максимальном растяжении саркомера перекрытия толстых и тонких филаментов нет, поэтому сила уменьшается до нуля. Если длина саркомера находится в интервале от 1,27 мкм до 3,65 мкм, значение силы отличается от нуля. Максимальная сила, которую способен развить саркомер, соответствует значениям его длины – от 1,67 до 2,25 мкм.
Жесткость
Жесткость материала – характеристика тела, отражающая его сопротивление изменению формы при деформирующих воздействиях (В.Б. Коренберг, 2004). Чем больше жесткость тела, тем меньше оно деформируется под воздействием силы. Закон Гука гласит, что сила упругости, возникающая при растяжении или сжатии тела, пропорциональна его удлинению.
Жесткость материала характеризуется коэффициентом жесткости (k). Единица измерения жесткости тела – Н/м. Жесткость линейной упругой системы, например, пружины, есть величина постоянная на всем участке деформации.
В отличие от пружины, мышца представляет собой систему с нелинейными свойствами. Это связано с тем, что структура мышцы очень сложна. Поэтому для мышцы зависимость силы от удлинения будет отлична от закона Гука. Возникающая в мышце сила упругости не пропорциональна удлинению. Вначале мышца растягивается легко, а затем даже для небольшого ее растяжения необходимо прикладывать все большую силу. Поэтому часто мышцу сравнивают с трикотажным шарфом, который вначале легко растягивается, а затем становится практически нерастяжимым. Иными словами, жесткость мышцы с ее удлинением возрастает. Из этого следует, что мышца представляет собой систему, обладающую переменной жесткостью. В этом случае коэффициент жесткости k равен первой производной силы по деформации материала. Установлено, что жесткость активной мышцы в 4-5 раз больше жесткости пассивной мышцы. В табл. 3.1. представлены значения коэффициентов жесткости мышц-сгибателей стопы у представителей разных видов спорта.
Таблица 3.1 Значения коэффициента жесткости мышц-сгибателей стопы у представителей различных видов спорта
(по: А.С. Аруину, В.М. Зациорскому, Л.М. Райцину, 1977)
Вязкость
Вязкость – свойство жидкостей, газов и «пластических» тел оказывать неинерционное сопротивление перемещению одной их части относительно другой (смещение смежных слоев). При этом часть механической энергии переходит в другие виды, главным образом в тепло (В.Б. Коренберг, 1999).
Это свойство сократительного аппарата мышцы вызывает потери энергии при мышечном сокращении, идущие на преодоление вязкого трения. Предполагается, что трение возникает между толстыми и тонкими филаментами при сокращении мышцы. Кроме того, трение возникает между возбужденными и невозбужденными мышечными волокнами. Это связано с тем, что соседние мышечные волокна «связаны» посредством эндомизия. Поэтому, если возбуждены все мышечные волокна, трение должно быть меньше. Показано, что при сильном возбуждении мышцы, ее вязкость резко уменьшается (Г.В. Васюков,1967).
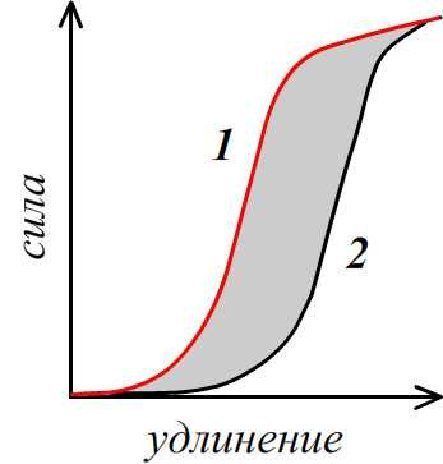
Если абсолютно упругое тело (например, пружину) вначале растянуть, а затем – снять деформирующую нагрузку, то кривая «удлинение – сила» будет идентичной во время обеих фаз. Если же мы имеем дело с упруговязким материалом (мышцей), кривые окажутся неидентичными. При нагрузке (растягивании мышцы) зависимость «удлинение – сила» соответствует кривой 1. Рис.3.2.
Рис. 3.2. Зависимость «удлинение – сила» при растягивании (кривая 1) и укорочении мышцы (кривая 2)
При укорочении мышцы зависимость «удлинение – сила» соответствует кривой 2. Кривые 1 и 2 образуют «петлю гистерезиса». Площадь фигуры, заключенной между кривыми 1 и 2, отражает потери энергии на трение. Мышца, обладающая большей вязкостью, будет характеризоваться большей площадью «петли гистерезиса». Вы знаете, что при выполнении физических упражнений температура мышц повышается. Повышение температуры мышц связано с наличием у мышц вязкости. Результатом наличия вязкости происходят потери энергии мышечного сокращения на трение. Разогрев мышц (разминка) приводит к тому, что вязкость мышц уменьшается.
Прочность
Прочностью материала называют его способность сопротивляться разрушению под действием внешних сил (И.Ф. Образцов с соавт., 1988).
Значительно снижает прочность связок и сухожилий иммобилизация. И, наоборот, при исследовании животных была найдена связь между уровнем физической активности и прочностью сухожилий и связок. Показано, что в подавляющем большинстве случаев прочность сухожилий более высока, чем прочность их прикрепления к костям. Поэтому при травмах сухожилий они не разрываются, а отрываются от места прикрепления. Следует учитывать также, что в процессе тренировок прочность сухожилий и связок увеличивается сравнительно медленно. При форсированном развитии скоростно-силовых качеств мышц может возникнуть несоответствие между возросшими скоростно-силовыми возможностями мышечного аппарата и недостаточной прочностью сухожилий и связок. Это грозит потенциальными травмами (А.С. Аруин, В.М. Зациорский, В.Н. Селуянов, 1981).
Релаксация
Релаксация мышц – свойство, проявляющееся в уменьшении с течением времени силы тяги при постоянной длине.
Для оценки релаксации используют показатель – время релаксации, то есть отрезок времени, в течение которого натяжение мышцы уменьшается в е раз от первоначального значения. Многочисленными исследованиями установлено, что высота выпрыгивания вверх с места зависит от длительности паузы между приседанием и отталкиванием. Чем больше эта пауза (изометрический режим работы мышц), тем меньше сила их тяги и, как следствие, высота выпрыгивания, табл. 3.2. Таким образом, релаксация мышц приводит к уменьшению высоты выпрыгивания.
Таблица 3.2 Влияние паузы на высоту прыжка с места (n = 31) (по: А.С. Аруин, В.М. Зациорский, Л.М. Райцин, 1977)