Соматотропин
Зачем необходим гормона роста:
Гормон препятствует поглощению тканями глюкозы, по своему действию противоположен инсулину. Это необходимо, чтобы не было переизбытка сахара.
Соматотропин активно выделяется во время глубокого сна, при активной физической нагрузке, при резком снижении сахара в крови.
Анализ назначают в основном детям. Педиатр может порекомендовать проверить соматотропин, если видит:
Взрослым могут назначать при подозрении на гликемию, в том числе на фоне алкогольной зависимости. Как дополнительное исследование при диагностике щитовидной железы.
Кровь необходимо сдавать натощак. В период с 8 до 14 часов, но лучше в первой половине дня. Последний ужин рекомендуется не позднее 6 вечера. Пить воду можно в неограниченном количестве. Но, помните, только чистую воду. Газировки, кофе, чай, соки и компоты запрещены.
Если вы на постоянной основе принимаете какие-либо лекарственные препараты, то необходимо сообщить об этом врачу.
Приходите на сдачу анализа за 15-20 минут до начала забора крови. Необходимо отдохнуть и успокоиться.
Единицы измерения: нг/мл ; мЕД/л ; коэффициент пересчета = нг/мл х 2,6 = мЕД/л
Референсные значения: 0.01-0,97 нг/мл
Повышение значений:
Снижение значений:
Поэтому интерпретацией результатов может заниматься только лечащий врач, а постановка диагноза только по уровню эритропоэтина невозможна. Срок выдачи зависит от срочности анализа.
Интерпретация результатов
Проверять гормон необходимо преимущественно детям и подросткам, поскольку он влияет на выработку других гормонов, а также на обмен веществ. Существует большое множество причин, которые приводят к нарушению соматотропина, поэтому необходимо обратиться к квалифицированному специалисту, который поможет установить причины нарушения. Занимается этим врач-эндокринолог. Возможно, понадобится дополнительная консультация онколога, нефролога и гастроэнтеролога.
Довольно часто опухоли в гипофизе влияют на выработку гормона. При больших размерах вероятно полное подавление и повреждение близлежащих тканей.
Детям, как правило, назначают синтетический гормон, который на 100 % заменяет соматотропин. При избытке назначают хирургические операции (опухоли), радиооблучение и медикаментозную терапию.
При длительном нарушении выработки гормона могут наблюдаться осложнения в виде полипов в кишечнике, диабет, заболевания органов зрения и повышения давления. Взрослым нередко назначают гормональную терапию.
В клинике ЦЭЛТ вы можете обратиться к специалисту, а также сдать анализ на соматотропный гормон. При необходимости врач назначает лечение и скорректирует выработку. Мы принимаем как взрослых, так и совсем маленьких пациентов.
Возможности медикаментозной коррекции недостатка гормона роста у взрослых
Каковы основные причины соматотропной недостаточности у взрослых? Каковы ее клинические проявления? Какие методы лабораторно подтверждают диагноз? Как известно, гормон роста (ГР) был последним из классических гормонов, который начали применять с
Каковы основные причины соматотропной недостаточности у взрослых?
Каковы ее клинические проявления?
Какие методы лабораторно подтверждают диагноз?
Как известно, гормон роста (ГР) был последним из классических гормонов, который начали применять с целью заместительной гормональной терапии у взрослых. У детей история медикаментозной коррекции низкорослости насчитывает около тридцати лет, ко взрослым же лечение с использованием биосинтетических препаратов ГР впервые было применено около десяти лет назад. В течение многих лет с целью терапии использовался ГР, получаемый из гипофизарных экстрактов, однако в 1985 году, когда были описаны четыре случая болезни Крейтцфельдта — Якоба у реципиентов гипофизарного ГР, использование последнего было запрещено. Это послужило отправной точкой для начала работ по производству биосинтетического ГР [2].
Использование ГР у детей и произошедший параллельно научный прорыв в отношении диагностирования дефицита гормона роста у взрослых привели к появлению в клинической эндокринологии новой нозологии и, соответственно, новых методов обследования и лечения. Ни один конгресс или симпозиум, проходящий в настоящее время, не обходится без докладов, посвященных проблемам диагностики дефицита ГР (ДГР) у взрослых, выявлению нарушений, сопровождающих заболевание, и принципам подбора терапии.
Для того чтобы создать более точное представление о спектре нарушений, развивающихся на фоне соматотропной недостаточности, необходимо кратко напомнить о структуре ГР, механизмах его секреции и влиянии на органы и системы. ГР, синтезируемый соматотрофами передней доли гипофиза, относится к особому семейству пептидных гормонов, в состав которого кроме ГР входят пролактин (ПРЛ) и плацентарный соматомаммотропин человека (СМЧ). Секреция ГР находится под контролем двух гипоталамических гормонов: соматостатина или соматотропин-ингибирующего фактора (СИФ), который оказывает блокирующее действие на синтез и секрецию соматотрофами ГР. Соматотропин — рилизинг гормон (СРГ) — оказывает стимулирующее действие на соматотрофы, что проявляется увеличением продукции ГР.
Как многие гормоны, ГР синтезируется в определенном импульсном режиме, пики секреции приходятся на 22.00 и 4.00 часа.
Несмотря на существование специфических рецепторов ГР, его действие осуществляется посредством специфических факторов, аналогичных по своей структуре инсулину: инсулиноподобного ростового фактора I (ИФР-I) и инсулиноподобного ростового фактора II (ИФР-II). ИФР-I, действуя через собственные рецепторы, оказывает ростовые эффекты преимущественно в постэмбриональном онтогенезе организма. Действие ИФР-II проявляется преимущественно в процессе эмбриогенеза.
Многочисленные исследования, результаты которых публикуются в современных медицинских изданиях, красноречиво свидетельствуют о наличии серьезных нарушений в соматическом и психологическом статусе пациентов с декомпенсированной недостаточностью гормона роста. Эти нарушения характеризуются изменением соотношения жировая/мышечная ткань в сторону снижения удельного веса последней, увеличения удельного веса жировой ткани и сопровождаются висцеральным отложением последней. При проведении денситометрии обнаруживается снижение плотности костной ткани (МПК). Scacchi at al отметили обратно пропорциональную зависимость между индексом массы тела (ИМТ) и периодом полужизни ГР, а также амплитудой секреции ГР. Процент содержания жировой ткани находился в обратной зависимости от интегрального показателя концентрации ГР, определяемого в течение 24 часов.
Со стороны метаболических нарушений необходимо выделить снижение толерантности к углеводам при проведении инсулинтолерантного теста, увеличение продукции инсулина, проинсулина, повышение содержания триглицеридов плазмы крови, липопротеидов низкой и очень низкой плотности [3].
Не до конца изучено влияние недостаточности ГР на увеличение риска развития сердечно-сосудистых заболеваний, однако при ретроспективном исследовании 333 пациентов с гипопитуитаризмом выявлено, что в течение 22 лет случаи кардиоваскулярной смерти встречались в два раза чаще по сравнению с группой контроля. При проведении эхокардиографии исследователи обнаруживали снижение массы левого желудочка, уменьшение толщины перегородки и задней стенки желудочков, а также снижение фракции выброса левого желудочка.
Еще сравнительно недавно проблема дефицита ГР у взрослых не находила отражения в исследованиях эндокринологов, хотя вопросы, связанные с недостаточностью секреторной функции гипофиза, возникали с того времени, когда были впервые описаны пациентки с синдромом Шиена (Шихана). Данная патология обусловлена развитием инфарктов и кровоизлияний в раннем послеродовом периоде и характеризуется развитием пангипопитуитаризма. Долгие годы пациентки получали заместительную гормональную терапию глюкокортикоидами, тиреоидными гормонами, половыми стероидами, однако при этом продолжали предъявлять неспецифические жалобы на повышенную утомляемость, слабость, немотивированное увеличение массы тела. При попытке исследовать уровень гормонов сыворотки крови с целью выяснения степени компенсации имеющихся нарушений патологических отклонений обнаружено не было, а сниженному уровню ГР не придавали значения. В дальнейшем многочисленные клинические и лабораторные исследования продемонстрировали, что снижение секреции ГР в организме взрослого человека приводит к целому ряду нарушений, которые остаются незамеченными и не имеют такой яркой клинической окраски, как, например, гиперсекреция ГР и развивающаяся вследствие этого акромегалия.
Перечислим причины развития соматотропной недостаточности у взрослых
Количество пациентов, подвергшихся тем или иным вмешательствам на селлярной области, растет год от года, и связано это с повышением разрешающей способности диагностических методов, используемых при обследовании больных, и расширением лечебных возможностей современной медицины. Исходя из этого можно прогнозировать, что количество пациентов, нуждающихся в проведении скринингового обследования ДГР, будет увеличиваться год от года. Современная фармакология, в свою очередь, располагает целым спектром препаратов, призванных компенсировать соматотропную недостаточность; ниже приводится перечень средств, имеющихся на сегодняшний день в отечественной аптечной сети.
«Золотым стандартом» в диагностике ДГР у взрослых справедливо считается инсулинотолерантный тест. Необходимо оговориться, что его проведение возможно только после компенсации вторичного гипотиреоза и вторичного гипокортицизма, в противном случае результаты теста могут быть недостоверными.
В рамках исследования, проведенного в клинике эндокринологии ММА им. И. М. Сеченова и посвященного изучению целесообразности назначения препарата генноинженерного гормона роста взрослым, была обследована группа больных с подозрением на наличие соматотропной недостаточности.
В группу вошли 15 человек в возрасте от 15 до 45 лет: 12 женщин (80%) и трое мужчин (20%). Девять женщин (60%) были прооперированы по поводу макропролактином гипофиза, трое мужчин (20%) и трое женщин (20%) подверглись оперативному вмешательству по поводу краниофарингиомы гипофиза, у одного мужчины (6,7%) при проведении МРТ выявлена агенезия гипофиза. Среди всех обследованных пациентов задержка роста зафиксирована у троих мужчин (20%) в возрасте 16, 21 и 27 лет, оценка роста у них проводилась с использованием таблицы «Перцентильный график роста для мальчиков». У первого пациента рост был равен 148 см, при оценке перцентильных значений величина стандартного отклонения (SDS) составила –3,5. Рост второго и третьего пациентов был равен 145 и 152 см соответственно, но в связи с невозможностью оценить величину SDS исходя из паспортного возраста последняя была рассчитана исходя из костного. В первом случае паспортный возраст ровнялся 13-14 годам и SDS –2, во втором случае костный возраст соответствовал 16 годам и SDS –3. Структура эндокринных заболеваний, выявленных у пациентов с подозрением на соматотропную недостаточность, отражена в табл. 2.
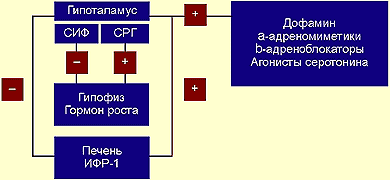 |
| Регуляция секреции гормона роста |
Перед проведением провокационных тестов, направленных на диагностику соматотропной недостаточности, всем пациентам был проведен комплекс лабораторно-диагностических мероприятий для уточнения соматического и гормонального статуса пациентов.
Большинство пациентов получали заместительную гормональную терапию по поводу вторичного гипотиреоза, вторичной надпочечниковой недостаточности, несахарного диабета; у всех было проведено скрининговое исследование концентрации свободного Т4, пролактина, ЛГ, ФСГ, эстрадиола с целью коррекции доз получаемых препаратов.
Исследование соматического статуса предусматривало определение следующих показателей: расчет индекса массы тела (ИМТ), вычисление отношения объем талии/объем бедер (ОТ/ОБ), определение уровня глюкозы, холестерина, триглицеридов, ЛПНП, ЛНВП, АЛТ, АСТ. Проводилось ЭКГ и измерение артериального давления с целью исключения патологии со стороны сердечно-сосудистой системы.
Для оценки качества жизни пациентов с рассматриваемой патологией использовался опросник, разработанный специально для пациентов с дефицитом ГР — QoL-AGHDA (Quality of Life — Assessment of Growth Hormone — Deficiency in Adults) и содержащий 25 вопросов, на которые необходимо было ответить «да» или «нет». Каждый положительный ответ оценивался в один балл; чем больше оказывалась полученная в результате сумма, тем ниже показатель качества жизни.
В ходе обследования были получены следующие результаты.
Нормальные показатели ИМТ (18 30) диагностировано у четырех человек (26,7%). У одного пациента наряду с задержкой роста был выявлен дефицит массы тела, ИМТ составил 15,9 (6,7%). У одной пациентки (6,7%) обнаружен сахарный диабет II типа. Признаки висцерального ожирения выявлены у четырех пациенток (26,7%).
При обследовании у шести пациенток обнаружено повышение гликемии натощак, которое составило 7,025 ± 0,12 ммоль/л; показатели гликемии у 11 пациентов были в пределах нормы и варьировали от 3,6 до 5,5 ммоль/л. Для исключения возможных нарушений углеводного обмена: тощаковой гипергликемии, нарушения толерантности к углеводам, сахарного диабета, гиперинсулинемии всем пациентам был проведен оральный глюкозотолерантный тест с 75 г глюкозы. При определении гликемии через 2 часа после приема 75 г глюкозы последняя составила 6,6 ± 0,14 ммоль/л. Сахарный диабет был выявлен у одной пациентки (гликемия 11,9 ммоль/л), еще у двоих пациентов определено нарушение толерантности к углеводам (гликемия 8,3 и 9,0 ммоль/л). При исследовании уровня С-пептида сыворотки крови были получены следующие результаты: базальная гиперинсулинемия (>2,5 нг/мл) обнаружена у пяти пациентов (3,33%) и составила 3,89 ± 0,1 нг/мл. Более чем двукратное увеличение концентрации С-пептида через 120 минут после стимуляции отмечено у девяти пациентов (60%) и составило 10,5 ± 0,4 нг/мл. При оценке липидного обмена гиперхолестеринемия выявлена у десяти пациентов (66,6%), гипертриглицеридемия обнаружена у семи пациентов (46,6%).
Всем пациентам был проведен инсулинотолерантный тест с целью подтверждения дефицита гормона роста. В условиях стационара пациентам внутривенно вводился инсулин короткого действия: Humulin R или Actrapid HM, из расчета 0,1 ЕД/кг [1]. Исходно через каждые 15 минут в дальнейшем пациентам проводилось определение гликемии в капиллярной крови и забор крови для последующего выявления уровня гормона роста в сыворотке крови.
В ответ на инсулин-индуцированную гипогликемию у 12 обследованных (80%) концентрация ГР не превысила 5 нг/мл, а составила в среднем 0,76 ± 0,013 нг/мл. У троих на фоне гипогликемии было зарегистрировано повышение уровня ГР до 30,78 ± 0,45 нг/мл.
По результатам проведенного теста девяти пациентам была назначена терапия генотропином (Pharmacia&Upjohn). Двое пациентов с задержкой роста получают препарат в настоящее время, у семи человек завершился шестимесячный курс терапии. При расчете дозы препарата использовались рекомендации Janssen и соавт., дозировка генотропина определялась из расчета 0,018 МЕ/кг для шести пациентов, а для трех пациентов с задержкой роста доза была вычислена из расчета 0,1 МЕ/кг [2].
Спустя 6 месяцев после начала терапии все пациенты прошли повторное обследование. Сколько-нибудь значимых изменений ИМТ отмечено не было, показатель ОТ/ОБ снизился у пяти человек, у двоих он остался на прежнем уровне. У троих пациентов выявлено некоторое снижение концентрации холестерина, составившее 8,4, 9,7 и 26,6% от первоначального уровня. У троих пациентов не определено каких-либо изменений, у одного пациента выявлено повышение концентрации холестерина на 17% от исходного. По показателям содержания триглицеридов выявлены следующие данные: у четверых пациентов снижение ТГ составило 56,4, 47,2, 3,7 и 6,3% от исходного. В одном случае динамики отмечено не было, а у двоих человек зафиксировано повышение концентрации ТГ, составившее 68 и 92% от исходного уровня. Снижение уровня ТГ и холестерина на фоне терапии генотропином подтверждается данными зарубежных исследователей, демонстрирующих нормализацию показателей липидного обмена на фоне заместительной терапии.
Перед началом терапии средний показатель качества жизни составил 12,5 балла, а на последней неделе терапии он снизился до 8,9 балла (необходимо отметить, что, по данным Holmes и соавт., у здоровых пациентов, обследованных в Швеции, он составляет 3,7).
Пациент с задержкой роста за 6 месяцев лечения вырос на 5 см, и его рост на момент окончания терапии составил 157 см.
Среди зафиксированных пациентами побочных эффектов чаще всего встречались: отеки, артралгии и миалгии, которые развивались на 3-6-й неделе терапии; о них сообщили четверо пациентов. Аналогичные данные демонстрируют и зарубежные исследователи, проводившие наблюдения за более многочисленными группами пациентов, получавших ГР.
По результатам проведенного исследования можно сделать следующие выводы.
Литература
1. Алгоритмы диагностики и лечения болезней эндокринной системы/ Под ред. И. И. Дедова, 1997.
2. Дедов И. И., Тюльпаков А. Н., Петеркова В. А. Соматотропная недостаточность, 1998.
3. Monson J. P. Growth Hormone Therapy. Oxf, 1999. Р. 93-103.
НутропинАq®
Инструкция
Торговое название
Международное непатентованное название
Лекарственная форма
Раствор для подкожного введения 10 мг/2 мл (30 МЕ)
Состав
Один картридж содержит
вспомогательные вещества: натрия хлорид, фенол жидкий, полисорбат 20, натрия цитрата дигидрат, кислота лимонная безводная, вода для инъекций.
Описание
Прозрачная или слегка опалесцирующая, бесцветная или слегка желтоватая жидкость.
Фармакотерапевтическая группа
Гипоталамо-гипофизарные гормоны и их аналоги. Гормоны передней доли гипофиза и их аналоги. Соматропин и его аналоги. Соматропин.
Фармакологические свойства
Фармакокинетика
Фармакокинетические свойства НутропинAq® были исследованы только у здоровых взрослых мужчин.
Абсорбция: Абсолютная биодоступность рекомбинантного человеческого гормона роста (ГР) при подкожном введении составляет 80%.
Распределение: Исследования соматропина на животных показали локализацию ГР в органах с высокой перфузией, особенно в печени и в почках. Объем распределения в стабильной фазе для соматропина у здоровых взрослых мужчин составляет около 50 мл/кг массы тела, приближаясь к объему сыворотки крови.
Метаболизм: Установлено, что печень и почки являются главными органами для катаболизма белка ГР. Исследования на животных показали, что почки являются доминантным органом выведения соматропина. ГР фильтруется в клубочках и реабсорбируется в проксимальных канальцах. Далее он расщепляется в клетках почки на составляющие аминокислоты, которые возвращаются обратно в системный кровоток.
Выведение: После подкожного струйного введения средний период полувыведения соматропина (Т½) составляет около 2,3 ч. После внутривенного струйного введения соматропина средний период полувыведения составляет около 20 минут, а средний клиренс находится в пределах 116-174 мл/час/кг.
Особые группы пациентов
Информация о фармакокинетике соматропина у пожилых и детей, в зависимости от расы и пола и у пациентов с почечной или печеночной недостаточностью является неполной.
Выведение и средний конечный период полувыведения Т½ соматропина у взрослых пациентов и детей с недостаточностью гормона роста аналогичны наблюдаемым у здоровых людей.
Доступные литературные данные свидетельствуют, что клиренс соматропина одинаков у детей и взрослых.
Ограниченные опубликованные данные свидетельствуют о том, что плазменный клиренс и средняя стабильная концентрация соматропина в плазме может не отличаться у молодых и пожилых пациентов.
Отмеченные значения периодов полураспада для эндогенного ГР у здоровых взрослых чернокожих мужчин не отличаются от наблюдаемых значений для здоровых взрослых белых мужчин. Данные для других рас не доступны.
Недостаточность гормона роста
Клиренс и средний терминальный период полувыведения соматотропина у взрослых и детей с дефицитом гормона роста аналогичны тем, которые наблюдаются у здоровых лиц.
Дети и взрослые с хронической почечной недостаточностью и терминальной стадией заболеваний почек, как правило, имеют сниженный клиренс по сравнению со здоровыми субъектами. Выработка эндогенного ГР также может повыситься у некоторых пациентов с терминальной стадией заболеваний почек. Однако кумуляция соматропина у детей с хронической почечной недостаточностью и терминальной стадией заболеваний почек, получавших дозировку по предписанной схеме, не отмечалась.
Имеется ограниченное число публикаций о том, что абсорбция, период полувыведения и время достижения максимальной концентрации экзогенно вводимого соматропина у пациентов с синдромом Шерешевского-Тернера аналогичны тем, которые наблюдаются у здоровых людей и у пациентов с дефицитом ГР.
У пациентов с тяжелой дисфункцией печени было отмечено снижение клиренса соматропина. Клиническое значение этого снижения неизвестно.
Исследований с НутропиномAq по фармакокинетике в зависимости от пола не проводилось. Доступные литературные данные указывают, что фармакокинетика одинакова у мужчин и женщин.
Фармакодинамика
Соматропин является человеческим гормоном роста, продуцируемым клетками Escherichia coli по технологии рекомбинантной ДНК.
Соматропин стимулирует темпы роста и увеличивает конечный рост у детей с недостаточностью эндогенного ГР и у детей с низкорослостью вследствие синдрома Шерешевского-Тернера или ХПН. Лечение недостаточности ГР у взрослых с приводит к уменьшению массы жировой ткани, увеличению мышечной массы и повышению минеральной плотности позвоночника. Метаболические изменения у этих пациентов включают нормализацию уровня инсулиноподобного фактора роста-1 (ИФР-1) в сыворотке крови.
Доклинические и клинические тесты in vitro и in vivo продемонстрировали, что соматропин терапевтически эквивалентен человеческому ГР гипофизарного происхождения.
Действия, продемонстрированные для человеческого ГР, включают:
1. Рост скелета: ГР и его медиатор ИФР-1 стимулируют скелетный рост у детей с недостаточностью ГР путем воздействия на эпифизарные зоны длинных трубчатых костей. Это приводит к заметному увеличению длины тела до закрытия эпифизарных зон в конце периода полового созревания.
2. Рост клеток: лечение соматропином приводит к увеличению как количества, так и размера клеток скелетных мышц.
3. Рост органов: ГР увеличивает размеры внутренних органов, включая почки, и увеличивает массу эритроцитов.
Линейному росту отчасти способствует стимулируемый ГР синтез белков. Это подтверждается задержкой азота, о чем свидетельствует снижение экскреции азота с мочой и снижение азота мочевины крови во время лечения препаратом ГР.
Пациенты с неадекватной секрецией ГР иногда испытывают гипогликемию натощак, что улучшается при лечении соматропином. Лечение ГР может уменьшить чувствительность к инсулину и нарушить толерантность к глюкозе.
Соматропин вызывает задержку натрия, калия и фосфора. Концентрация неорганического фосфора в сыворотке крови увеличена у пациентов с недостаточностью ГР после терапии НутропиномAq из-за метаболической активности, связанной с ростом костей, и увеличения реабсорбции в почечных канальцах. Соматропин не оказывает значительного влияния на уровень кальция в сыворотке крови. У взрослых с дефицитом ГР наблюдается низкая минеральная плотность костной ткани, а у пациентов, получавших НутропинAq® с детского возраста, было показано увеличение минеральной плотности костей позвоночника в зависимости от дозы.
Соматропин стимулирует синтез хондроитинсульфата и коллагена, а так же выделение гидроксипролина с мочой.
Композиционный состав тела:
У взрослых пациентов с недостаточностью ГР, получавших лечение соматропином в средней дозе по 0.014 мг/кг массы тела ежедневно, наблюдалось уменьшение массы жировой ткани и увеличение мышечной массы. Данные изменения отмечаются наряду с повышением общего количества воды в организме и увеличением костной массы. Таким образом, полным эффектом лечения соматропином является изменение состава тела, сохраняющееся при продолжении лечения.
Показания к применению
длительное лечение детей с задержкой роста вследствие недостаточной эндогенной секреции гормона роста
длительное лечение низкорослости у девочек с синдромом Шерешевского-Тернера в возрасте старше 2-х лет
лечение детей препубертатного возраста с низкорослостью, обусловленной хронической почечной недостаточностью, до момента трансплантации почки
заместительная терапия у взрослых с недостаточностью эндогенного гормона роста, возникшей в детском или зрелом возрасте.
Недостаточность гормона роста должна быть подтверждена соответствующим образом до начала лечения.
У взрослых с недостаточностью гормона роста диагноз должен быть установлен в зависимости от этиологии:
Начало в зрелом возрасте: У пациента должны быть дефицит ГР в результате заболевания гипоталамуса или гипофиза, и диагностированный дефицит, по меньшей мере, одного другого гипофизарного гормона (за исключением пролактина). Тест на дефицит ГР не должен проводиться до проведения адекватной заместительной терапии дефицита других гормонов.
Начало в детском возрасте: Пациенты, страдавшие недостаточностью ГР в детстве, должны быть повторно обследованы для подтверждения наличия дефицита ГР до начала заместительной терапии НутропиномAq.
Способ применения и дозы
Диагностику и лечение соматропином должны проводить и контролировать врачи, имеющие соответствующую квалификацию и опыт в диагностике и наблюдении за пациентами, имеющими показания к лечению соматропином.
Дозировка и режим применения НутропинаAq устанавливаются индивидуально для каждого пациента.
Задержка роста у детей вследствие недостаточной эндогенной секреции гормона роста: 0,025-0,035 мг/кг массы тела в виде ежедневных подкожных инъекций. Лечение следует продолжать до закрытия эпифизарных зон роста.
Задержка роста при синдроме Шерешевского-Тернера: до 0,05 мг/кг массы тела в виде ежедневных подкожных инъекций. Лечение следует продолжать до закрытия эпифизарных зон роста.
Задержка роста при хронической почечной недостаточности: до 0,05 мг/кг массы тела в виде ежедневных подкожных инъекций. Лечение следует продолжать до закрытия эпифизарных зон роста или до момента пересадки почки.
Инструкция по введению препарата:
Раствор для инъекций должен вводиться подкожно, ежедневно. Следует менять места инъекций.
НутропинAq® выпускается в виде стерильного раствора с консервантом для многократного использования. Раствор должен быть прозрачным сразу после извлечения препарата из холодильника. В случае наличия мутности раствор не должен вводиться. Перемешивайте осторожно. Раствор нельзя сильно взбалтывать, чтобы не вызвать денатурацию белка.
НутропинAq® можно вводить только при помощи шприц-ручки NutropinAq® Pen.
Протрите резиновую пробку картриджа медицинским спиртом или раствором антисептика, чтобы предотвратить загрязнение содержимого микроорганизмами, которые могут проникнуть внутрь картриджа при повторных введениях иглы. Рекомендуется вводить НутропинAq® с помощью стерильных одноразовых игл.
Шприц-ручка NutropinAq® Pen предназначена для введения от минимальной дозы 0,1 мг до максимальной дозы 4,0 мг с пошаговым увеличением в 0,1 мг. Картридж, находящийся в шприц-ручке NutropinAq® Pen, не должен выниматься между инъекциями.
Побочные действия
Данные о побочных эффектах как у взрослых, так и у детей, получавших НутропинAq®, перечисленных в таблице ниже, основаны на данных клинических исследований по всем утвержденным показаниям (642 пациента) и постмаркетинговых наблюдений (Национальное Кооперативное Исследование Роста, НКИР, 35 344 пациента). Около 2.5 % пациентов из НКИР испытывали нежелательные реакции, связанные с применением препарата.
Во время клинических исследований наиболее часто сообщалось о следующих побочных реакциях: гипотиреоз, нарушение толерантности к глюкозе, головная боль, гипертония, боль в суставах, боль в мышцах, периферические отеки, отек, астения, реакции в месте инъекции и наличие лекарственных специфических антител.
Наиболее серьезными побочными реакциями во время клинических исследований были новообразования и внутричерепная гипертензия. Новообразования (доброкачественные и злокачественные) были зарегистрированы как в ключевых, так и во вспомогательных клинических исследованиях и при постмаркетинговом наблюдении. Большинство новообразований были рецидивами прежних новообразований и вторыми новообразованиями.
В постмаркетинговом наблюдении сообщалось о внутричерепной гипертензии. Это, как правило, сопровождалось отеком диска зрительного нерва, изменениями зрения, головной болью, тошнотой и/или рвотой; эти симптомы обычно встречаются в течение восьми недель от начала терапии препаратом НутропинAq®.
НутропинAq® снижает чувствительность к инсулину. О нарушении толерантности к глюкозе сообщалось во время клинических исследований и в постмаркетинговом наблюдении. О случаях сахарного диабета и гипергликемии сообщалось в обзоре постмаркетингового наблюдения.
О реакциях в месте инъекции, таких как кровотечение, атрофия, крапивница и зуд сообщалось в клинических испытаниях и/или в обзоре постмаркетингового наблюдения. Этих событий можно избежать при правильной технике инъекции и изменении мест инъекций.
У небольшой части пациентов могут появиться антитела к белку соматропину. Связывающая способность антител к гормону роста у пациентов, получавших НутропинAq®, была менее 2 мг/л, что не оказывало отрицательного влияния на динамику роста.



