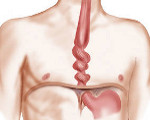
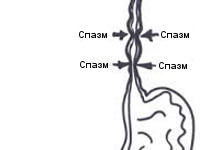
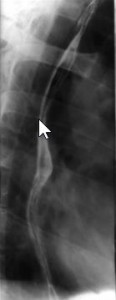
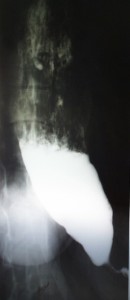
Спазм пищевода
Общие сведения
Спазм пищевода – эпизодические функциональные расстройства эзофагеальной перистальтики, сопровождающиеся спазмированием стенок пищевода. Данная патология занимает первое место среди всех заболеваний пищевода. Является наиболее частой причиной дисфагии с загрудинными болями. Болеют чаще женщины в возрасте 30-70 лет, с возрастом уровень заболеваемости растет, а половые различия сглаживаются. Диффузный эзофагоспазм выявляется у 3% пациентов, которым проводят эндоскопическое исследование в связи с патологией пищеварительного тракта. Тем не менее, скудость клинической картины часто приводит к тому, что пациенты не обращаются за медицинской помощью. Кроме того, спазм пищевода нередко принимают за гастроэзофагеальную рефлюксную болезнь. Диагностикой и лечением заболевания занимаются врачи-эндоскописты, гастроэнтерологи, хирурги.
Причины
Точные причины возникновения спазма пищевода неизвестны. Первичный спазм пищевода является самостоятельным заболеванием, которое развивается на фоне психических (стрессы) и неврологических (поражение межмышечных нервных волокон пищевода) расстройств. Поражение нейронов может быть обусловлено воздействием токсинов, бактерий и вирусов как на сами нервные волокна в пищеводе, так и на головной мозг (менингоэнцефалит). Чаще всего спазм возникает в самых проксимальных и дистальных отделах пищевода, так как они имеют наиболее богатую иннервацию.
Некоторые исследователи в области гастроэнтерологии предполагают связь спазма пищевода с дефицитом окиси азота, которая нужна для передачи информации в нейросинапсах. Патогенез данного заболевания схож с ахалазией кардии; более того – при прогрессировании двигательных расстройств возможен переход диффузного спазма в ахалазию (эта патология характеризуется повышением тонуса нижнего эзофагеального сфинктера, которое сопровождается нарушением его расслабления). Связано это с тем, что длительно существующие функциональные спазмы, особенно не подвергающиеся коррекции, приводят к формированию органических изменений в тканях (дегенерация миоцитов и нервных узлов, фиброз тканей и др.).
Вторичный спазм пищевода развивается на фоне другой патологии (эзофагит, язва либо рак пищевода) из-за рефлекторных реакций слизистой оболочки, чувствительность которой повышается по вине патологического процесса. Также возможно внезапное развитие спазма пищевода у здорового человека при глотании слишком больших порций пищи, употреблении очень горячей, холодной либо сухой еды, крепких алкогольных напитков, при поспешном питании.
Спазмы пищевода разделяют на легкие, непостоянные, острые либо хронические, локальные (поражаются сфинктеры пищевода) и диффузные (задействуется вся мышечная оболочка).
Симптомы спазма пищевода
Клиническая картина спазма пищевода зависит от локализации и формы патологического процесса. Наиболее типичными признаками любой из форм заболевания являются загрудинные боли и нарушение глотания. Боль пациенты чаще всего связывают с глотанием пищи и слюны, хотя она может возникнуть и спонтанно. Стрессы приводят к усугублению боли. Возможна иррадиация болевых ощущений в лопатки, плечи, нижнюю челюсть, спину. Чаще всего приступ длится не более часа, хотя не исключается и более длительная его продолжительность. Обычно пациенты описывают свои ощущения как чувство давления за грудиной. На фоне приема спазмолитиков боль ослабевает или исчезает.
Дисфагия может развиться на фоне приема как твердой, так и жидкой пищи. Чаще всего она непостоянна и возникает одновременно с болью. Изжога беспокоит каждого пятого пациента, а срыгивание пищи отмечается только на фоне очень сильных спазмов или значительного скопления пищевых масс в пищеводе.
Спазмирование верхнего сужения пищевода (наиболее частая форма патологии) чаще всего возникает у пациентов, склонных к истерии, неврозам, перепадам настроения. Клинически проявляется давящей болью за грудиной, тошнотой, кашлем, покраснением лица, страхом и волнением. Спазм пищевода может возникать остро, либо его проявления нарастают постепенно, перемежаясь периодами ремиссии. Интермиттирующий характер патологии приводит к тому, что пациент становится беспокойным, питается нерегулярно, боится возврата симптомов, а это еще больше усугубляет патологические проявления спазма пищевода.
Хронический спазм в области верхнего сужения чаще всего развивается у пожилых пациентов с дефектами зубного ряда, нарушением жевания, склонных к проглатыванию больших непережеванных кусков пищи; особенно если в анамнезе имеются указания на острый спазм пищевода. В клинической картине преобладают неприятные ощущения за грудиной, затруднения при прохождении твердой пищи, необходимость запивать водой каждый глоток. Постоянная непроходимость пищевода приводит к формированию его компенсаторного расширения над спазмированным участком.
Спазм нижних отделов пищевода и кардии также может быть острым и хроническим. Острый спазм проявляется болями в эпигастрии и за грудиной, ощущением задержки пищевых масс над желудком; запивание пищи водой не приносит облегчения. Отдельно рассматривается несфинктерный спазм пищевода (синдром Баршоня-Тешендорфа), при котором одновременно поражается несколько отделов органа на всем протяжении. Пациенты предъявляют жалобы на эпизодические эпизоды дисфагии (от пары минут до нескольких недель), сопровождающиеся загрудинной болью, срыгиванием слизи. Патология часто возникает на фоне язвенной, желчнокаменной болезни; для нее характерно повышение аппетита.
Диагностика спазма пищевода
Постановка диагноза «спазм пищевода» требует исключения органических и механических причин патологии. К наиболее достоверным методам диагностики относят рентгенографию пищевода, эзофагеальную манометрию и эндоскопическое исследование.
Примерно у половины пациентов рентгенологическое исследование не выявляет признаков патологии. На эзофагоспазм указывают некоординированные спастические сокращения мышц пищевода, из-за чего орган приобретает вид штопора, четок, псевдодивертикулов. Контрастная эзофагография при спазме верхнего сужения пищевода демонстрирует задержку контраста на уровне перстневидного хряща. При хроническом спазме контраст скапливается в области супрастенотического расширения. Для синдрома Баршоня-Тешендорфа характерно выявление кольцевидных спазмированных участков на всем протяжении пищевода. От ахалазии кардии спазм пищевода отличается нормальным прохождением контраста через нижний пищеводный сфинктер.
ЭГДС при спазме пищевода имеет меньшее диагностическое значение, чаще применяется для дифференциального диагноза. Эзофагоскопия при спазме верхнего сужения затруднена, обычно ввести фиброскоп в просвет пищевода удается только после тщательной инфильтративной анестезии слизистой оболочки. При наличии хронического спазма слизистая оболочка гиперемирована, возможно выявление рубцовых стриктур и деформаций. При спазме нижнего отдела пищевода проведение фиброскопа в желудок затруднено из-за скопившихся пищевых масс, слизистая оболочка не изменена.
Результат эзофагеальной манометрии у части больных может не отличаться от нормы. У остальных пациентов могут обнаружиться спастические волнообразные сокращения мышц пищевода с повышением давления в нем более 30 мм.рт.ст., перемежающиеся с нормальной пищеводной перистальтикой. Для дифференциации с ГЭРБ может назначаться внутрипищеводная рН-метрия.
Лечение спазма пищевода
Терапия спазма пищевода включает медикаментозные и немедикаментозные методы. Рекомендуется соблюдение строгого режима питания, употребление большого количества жидкости. Следует исключить из рациона слишком холодные и горячие блюда, алкоголь, грубую клетчатку, газированные напитки. Для предупреждения повышения уровня давления в брюшной полости пациенту нужно избегать переедания, наклонов туловища, подъема тяжестей.
Медикаментозное лечение включает в себя введение спазмолитиков и препаратов, нормализующих эзофагеальную перистальтику. С этой целью назначают нитраты, антихолинергические средства, блокаторы кальциевых каналов. Большинству пациентов рекомендуют принимать седативные препараты для предупреждения спазма пищевода.
Прогноз и профилактика
Спазм пищевода обычно ухудшает качество жизни больного даже при отсутствии тяжелых осложнений. Прогноз зависит от многих факторов: формы, локализации и степени тяжести заболевания, возраста пациента, длительности симптомов до момента обращения за медицинской помощью. Профилактика спазма пищевода вторична, заключается в лечении фоновых заболеваний, ежегодном эндоскопическом обследовании. Для предупреждения рецидивов рекомендуют санаторно-курортное лечение.
Что такое спазмы кардии
В чем отличие кардиоспазма от ахалазии кардии?
При КАРДИОСПАЗМЕ основным является повышенный тонус нижнего пищеводного сфинктера, при этом заболевании давление в этой зоне в несколько раз превышает норму. При АХАЛАЗИИ КАРДИИ давление нижнего пищеводного сфинктера повышается не столь значимо, основной проблемой является нарушение своевременного расслабления этой зоны при прохождении пищевого комка.
Как проявляются кардиоспазм и ахалазия кардии?
Основной жалобой является ощущение задержки пищи за грудиной, возникающее после проглатывания (ДИСФАГИЯ). Жалобы могут развиваться медленно, либо возникать внезапно, чаще на фоне стресса. Больные могут отмечать, что жидкая пища проходит хуже, чем твердая («парадоксальная» ДИСФАГИЯ). Пациенты часто прибегают к различным приемам для улучшения прохождения пищи (встают во время еды, запивают пищу водой, меняют положение тела). Типичными симптомами являются отрыжка и срыгивание непереваренной пищей, слюной, чаще в ночное время (симптом «мокрой подушки»), а также боли за грудиной во время и после еды, которые могут отдавать в спину, под лопатку, в шею.
У кого возникает кардиоспазм и ахалазия кардии?
Заболевание может возникать в любом возрасте, наиболее часто в 20-40 лет, как у мужчин, так и у женщин. Нередко заболевание возникает на фоне стресса и в дальнейшем стрессовые ситуации приводят к обострениям заболевания.
Как развивается заболевание?
Как выявляется кардиоспазм и ахалазия кардии?
Очень типичной является рентгенологическая картина заболевания. Этот широкодоступный метод является основным при постановке диагноза. Важным дополнением служит эндоскопическое исследование, а также ЗЗОФАГОМАНОМЕТРИЯ – исследование, направленное на измерение давления в пищеводе и в нижнем пищеводном сфинктере.
Пищевод нормального диаметра (по стрелке) при рентгенологическом исследовании.
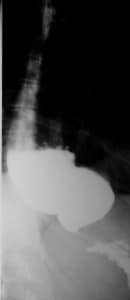
Кардиоспазм 3 и 4 стадии (пищевод заполнен контрастным веществом)
Обязательно ли выполнять эндоскопическое исследование больным с кардиоспазмом и ахалазией кардии?
Эндоскопическое исследование пищевода у больных с КАРДИОСПАЗМОМ И АХАЛАЗИЕЙ КАРДИИ обязательно, так как схожая симптоматика может быть у больных со злокачественной опухолью пищеводно-желудочного перехода.
Чем опасны кардиоспазм и ахалазия кардии?
Опасность КАРДИОСПАЗМА И АХАЛАЗИИ КАРДИИ не только в затруднениях в питании. Для этих больных нередки серьезные осложнения со стороны легких и верхних дыхательных путей, связанные с риском попадания в них скопившихся в пищеводе пищевых масс. Зачастую это происходит ночью, во сне, во время срыгивания содержимого пищевода (аспирация). Как следствие, у больных развиваются такие заболевания как хронический бронхит, бронхиальная астма и, даже, пневмония. Особенно часто эти осложнения встречаются у больных со значительным расширением пищевода, вот почему так важно своевременное лечение, на ранних стадиях заболевания.
Есть ли методы медикаментозного лечения кардиоспазма и ахалазии кардии?
Возможности консервативного лечения КАРДИОСПАЗМА И АХАЛАЗИИ КАРДИИ очень ограничены. Лишь на ранних стадиях, при незначительном расширении просвета пищевода возможен эффект от приема лекарственных средств (спазмолитики, нитраты, обезболивающие и седативные препараты растительного происхождения). К сожалению, эффект от приема этих препаратов кратковременный и проявляется он только у 10% больных.
Эффективен ли способ лечения кардиоспазма и ахалазии кардии с использованием ботулотоксина (ботокса)?
Введение ботулотоксина в мышцу пищевода с последующим ее параличом позволяет добиться хороших результатов у половины больных с ранними стадиями КАРДИОСПАЗМА И АХАЛАЗИИ КАРДИИ. Эффект введение ботокса временный, спустя несколько месяцев его приходится повторять. У больных со значительным расширением пищевода этот вариант лечения неэффективен.
Место кардиодилатаций в лечении больных с кардиоспазмом и ахалазией кардии?
Как выполняется кардиодилатация при кардиоспазме и ахалазии кардии, нужна ли специальная подготовка?
На ранних стадиях заболевания эта процедура не требует специальной подготовки. Достаточно прийти в клинику натощак. Больным со значительным расширением пищевода и длительной задержкой пищи в нем показано промывание пищевода для эвакуации содержимого. Кардиодилатации при АХАЛАЗИИ КАРДИИ И КАРДИОСПАЗМЕ выполняются, как правило, амбулаторно и не требует анестезии. Суть манипуляции заключается в установке в области нижнего пищеводного сфинктера латексного баллона с его последующим контролируемым раздуванием. Для точного позиционирования баллона его устанавливают под строгим контролем рентгеноскопии или эндоскопии. Баллон соединен с манометром, степень его раздувания во время процедуры четко контролируется. Сеанс продолжается несколько минут, после чего баллон сдувается и извлекается из пищевода. Курс лечения состоит из нескольких процедур (обычно 2-4 дилатаций), которые выполняются через 1 – 2 дня.
Баллонный дилататор
Какие ощущения испытывает больной во время кардиодилатации и после нее?
Во время процедуры могут быть очень непродолжительные и не интенсивные болевые ощущения за грудиной, проходящие после ее завершения. Эти ощущения могут сохраняться в течение нескольких часов или суток после процедуры, после чего полностью проходят.
Какие рекомендации следует соблюдать после дилатации?
Стандартной рекомендацией является ограничение приема пищи и воды в течение 2 — 3 часов после манипуляции и твердой пищи в течение суток.
Какова эффективность кардиодилатаций?
Кардиодилатации — высокоэффективный метод лечения КАРДИОСПАЗМА И АХАЛАЗИИ КАРДИИ, во многих случаях больные на многие годы избавляются от неприятных ощущений. Тем не менее, рецидивы возможны, чаще всего на фоне стресса. В этом случае, как правило, достаточно повторного курса дилатаций с таким же хорошим и стойким эффектом.
Когда возникают показания к хирургическому лечению кардиоспазма и ахалазии кардии?
Основными показаниями к выполнению хирургических вмешательств у больных с КАРДИОСПАЗМОМ И АХАЛАЗИЕЙ КАРДИИ является неэффективность иных способов лечения заболевания. Как правило, операция требуется больным с выраженным расширением пищевода и нарушением его двигательной активности, то есть в случаях длительной истории болезни и отсутствии своевременного лечения.
Виды операций у больных с кардиоспазмом и ахалазией кардии?
Гипермоторная дискинезия, как лечить спазм пищевода, кардиоспазм на нервной почве?
Что такое спазм пищевода, эзофагоспазм, кардиоспазм?
По сравнению с заболеваниями желудка и кишечника заболевания пищевода встречаются редко. У здорового человека пища в пищеводе не задерживается, и поэтому пищевод меньше подвергается различным раздражениям. Из болезней пищевода наиболее часто встречаются эзофагоспазмы, воспаление (эзофагиты, эзофагит), иногда с последующим сужением, и рак пищевода.
Причины спазма пищевода
Спазм пищевода: классификация, виды
Гастроэнтерологи и рефлексотерапевты Саратова подразделяют спазм пищевода на 2 вида.
1. Диффузный спазм пищевода, характеризующийся нескоординированными сокращениями пищевода по всей его протяженности (при нем наблюдается дисфагия);
2. Сегментарный спазм пищевода, характеризующийся сокращениями пищевода на определенном участке с чрезмерной амплитудой (при данном виде пища проходит, но человек испытывает боль, при этом происходит деформация пищевода).
Почему происходит спазм пищевода? Патогенез
Часто спазм пищевода происходит из-за нарушения двигательной функции на фоне неврастении, депрессии, стрессовых ситуаций, переживаний, волнений, у пациентов с нарушениями психики органического и функционального характера, а также когда спастические сокращения стенки пищевода возникают в результате патологических висцеро-висцеральных рефлексов со слизистой оболочки пищевода при ее повышенной чувствительности из-за патологического процесса (эзофагит, язва, рак).
Спастические сокращения пищевода возможны у здоровых людей при быстрой еде, проглатывании большого куска непрожеванной пищи, при употреблении острой, сухой или слишком горячей пищи.
Основными патогенетическими факторами в развитии спазма пищевода являются дистрофические изменения межмышечного нервного сплетения пищевода, не исключая действие NO-эргических рецепторов.
Спазм пищевода, кардиоспазм: симптомы, признаки
Чаще наблюдается интенсивная боль, которая локализуется в области грудины или в эпигастральной области. Боль иррадиирует по передней поверхности грудной клетки вверх до шеи, в плечи, в нижнюю челюсть. Боль начинается спонтанно, а также при проглатывании слюны или пищи, может длиться несколько часов или внезапно прекратиться от проглатывания глотка теплой жидкости. Периодичность появления болей различная: иногда спазмы пищевода появляются несколько раз во время приема пищи, а в других случаях – несколько раз в месяц. Часто наблюдаются случаи развития спазма пищевода в момент сильных переживаний, волнений, нервно-психических стрессов. Иногда загрудинная боль при эзофагоспазме напоминает боль при приступах стенокардии. Может наблюдаться парадоксальная дисфагия, при которой твердая пища проходит лучше, чем жидкая. В конце приступа нередко возможно срыгивание небольшим количеством слизи.
Спазм пищевода может продолжаться от нескольких секунд до многих часов. В некоторых случаях выше спастического сокращения развивается дилятация пищевода. При кардиоспазме иногда наблюдается дилятация (расширение) всего пищевода, которая может сопровождаться рвотой съеденной пищи. Так называемая пищеводная рвота отличается от желудочной тем, что наступает вскоре после еды, и рвотные массы состоят из только что съеденной пищи и не содержат желудочного сока (пепсина и соляной кислоты). Под влиянием тех или иных жизненных условий спазмы пищевода могут периодически повторяться.
Лечение спазма пищевода в Саратове, России, лечение эзофагоспазма
Как лечить спазм пищевода, как вылечить эзофагоспазм в Саратове, в России
Как снять спазм пищевода, как снять эзофагоспазм в Саратове, в России
Запись на консультации.
Имеются противопоказания. Необходима консультация специалиста.
Ахалазия кардии и кардиоспазм
Общая информация
Краткое описание
Этиология и патогенез
Несмотря на многовековую историю изучения ахалазии кардии, ее этиология до сих пор неизвестна. В настоящее время рассматриваются три основные гипотезы: генетическая, аутоиммунная и инфекционная.
Кроме NO, нейротрансмиттером тормозящих нейронов является ВИП. Один из его рецепторов — рецептор 1, который принадлежит к семейству секретиновых и экспрессируется различными иммунными клетками, такими как Т-лимфоциты, макрофаги и дендритные клетки. Полиморфизм этого гена (VIPR1) также может играть роль в развитии идиопатической ахалазии. VIPR1 локализуется в хромосоме 3p22. В некоторых исследованиях были установлены пять его простых нуклеотидных полиморфизмов: (rs421558) Intron‑1, (rs437876) Intron‑4, (rs417387) Intron‑6, rs896 и rs9677 (3’UTR).
Рассматривая аутоиммунную природу заболевания, необходимо напомнить о циркулирующих аутоантителах. У пациентов с ахалазией кардии чаще всего обнаруживают следующие нейрональные аутоантитела: антитела к никотиновым рецепторам ацетилхолина — ганглионарного и мышечного типа, к кальциевым каналам — P/Q- и N-типа, к декарбоксилазе глутаминовой кислоты, к скелетным мышцам и антинейрональные нуклеарные антитела, известные также под названием anti-Hu. Так, в одном из последних крупных исследований, проведенном в клинике Mayo, установлено, что у 26% больных с идиопатической ахалазией кардии выявляют антитела к скелетным мышцам, а у 21% — к декарбоксилазе глутаминовой кислоты.
Эпидемиология
Клиническая картина
Cимптомы, течение
Основные симптомы заболевания — прогрессирующая дисфагия, регургитация и загрудинные боли, связанные с неполным опорожнением пищевода и хроническим эзофагитом [21, 22, 30, 34, 35, 45, 71 и др.].
Пациент может самостоятельно уменьшить выраженность дисфагии, используя различные приемы: запивание пищи большим количеством жидкости, заглатывание воздуха, повторные глотательные движения, ходьба. Немаловажное значение имеет и температура принимаемой пищи: большинство больных отмечают, что лучше проходит теплая и горячая пища.
Ярким симптомом заболевания является активная и пассивная регургитация, которая отмечается у 84 и 68% больных соответственно. Активная регургитация представляет собой срыгивание только что съеденной пищи или слизи и более характерна для начальных стадий болезни. Она возникает при незначительной дилатации пищевода, тогда как значительное расширение пищевода может привести к отсроченной регургитации, объем которой значительно больше. Пассивная регургитация возникает вне приема пищи, обычно в горизонтальном положении пациента или при наклоне туловища вперед, чаще наблюдается при ахалазии кардии. Регургитация, особенно пассивная, может сопровождаться аспирацией пищи в дыхательные пути, которая может привести к нарушению функции органов дыхания, сопровождающемуся одышкой и кашлем, и маскировать основное заболевание. Необходимо отметить, что ночной кашель наряду с симптомом «мокрой подушки» свидетельствуют о декомпенсации заболевания и служат абсолютным показанием к проведению пневмокардиодилатации.
Еще одна характерная жалоба больных — боли в груди, которые наблюдаются примерно у 59% из них, чаще в молодом возрасте. При повышении давления в НПС и грудном отделе пищевода возникает интенсивная спастическая загрудинная боль, тогда как при атонии грудного отдела пищевода отмечаются умеренно выраженные боли за грудиной распирающего характера. Боли могут возникать во время приема пищи вследствие перерастяжения стенок пищевода и проходить после срыгивания или «проваливания» пищи в желудок. Они также могут быть вызваны спазмом гладкой мускулатуры пищевода и возникать как во время приема пищи, так и без четкой связи с ним. Для 1/3 больных с ахалазией кардии характерна жгучая боль по ходу пищевода, возникающая вследствие прямого раздражающего действия на пищевод остатков задержавшихся в нем пищи и лактата, продукция которого повышена при избыточной бактериальной ферментации сохраняющихся в пищеводе углеводов.
Диагностика
Для подтверждения диагноза идиопатической ахалазии необходимо использовать инструментальные методы обследования, такие как рентгенография пищевода с контрастированием, ЭГДС и манометрия, которая признана «золотым стандартом» диагностики. Некоторые авторы рекомендуют перед проведением рентгеноконтрастного исследования выполнить обзорную рентгенографию грудной клетки, по результатам которой можно определить наличие уровня жидкости в средостении, обусловленного застоем пищевых масс в пищеводе, а также выявить расширение средостения и отсутствие газового пузыря желудка. Рентгеноконтрастное исследование выполняют с бариевой взвесью, при этом оценивают степень расширения пищевода, его деформацию (S-образный пищевод), длительность задержки контрастной массы в пищеводе, рельеф абдоминального отдела пищевода и области пищеводно-желудочного перехода в момент открытия кардиоэзофагеального сфинктера, наличие или отсутствие газового пузыря желудка и некоторые другие параметры (рис. 1).
При II стадии определяется умеренное (до 3–4 см) расширение просвета пищевода; остатков пищи в пищеводе, как правило, нет, может быть небольшое количество прозрачной жидкости или слизи; слизистая оболочка гладкая, ровная, блестящая, ее складки расположены продольно; перистальтика усилена; кардия расположена по центру, обычно плотно сомкнута, но достаточно легко раскрывается при избыточной (по сравнению с обычным эндоскопическим исследованием) инсуффляции воздуха (рис. 2). При ретроградном осмотре складки в области пищеводно-желудочного перехода плотно обхватывают эндоскоп, слизистая оболочка мягкая, эластичная.

Как правило, каждой клинико-рентгенологической стадии кардиоспазма и ахалазии кардии соответствует определенная эндоскопическая картина, на основании которой стадия болезни может быть установлена и без предшествующего рентгенологического исследования, если оно не может быть выполнено по каким-либо причинам (рис. 3–5).
Рис. 3. Кардиоспазм II стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»).
Рис. 4. Кардиоспазм III стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»)
«Золотым стандартом» обследования пациентов при подозрении на ахалазию кардии является манометрия. В настоящее время для исследования двигательной функции пищевода можно использовать как метод открытых катетеров (водно-перфузионная манометрия), так и современные высокотехнологичные методы — манометрию высокой разрешающей способности (high resolution manometry — HRM) и объемную 3D-манометрию, которые имеют явные преимущества по сравнению с манометрией, выполняемой с помощью 4- или 8-канального водно-перфузионного катетера. При расположении датчиков давления на расстоянии 5 см друг от друга большие участки перистальтической волны грудного отдела пищевода «выпадают» из анализа. Так, подтягивание НПС и укорочение грудного отдела пищевода у больных с ахалазией кардии часто принимают за истинное, хотя и недостаточное, расслабление сфинктера («псевдорелаксация»). Использование многоканальных катетеров при манометрии высокой разрешающей способности позволяет избежать подобных ошибок (рис. 6).
При анализе результатов обследования пациентов с ахалазией кардии, проведенного с использованием манометрии высокого разрешения, следует учитывать Чикагскую классификацию нарушений моторики пищевода, созданную в 2008 г. Применение этого метода исследования позволило выделить три типа ахалазии кардии в зависимости от выявленных изменений двигательной активности грудного отдела пищевода, что дает возможность более точно прогнозировать эффективность лечения с помощью пневмокардиодилатации (рис. 7).
Дифференциальный диагноз
– кардиоэзофагеальным раком, для которого характерна прогрессирующая дисфагия, как и для истинной ахалазии. Однако быстрое уменьшение массы тела, короткий анамнез, часто пожилой возраст пациентов к моменту появления дисфагии свидетельствуют о злокачественном поражении. При физикальном осмотре можно выявить пальпируемое образование в брюшной полости и лимфаденопатию. При рентгенологическом исследовании с бариевой взвесью просвет пищевода может быть умеренно дилатирован, но степень расширения не коррелирует с выраженностью дисфагии. В дистальном отделе имеется сужение, но в отличие от такового при ахалазии оно не имеет характерного вида птичьего клюва или мышиного хвостика с постепенным симметричным сужением просвета и гладкими стенками, а чаще эксцентрично, с обрывом по типу ступеньки и неровными бугристыми контурами. Для установления точного диагноза необходимо проведение эзофагогастродуоденоскопии (ЭГДС). При малейшем подозрении на наличие злокачественного процесса в области кардии обязательным является получение материала для гистологического и цитологического исследований, поскольку рак развивается у 3–8% больных с ахалазией [30]. Необходимо помнить о возможности развития рака не только в области пищеводно-желудочного перехода, но и в стенке воспаленного расширенного пищевода;
– пептической стриктурой, являющейся осложнением длительно текущей гастроэзофагеальной рефлюксной болезни (ГЭРБ). Для нее также характерна дисфагия: в начальных стадиях отмечается затрудненное прохождение по пищеводу только твердой пищи, тогда как в более поздних стадиях присоединяется нарушение пассажа кашицеобразной пищи и жидкостей. Дисфагии, как правило, предшествует длительно существующая изжога, часто возникающая в ночное время, однако к моменту формирования стриктуры изжога прекращается. Для дифференциальной диагностики важно проведение манометрии и рентгенографии пищевода с контрастированием, результаты которого свидетельствуют об отсутствии значимого расширения просвета пищевода, а в вертикальном положении больного контрастное вещество (взвесь сульфата бария) в отличие от ахалазии кардии длительно в пищеводе не задерживается. При ЭГДС могут быть выявлены эрозии;
– ишемической болезни сердца (ИБС), основное клиническое проявление которой — боли в груди. Этот симптом практически невозможно отличить от такового при ахалазии кардии, особенно если ИБС провоцируется приемом пищи. Не помогает в плане дифференциальной диагностики и эффект от приема нитроглицерина, так как боли при ахалазии, как и при ИБС, купируются после его приема. ЭКГ также не всегда позволяет уточнить диагноз, так как ишемия миокарда очень часто имеет скрытый характер и выявляется лишь при физической нагрузке. В связи с этим в спорных ситуациях необходимо проводить комплексное кардиологическое обследование, включающее велоэргометрию или тредмил-тест, эхокардиографию и комбинированное исследование — суточное холтеровское мониторирование и 24-часовую pH-метрию;
Лечение
Существующие методы лечения кардиоспазма и ахалазии кардии (консервативные, эндоскопические, хирургические) направлены на расширение кардии тем или иным способом либо снижение ее тонуса, для того чтобы улучшить прохождение пищи через область пищеводно-желудочного перехода.
Пациентам с ахалазией кардии необходимо назначить диету по типу пищеводного стола с исключением острых и кислых продуктов; пища должна быть теплой, принимать ее нужно медленно, тщательно пережевывая. Оптимальным считается 4- или 5-разовое питание небольшими по объему порциями. Следует также отметить, что существует индивидуальный набор продуктов, усиливающих дисфагию у конкретных пациентов, которые целесообразно исключить из рациона. После приема пищи не следует принимать горизонтальное положение во избежание ее регургитации. Во время сна пациент не должен находиться в строго горизонтальном положении, так как пища может задерживаться в пищеводе до нескольких часов, а верхний пищеводный сфинктер расслабляется во время сна, что приводит к пассивной регургитации и возможной аспирации дыхательных путей.
Для консервативного лечения пациентов с ахалазией кардии используют две группы препаратов: блокаторы кальциевых каналов и нитраты. Чаще всего применяют нифедипин и изосорбида мононитрат в дозе 5–10 мг, которые следует принимать за 20—30 мин до приема пищи. Эти лекарственные средства снижают давление НПС в среднем на 47–63%, однако полностью купировать симптомы ахалазии удается редко. Необходимо также помнить о возможных побочных эффектах этих препаратов, из которых наиболее часто возникают головная боль, артериальная гипотензия, головокружение. В связи с этим лекарственную терапию применяют в случае невозможности использовать альтернативные методы при лечении пациентов, ожидающих выполнения пневмокардиодилатации или хирургического лечения, и как сопутствующую терапию у больных с ахалазией кардии, сопровождающейся рефрактерной болью в груди.
Процедура основана на расширении суженного участка пищеводно-желудочного перехода с помощью кардиодилататора, в результате чего снижается давление НПС и улучшается пассаж пищи по пищеводу. Для этого используют пневмодилататоры, смонтированные на желудочном зонде, которые имеют форму гантели для лучшей фиксации в зоне пищеводно-желудочного перехода (ЗАО «МедСил», Россия). Дилатацию выполняют под рентгенологическим контролем, однако в случаях выраженного расширения, удлинения и деформации пищевода, проявляющейся в значительном отклонении его от продольной оси (С- или S-образный пищевод), проведение пневмодилататора под рентгенологическим контролем затруднено или невозможно. Использование эндоскопической техники позволяет выполнить дилатацию под контролем зрения при заболевании в любой стадии, а также оценить состояние слизистой оболочки в зоне пищеводно-желудочного перехода непосредственно после окончания вмешательства и немедленно диагностировать возникшие осложнения. Эндоскопические вмешательства являются методом выбора при поздних стадиях кардиоспазма и ахалазии кардии у пациентов, у которых высок операционно-анестезиологический риск.
Лечебную процедуру выполняют с помощью кардиодилататора, который надевают на дистальную часть эндоскопа. Диаметр баллона для дилатации кардии в широкой части составляет 30 и 40 мм, в области «талии» — 25 и 30 мм, длина — 12–15 см. Баллон укреплен на полой трубке, внутренний диаметр которой соответствует наружному диаметру эндоскопа и составляет 9–10 мм, длина — 17–20 см. К проксимальному концу баллона присоединена трубка диаметром около 3 мм для инсуффляции воздуха или введения воды в баллон. «Талия» в средней части баллона облегчает его фиксацию в кардии.
Давление при кардиодилатации повышают постепенно — от 120–160 мм рт. ст. в начале лечения до 300–320 мм рт. ст. в конце курса. Экспозиция составляет 1–2 мин, для достижения эффекта требуется в среднем 4–5 сеансов. Уровень давления контролируют с помощью манометра.
Для проведения дилатации кардии применяют также дилататоры «Rigiflex» («Boston Scientific», MA, США), представляющие собой полиэтиленовые баллоны трех диаметров — 30, 35 и 40 мм. Аналогичные баллоны диаметром 30 и 35 мм производит фирма «Cook Medical» (США).
ПД можно проводить как под рентгенологическим контролем, так и с помощью эндоскопической техники по введенной в желудок через канал эндоскопа направляющей струне. Процедура заключается в установке баллона точно в месте перехода пищевода в желудок. При извитом пищеводе для правильного позиционирования баллона в кардии необходим визуальный контроль, для чего параллельно баллону вводят эндоскоп. Для предупреждения осложнений (перфорация, кровотечение) очень важно избегать форсированной дилатации и повышать давление в баллоне постепенно в течение нескольких сеансов от 160 до 300 мм рт. ст. в течение 40–60 с. Баллон может быть заполнен не только воздухом, но и жидкостью — водой или водорастворимым контрастным веществом для лучшей визуализации. Такая процедура называется гидродилатацией кардии, ее выполняют, как правило, при давлении 0,5–2 атм в течение 2 мин. Уровень давления контролируют с помощью манометра.
Эффективность терапии достаточно высокая, зависит от диаметра кардиодилататора и через 3 года составляет в среднем 74, 86 и 90% при использовании баллонов диаметром 30, 35 и 40 мм соответственно.
После дилатации и для мониторирования состояния после лечения, которое необходимо проводить 1 раз в год, жалобы пациентов могут быть оценены по шкале Eckardt.
Шкала Eckardt
| Симптомы | Баллы* | |||
| 0 | 1 | 2 | 3 | |
| Дисфагия | Никогда | Периодически | 1 раз в день | Каждый прием пищи |
| Регургитация | Никогда | Периодически | 1 раз в день | Каждый прием пищи |
| Боли в груди | Никогда | Периодически | 1 раз в день | Каждый прием пищи |
| Уменьшение массы тела, кг | Нет | 5–10 | >10 | |
* 0–3 балла — ремиссия, более 4 баллов — неэффективность ПД.
Кроме улучшения клинического течения заболевания, предиктором длительной ремиссии после ПД является давление НПС
На эффективность ПД оказывают положительное влияние ряд факторов, такие как возраст пациентов более 40 лет, II тип ахалазии кардии по данным HRM, начальная стадия заболевания, давление НПС 15 мм рт. ст. после ранее выполненной ПД, эвакуация из пищевода менее 50% бариевой взвеси через 1 мин от начала рентгеноскопии пищевода, однократно проведенная ПД с использованием баллона диаметром 30 мм.
Необходимо помнить, что самым тяжелым осложнением ПД, которое наблюдается в 1,5–3% случаев, является перфорация стенки пищевода. Однако использование современных дилататоров и опыт специалистов, выполняющих ПД, позволяют значительно снизить риск ее возникновения. После ПД могут отмечаться также боли в груди, повреждение слизистой оболочки пищевода и гематома, повышение температуры тела и аспирационная пневмония, однако риск их развития очень мал. Достаточно редко после процедуры развивается ГЭРБ.
Еще в 1994 г. в зарубежной литературе появились сообщения об использовании ботулинового токсина А для эндоскопического лечения кардиоспазма и ахалазии кардии [42, 43, 49, 60, 79 и др.]. Ботулиновый токсин оказывает расслабляющее действие на гладкую мускулатуру путем блокирования выброса медиатора парасимпатической нервной системы ацетилхолина холинергическими нейронами и нарушения нервно-мышечной передачи. При этом процесс синтеза и депонирования ацетилхолина в пресинаптической терминали синапса не нарушается [20, 55]. Введение ботулинового токсина А в зону кардии приводит к снижению базального и остаточного давления НПС.
Процедура основана на интрамуральном эндоскопическом введении ботулинового токсина А в НПС в дозе 80–100 ЕД, при этом 1 мл препарата (20–25 ЕД) вводят с помощью иглы диаметром 5 мм для склеротерапии в каждый из четырех квадрантов НПС под визуальным контролем.
Эффективность терапии составляет около 80% в течение 1-го месяца наблюдения, 70% после 3 мес, 50% через 6 мес и около 40% через 1 год, в связи с чем иногда требуется повторная инъекция ботулинового токсина.
Несмотря на безопасность и простоту выполнения, этот метод можно рассматривать в качестве альтернативного варианта только при лечении пациентов, имеющих абсолютные противопоказания к пневмокардиодилатации, эндоскопическому и оперативному вмешательству, особенно если речь идет о лицах старшей возрастной группы, наличии тяжелой сопутствующей патологии сердечно-сосудистой и бронхолегочной систем, а также при наличии S-образного пищевода [9].
К факторам, оказывающим негативное влияние на эффективность этого метода, относят: молодой возраст пациентов, мужской пол, высокое давление покоя НПС, отсутствие эффекта от предыдущих инъекций ботулинового токсина, а наиболее выраженный эффект от лечения можно ожидать у людей пожилого возраста и пациентов с ахалазией и выраженной гипермоторной дискинезией грудного отдела пищевода. Следует также отметить, что до настоящего времени в Российской Федерации препарат «Диспорт» не зарегистрирован в качестве средства для применения в гастроэнтерологии, его разрешено использовать лишь в неврологии и косметологии. Для лечения ахалазии кардии препарат применяют в Республике Татарстан по специальному разрешению Министерства здравоохранения этого субъекта РФ.
При неэффективности нехирургических методов лечения решают вопрос о необходимости выполнения оперативного вмешательства. Следует отметить, что выполняемая в ряде лечебных учреждений эзофагокардиомиотомия по Геллеру, заключающаяся в рассечении мышечной оболочки нижнего конца расширенного сегмента пищевода и кардиальной части желудка по передней и задней стенкам, у 15% больных осложняется развитием ГЭРБ. В связи с этим основным оперативным вмешательством является эзофагокардиомиотомия с неполной фундопликацией для предупреждения рефлюкса. Согласно отдаленным результатам, по эффективности она превосходит ПД, однако из-за травматичности любого оперативного вмешательства, необходимости анестезиологического пособия и вероятности развития послеоперационных осложнений этот метод лечения применяют при неэффективности повторных ПД.
В настоящее время для лечения кардиоспазма широко применяют лапаро- и торакоскопические операции, из которых предпочтение отдают лапароскопической миотомии с частичной фундопликацией в различных модификациях, обеспечивающей беспрепятственное прохождение пищи у пациентов с ослабленной моторикой пищевода, с одной стороны, и предупреждающей рефлюкс — с другой [1, 71, 92, 101 и др.]. Эффективность минимально инвазивных вмешательств не уступает таковой открытых хирургических операций — 94 и 84% соответственно, а частота послеоперационных осложнений ниже. К сожалению, после хирургического лечения также в ряде случаев возникает рецидив дисфагии, в связи с чем требуется повторное проведение консервативного, в том числе с использованием эндоскопических методов, или хирургического лечения.
В терминальной стадии заболевания выполняют экстирпацию или субтотальную резекцию пищевода с одномоментной пластикой желудочной трубкой, в том числе с применением лапарои торакоскопической техники. Показания к выбору метода оперативного вмешательства определяют индивидуально [1, 36 и др.].
В 2007 г. был предложен и апробирован на живых свиньях новый метод лечения ахалазии, заключающийся в обеспечении прямого доступа к мышечному слою пищевода через туннель, созданный в подслизистом слое (один из вариантов NOTES — внутрипросветной эндоскопической хирургии через естественные отверстия) [80]. У человека эта операция, получившая название «пероральная эндоскопическая миотомия» (POEM), впервые выполнена в 2008 г. [62]. С этого времени операцию стали быстро внедрять в клиническую практику, и к настоящему времени она выполнена уже нескольким сотням пациентов [52, 63, 86, 87, 96, 109, 111 и др.].
Авторы рассматривают эту методику в качестве альтернативы баллонной кардиодилатации и эзофагокардиомиотомии по Геллеру. Суть ее состоит в следующем: с помощью специальных инструментов, введенных по инструментальному каналу гибкого эндоскопа, делают продольный надрез слизистой оболочки пищевода на протяжении 1,5–3 см примерно на 10–12 см выше пищеводно-желудочного перехода, через который в подслизистый слой вводят эндоскоп. Вместо воздуха инсуффлируют углекислый газ для предупреждения развития пневмомедиастинума и пневмоперитонеума. Под визуальным контролем на всем протяжении вплоть до малой кривизны желудка как минимум на 3 см ниже пищеводно-желудочного перехода создают туннель между слизистой оболочкой и мышечным слоем путем последовательного пересечения соединительнотканных волокон и сосудов после порционного введения изотонического раствора натрия хлорида с добавлением, как правило, раствора высокой вязкости, чаще всего на основе глицерола и гиалуроновой кислоты, подкрашенного индигокармином или метиленовым синим для лучшей визуализации. Рассечение волокон выполняют специальными ножами различной формы разных производителей («Olympus», «Fujifilm», «ERBE» и др.). Затем постепенно рассекают циркулярные мышечные волокна в направлении сверху вниз. Дефект в слизистой оболочке клипируют.
POEM — эффективная и достаточно безопасная процедура. Исследователи сообщают об уменьшении выраженности симптомов дисфагии с 10 баллов до 1,3 балла, снижении давления НПС с 52,4 (14,2–80,5) до 19,8 (9,3–42,7) мм рт. ст. в течение в среднем 5 мес. При оценке жалоб пациентов по шкале Eckardt отмечается значительное улучшение состояния: если до операции средняя оценка составляла 7–8 баллов, то после нее у всех пациентов она была ниже 3 баллов, в основном 0–1 балл. Частота развития ГЭРБ варьирует, согласно данным разных авторов, от 0 до 37% [109].
Прогноз
Информация
Источники и литература
Информация
3 ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А. И. Евдокимова» Минздрава России, Москва, Российская Федерация