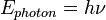Как сказал.
Информация в чистом виде ‒ это не знание. Настоящий источник знания ‒ это опыт.
Альберт Эйнштейн
Вопросы к экзамену
Для всех групп технического профиля

Я учу детей тому, как надо учиться
Часто сталкиваюсь с тем, что дети не верят в то, что могут учиться и научиться, считают, что учиться очень трудно.
Урок 52. Виды спектров. Различные виды электромагнитных излучений, их свойства.
Совокупность монохроматических компонент в излучении называется спектром.
Спектры излучения
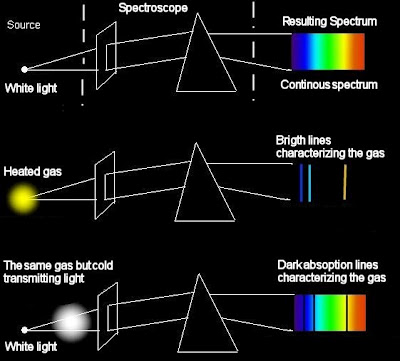
Спектральный состав излучения веществ весьма разнообразен. Но, несмотря на это, все спектры, как показывает опыт, можно разделить на три типа.
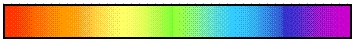
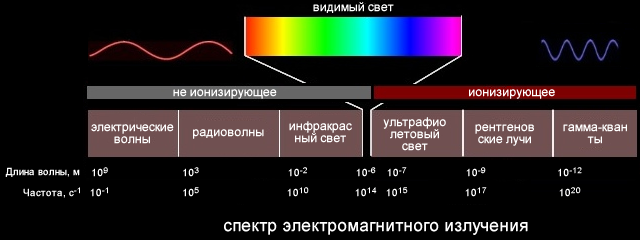
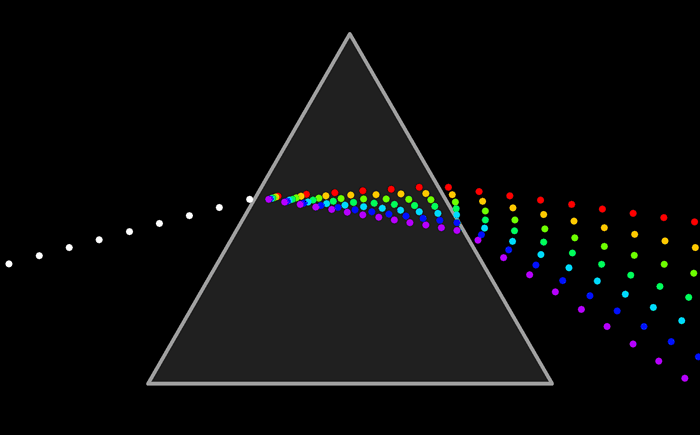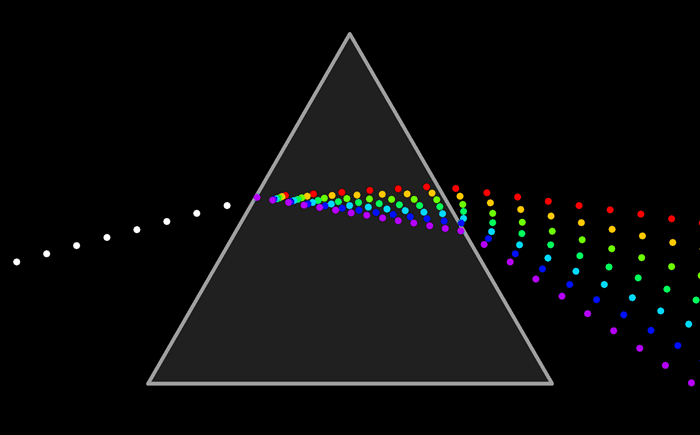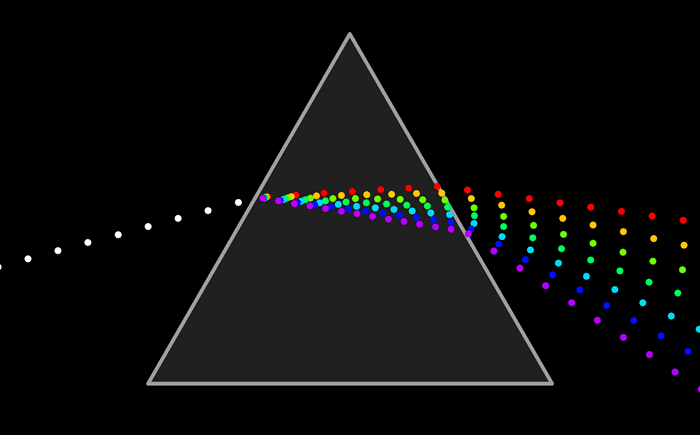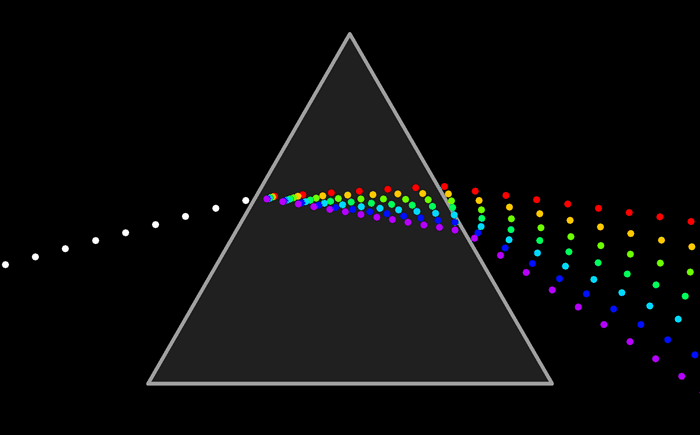
Непрерывные спектры
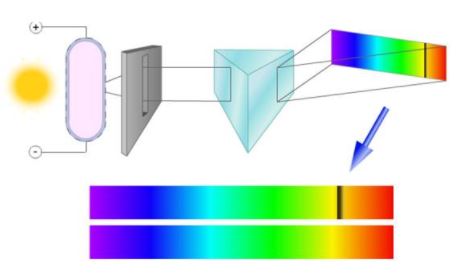
Непрерывный спектр представлет собой сплошную разноцветную полосу.
Белый свет имеет непрерывный спектр. Солнечный спектр или спектр дугового фонаря является непрерывным. Это означает, что в спектре представлены волны всех длин. В спектре нет разрывов, и на экране спектрографа можно видеть сплошную разноцветную полосу.
Непрерывные (или сплошные) спектры, как показывает опыт, дают тела, находящиеся в твердом или жидком состоянии, а также сильно сжатые газы. Для получения непрерывного спектра нужно нагреть тело до высокой температуры. Непрерывный спектр дает также высокотемпературная плазма. Электромагнитные волны излучаются плазмой в основном при столкновении электронов с ионами.
Характер непрерывного спектра и сам факт его существования определяются не только свойствами отдельных излучающих атомов, но и в сильной степени зависят от взаимодействия атомов друг с другом.
Излучение источников, в которых свет испускается атомами вещества, имеет дискретный спектр. Они делятся на:
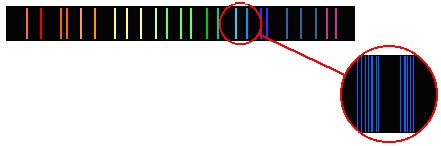
Линейчатые спектры
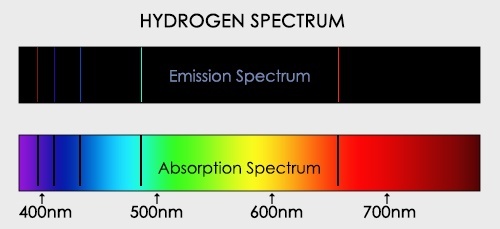
Линейчатый спектр состоит изотдельных цветных линий различной яркости, разделенных широкими темными полосами.
Внесем в бледное пламя газовой горелки кусочек асбеста, смоченного раствором обыкновенной поваренной соли. При наблюдении пламени в спектроскоп на фоне едва различимого непрерывного спектра пламени вспыхнет яркая желтая линия. Эту желтую линию дают пары натрия, которые образуются при расщеплении молекул поваренной соли в пламени. На рисунке приведены также спектры водорода и гелия. Такие спектры называются линейчатыми. Наличие линейчатого спектра означает, что вещество излучает свет только вполне определенных длин волн (точнее, в определенных очень узких спектральных интервалах).
Линейчатые спектры дают все вещества в газообразном атомарном (но не молекулярном) состоянии. В этом случае свет излучают атомы, которые практически не взаимодействуют друг с другом. Это самый фундаментальный, основной тип спектров.
Изолированные атомы излучают строго определенные длины волн.
Обычно для наблюдения линейчатых спектров используют свечение паров вещества в пламени или свечение газового разряда в трубке, наполненной исследуемым газом.
При увеличении плотности атомарного газа отдельные спектральные линии расширяются, и, наконец, при очень большом сжатии газа, когда взаимодействие атомов становится существенным, эти линии перекрывают друг друга, образуя непрерывный спектр.
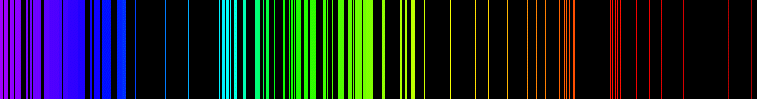
Полосатые спектры
Полосатый спектр состоит из отдельных полос, разделенных темными промежутками.
С помощью очень хорошего спектрального аппарата можно обнаружить, что каждая полоса представляет собой совокупность большого числа очень тесно расположенных линий. В отличие от линейчатых спектров полосатые спектры создаются не атомами, а молекулами, не связанными или слабо связанными друг с другом.
Для наблюдения молекулярных спектров так же, как и для наблюдения линейчатых спектров, обычно используют свечение паров в пламени или свечение газового разряда.
Спектры поглощения
Все вещества, атомы которых находятся в возбужденном состоянии, излучают световые волны, энергия которых определенным образом распределена по длинам волн. Поглощение света веществом также зависит от длины волны. Так, красное стекло пропускает волны, соответствующие красному свету, и поглощает все остальные.
Если пропускать белый свет сквозь холодный, неизлучающий газ, то на фоне непрерывного спектра источника появляются темные линии. Это будет спектр поглощения.
Спектр поглощения представляет собой темные линии на фоне непрерывного спектра источника.
Газ поглощает наиболее интенсивно свет как раз тех длин волн, которые он испускает в сильно нагретом состоянии. Темные линии на фоне непрерывного спектра — это линии поглощения, образующие в совокупности спектр поглощения.
Существуют непрерывные, линейчатые и полосатые спектры поглощения.
Различные виды электромагнитных излучений, их свойства и практические применения.
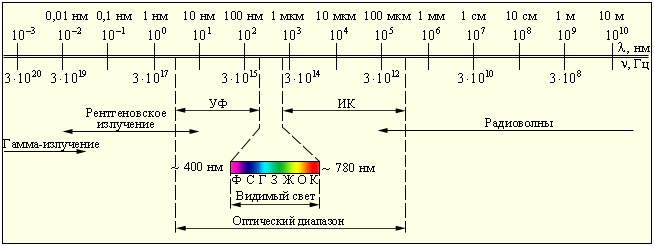
Шкала электромагнитных волн. Границы между различными диапазонами условны
Постоянный ток – частота ν = 0 – 10 Гц.
Атмосферные помехи и переменный ток – частота ν = 10 – 10 4 Гц
Частота ν =10 4 – 10 11 Гц
Получают с помощью колебательных контуров.
Радиоволны различных частот и с различными длинами волн по разному поглощаются и отражаются средами, проявляют свойства дифракции и интерференции.
Радиосвязь, телевидение, радиолокация.
Частота ν =3·10 11 – 4·10 14 Гц
Излучаются атомами и молекулами вещества.
Получают изображения предметов в темноте, приборах ночного видения, в тумане. Используют в криминалистике, в физиотерапии,. в промышленности для сушки окрашенных изделий, стен зданий, древесины, фруктов.
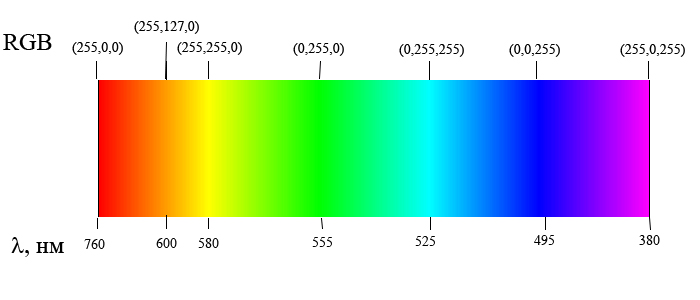
Часть электромагнитного излучения, воспринимаемая глазом (от красного до фиолетового).
Частота ν =4·10 14 – 8·10 14 Гц
Отражается, преломляется, воздействует на глаз, способно к явлениям дисперсии, интерференции, дифракции.
Частота ν =8·10 14 – 3·10 15 Гц
Источники: газоразрядные лампы с трубками из кварца(кварцевые лампы).
Излучается всеми твердыми телами, у которых t > 1000°С, а также светящимися парами ртути.
В медицине, в косметологии (солярий, загар), в промышленности.
Частота ν =3·10 15 – 3·10 19 Гц
Излучаются при резком торможении электронов, движущихся с большим ускорением.
Получают при помощи рентгеновской трубки: электроны в вакуумной трубке ускоряются электрическим полем при высоком напряжении, достигая анода, при соударении резко тормозятся. При торможении электроны движутся с ускорением и излучают электромагнитные волны с малой длиной (от 100 до 0,01 нм).
В медицине (диагностика заболеваний внутренних органов), в промышленности (контроль внутренней структуры различных изделий, сварных швов).
Гамма – излучение (γ – излучение).
Частота ν =3·10 20 Гц и выше
Источники: атомное ядро (ядерные реакции).
В медицине, в производстве (γ – дефектоскопия).
Физика. 11 класс
§ 32. Излучение и поглощение света атомом. Спектры испускания и поглощения
 |
 |
| Спектр угольной дуги (полосы молекул CN и C2) |
 |
| Спектр испускания паров молекулы йода |
 |
| Спектр молекулы Н2 |
В 1860 г. немецкие ученые Г. Кирхгоф и Р. Бунзен, изучая спектры металлов, установили следующие факты:
1) каждый металл имеет свой спектр;
2) спектр каждого металла строго постоянен;
3) введение в пламя горелки любой соли одного и того же металла всегда приводит к появлению одинакового спектра;
4) при внесении в пламя смеси солей нескольких металлов в спектре одновременно появляются все их линии;
5) яркость спектральных линий зависит от концентрации элемента в данном веществе.
Спектры поглощения
Если белый свет от источника, дающей сплошной спектр, пропускается через пары исследуемого вещества и затем разлагается в спектр, то на фоне сплошного спектра наблюдаются темные линии поглощения в тех же сам ых местах, где находились бы линии спектра испускания паров исследуемого элемента. Такие спектры получили название атомных спектров поглощения.
Все вещества, атомы которых находятся в возбужденном состоянии, излучают световые волны, энергия которых определенным образом распределена по длинам волн. Поглощение света веществом также зависит от длины волны. Атомы поглощают излучение лишь тех длин волн, которые они могут испускать при данной температуре.
Спектральный анализ
Спектральным анализом называется метод изучения химического состава вещества, основанный на исследовании его спектров. Отдельные линии в спектрах различных элементов могут совпадать, но в целом спектр каждого элемента является его индивидуальной характеристикой.
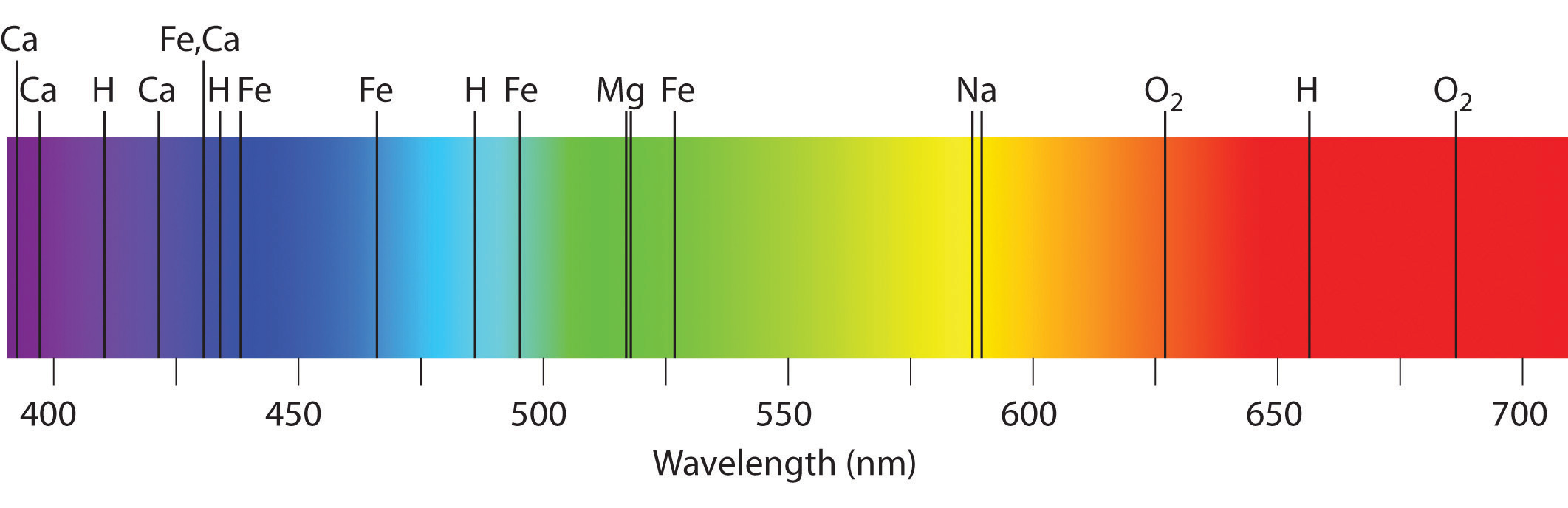
Спектральный анализ сыграл большую роль в науке. Например, в спектре Солнца (1814) были открыты фраунгоферовы темные линии, происхождение которых объясняется следующим образом. Солнце, являясь раскаленным газовым шаром (Т
6000 °С), испускает сплошной спектр. Солнечные лучи проходят через атмосферу Солнца (солнечную корону, температура которой
2000— 3000 °С. Корона поглощает из сплошного спектра излучение определенной частоты, а на Земле регистрируется солнечный спектр поглощения, по которому можно определить, какие химические элементы присутствуют в короне Солнца. По спектрам поглощения на Солнце были обнаружены все земные элементы, а также неизвестный ранее элемент, который назвали гелий. Через 26 лет (1894) открыли гелий на Земле. Благодаря спектральному анализу на Земле было открыто еще 25 химических элементов.
Фраунгоферовы линии дают информацию не только о химическом составе звезды, но и о ее температуре и давлении на поверхности. Более того, спектральный анализ Солнца и звезд показал, что входящие в их состав химические элементы имеются и на Земле, т.е. вещество Вселенной состоит из одного и того же набора элементов.
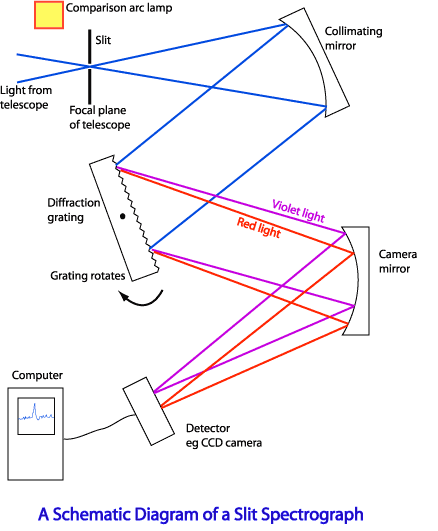
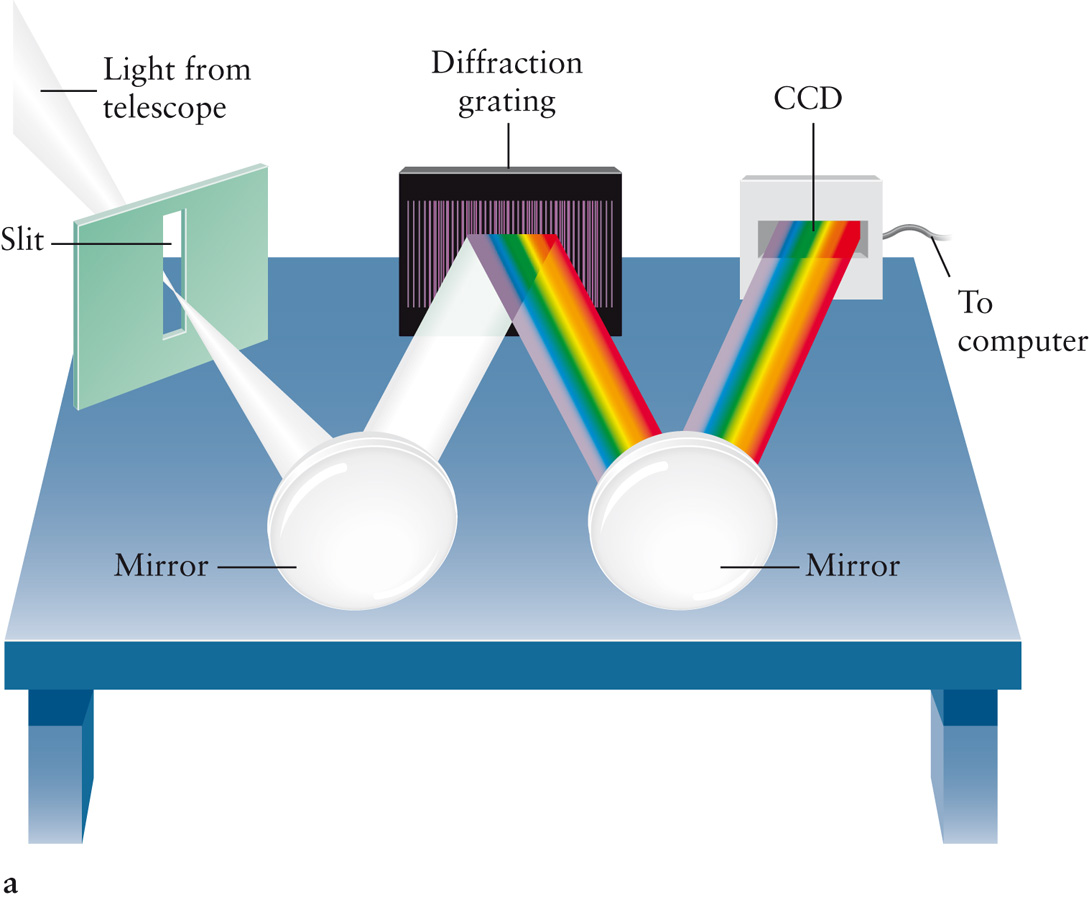
Спектральные аппараты
Спектроскопом называется прибор, с помощью которого визуально исследуется спектральный состав света, испускаемого некоторым источником. Если регистрация спектра происходит на фотопластинке, то прибор называется спектрографом.
Для точного исследования спектров такие простые приспособления, как узкая щель, ограничивающая световой пучок, и призма, уже недостаточны. Необходимы приборы, дающие четкий спектр, т.е. приборы, хорошо разделяющие волны различной длины и не допускающие перекрытия отдельных участков спектра. Такие приборы называют спектральными аппаратами. Чаще всего основной частью спектрального аппарата является призма или дифракционная решетка.
Применение спектрального анализа
Линейчатые спектры играют особо важную роль, потому что их структура прямо связана со строением атома. Ведь эти спектры создаются атомами, не испытывающими внешних воздействий. Состав сложных, главным образом органических смесей анализируется по их молекулярным спектрам.
Спектральный анализ можно проводить и по спектрам поглощения. В астрофизике по спектрам можно определить многие физические характеристики объектов : температуру, давление, скорость движения, магнитную индукцию и др. с помощью спектрального анализа определяют химический состав руд и минералов.
Основные направления применения спектрального анализа таковы: физико-химические исследования; машиностроение, металлургия; атомная индустрия; астрономия, астрофизика; криминалистика.
Современные технологии создания новейших строительных материалов (металлопластиковые, пластиковые) непосредственно взаимосвязаны с такими фундаментальными науками как химия, физика. Данные науки используют современные методы исследования веществ. Поэтому спектральный анализ можно применять для определения химического состав состава строительных материалов по их спектрам.