Специфичность действия ферментов
Специфичность действия ферментов
Ферменты обладают более высокой специфичностью действия по сравнению с неорганическими катализаторами. Различают специфичность по отношению к типу химической реакции, катализируемой ферментом, и специфичность по отношению к субстрату. Эти два вида специфичности характерны для каждого фермента.
Специфичность по отношению к субстрату – это предпочтительность фермента к субстрату определенной структуры в сравнении с другими субстратами.
Различают 4 вида субстратной специфичности ферментов:
1. Абсолютная специфичность – способность фермента катализировать превращение только одного субстрата. Например – глюкокиназа фосфорилирует только глюкозу, аргиназа расщепляет только аргинин, уреаза – мочевину.
2. Относительная специфичность – фермент катализирует превращение нескольких субстратов, имеющих один тип связи. Например – липаза расщепляет сложноэфирную связь в триацилглицеролах.
3. Относительная групповая специфичность – фермент катализирует превращение нескольких субстратов, имеющих один тип связи, но требуется наличие определенных функциональных групп, входящих в состав субстратов. Например, все протеолитические ферменты расщепляют пептидную связь, но пепсин – образованную аминогруппами ароматических аминокислот, химотрипсин – образованную карбоксильными группами этих же аминокислот, трипсин – пептидную связь, образованную карбоксильной группой лизина, аргинина.
4. Стереохимическая специфичность – фермент катализирует превращение только одного стереоизомера. Например, бактериальная аспартатдекарбоксилаза катализирует декарбоксилирование только L-аспартата и не действует на D-аспарагиновую кислоту.
Специфичность по отношению к реакции
Каждый фермент катализирует одну реакцию или группу реакций одного типа. Часто одно и то же химическое соединение выступает как субстрат для разных ферментов, причем каждый из них катализирует специфическую для него реакцию, приводящую к образованию разных продуктов. Специфичность по типу реакции лежит в основе единой классификации ферментов.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Читайте также
МЕСТО ДЕЙСТВИЯ — АФРИКА
МЕСТО ДЕЙСТВИЯ — АФРИКА Заглянем в 1924 год и выясним, что так внимательно рассматривает профессор Раймонд Дарт, стоя возле только что распакованных ящиков, которые привезли его ученики из известкового карьера Таунг, что в Бечуаналенде. В руках у профессора из
Микробы — продуценты ферментов
Микробы — продуценты ферментов Мы уже знаем, что ферменты — это биологические катализаторы, то есть вещества, способствующие осуществлению многих химических реакций, которые-происходят в живой клетке и необходимы для получения питательных веществ и построения ее
Механизм действия нервной системы
Механизм действия нервной системы Теперь, вероятно, следует присмотреться к механизму действия этой сложной структуры, начав с простого примера. Если направить в глаза яркий свет, зрачок человека сужается. Эта реакция зависит от целой серии событий, которые начинаются в
Глава 3. Ферменты. Механизм действия ферментов
Глава 3. Ферменты. Механизм действия ферментов Ферментами или энзимами называют специфические белки, входящие в состав всех клеток и тканей живых организмов и выполняющие роль биологических катализаторов.Общие свойства ферментов и неорганических катализаторов:1. Не
Структура молекулы ферментов
Структура молекулы ферментов По строению ферменты могут быть простыми и сложными белками. Фермент, являющийся сложным белком называют холоферментом. Белковая часть фермента называется апоферментом, небелковая часть – кофактором. Различают два типа кофакторов:1.
Механизм действия ферментов
Глава 4. Регуляция активности ферментов. Медицинская энзимология
Глава 4. Регуляция активности ферментов. Медицинская энзимология Способы регуляции активности ферментов:1. Изменение количества ферментов.2. Изменение каталитической эффективности фермента.3. Изменение условий протекания реакции.Регуляция количества
Применение ферментов в медицине
Применение ферментов в медицине Ферментные препараты широко используют в медицине. Ферменты в медицинской практике находят применение в качестве диагностических (энзимодиагностика) и терапевтических (энзимотерапия) средств. Кроме того, ферменты используют в качестве
Глава 13. Особенности действия гормонов
Глава 13. Особенности действия гормонов Гормоны гипоталамуса ЦНС оказывает регулирующее действие на эндокринную систему через гипоталамус. В клетках нейронов гипоталамуса синтезируются пептидные гормоны двух типов. Одни через систему гипоталамо-гипофизарных сосудов
Диапазон действия экологических факторов
Диапазон действия экологических факторов Все живые организмы способны воспринимать только определенный диапазон интенсивности воздействий любого экологического фактора, что определяется нормой реакции генотипа. Этот диапазон выработался в процессе
6.4. Возрастающая специфичность морфического резонанса в процессе морфогенеза
6.4. Возрастающая специфичность морфического резонанса в процессе морфогенеза Энергетический резонанс не является процессом типа «все или ничего»: система резонирует в ответ на диапазон частот, более или менее близких к ее естественной частоте, хотя максимальный отклик
Как наши действия рассказывают нам о мире
Как наши действия рассказывают нам о мире Для мозга между восприятием и действиями существует тесная связь. Наше тело служит нам, чтобы познавать окружающий мир. Мы взаимодействуем с окружающим миром посредством своего тела и смотрим, что из этого выйдет. Этой
Программа действия
Программа действия Выбор или создание программы действия непосредственно предшествует двигательному акту. В подавляющем большинстве случаев ни человек, ни животные не разрабатывают программу действия, а используют ту, которая уже применялась ранее при схожей
2.2. Общая характеристика пищеварительных ферментов
2.2. Общая характеристика пищеварительных ферментов Обращает на себя внимание принципиальное сходство, а иногда и поразительное совпадение ферментных систем, реализующих пищеварение у различных организмов. Поэтому те характеристики, которые будут представлены ниже,
Изменение активности некоторых Ферментов крови и печени крыс при экспериментальном голодании А. А. ПОКРОВСКИЙ, Г. К. ПЯТНИЦКАЯ (Москва)
Изменение активности некоторых Ферментов крови и печени крыс при экспериментальном голодании А. А. ПОКРОВСКИЙ, Г. К. ПЯТНИЦКАЯ (Москва) Проблема влияния голодания на разные показатели обменных процессов в организме животных и человека продолжает привлекать внимание
Влияние голодания на активность ферментов пентозофосфатного пути в печени и мозге крыс Ю. Л. ЗАХАРЬИН (Москва)
Влияние голодания на активность ферментов пентозофосфатного пути в печени и мозге крыс Ю. Л. ЗАХАРЬИН (Москва) В последние годы в клинике часто применяется с лечебными целями, в частности, для лечения психических заболеваний, полное голодание. Не вызывает сомнения, что
Ферменты
Жизнь любого организма возможна благодаря протекающим в нем процессам обмена веществ. Этими реакциями управляют природные катализаторы, или ферменты. Другое название этих веществ – энзимы. Термин «ферменты» происходит от латинского fermentum, что означает «закваска». Понятие появилось исторически при изучении процессов брожения.

Рис. 1 — Брожение с использованием дрожжей – типичный пример ферментативной реакции
Человечество давно пользуется полезными свойствами этих ферментов. Например, уже много веков из молока с помощью сычужного фермента делают сыр.
Ферменты отличаются от катализаторов тем, что действуют в живом организме, тогда как катализаторы – в неживой природе. Отрасль биохимии, которая изучает эти важнейшие для жизни вещества, называется энзимологией.
Общие свойства ферментов
Ферменты представляют собой молекулы белковой природы, которые взаимодействуют с различными веществами, ускоряя их химическое превращение по определенному пути. При этом они не расходуются. В каждом ферменте есть активный центр, присоединяющийся к субстрату, и каталитический участок, запускающий ту или иную химическую реакцию. Эти вещества ускоряют протекающие в организме биохимические реакции без повышения температуры.
Основные свойства ферментов:
Роль ферментов в организме человека невозможно переоценить. В то время, когда еще только открыли структуру ДНК, говорили, что один ген отвечает за синтез одного белка, который уже определяет какой-то определенный признак. Сейчас это утверждение звучит так: «Один ген – один фермент – один признак». То есть без активности ферментов в клетке жизнь не может существовать.
Классификация
В зависимости от роли в химических реакциях, различаются такие классы ферментов:
Классы
Особенности
Катализируют окисление своих субстратов, перенося электроны или атомы водорода
Участвуют в переносе химических групп из одного вещества в другое
Расщепляют крупные молекулы на более мелкие, добавляя к ним молекулы воды
Катализируют расщепление молекулярных связей без процесса гидролиза
Активируют перестановку атомов в молекуле
Образуют связи с атомами углерода, используя энергию АТФ.
В живом организме все ферменты делятся на внутри- и внеклеточные. К внутриклеточным относятся, например, ферменты печени, участвующие в реакциях обезвреживания различных веществ, поступающих с кровью. Они обнаруживаются в крови при повреждении органа, что помогает в диагностике его заболеваний.
Внутриклеточные ферменты, которые являются маркерами повреждения внутренних органов:
Внеклеточные ферменты выделяются железами во внешнюю среду. Основные из них секретируются клетками слюнных желез, желудочной стенки, поджелудочной железы, кишечника и активно участвуют в пищеварении.
Пищеварительные ферменты
Пищеварительные ферменты – это белки, которые ускоряют расщепление крупных молекул, входящих в состав пищи. Они разделяют такие молекулы на более мелкие фрагменты, которые легче усваиваются клетками. Основные типы пищеварительных ферментов – протеазы, липазы, амилазы.
Основная пищеварительная железа – поджелудочная. Она вырабатывает большинство этих ферментов, а также нуклеаз, расщепляющих ДНК и РНК, и пептидаз, участвующих в образовании свободных аминокислот. Причем незначительное количество образующихся ферментов способно «обработать» большой объем пищи.
При ферментативном расщеплении питательных веществ выделяется энергия, которая расходуется для процессов обмена веществ и жизнедеятельности. Без участия ферментов, подобные процессы происходили бы слишком медленно, не обеспечивая организм достаточным энергетическим запасом.
Кроме того, участие ферментов в процессе пищеварения обеспечивает распад питательных веществ до молекул, способных проходить через клетки кишечной стенки и поступать в кровь.
Амилаза
Амилаза вырабатывается слюнными железами. Она действует на крахмал пищи, состоящий из длинной цепи молекул глюкозы. В результате действия этого фермента образуются участки, состоящие из двух соединенных молекул глюкозы, то есть фруктоза, и другие короткоцепочечные углеводы. В дальнейшем они метаболизируются до глюкозы в кишечнике и оттуда всасываются в кровь.
Слюнные железы расщепляют только часть крахмала. Амилаза слюны активна в течение короткого времени, пока пища прожевывается. После попадания в желудок фермент инактивируется его кислым содержимым. Большая часть крахмала расщепляется уже в 12-перстной кишке под действием панкреатической амилазы, вырабатываемой поджелудочной железой.
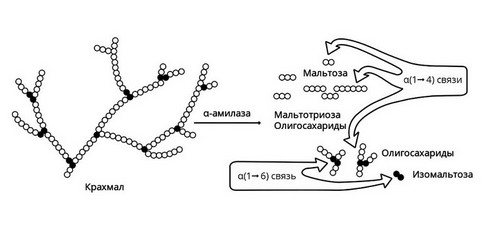
Рис. 2 — Амилаза начинает расщепление крахмала
Короткие углеводы, образовавшиеся под действием панкреатической амилазы, попадают в тонкий кишечник. Здесь с помощью мальтазы, лактазы, сахаразы, декстриназы они расщепляются до молекул глюкозы. Нерасщепляющаяся ферментами клетчатка выводится из кишечника с каловыми массами.
Протеазы
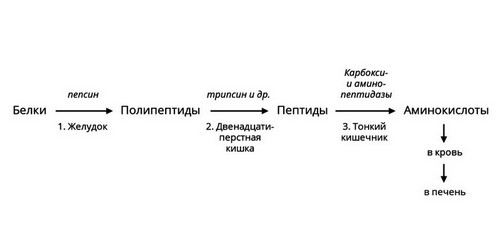
Рис. 3 — Ферментативное расщепление белков
Протеазы расщепляют пищевые белки на более мелкие фрагменты – полипептиды. Ферменты – пептидазы разрушают их до аминокислот, которые усваиваются в кишечнике.
Липазы
Пищевые жиры разрушаются ферментами-липазами, которые также вырабатываются поджелудочной железой. Они расщепляют молекулы жира на жирные кислоты и глицерин. Такая реакция требует наличия в просвете 12-перстной кишки желчи, образующейся в печени.
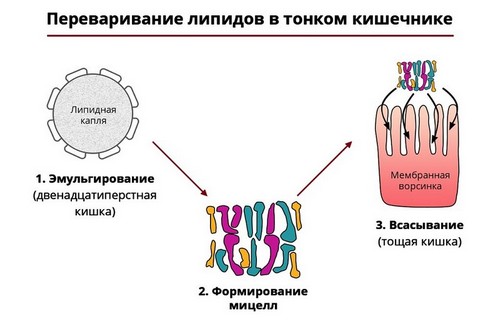
Рис. 4 — Ферментативный гидролиз жиров
Роль заместительной терапии препаратом «Микразим»
Для многих людей с нарушением пищеварения, прежде всего с заболеваниями поджелудочной железы, назначение ферментов обеспечивает функциональную поддержку органа и ускоряет процессы выздоровления. После купирования приступа панкреатита или другой острой ситуации прием ферментов можно прекратить, так как организм самостоятельно восстанавливает их секрецию.
Длительный прием ферментативных препаратов необходим лишь при тяжелой внешнесекреторной недостаточности поджелудочной железы.
Одним из наиболее физиологичных по своему составу является препарат «Микразим». В его состав входят амилаза, протеазы и липаза, содержащиеся в панкреатическом соке. Поэтому нет необходимости отдельно подбирать, какой фермент нужно использовать при разнообразных болезнях этого органа.
Показания для использования этого лекарства:
Прием пищеварительных ферментов с заместительной целью помогает избежать вздутия живота, жидкого стула, болей в животе. Кроме того, при тяжелых хронических заболеваниях поджелудочной железы Микразим полностью принимает на себя функцию по расщеплению питательных веществ. Поэтому они могут беспрепятственно усваиваться в кишечнике. Это особенно важно для детей, страдающих муковисцидозом.
Важно: перед применением ознакомьтесь с инструкцией или проконсультируйтесь с лечащим врачом.
Научная электронная библиотека
Морозова В. С., Габрильянц О. А., Мягкова М. А.,
3.2.3. Иммуноферментный метод (ИФА)
Иммуноферментный анализ (сокращённо ИФА, англ. enzyme-linked immunosorbent assay, ELISA) – лабораторный иммунологический метод качественного или количественного определения различных соединений, макромолекул, вирусов и пр., в основе которого лежит специфическая реакция антиген-антитело. Выявление образовавшегося комплекса проводят с использованием фермента в качестве метки для регистрации сигнала.
Твердофазный ИФА был предложен в 1971 году. Основные принципы твердофазного ИФА, независимо от модификации, заключаются в следующем:
1. На 1 этапе реакции адсорбируют антигены или антитела на твердой фазе. При этом не связавшиеся с твердой фазой реагенты легко удаляются отмыванием.
2. В сенсибилизированных лунках инкубируют исследуемый образец. В лунках с положительным контролем – стандартные реагенты. При этом на поверхности твердой фазы формируются иммунные комплексы. Несвязавшиеся компоненты удаляют отмыванием.
3. При добавлении конъюгата антитело-фермент или антиген-фермент и связывании его с иммобилизованным иммунным комплексом активный центр фермента остается доступным для последующего взаимодействия с субстратом. Инкубация субстрата в лунках с иммобилизованным конъюгатом приводит к развитию цветной реакции. Эту реакцию можно остановить на нужной стадии, выраженность окрашивания можно оценить визуально или по оптической плотности.
Из-за разнообразия объектов исследования – от низкомолекулярных соединений до вирусов и бактерий, и многообразия условий проведения ИФА существует большое количество вариантов этого метода.
Одним из принципов классификации методов ИФА является их разделение по типу проводимых на каждой из иммунохимических стадий реакций. В соответствии с эти все методы можно разделить на две группы –
гомогенные и гетерогенные. Если в ходе выполнения анализа все реакции, включая ферментативную стадию, протекают в растворе, то метод является гомогенным. Гетерогенный ИФА объединяет методы, в которых анализ проводится в двухфазной системе, при этом разделение на фазы может происходить на любой стадии определения [16].
В настоящее время EMIT (гомогенный ИФА) широко распространен во всем мире наряду с твердофазным ИФА (тИФА). EMIT по сравнению с тИФА является более экспрессным (до 2-х минут) и менее трудоемким, хотя менее чувствительный, и поэтому используется только в качественном анализе.
Возможна также классификация по типу иммунохимического взаимодействия на первой стадии анализа (в которой происходит связывание определяемого вещества). Если в системе присутствуют только анализируемое соединение и соответствующие ему центры связывания (антиген и специфические антитела), то метод является неконкурентным. Если же на первой стадии в системе одновременно присутствует анализируемое соединение и его аналог (меченное ферментом анализируемое соединение или анализируемое соединение, иммобилизованное на твердой фазе), конкурирующие за ограниченное количество центров специфического связывания, то метод является конкурентным.
Рис. 10. Конкурентный (а) и неконкурентный (б) ИФА
Примером неконкурентного формата ИФА является «сэндвич»-метод. К носителю с иммобилизованными антителами добавляют раствор, содержащий анализируемый антиген. В процессе инкубации на первой стадии на твердой фазе образуется комплекс антиген-антитело. Затем носитель отмывают от несвязавшихся компонентов и добавляют меченные ферментом специфические антитела. После вторичной инкубации и удаления избытка конъюгата антител с ферментом определяют ферментативную активность носителя, которая пропорциональна начальной концентрации исследуемого антигена. На стадии выявления специфического иммунокомплекса антиген оказывается как бы зажатым между молекулами иммобилизованных и меченных антител, что послужило поводом для широкого распространения названия «сэндвич»-метод.
Ферментативная реакция (цветная реакция) проходит в присутствии перекиси водорода и субстрата, представленного неокрашенным соединением, которое в процессе пероксидазной реакции окисляется до окрашенного продукта реакции на заключительном этапе проведения исследования. Интенсивность окрашивания зависит от количества выявленных специфических антител. Результат оценивается спектрофотометрически или визуально.
«Сэндвич»-метод может быть использован для анализа только тех антигенов, на поверхности которых существуют, по крайней мере, две антигенные детерминанты. На этом формате основано большое количество тест-систем для иммуноферментной диагностики различных инфекций: ВИЧ-инфекция, вирусные гепатиты, цитомегаловирусная, герпесная, токсоплазменная и другие инфекции.
Другим типом классификации схем ИФА является разделение по типу определения концентрации анализуемого вещества:
1) прямое определение образовавшихся иммунокомплексов (аналитический сигнал прямо пропорционален концентрации определяемого вещества) – прямой ИФА;
2) определение концентрации оставшихся свободными, т.е. не вступившими в реакцию компексообразования антител – непрямой ИФА.
Так, среди конкурентных схем твердофазного ИФА существует два основных формата:
Прямой конкурентный формат ИФА использует в качестве меченного ферментом реагента одного из участников иммунохимической реакции (рис. 3) – определяемое соединение или специфический к нему диагностический реагент (антитела). В результате схема ИФА состоит из 3-х стадий:
– сорбции (иммобилизации) специфических антител, либо конъюгата антигена,
– аналитической стадии: конкурентной реакция Аг-Ат с участием меченого ферментом реагента (антигена или антител),
– фермент-субстратной реакции, в результате которой образуется окрашенный (или люминисцентный) продукт.
Например, на полистирольный планшет иммобилизуют специфические антитела (рис. 11 в) иммобилизованые на твердой фазе специфические антитела. На второй стадии к иммобилизованным антителам добавляют раствор, содержащий определяемое вещество и фиксированную концентрацию меченого антигена, инкубируют и после отмывки носителя от несвязавшихся компонентов регистрируют ферментативную активность образовавшихся на твердой фазе специфических иммунных комплексов. В этой схеме меченый ферментом и немеченый антиген конкурируют за связывание с иммобилизованными специфическими антителами.
Рис. 11. Виды конкурентного ИФА:
а – непрямой конкурентный ИФА с иммобилизацией конъюгата антигена с высокомолекулярным веществом и использованием меченых антивидовых антител; б – непрямой конкурентный ИФА с иммобилизацией конъюгата антигена с высокомолекулярным веществом и использованием меченых специфических антител; в – прямой конкурентный ИФА с иммобилизацией специфических антител и использованием меченого антигена (аналита)
Преимуществом прямой схемы является небольшое число стадий, что позволяет легко автоматизировать анализ. К недостаткам схемы относятся сложность методов синтеза ферментных конъюгатов, а также возможное влияние компонентов образца на активность фермента.
В непрямом конкурентном формате ИФА используются меченные ферментом антитела (специфические или вторичные) и иммобилизованный на твердой фазе конъюгат антиген-белок-носитель
(рис. 11 а, б). Непрямая схема с использованием меченых антивидовых антител является одной из наиболее распространенных схем ИФА (рис. 11 а). На поверхности носителя иммобилизуют конъюгат антиген-белок, к которому добавляют раствор, содержащий определяемый антиген и фиксированную концентрацию немеченых специфических антител, инкубируют и после удаления несвязавшихся компонентов добавляют фиксированную концентрацию меченых антивидовых антител. После инкубации и отмывки носителя детектируют ферментативную активность образовавшихся на твердой фазе специфических иммунных комплексов. Величина аналитического сигнала в этом случае находится в обратно-пропорциональной зависимости от концентрации определяемого антигена.
Применение универсального реагента – меченых антивидовых антител – даёт возможность выявлять антитела к разным антигенам. Кроме того, анализируемый образец и меченый реагент вводятся в систему на разных стадиях, что устраняет влияние различных эффекторов, содержащихся в образце, на каталитические свойства ферментной метки. Однако такая схема анализа усложняет его проведение из-за введения дополнительных стадий.
ИФА наркотических веществ и их метаболитов в биологических жидкостях и тканях широко используется в ХТЛ, бюро судмедэкспертизы, клинико-диагностических лабораториях, медицинских центрах. Чаще всего применяется полуколичественный вариант методики, т.к. в большинстве случаев необходимо дать заключение о том, превышает ли уровень метаболитов ПАВ в образце определенную пороговую концентрацию. Однако метод ИФА может использоваться (и используется в некоторых случаях) для количественного определения метаболитов ПАВ с высокой чувствительностью – до 10–9 г/л.
Отдельно следует выделить иммунохимический метод выявления фактов употребления наркотиков в отдаленные промежутки времени (до 4 месяцев после последнего употребления ПАВ), основанный на определении антител к наркотическим веществам в крови человека [4, 5]. Данный метод использует прямую неконкурентную схему ИФА.
Компоненты, используемые в ИФА
Ферментные метки обладают чрезвычайно мощным каталитическим действием, одна молекула фермента может реагировать с большим количеством молекул субстрата. Таким образом, фермент, присутствующий в ничтожных количествах, можно выявить и количественно определить по образованию продуктов катализируемой им реакции. Другое преимущество применения ферментов в качестве меток обусловлено наличием в молекуле многочисленных функциональных групп (сульфгидрильных, карбоксильных, остатков тирозина и др.), через которые можно ковалентно присоединить молекулы лиганда.
В ИФА может использоваться не менее 15 различных ферментов. Наибольшее применение, в соответствии с вышеназванными требованиями, нашли пероксидаза хрена (ПХ), щелочная фосфотаза (ЩФ) и β-D-галактозидаза. Все три стабильны и катализируют высокочувствительные реакции. Кроме того, продукты, получаемые в результате реакций, катализируемых этими ферментами, в зависимости от используемого субстрата, могут выявляться не только колориметрическими методами, но также флуоресцентными методами. Другие ферменты используются значительно реже. Это объясняется их более низкой в сравнении с ПХ и ЩФ удельной активностью.
Выбор субстрата в первую очередь определяется используемым в качестве метки ферментом, так как реакция фермент-субстрат высоко специфична.
Чаще используют хромогенные субстраты, которые, разрушаясь, образуют окрашенное вещество. Перспективным является использование высокоэнергетических субстратов – флуоресцентных, хемилюминесцентных.
3. Антигены и антитела.
Аг и Aт, используемые в ИФА, должны быть высокоочищенными и высокоактивными. Кроме того, Аг должны обладать высокой антигенностью, оптимальной плотностью расположения и количеством антигенных детерминант и гомогенностью. Многие синтетические и рекомбинантные Аг вирусов и бактерий хорошо себя зарекомендовали при использовании в ИФА. Это существенно повысило специфичность и воспроизводимость метода за счет сведения к минимуму перекрестных реакций.
Одним из наиболее важных реагентов в ИФА являются антитела. Чувствительность ИФА зависит от концентрации, активности и специфичности используемых антител. Используемые антитела могут быть поли- или моноклинальными, различного класса (IgG или IgM) и подкласса (IgGl, IgG2), антиаллотипическими или антиидиотипическими. При низкой аффинности Ат распад комплекса Аг-Ат приводит к удалению связанного Аг из системы. Чувствительность и специфичность метода повышается при использовании моноклональных антител. В этом случае появляется возможность обнаруживать низкие концентрации Аг (Aт) в испытуемых образцах.
4. Получение конъюгата.
Конъюгат – это антиген или антитело, «сшитые» с ферментной меткой или белком-носителем. Получение коньюгата – один из важных этапов разработки ИФА.
При синтезе конъюгата с ферментом подбирают такой оптимальный метод введения ферментной метки, чтобы оба компонента конъюгата сохраняли свою биологическую активность: фермент – способность взаимодействовать с субстратом, а антиген или антитело – антигенность и антигенсвязывающую активность, соответственно. Наличие меченого, высокоочищенного антигена позволяет использовать конкурентные методы ИФА. Однако антигены разнообразны по своим физико-химическим свойствам и строению, а значит невозможно разработать универсальные методики для получения конъюгата с антигеном. В этом случае получение конъюгата антигена с ферментом представляет собой отдельную сложную задачу. Приготовление меченых антител для ИФА методически более доступно.
Конъюгирование фермента с иммунохимически активными белками производится различными методами: химическая сшивка, ковалентное связывание молекулы фермента с Аг или Aт и образование соединений через нековалентные связи, например, когда связь между ферментом и Аг или Aт осуществляется иммунологически, через взаимодействие антиген-антитело.
В качестве твердой фазы для проведения ИФА можно применять различные материалы: полистирол, поливинилхлорид, полипропилен и другие вещества. Твердой фазой могут служить стенки пробирки, 96-луночные и др. планшеты, шарики, бусины, а также нитроцеллюлозные и другие мембраны, активно сорбирующие белки.
Иммобилизация антигена или антител на твердой фазе возможна тремя путями:
– пассивная адсорбция, основанная на сильных гидрофобных взаимодействиях между белками и синтетической поверхностью;
– ковалентное прикрепление к твердой фазе;
– иммунохимическое и др. (нековалентное и неадсорбционное присоединение).
Пассивная адсорбция белков широко используется при проведении ИФА на платах для титрования, на нитроцеллюлозных мембранах. Пассивная адсорбция идет по принципу насыщения и коррелирует с молекулярной массой адсорбируемого вещества. В стандартных наборах ИФА используются 96-тилуночные прозрачные полистирольные планшеты.
Рис. 12. Набор для ИФА-определения наркотических еществ в биологических жидкостях: – планшет с нанесенным антигеном; 2 – положительный и отрицательный контрольный образец; 3 – реагент для выявления образовавшихся иммунных комплексов; 4 – растворы буфера для приготовления анализируемых образцов; 5 – раствор буфера для проведения фермент-субстратного окрашивания; – раствор для остановки реакции окрашивания субстрата; – инструкция по применению
Свободные сайты на поверхности твердой фазы, не связавшиеся с сорбируемым агентом, могут фиксировать в ходе теста другие молекулы, в том числе и конъюгаты, что приводит к повышению фонового сигнала. Для предотвращения неспецифического связывания после иммобилизации на твердую фазу основного материала проводят обработку нейтральными для теста веществами. Наиболее популярные блокирующие агенты – бычий сывороточный альбумин (БСА), казеин и др. Выбор блокирующего агента и условия проведения этого этапа зависят от типа твердой фазы, чувствительности системы.
Готовый набор для ИФА-определения наркотических веществ в биологических жидкостях выглядит следующим образом (рис. 12).







