Что такое стандарты gmp
Международный стандарт GMP считается одним из основных в мире, определяющих требования к производству лекарственных средств, БАДов и даже продуктов питания.
Для чего предназначен стандарт?
Полное название этого набора требований – Good Manufacturing Practice for Medicinal Products, что в переводе означает «Правила производства медицинской продукции». Международный стандарт GMP имеет следующие цели:
1. Обеспечить высокий уровень качества продукции.
2. Гарантировать, что:
История возникновения
Начало стандарту было положено в США в 1963 году, когда появились на свет первые правила безопасного и качественного изготовления лекарственных средств. Стандартную форму официального документа, впрочем, они приняли лишь в 1968 году. А через год Всемирная организация здравоохранения (ВОЗ) рекомендовала всем странам применять международный стандарт GMP. Впоследствии эти правила неоднократно дополнялись и корректировались, пока не приняли нынешний вид.
Откровенно игнорировал стандарт на начальном этапе его внедрения лишь Советский Союз, Минздрав которого разработал свои нормы, по строгости иногда превышающие GMP. Интерес к международному стандарту начал проявляться лишь с 1991 года, когда начались процессы по импорту и экспорту лекарств. Однако на первых порах достичь гармонии столь различных правил не удавалось. Лишь с 90-х годов появились какие-то реальные подвижки.
Российский стандарт
Нормативная база на территории стран СНГ начала разрабатываться после распада СССР. Главная цель была – на основе прежних нормативов максимально сблизить два стандарта, постепенно приближаясь к правилам, которые определял GMP (международный стандарт качества).
Процесс оказался долгим. Только в 2001 году в РФ появился близкий международному стандарт. Он предусматривает, что с 01.07.2000 все создаваемые и реконструируемые предприятия по выпуску лекарств будут получать лицензии на производство, хранение и реализацию продукции только при условии соответствия российскому аналогу GMP.
Разработкой его занималась организация под названием Ассоциация инженеров по контролю микрозагрязнений (АСИНКОМ). Отечественные правила были утверждены 10.04.2004 Госстандартом РФ, в результате чего появился ГОСТ Р 52249-2004 «Правила производства и контроля качества лекарственных средств». Он был введен в действие 01.01.2005, и считалось, что этот стандарт максимально сближен с международным. Однако с 01.01.2010 начал работать национальный российский стандарт GMP. Он взял за основу европейские правила, и прежний ГОСТ утратил актуальность.
Где в РФ расположены применяющие стандарт предприятия
Подавляющее большинство предприятий, которые получили сертификаты качества, соответствующие международным правилам, пока расположены в Москве, Санкт-Петербурге и других крупных промышленных и научных центрах страны.
Планируется полный перевод на GMP (международный стандарт) всех предприятий. Более того, он должен был закончиться еще в 2014 году, но возникло множество трудностей. Выяснилось, что далеко не каждое отечественное предприятие фармацевтической отрасли способно получить соответствующий сертификат качества. Главная проблема – нет кадров, имеющих достаточную теоретическую и, что особенно важно, практическую подготовку по внедрению стандарта на российской территории.
Основные элементы стандарта GMP
Стандарт GMP (Good Manufacturing Practice) предусматривает множество показателей, которым должны соответствовать производители продукции. Причем для фармацевтов детально регламентированы требования к каждому этапу изготовления – от концентрации бактерий, содержащихся в одном кубометре воздуха, до маркировки продукции.
В качестве примера можно привести требование к предприятию, изготавливающему лекарства в таблетках. В таких случаях GMP (международный стандарт) требует от организации «особо чистых цехов», в которых повышенная стерильность процесса достигается входными шлюзами для персонала, специальным режимом воздушной фильтрации и т. п. В России в таких цехах изготавливали лишь кремниевые кристаллы и особые микросхемы.
Какие условия нужны для перехода на стандарт?
Чтобы перевести российские предприятия на международный стандарт GMP, нужны и внешние, и внутренние условия. На государственном уровне требуется:
Чтобы выполнялся GMP-стандарт, правила GMP на уровне предприятий должны предусматривать следующие позиции:
Нужен ли стандарт для потребления лекарств внутри РФ?
При ответе на вопрос о том, нужен ли GMP (международный стандарт) в России, обычно рассматривается два аспекта.
1. С одной стороны, соблюдение его строжайших правил позволяет поднять планку качества лекарственных средств на очень высокий уровень. Население России тогда получит высокоэффективные и чистые лекарства, что позволит меньше болеть и скорее выздоравливать.
2. С другой стороны, отечественные предприятия финансово просто не «тянут» преобразования. Если же предприятие удается перевести на современные рельсы, то себестоимость лекарств существенно возрастает, и их реализация усложняется.
Оба эти фактора в России постоянно вступают в противоречие и тормозят внедрение стандарта. Впрочем, в связи с новыми геополитическими реалиями и необходимостью в импортозамещении лекарственных средств процесс должен в ближайшее время ускориться.
Сертификат GMP: подтверждение качества лекарственных средств
Сертификат GMP — это соблюдение изготовителем лекарственных препаратов требований надлежащей производственной практики. В России они сформулированы в национальном стандарте ГОСТ Р 52249-2009, который идентичен правилам, действующим в Европейском Союзе.
К каким производствам применима эта процедура?
В настоящее время в странах, которые контролируют соответствие стандарту GMP на своих территориях, его правила применяются для проверки качества следующих категорий продукции:
При этом для понимания ситуации следует принимать во внимание, что новая версия сертификации GMP — это не единственная система требований, которые в международной практике применяются в целях стандартизации медицинского обслуживания населения. Кроме них, производителям, работающим в такой сфере как фармация, необходимо соответствовать требованиям комплекса правил, объединенных под общим наименованием GxP:
Нормативная база
В Российской Федерации получение сертификата GMP осуществляется на основании действующей нормативной базы, включающей следующие основные правовые акты:
При этом необходимо принимать во внимание, что в настоящий момент наша страна вместе с другими государствами, входящими в состав Евразийского экономического союза, находится на этапе становления общего рынка, объединяющего фармацевтическое и косметическое производство в границах Союза. Это предполагает в том числе введение в действие единых требований к качеству и безопасности таких продуктов. В соответствии с принятым в мире порядком они реализуются в форме внедрения стандартов надлежащей производственной практики. Применение таких стандартов регулируется следующими нормативными документами:
Обратите внимание!
Для полноценного применения разработанного административного регламента необходимо решение Правительства о порядке реализации некоторых процедур, связанных с проведением фармацевтических инспекций. Приказ № 2945 вступит в силу только после принятия соответствующего постановления: пока этого не произошло.
Преимущества обладания сертификатом
Несмотря на необходимость проведения достаточно сложной и дорогостоящей процедуры, производители знают, что сертификация по стандартам GMP является весьма важной для представителей фармацевтической отрасли. В частности, оно обеспечивает продукции и производству следующие серьезные преимущества:
КОММЕНТАРИЙ ЭКСПЕРТА АТТЭК
Каков срок действия сертификата?
Срок действия российских сертификатов составляет 3 года. При этом срок действия иностранного сертификата GMP составляет от 1 до 3 лет. По истечении этого периода сертификацию потребуется проходить заново. Кроме того, это означает, что на протяжении всего этого срока компании необходимо обеспечить соответствие своего производства и продукции требованиям комплекса правил GMP.
Кто в России занимается сертификацией по стандартам GMP?
Сейчас сертификация контролируется департаментом развития медицинской и фармацевтической промышленности Министерства промышленности и торговли РФ. Он является организацией, ответственной за обеспечение надлежащего контроля за качеством, безопасностью и эффективностью лекарственных средств. Осуществлением требуемых сертификационных процедур занимается Государственный институт лекарственных средств и надлежащих практик (ФГБУ «ГИЛС и НП»).
Стандарт GMP в международной практике
Процесс сертификации на соответствие лекарственного препарата стандартам GMP в международной практике имеет комплексный характер, а ее основной целью является подтверждение безопасности и действенности продукции. В этой связи для достижения поставленной цели специалисты аккредитованных сертификационных организаций не ограничиваются оценкой ряда выборочных образцов лекарственных препаратов, как это часто предусматривается другими стандартами. В процедуру установления требуемого уровня качества лекарств любой международный центр сертификации лекарственных средств включает оценку предприятия, занимающегося его выпуском. В результате эксперты, занимающиеся проведением сертификации, анализируют конкретный препарат и процесс его выпуска в следующих областях:
Правила GMP в России
Порядок и сроки проведения всех операций в рамках этой процедуры, список лиц и организаций, ответственных за их осуществление, размер платы за проведение экспертной оценки и другие аспекты выполнения сертификации определены постановлением Правительства № 1314.
Процедура получения сертификата в России
Первым шагом для производителя, который желает пройти сертификацию, является подача соответствующего заявления в Минпромторг. В течение 10 рабочих дней специалисты ведомства проводят проверку корректности представленных в заявлении сведений и определяют возможность проведения сертификации.
В случае необходимости они вправе запросить у заявителя дополнительные документы, которые он обязан предоставить в течение 20 рабочих дней. В случае, если в отношении данного препарата принято положительное решение о проведении процедуры сертификации, необходимые данные направляются в ФГБУ «ГИЛС и НП», который в течение 20 рабочих дней с момента их получения обязан определить дату проведения сертификационных мероприятий и внести ее в график. Такая дата должна наступить не позднее 160 рабочих дней со дня, когда специалисты Минпромторга приняли положительное решение о сертификации, а сама экспертиза и расшифровка ее результатов должны занимать не более 10 рабочих дней.
На подготовку итогового отчета по результатам ее проведения исполнителю отводится 30 рабочих дней, а на его направление заявителю — 3 рабочих дня. Копия такого отчета также направляется в Минпромторг. На основании отчета формируется окончательное заключение, которое в случае положительного характера сопровождается выдачей сертификата производителю лекарственного препарата.
Документы для сертификации
Чтобы получить сертификат GMP в России, производитель обращается в уполномоченный орган с заявлением, к которому прилагает пакет документов, включающий:
Важнейшие документы предоставляются заявителем в копиях, поскольку при утере их восстановить невозможно или очень сложно. Правила регламентируют, что если заявление подает иностранный производитель, и некоторые документы в составе пакета представлены на другом языке, они должны быть переведены на русский язык и заверены в установленном порядке.
Сроки сертификации
Общая продолжительность процедуры сертификации складывается из следующих сроков.
Этап сертификационной процедуры
Максимальная допустимая продолжительность
Проверка полноты пакета документации, представленной с заявлением о сертификации, и правильности ее оформления, назначение инспекции
Направление информации о назначении инспектирования в уполномоченное учреждение, которое проводит проверку
Инспектирование и анализ лекарственного средства
Принятие решения о выдаче заключения по результатам инспекционного отчета
160-дневный период инспектирования включает внесение производителя в график инспекций, ожидание процедуры и проведение самой инспекции. Она должна занимать не более 10 рабочих дней.
Такой порядок действует, если в документации, поданной производителем, не обнаружат ошибок и недочетов, из-за которых ее могут направить на доработку. В этом случае вся процедура займет немногим более 180 рабочих дней, то есть свыше 8 месяцев.
Стоимость получения сертификата
Обязательной для всех производителей лекарственных средств, претендующих на получение сертификата, подтверждающего соответствие их продукции стандартам GMP, является оплата государственной пошлины за рассмотрение соответствующего заявления в Министерстве промышленности и торговли. Ее размер составляет 7500 рублей. Оплатить данную сумму необходимо еще до подачи заявления в ведомство, а ее размер никак не зависит от результатов рассмотрения документа.
Однако данная пошлина — это далеко не единственный и не самый крупный платеж, который потребуется осуществить производителю лекарств. Другой значительной статьей расходов станет плата за проведение экспертной оценки производства и продукции заявителя. Такая процедура выполняется специалистами ФГБУ «ГИЛС и НП»: для каждого из них предварительно проводится аттестация эксперта по GMP в России.
При этом размер платы за проведение оценки не является строго установленным, а определяется в зависимости от объема, характера и сложности необходимых процедур в соответствии с положениями приказа Министерства промышленности и торговли Российской Федерации от 11.01.2016 № 9 «Об утверждении методики определения размера платы за оказание услуги по инспектированию GMP». В случае, если проверка потребует проведения значительного объема работы и привлечения большого количества высококвалифицированных экспертов, размер платы за ее проведение может превышать 2,5 миллиона рублей.
Надлежащие фармацевтические практики (Good Practice, GxP)
Отраслевые стандарты серии GxP (GLP/GCP/GMP)
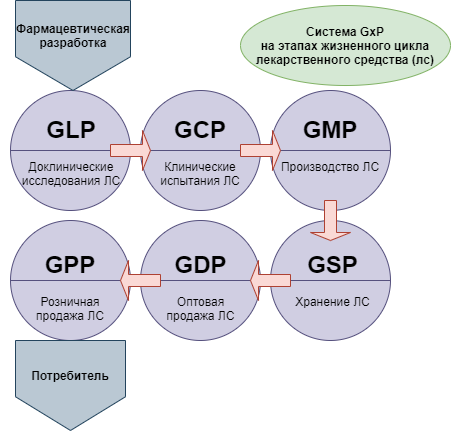
GxP (Good … Practice, Надлежащая … практика) — признанная во всем мире система обеспечения качества лекарственных средств. Система GxP охватывает все этапы жизненного цикла лекарственного средства, от фармацевтической разработки, испытаний, изготовления, хранения до использования конечным потребителем, а именно:
Русский Регистр оказывает услуги по сертификации на соответствие стандартам серии GxP: практикам GLP, GCP и GMP.
GLP. Надлежащая лабораторная практика
GLP (Good Laboratory Practice, Надлежащая лабораторная практика) – система качества, охватывающая организационный процесс и условия, при которых выполняются неклинические исследования лекарственных средств, связанные со здоровьем и экологической безопасностью.
Правила GLP включают в себя:
Национальным аналогом GLP в РФ является стандарт ГОСТ 33044–2014 Межгосударственный стандарт «Принципы надлежащей лабораторной практики», текст которого идентичен GLP.
GСP. Надлежащая клиническая практика
GCP (Good Clinical Practice, Надлежащая клиническая практика) — международный этический и научный стандарт планирования и проведения исследований с участием человека в качестве субъекта, а также документального оформления и представления результатов таких исследований.
Правила GCP призваны обеспечить достоверность результатов клинических испытаний, а также безопасность и охрану прав и здоровья людей, принимающих участие в данных испытаниях в качестве субъектов.
Национальным аналогом GCP в РФ является стандарт ГОСТ Р 52379–2005 «Надлежащая клиническая практика», текст которого идентичен GСP.
GMP. Надлежащая производственная практика
GMP (Good Manufacturing Practice, Надлежащая производственная практика) – международный стандарт, который устанавливает требования к производству и контролю качества лекарственных средств для человека и животных, а также специальные требования к производству активных фармацевтических субстанций и отдельных видов лекарственных средств. Стандарт GMP регулирует и оценивает параметры производства и лабораторной проверки.
Национальным аналогом GMP в РФ является стандарт ГОСТ Р 52249–2009 «Правила производства и контроля качества лекарственных средств», текст которого идентичен GMP.
Что такое стандарты gmp
Для клиентов
Актуальные виды услуг
ОБЩАЯ ИНФОРМАЦИЯ
Стандарт GMP (Good Manufacturing Practice — Надлежащая производственная практика) — система норм, правил и указаний в отношении производства:
В отличие от процедуры контроля качества путём исследования выборочных образцов таких продуктов, которая обеспечивает пригодность к использованию лишь самих этих образцов (и, возможно, партий, изготовленных в ближайшее к данной партии время), стандарт GMP отражает целостный подход и регулирует и оценивает собственно параметры производства и лабораторной проверки.
Для стандартизации качества медицинского обслуживания населения применяется вместе со стандартами:
ВЫГОДЫ ОТ ВНЕДРЕНИЯ (СЕРТИФКАЦИИ)
ПОЧЕМУ БЕЛПРОЕКТКОНСАЛТИНГ?
Обратившись в нашу компанию, Вы можете получить:
ОБЩАЯ СХЕМА РАБОТ ПО ВНЕДРЕНИЮ И СЕРТИФИКАЦИИ ФАРМАЦЕВТИЧЕСКОЙ СИСТЕМЫ КАЧЕСТВА ПО ТРЕБОВАНИЯМ GMP
Общий детализированный план разработки фармацевтической системы качества, оказания помощи по её внедрению, подготовки и прохождения сертификационной проверки ФСК Предприятия в соответствии с требованиями GMP
1. Разработка документации по фармацевтической системе качества :
2. Первоначальные контрольно-информационные мероприятия по подготовке к сертификации по GMP :
3. Разработка дополнительной документации для сертификации по GMP:
ОРГАНИЗАЦИЯ ПОТОЧНОСТИ ПРОИЗВОДСТВА ДЛЯ ОПТИМАЛЬНОГО ВНЕДРЕНИЯ GMP (ДЛЯ СТРОЯЩИХСЯ ПРОИЗВОДСТВЕННЫХ ПЛОЩАДОК)
Наша компания оказывает улуги как по разработке системы менеджмента GMP, так и помогает в построении поточности производства и производственной инфраструктуры в соответствии с требованиями Надлежащей производственной практики на строящихся площадках до запуска производства.
Примерный перечень основных работ, выполняемых нашими консультантами в рамках договора по организации поточности производства:
Внедрение GMP
Надлежащая произвосдвтенная практика. Правила производства и контроля качества лекарственных средств GMP (ГОСТ Р 52249-2009)
Разработка и внедрение СМК по GMP
Получите в подарок!*
Сертификат международного образца на английском языке
Видеозапись эксклюзивных курсов
*при заключении договора
Для чего нужно внедрение СМК по стандарту GMP?
Участие в тендерах и закупках
Сертификация предприятия по российским и международным стандартам
Экспорт продукции за пределы России
Что изменится в компании после внедрения СМК по стандарту GMP?
Увеличивается эффективность работы сотрудников
Упорядочивается работа компании
Снижаются издержки, связанные с производством некачественной продукции
Повышается доверие к компании со стороны клиентов, общества и государства
Повышается эффективность производственных процессов
Появляются дополнительные возможности для выхода на международные рынки