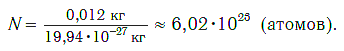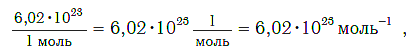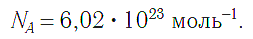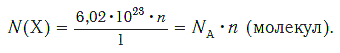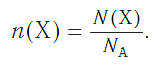Урок 8. Химическое количество вещества и моль
В уроке 8 «Химическое количество вещества и моль» из курса «Химия для чайников» выясним, что такое химическое количество вещества; рассмотрим моль в качестве единицы количества вещества, а также познакомимся с постоянной Авогадро. Напоминаю, что в прошлом уроке «Относительная молекулярная и относительная формульная массы» мы научились вычислять относительную молекулярную массу, а также относительную формульную массу веществ; кроме того, выяснили что такое массовая доля и привели формулу для ее вычисления.
Любое чистое вещество имеет свою химическую формулу, т. е. характеризуется определенным качественным и количественным составом.
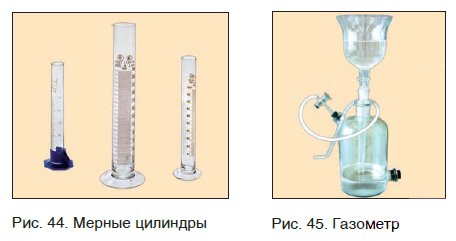
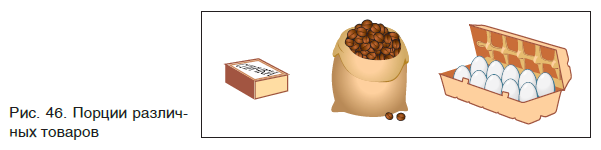
Если необходима какая-то порция твердого вещества, то для этого следует взять нужную его массу, т. е. взвесить вещество (рис. 43). Нужный объем жидкого вещества обычно отмеряют с помощью мензурки или мерного цилиндра (рис. 44). Для отбора необходимой порции (объема) газообразных веществ применяют специальные емкости — газометры (рис. 45).
Следовательно, объем и масса — это величины, характеризующие данную порцию вещества.
Химическое количество вещества
В жизни мы часто не различаем понятия «масса» и «количество». А это разные понятия. Когда вы говорите: «Я купил 2 кг груш», то здесь речь идет о массе груш. Но если вы говорите: «Я купил 10 груш», то в этом случае речь идет о количестве груш. Массу вещества измеряют в граммах, килограммах, тоннах, а количество — в штуках.
Груши можно пересчитать поштучно, а если это, например, зерна? Тут уже посчитать каждое зернышко даже в небольшой емкости сложно. Поэтому зерно обычно продают мешками, т. е. определенными порциями. В каждой такой порции — мешке (если они равны по массе и все зерна одинаковы) — будет находиться практически одно и то же число зерен. Подобным образом продают многие товары. Например, яйца — десятками, спички — спичечными коробками, в каждом из которых находится по 45 спичек (рис. 46).
В химической практике, помимо массы или объема, необходимо знать число структурных единиц (атомов, молекул, формульных единиц), которые содержатся в данной порции вещества, поскольку именно они участвуют в химических реакциях. Поэтому в химии, как и в других естественных науках, используют физическую величину, характеризующую число частиц в рассматриваемой порции вещества. Эта физическая величина называется количеством вещества или, как следует называть ее при химических расчетах, — химическое количество вещества.
Химическое количество вещества — физическая величина, пропорциональная числу структурных единиц, содержащихся в данной порции вещества.
Другими словами, химическое количество вещества — это порция данного вещества, содержащая определенное число его структурных единиц. Химическое количество вещества обозначают латинской буквой n . Это одна из семи основных физических величин Международной системы единиц (СИ).
Моль — единица химического количества вещества
Каждая из основных физических величин имеет свою единицу. Например, единица длины — метр (м), массы — килограмм (кг), времени — секунда (с). Единицей химического количества вещества является моль.
Моль — порция вещества (т. е. такое его химическое количество), которая содержит столько же структурных единиц, сколько атомов содержится в углероде массой 0,012 кг.
Сокращенное обозначение единицы химического количества записывается, как и полное, — моль. Поэтому, если слово «моль» стоит после числа, то оно не склоняется, так же, как и другие сокращенные единицы величин: 3 кг, 5 л, 8 моль. При чтении вслух и при записи числительного буквами слово «моль» склоняется: три килограмма, пять литров, восемь молей.
На заметку. Термины «молекула» и «моль», как нетрудно заметить, однокоренные. Они действительно произошли от одного и того же латинского слова «moles». Но это слово имеет, по крайней мере, два значения. Первое — «маленькая масса». Именно в этом смысле в XVII в. оно превратилось в термин «молекула». А понятие «моль» (в смысле кучка, порция) появилось значительно позже, в начале ХХ в. Автор этого термина известный немецкий химик и физик Оствальд толковал его смысл как «большая масса», как бы противопоставляя термину «молекула».
получила название постоянной Авогадро. Она является одной из важнейших универсальных постоянных и обозначается символом NA :
Единица в числителе дроби (1/моль) заменяет название структурной единицы.
если 1 моль вещества содержит 6,02·10 23 молекул, то n моль вещества содержат N(Х) молекул.
И наоборот, по числу структурных единиц можно рассчитать химическое количество вещества:
Пример 1. Определите число молекул, содержащихся в серной кислоте химическим количеством 3 моль.
Пример 2. Рассчитайте химическое количество CuSO4 в порции, содержащей 36,12·10 23 формульных единиц (ФЕ).
Краткие выводы урока:
Надеюсь урок 8 «Химическое количество вещества и моль» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Основные структурные единицы
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
Филиал ФБГОУ ВПО Московского государственного университета технологий и управления имени К.Г. Разумовского
В Ростове-на-Дону
Кафедра химии и биологии
Бинеев Э.А.
ХИМИЯ
Печатается по решению кафедры химии и биологии
Филиала МГУТУ в г. Ростове-на-Дону
Протокол № 1 от 26.08.2014 г.
Химия. Конспект лекций (электронная версия). Ростов н/Д, 2014. – 25 с.
Конспект лекций предназначается для студентов заочной формы обучения направления 15.03.02 «Технологические машины и оборудование».
Основные структурные единицы
Под структурными единицами подразумеваются те «кирпичики», из которых строится вещество. Основными структурными единицами являются электрон, атом, молекула, ион. Атомы, молекулы, ионы переходят друг в друга с помощью валентных электронов.
Атом – наименьшая электронейтральная частица химического элемента, сохраняющая его химические свойства. Атом состоит из положительно заряженного ядра, вокруг которого по определенным орбитам вращаются электроны. Ядро атома состоит из протонов и нейтронов. Свойства элементарных частиц, из которых состоит атом, приведены в таблице 1.
Свойства элементарных частиц, образующих атомы
Так как заряд электрона является минимальной величиной заряда, то этот заряд принят за (-1). И оказалось, что число протонов в ядре, а, следовательно, и
число электронов в атоме, равно порядковому номеру элемента в таблице Менделеева.
В современной модели атома состояние в нем электрона определяется четырьмя параметрами – квантовыми числами:главным (n), побочным или орбитальным (l), магнитным (m) и спиновым (s). Сочетание первых трех квантовых чисел (n, l, m) показывает, где в данный момент времени находится электрон в околоядерном пространстве, а спиновое (s) является собственной характеристикой электрона. Оно может принимать только два значения. Электроны, находящиеся на внешних орбитах (атомных орбиталях, энергетических уровнях) различных атомов, могут взаимодействовать при столкновении этих атомов. В результате этого электроны, называемые валентными, «обслуживают» ядра всех взаимодействующих атомов. Такое состояние энергетически выгодно. Между атомами возникает химическая связь, и они создают молекулу. Таким образом, химическая связь между атомами возникает за счет взаимодействия электронов внешних орбит атомов. Следовательно, молекула– наименьшая частица данного вещества, обладающая его химическими свойствами. Молекула состоит из атомов, между которыми существует химическая связь. Химические свойства молекулы определяются ее составом (атомами) и строением (химическими связями).
Ион – отрицательно или положительно заряженная частица. Для получения положительно заряженного иона от атома надо «оторвать» валентные электроны. Для получения отрицательного иона надо на внешнюю орбиту атома добавить электроны до завершения этой орбиты. Ионы могут быть получены и при распаде молекул. Например, про растворении в воде электронейтральные молекулы электролитов распадаются на положительно и отрицательно заряженные ионы.
Различают простые и сложные вещества. Простое вещество состоит из атомов одного элемента. Например, железо состоит из атомов Fe; кислород состоит из молекул O2, состоящих из атомов O.
Сложное вещество состоитиз атомов разных элементов. Например вода состоит из молекул H2O, состоящих из атомов H и O.
Значения относительных атомных масс приведены в периодической системе элементов.
Относительная молекулярная масса М0 –масса молекулы, выраженная в а.е.м. Например, относительная молекулярная масса воды:
Относительную молекулярную массу можно вычислить по сумме произведений относительных атомных масс атомов на их число в молекуле:
Число структурных единиц вещества определяется физическим параметром, который называется количеством вещества. Единицей измерения количества вещества является моль.
Один моль – это количество вещества, в котором содержится столько же структурных единиц, сколько атомов содержится в 0,012 кг изотопа углерода 12 C.
Зная абсолютную массу атома углерода можно рассчитать, сколько атомов углерода содержится в 0,012 кг 12 C или в 1 моле любого вещества:
Число NA = 6,02 ∙ 10 23 называется числом Авогадро. Таким образом,
1 моль любого вещества содержит 6,02 ∙ 10 23 штук структурных единиц, из которых состоит данное вещество.NA не зависит ни от природы вещества, ни от агрегатного состояния.
Масса одного моля вещества называется молярной массой (M)и определяется частным от деления массы вещества (m) на его количество (n):
Размерность молярной массы: г/моль, или кг/моль.
Важно помнить, что молярная масса M, выраженная в г/моль, численно равна относительной молекулярной массе М0, а следовательно её можно вычислить по сумме произведений относительных атомных масс атомов на их число в молекуле. Например:
М(H2O) = 2∙ A0(Н) + 1∙ A0(О) = 2 ∙ 1 + 1 ∙ 16 = 18 г/моль.
Количество вещества
Содержание:
Количество вещества — физическая величина, характеризующая количество однотипных структурных единиц, содержащихся в веществе. Под структурными единицами понимаются любые частицы, из которых состоит вещество (атомы, молекулы, ионы, электроны или любые другие частицы).
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Количество вещества
Химическое количество вещества — физическая величина, пропорциональная числу структурных единиц, содержащихся в данной порции вещества.
Относительная атомная и молекулярная масса:
Часто при решении расчетных задач по химии приходится вычислять массу, объем реагирующих веществ или продуктов реакций. Кроме этих величин, в химии используется также величина количество вещества. Как измеряют количество вещества?
Каждое вещество состоит из огромного числа частиц, поэтому для удобства была выбрана единица измерения, содержащая большое число частиц, – моль. Моль – мера количества вещества (атомов, молекул, ионов), обозначается греческой буквой 
Из курса физики вам знакомо число Авогадро:
В одном моль любого вещества число структурных единиц равно числу Авогадро.
Масса одного моль вещества называется молярной массой, обозначается буквой М. Молярная масса вещества (г/моль) численно равна относительной молекулярной массе вещества.
Рассмотрите внимательно таблицу 7. Из нее видно, что в 18 г воды, 44 г углекислого газа, 23 г Na содержится столько же структурных единиц, сколько содержится в 12 г атома углерода.
Моль – мера количества вещества, в котором содержится столько структурных единиц, сколько атомов содержится в 12 граммах углерода.
При решении расчетных задач по химии удобно пользоваться этой единицей измерения. Допустим, вам нужно определить число молекул в два моль воды.
Для этого составляется пропорция: первая часть – по определению, а вторая – по условию задачи.
Для решения этой задачи можно использовать формулы
Моль, количество вещества, молярная масса, число Авогадро.
Взаимосвязь массы, молярной массы и количества вещества
Из пройденного материала вам известны такие формулы:
Объединив формулы (1) и (2), можно получить:
А. Определение массы вещества по количеству вещества.
Рассчитайте массу воды количеством вещества 2 моль.

B. Определение количества вещества по его массе.
Сколько молей составляет 176 г углекислого газа?

C. Расчет числа структурных единиц.
Рассчитайте число структурных частиц, которое содержат 2 моль элемента
водорода, 3 моль газообразного водорода, 5 моль серной кислоты.
В молекуле 
D. Расчет молярной массы вещества.
Рассчитайте молярную массу вещества, если 1,204 · 1024 молекул вещества весит 160 г.

Услуги по химии:
Лекции по химии:
Лекции по неорганической химии:
Лекции по органической химии:
Присылайте задания в любое время дня и ночи в ➔ 
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
§ 4. Количественные характеристики вещества
| Сайт: | Профильное обучение |
| Курс: | Химия. 11 класс |
| Книга: | § 4. Количественные характеристики вещества |
| Напечатано:: | Гость |
| Дата: | Среда, 29 Декабрь 2021, 21:08 |
Оглавление
Наука начинается с тех пор, как начинают измерять.
Точная наука немыслима без меры.
Свойства веществ, которые можно оценить количественно, с помощью чисел, называются физическими величинами.
Величины, характеризующие массу частиц вещества (Аr, Мr, ma) или содержание вещества в смеси (массовая доля ω(в-ва), объёмная доля φ(в-ва)), мы рассмотрели в предыдущих параграфах. Некоторые величины (объём V, плотность ρ, масса m) подробно изучались в курсе физики.
В данном параграфе более детально рассмотрим особенности одной из семи основных физических величин Международной системы единиц СИ — количество вещества, также известной вам по предыдущим годам изучения химии и физики.
Количество вещества (химическое количество)
Вещества участвуют в химических реакциях в определённых количественных соотношениях.
Чтобы установить взаимосвязь числа взаимодействующих частиц с массой и объёмом, ввели физическую величину — количество вещества.
Количество вещества (химическое количество) — это физическая величина, равная отношению числа структурных единиц, составляющих его порцию, к постоянной Авогадро.
Условное обозначение количества вещества — n, единица величины — 1 моль. Количество вещества характеризует число любых конкретных частиц (атомов, молекул, ионов, формульных единиц) в данной порции.
Моль — это единица количества вещества (химического количества).
1 моль — количество вещества, которое содержит 6,02 ∙ 10 23 структурных единиц вещества (атомов, молекул, ионов или формульных единиц).
Количество вещества в некоторой порции можно рассчитать делением числа всех частиц на число частиц, содержащихся в 1 моль вещества:
Таким образом, вводя единицу измерения 1 моль, переходим от рассмотрения взаимодействия отдельных частиц к рассмотрению взаимодействия порций веществ.
Использование единицы измерения количества вещества позволяет взвешивать вещества определёнными порциями количеством 1 моль или несколько молей. Масса одного моля вещества численно равна молярной массе М. Её также можно рассчитать делением массы порции вещества m на его химическое количество (число молей):
Таким образом, молярная масса — величина, равная отношению массы порции вещества к его химическому количеству.
Зная требуемое для химической реакции количество вещества, легко рассчитать его массу по формуле:
Помимо молярной массы, каждое вещество имеет молярный объём Vm, то есть объём вещества количеством 1 моль.
Молярный объём газа Vm — величина, равная отношению объёма данной порции вещества V(Х) к его химическому количеству n(Х) в этой порции:
Молярный объём твёрдых веществ и жидкостей зависит от их плотности. Молярный объём воды, кислоты, металла и соли различен, потому что их плотности тоже отличаются (рис. 8). Молярный объём вещества можно также рассчитать, применив известную формулу :
где ρ — плотность вещества.
Например, молярный объём уксусной кислоты:
Рассчитаем молярный объём двух произвольно выбранных газов — азота и метана (при нормальных условиях):
Равенство объёмов разных газов количеством 1 моль, измеряемых в одних и тех же условиях, объясняется одинаковым числом молекул в случае обоих газов и одним и тем же расстоянием между молекулами. В газах, в отличие от жидких и твёрдых веществ, размеры молекул не оказывают значительного влияния на молярный объём.
Систематизируем важнейшие количественные характеристики вещества и их смесей ( табл. 3 ).
Таблица 3. Количественные характеристики вещества, порции вещества и вещества в смеси
| Количественные характеристики | |||||
| Вещество | Порция вещества | ||||
| Величина | Обозначение и единицы измерения | Величина | Обозначение и единицы измерения | ||
| Относительная молекулярная (формульная) масса | Mr | — | Масса | m | кг, г |
| Молярная масса | M | г/моль | Объём | V | м 3 |
| Молярный объём | Vm | дм 3 /моль | Количество вещества | n | моль |
| Плотность | ρ | кг/м 3 | Число структурных единиц (частиц) | N | — |
| Массовая доля элемента | ω | —; % | |||
| Вещество в смеси | |||||
| Массовая доля вещества | ω | —; % | Молярная концентрация вещества | с | моль/дм 3 |
| Объёмная доля вещества | φ | —; % | |||
Количество вещества (химическое количество) — это физическая величина, равная отношению числа структурных единиц, составляющих его порцию, к постоянной Авогадро.
Количество вещества может быть рассчитано по одной из трёх формул:
Вопросы, задания, задачи
2. Запишите названия физических величин, для измерения которых предназначено лабораторное оборудование, представленное на рисунке 9.
3. Рассчитайте количество углекислого газа (моль), содержащего 1,505 · 10 23 молекул.
4. Определите, какой объём (н. у.) занимает метан:
6. Рассчитайте массу молекул О2 и Н2О в а. е. м., граммах, килограммах.
7. Определите массу смеси, состоящей из 12 моль водорода и 8 моль азота.
10. Определите массовую долю углерода в смеси, состоящей из 3 моль углекислого и 5 моль угарного газов.
1. К количественным характеристикам вещества относят величины, обозначаемые символами:
2. Объём жидкости в лаборатории определяют с помощью:
3. Масса и объём (н. у.) порции кислорода количеством 0,2 моль равны:
4. Количество сжиженного азота массой 1,4 г равно:
5. Масса смеси, содержащей кислород О2 и озон О3 количеством 2 моль и 0,1 моль соответственно, равна: