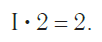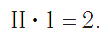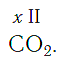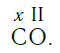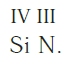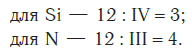Что такое валентность в химии 8 класс видеоурок
Письмо с инструкцией по восстановлению пароля
будет отправлено на вашу почту
В свое время, состав всех веществ был установлен на основании данных эксперимента. Однако можно составлять химические формулы, не прибегая к предварительному выполнению сложных опытов, требующих длительной, кропотливой работы.
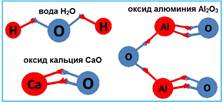
Если сравнить между собой формулы таких веществ, как вода H2O, оксид кальция СаО, оксид алюминия Al2O3, оксид углерода СО2, оксид фосфора Р2О5, оксид серы SО3 и оксид хлора Cl2О7, то можно заметить, что кислород во всех этих соединениях присоединяет к себе неодинаковое число атомов других химических элементов.
Для определения состава бинарных или двухэлементных, то есть состоящих из атомов двух химических элементов соединений, и составления их формул, достаточно знать валентность химических элементов.
Валентность (от латинского слова Valentia – «сила») – свойство атома химического элемента присоединять или замещать определённое число атомов другого химического элемента
Поскольку атомы в молекуле соединены между собой химическими связями, валентность определяется числом простых (одинарных) химических связей, которые данный атом образует с другими атомами.
Как это можно представить себе, если не прибегать к теории строения атома? Каждый атом имеет определенное число потенциальных химических связей – валентных возможностей.
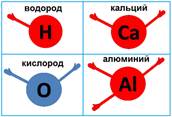
Например, водород – одну, кислород и кальций – по две, алюминий – три, углерод – четыре, фосфор – пять, сера – шесть, хлор – семь. Соединяться друг с другом эти атомы могут, только используя эти самые валентные возможности.
Поэтому атомы химических элементов и образуют соединения, подчиняясь закону постоянства состава.
Закон постоянства состава утверждает, что вещества, независимо от нахождения в природе или способа получения их в лаборатории, всегда имеют один и тот же состав.
Способность элементов проявлять то или иное значение валентности определяется строением их атомов. Поскольку строение атомов обычно изучается позднее, научимся определять валентность, исходя из положения элементов в периодической системе.
Для этого следует учитывать, что каждая группа (вертикальный столбец) элементов состоит из двух подгрупп: главной А и побочной В.
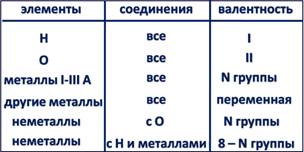
Элементы-металлы, располагающиеся в главных подгруппах I и II групп, проявляют постоянную валентность, равную номеру группы. Это же относится и к алюминию (III группа). А вот металлические элементы IV группы (главная подгруппа) олово и свинец служат исключением и проявляют переменную валентность, численно равную 2 и 4. Длямногих металлов побочных подгрупп также характерно наличие переменной валентности, однако высшее значение валентности обычно равно номеру группы!
Большая часть неметаллов, располагающихся в главных подгруппах групп с четвёртой по седьмую, проявляет переменную валентность. В ряду возможных значений валентностей неметаллов следует выделять высшую и низшую. Высшая валентность равна номеру группы, низшая – разности, полученной вычитанием числа, равного номеру группы, из числа 8. Например: высшая валентность элемента фосфора, стоящего в V группе, равна 5,
низшая: 8-5=3. Следовательно, валентность фосфора переменная – 3 и 5. Следует помнить, что высшая валентность неметаллов проявляется только в соединениях с кислородом, а низшая – в соединениях с металлами и водородом. Валентность водорода всегда во всех соединениях равна 1, валентность кислорода всегда 2.
Для составления формул сложных веществ, состоящих из атомов двух неметаллов, следует учитывать, что высшую валентность проявит тот элемент, который стоит в периодической системе левее или ниже, а низшую – соответственно тот, который стоит правее или выше.
Составляем формулы и названия веществ по валентности, используя следующий алгоритм:
1. записываем знаки элементов (по наличию) в порядке: металл, водород, неметалл, кислород;
2. расставляем значения валентностей элементов по периодической системе химических элементов;
3. находим наименьшее общее кратное значений валентностей (наименьшее число, которое делится на оба значения валентностей), делим его на валентность каждого элемента, получаем и записываем индекс;
4. называем вещество. К латинскому корню второго элемента прибавляем суффикс ид, указываем русское название первого элемента и его валентность, если она не постоянная.
Составим формулу и название для вещества, состоящего из атомов фосфора и кислорода:
1. записываем знаки Р и О;
2. валентность фосфора высшая, равна 5, валентность кислорода, как и во всех соединениях равна 2;
3. наименьшее общее кратное 10
10/5=2, пишем индекс у знака Р
10/2=5, пишем индекс у знака О
4. назовем вещество: корень латинского названия кислорода «оксигениум» окс, к нему прибавляем суффикс ид, получаем оксид. Русское название первого элемента – фосфор, валентность его переменная, равная 5. Получилось название «оксид фосфора 5».
Таким образом, при составлении названия вещества, имеющего определенную химическую формулу, необходимо указывать валентность, а чтобы ее указать, необходимо определить. По периодической системе это получается не всегда. Определить валентность и составить название веществаможно, используя алгоритм:
1. указать валентность известного элемента;
2. умножить указанную валентность на соответствующий индекс;
3. полученный результат делим на индекс элемента с неизвестной валентностью;
4. называем вещество. К латинскому корню второго элемента прибавляем суффикс ид, указываем русское название первого элемента и его валентность.
Определим валентность и составим название вещества, имеющего формулу CrO3:
1. валентность кислорода постоянна и равна 2;
3. 6/1=6. Валентность хрома равна 6;
4. название вещества – оксид хрома 6.
Теперь научимся составлять формулу по названию вещества
1. записываем знаки химических элементов в нужном порядке;
2. указываем валентности, обращая внимание на название. Если валентность первого элемента переменная, она будет указана. Валентность второго элемента – низшая;
3. находим наименьшее общее кратное значений валентностей (наименьшее число, которое делится на оба значения валентностей), делим его на валентность каждого элемента, получаем и записываем индекс.
Определим формулу оксида серы:
1. записываем знаки S и О.
2. валентность серы равна 4, валентность кислорода, как и во всех соединениях – два.
Урок 6. Валентность
В уроке 6 «Валентность» из курса «Химия для чайников» дадим определение валентности, научимся ее определять; рассмотрим элементы с постоянной и переменной валентностью, кроме того научимся составлять химические формулы по валентности. Напоминаю, что в прошлом уроке «Химическая формула» мы дали определение химическим формулам и их индексам, а также выяснили различия химических формул веществ молекулярного и немолекулярного строения.
Вы уже знаете, что в химических соединениях атомы разных элементов находятся в определенных числовых соотношениях. От чего зависят эти соотношения?
Рассмотрим химические формулы нескольких соединений водорода с атомами других элементов:
Нетрудно заметить, что атом хлора связан с одним атомом водорода, атом кислорода — с двумя, атом азота — с тремя, а атом углерода — с четырьмя атомами водорода. В то же время в молекуле углекислого газа СО2 атом углерода связан с двумя атомами кислорода. Из этих примеров видно, что атомы обладают разной способностью соединяться с другими атомами. Такая способность атомов выражается с помощью численной характеристики, называемой валентностью.
Валентность — численная характеристика способности атомов данного элемента соединяться с другими атомами.
Поскольку один атом водорода может соединиться только с одним атомом другого элемента, валентность атома водорода принята равной единице. Иначе говорят, что атом водорода обладает одной единицей валентности, т. е. он одновалентен.
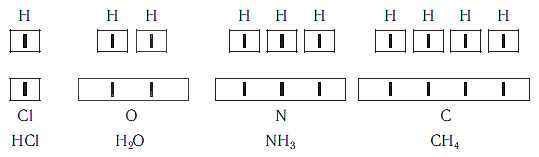
Валентность атома какого-либо другого элемента равна числу соединившихся с ним атомов водорода. Поэтому в молекуле HCl у атома хлора валентность равна единице, а в молекуле H2O у атома кислорода валентность равна двум. По той же причине в молекуле NH3 валентность атома азота равна трем, а в молекуле CH4 валентность атома углерода равна четырем. Если условно обозначить единицу валентности черточкой |, вышесказанное можно изобразить схематически:
Следовательно, валентность атома любого элемента есть число, которое показывает, со сколькими атомами одновалентного элемента связан данный атом в химическом соединении.
Численные значения валентности обозначают римскими цифрами над символами химических элементов:
Определение валентности
Однако водород образует соединения далеко не со всеми элементами, а вот кислородные соединения есть почти у всех элементов. И во всех таких соединениях атомы кислорода проявляют валентность, равную двум. Зная это, можно определять валентности атомов других элементов в их бинарных соединениях с кислородом. (Бинарными называются соединения, состоящие из атомов двух химических элементов.)
Чтобы это сделать, необходимо соблюдать простое правило: в химической формуле вещества суммарные числа единиц валентности атомов каждого элемента должны быть одинаковыми.
Так, в молекуле воды H2O общее число единиц валентности двух атомов водорода равно произведению валентности одного атома на соответствующий числовой индекс в формуле:
Так же определяют число единиц валентности атома кислорода:
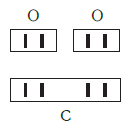
По величине валентности атомов одного элемента можно определить валентность атомов другого элемента. Например, определим валентность атома углерода в молекуле углекислого газа СО2:
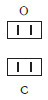
Существует и другое соединение углерода с кислородом — угарный газ СО, в молекуле которого атом углерода соединен только с одним атомом кислорода:
Постоянная и переменная валентность
Как видим, углерод соединяется с разным числом атомов кислорода, т. е. имеет переменную валентность. У большинства элементов валентность — величина переменная. Только у водорода, кислорода и еще нескольких элементов она постоянна (см. таблицу).
Составление химических формул по валентности
Зная валентность элементов, можно составлять формулы их бинарных соединений. Например, необходимо записать формулу кислородного соединения хлора, в котором валентность хлора равна семи. Порядок действий здесь таков.
Записываем рядом символы элементов в следующем виде:
Затем находим НОК валентностей обоих элементов. Оно равно 12 ( IV·III ).
Определяем индексы каждого элемента:
Записываем формулу соединения: Si3N4.
В дальнейшем при составлении формул веществ не обязательно указывать цифрами значения валентностей, а необходимые несложные вычисления можно выполнять в уме.
Краткие выводы урока:
Надеюсь урок 6 «Валентность» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок химии в 8-м классе по теме: «Валентность. Определение валентности по формулам»
Разделы: Химия
Цели урока.
Понятия, впервые вводимые на уроке: валентность, постоянная и переменная валентность.
Организационные формы: беседа, индивидуальные задания, самостоятельная работа.
Средства обучения: алгоритм определения валентности.
Демонстрационное оборудование: шаростержневые модели молекул хлороводорода, воды, аммиака, метана.
Оборудование для учащихся: на каждом столе “Алгоритм определения валентности”.
Опережающее задание: индивидуальное задание – подготовить сообщение на тему “Эволюция понятия “валентность”.
Ход урока
I. Ориентировочно-мотивационный этап.
1. Фронтальная беседа с учащимися по пройденной теме “Химическая формула”.
Задание: Что здесь написано? (Демонстрация учителем формул, отпечатанных на отдельных листах).
2. Индивидуальная работа по карточкам трёх учащихся по теме “Относительная молекулярная масса”. (Выполняют решение на доске). Проверка учителем.
Карточка № 1. Рассчитайте относительную молекулярную массу данных веществ: NaCl, K2O.
Карточка № 2. Рассчитайте относительную молекулярную массу данных веществ: CuO, SO2.
Карточка № 3. Рассчитайте относительную молекулярную массу данных веществ: CH4, NO.
3. Самостоятельная работа учащихся в тетрадях.
Задача информационно-вычислительного характера (условие записано в раздаточном материале).
Эффективность зубных паст в профилактике кариеса можно сравнить по содержанию в них активного фтора, способного взаимодействовать с зубной эмалью. Зубная паста “Crest” (производство США) содержит, как указано на упаковке, SnF2, а зубная паста “FM extra DENT” (производство Болгария) содержит NaF. Вычислите, какая из этих двух паст более сильнодействующее средство для профилактики кариеса.
Проверка: один учащийся устно читает решение.
II. Операционно-исполнительный этап.
1. Объяснение учителя. Постановка проблемы.
Понятие о валентности.
– До сих пор мы пользовались готовыми формулами, приведёнными в учебнике. Химические формулы можно вывести на основании данных о составе веществ. Но чаще всего при составлении химических формул учитываются закономерности, которым подчиняются элементы, соединяясь между собой.
Беседа с учащимися:
– Что общего в составе молекул?
Предполагаемый ответ: Наличие атомов водорода.
– Чем они отличаются друг от друга?
Демонстрация шаростержневых моделей.
Проблема: Почему различные атомы удерживают различное количество атомов водорода?
(Выслушиваем варианты ответов учащихся).
Вывод: У атомов разная способность удерживать определённое количество других атомов в соединениях. Это и называется валентностью. Слово “валентность” происходит от лат. valentia – сила.
Валентность – это свойство атомов удерживать определённое число других атомов в соединении.
Валентность обозначается римскими цифрами.
Записи на доске и в тетрадях:
I I
HCl
H2O
H3N
H4C
Валентность атома водорода принята за единицу, а у кислорода – II.
2. Эволюция понятия “валентность” (сообщение учащегося).
– В начале XIX века Дж. Дальтоном был сформулирован закон кратных отношений, из которого следовало, что каждый атом одного элемента может соединяться с одним, двумя, тремя и т.д. атомами другого элемента (как, например, в рассмотренных нами соединениях атомов с водородом).
В середине XIX века, когда были определены точные относительные веса атомов (И.Я. Берцелиус и др.), стало ясно, что наибольшее число атомов, с которыми может соединяться данный атом, не превышает определённой величины, зависящей от его природы. Эта способность связывать или замещать определённое число других атомов и была названа Э.Франклендом в 1853 г. “валентность”.
Поскольку в то время для водорода не были известны соединения, где он был бы связан более чем с одним атомом любого другого элемента, атом водорода был выбран в качестве стандарта, обладающего валентностью, равной 1.
В конце 50-х гг. XIX вeка А.С. Купер и А.Кекуле постулировали принцип постоянной четырёхвалентности углерода в органических соединениях. Представления о валентности составили важную часть теории химического строения А.М. Бутлерова в 1861 г.
Периодический закон Д.И. Менделеева в 1869 г. вскрыл зависимость валентности элемента от его положения в периодической системе.
Вклад в эволюцию понятия “валентность” в разные годы внесли В.Коссель, А.Вернер, Г.Льюис.
Начиная с 30-х гг. XX века представления о природе и характере валентности постоянно расширялись и углублялись. Существенный прогресс был достигнут в 1927 г., когда В.Гейтлер и Ф.Лондон выполнили первый количественный квантово-химический расчёт молекулы водорода H2.
3. Определение валентности атомов элементов в соединениях.
Правило определения валентности: число единиц валентностей всех атомов одного элемента равно числу единиц валентности всех атомов другого элемента.
Алгоритм определения валентности.
Алгоритм определения валентности
Пример
H2S,
II
Cu2O
I
H2S
2
II
Cu2O
I II
H2S
2
I II
Cu2O
H2S
(2=2)
Cu2O
(2=2)
4. Упражнение: определить валентность элементов в веществах (тренажёр: ученики цепочкой выходят к доске). Задание в раздаточном материале.
III. Оценочно-рефлексивный этап.
Первичная проверка усвоения знаний.
Проверка выборочная. Консультант из числа учащихся по готовому шаблону проверяет 4 тетради учащихся.
Работа над ошибками. Ответы на обратной стороне доски.
IV. Подведение итогов урока.
Оценка работы учащихся в целом и отдельных учащихся.
Домашнее задание: § 4, стр. 23–25, упр. на стр. 25.
Урок химии «Валентность химических элементов» (8 класс)
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Тема урока. ВАЛЕНТНОСТЬ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ.
Тип урока: комбинированный урок.
Цель урока: сформировать понятие валентность и умение определять валентность по химическим формулам.
Образовательные: познакомить учащихся с понятием валентность; сформировать и закрепить умение определять валентность по химическим формулам.
Воспитательные: показать единство материального мира.
Развивающие: приобретение навыков самостоятельной работы.
Основные понятия темы: валентность, индекс, постоянная и переменная валентность, бинарное соединение.
Методы и приемы: фронтальная беседа, индивидуальная, самостоятельная работа.
Проверка домашнего задания.
— Какие по составу вещества вам известны? (Простые и сложные).
— Чем различаются простые и сложные вещества? (Количеством входящих в них элементов).
-Что такое химическая формула? (Химическая формула – это запись, выражающая качественный и количественный состав данного вещества).
— Что называют индексом? (Индекс обозначает число атомов элемента, входящих в состав данного вещества).
-Какую информацию можно получить о веществе по его химической формуле? (Качественный состав – это какие элементы входят в состав данного вещества, а количественный – в каком соотношении).
— Что необходимо для того, чтобы вывести химическую формулу вещества? (Необходимо знать массовые доли химических элементов).
Индивидуальное задание. (Выполняется на доске учащимся).
Выведите простейшую формулу соединения, в котором массовая доля натрия равна 32,4%, серы – 22,5%, кислорода – 45,1%.
Из условия задачи следует, что в 100 единицах массы вещества 32,4 единицы натрия, 22,5 единицы серы и 45,1 единицы кислорода. Находим число атомов каждого элемента в 100 единицах вещества:
32,4 : 23 = 1,4 атома натрия
22,5 : 32 = 0,7 атома серы
45,1 : 16 = 2,8 атома кислорода
Следовательно, можно определить соотношение чисел атомов в формуле вещества:
x : y : z = 1,4: 0,7 : 2,8 = 2: 1: 4
Числовые индексы в химических формулах указывают на то, что атомы соединяются друг с другом не произвольно, а в определенных соотношениях.
А как же узнают состав каждого вещества? С помощью сложных экспериментов. Однако на практике для составления химических формул веществ часто опираются на закономерности элементов, с которыми вы сегодня познакомитесь на уроке. Запишите тему урока в тетрадях.
Обсуждение качественного и количественного состава этих веществ.
В молекуле HCl атом хлора удерживает один атом водорода, в молекуле H 2 O атом кислорода удерживает два атома водорода, в молекуле NH 3 атом азота удерживает три атома водорода, в молекуле CH 4 атом углерода удерживает четыре атома водорода.
Проблемный вопрос. Почему атомы разных элементов удерживают неодинаковое число атомов водорода?
Изучение нового материала.
Свойство атомов удерживать при себе определенное число атомов называется валентностью. Зная валентность можно составить формулу любого вещества. Итак, запишем, что же такое валентность:
Валентность – это способность атомов удерживать при себе определенное число атомов других элементов.
HCl – атом хлора удерживает один атом водорода, значит, хлор одновалентен.
H 2 O – атом кислорода удерживает два атома водорода, значит, кислород двухвалентен.
NH 3 – атом азота удерживает три атома водорода, следовательно, азот трехвалентен.
CH 4 – атом углерода удерживает четыре атома водорода, следовательно, углерод четырехвалентен.
Валентность обозначается римской цифрой, которая ставится над знаком химического элемента в формуле вещества.
Атомы одних химических элементов имеют постоянную валентность, а других переменную.
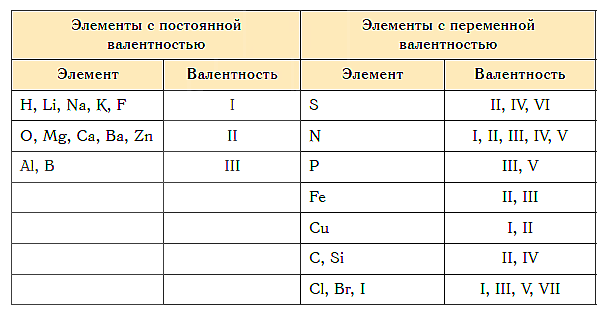
Водород и фтор всегда одновалентны, а кислород – двухвалентен. Другие элементы с постоянной валентностью находятся в I – III группах периодической системы, причем значение валентности каждого элемента совпадает с номером группы. Например, элемент I группы натрий одновалентен, элемент II группы кальций двухвалентен, а элемент III группы алюминий трехвалентен. Исключениями являются элементы I группы медь (значение валентности – 1 и 2) и золото (1 и 3).
Большинство элементов имеют переменную валентность (т.е. в разных соединениях один и тот же элемент может проявлять разную валентность).
В учебнике на странице 56 в таблице 3 приведены значения валентности некоторых химических элементов в соединениях. Назовите элементы с переменной валентностью.
Зная формулы веществ, состоящих из двух элементов, и валентность одного из них, можно определить валентность другого элемента.
Запишем правила определения валентности по формулам бинарных соединений (т.е соединений, состоящих из двух атомов).
Правила определения валентности элементов в соединениях ( алгоритм определения валентности по формуле бинарного соединения (§ 16 с.57- 58)):
1. Записать химическую формулу вещества и указать валентность известного элемента.
2. Найти наименьшее общее кратное (НОК) между известным значением валентности и индексом этого элемента.
Для этого умножаем валентность известного элемента на индекс при этом элементе:
2 × II = 4 – это и есть НОК
3. Наименьшее общее кратное разделить на индекс другого элемента, полученное число и есть значение валентности. Индекс при атоме углерода равен 1, значит:
4 : 1 = IV – это и есть валентность атома углерода.
Разберем еще один пример:
3. 6 : 2 = III – это и есть валентность атома железа.
Закрепление изученного материала.
Выполняются задания по карточкам ( Приложение 2 ).
Определите валентность элементов в соединениях с кислородом:
Определите валентность элементов в соединениях с водородом:
Определите валентность элементов в следующих соединениях:
Выполните тестовые задания из учебника (с. 58).