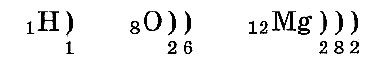Что такое валентный слой
Ключевые слова конспекта: строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева, завершенный электронный слой, валентный слой, энергетические уровни, правило октета, орбиталь,
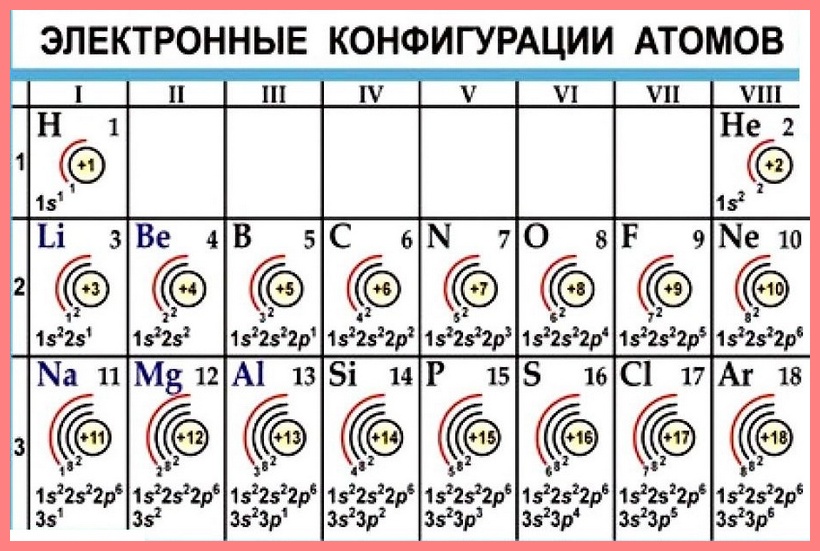
Электронная оболочка атома — это все электроны атома. Электроны в электронной оболочке атома расположены слоями. Электроны в разных слоях различаются энергией взаимодействия с ядром атома. Чем дальше от ядра находится электрон, тем меньше энергия его взаимодействия с ядром.
Вместимость электронных слоев различная. В слое № 1, или в первом слое, у всех элементов, кроме водорода, находится 2 электрона. (В атоме водорода всего 1. электрон, и он — в первом слое.) Во втором слое может находиться не больше восьми электронов. В третьем слое максимально может расположиться 18 электронов. В четвертом слое максимально бывает 32 электрона.
Завершенный электронный слой — это слой в атоме, содержащий максимально возможное для него число электронов.
Электронные слои заполняются так: сначала первый, потом второй и последующие — по мере уменьшения энергии их взаимодействия с ядром. Расположение по слоям электронов в атомах водорода, кислорода и магния:
Число электронных слоев атома равно номеру периода химического элемента в таблице Менделеева. Поэтому у атома водорода один электронный слой, у кислорода — два слоя, а у магния — три слоя.
Валентный слой — это внешний электронный слой. У водорода это 1-й слой, у кислорода — 2-й слой, у магния — 3-й слой. Валентные электроны — это электроны внешнего слоя. Внешний слой всегда содержит не больше восьми электронов. Восьми-электронный внешний слой характеризуется повышенной устойчивостью. (Это — «правило октета».)
Зная максимальное число электронов в каждом электронном слое атома, можно составить схему расположения электронов по слоям в заданном элементе. Электронные слои атомов называют энергетическими уровнями.
Химические свойства атомов определяются свойствами их электронов. Движение электронов в атоме описывают с привлечением понятия орбитали. Каждый электрон в атоме находится на своей орбитали.
Орбиталь — это часть электронного облака, создаваемого электронами при движении в атоме. Орбиталь — это пространство около ядра, где чаще всего находится электрон.
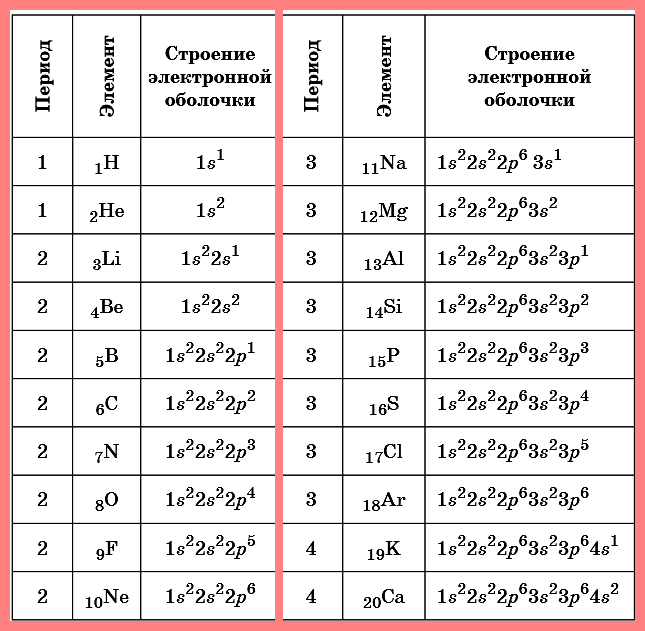
Таблица. Строение электронных оболочек атомов
первых 20 элементов Периодической системы Д.И. Менделеева
Фтор — элемент 2-го периода, т.к. в его электронной формуле два электронных слоя. Сумма всех надстрочных индексов — 9 (общее число электронов), это и атомный номер фтора. Элементы, у которых очередные электроны помещаются на s- и р-орбиталях, относятся к главным подгруппам таблицы Менделеева. Сумма электронов 2-го внешнего слоя дает номер группы — VII.
Конспект урока «Строение электронных оболочек атомов».
Другим элементам необходимо создать химические связи, чтобы получить недостающие электроны и достичь восьми электронов валентной оболочки.
Слои электросферы
Согласно модели атома Резерфорда-Бора, электроны вращаются вокруг ядра атома в разных энергетических слоях.
Существует семь слоев, обозначенных буквами K, L, M, N, O, P и Q. Каждый из них поддерживает максимальное количество электронов.
Электронные слои и количество поддерживаемых ими электронов
Читайте тоже:
Как определить слой Валенсии?
Электронная раздача
Для определения валентного слоя посредством электронного распределения используется диаграмма Линуса Полинга.
1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 14 6d 10 7p 6
Примеры :
Также прочтите о квантовых числах.
До сих пор использовавшиеся примеры касались фундаментальных элементов. Но тот же принцип можно использовать для ионов, катионов и анионов. См. Пример:
Сначала сделайте электронное распределение для элемента Хлор:
1с 2 2с 2 2п 6 3с 2 3п 5
Получив еще один электрон, добавьте в последний слой:
См. Также: Упражнения по электронной рассылке.
Периодическая таблица
Чтобы определить валентный слой с помощью таблицы Менделеева, необходимо определить период и семейство элемента.
Таким образом, в то время как семейство 1A имеет 1 валентный электрон, 2A имеет 2 и так далее. Химические элементы в одном семействе периодической таблицы имеют одинаковое количество электронов в валентной оболочке.
Однако это действительно только для групп 1, 2, 13, 14, 15, 16 и 17, которые имеют следующие номера электронов в валентном слое 1, 2, 3, 4, 5, 6 и 7 соответственно.
Для элементов, в которых эта взаимосвязь невозможна, следует использовать электронное распространение.
Не забудьте! Химические связи возникают из-за необходимости стабилизировать атомы и, таким образом, образовывать молекулы. Это происходит за счет донорства электронов от валентной оболочки, которые, поскольку находятся дальше от ядра, склонны отдавать.
Также прочтите о молекулярной геометрии.
Упражнения
1. Найдите валентный слой следующих элементов:
Бром
1с 2 2с 2 2п 6 3с 2 3п 6 4с 2 3d 10 4п 5
Валентный слой Bromo (семейство 7A) имеет 7 электронов. Это потому, что 4s 2 и 4p 5 принадлежат слою N, а 3d 10 принадлежит слою M.
Алюминий
1с 2 2с 2 2п 6 3с 2 3п 1
Валентный слой алюминия (семейство 3A) имеет 3 электрона.
2. (UFSC) Число электронов на каждом подуровне атома стронция ( 38 Sr) в порядке возрастания энергии составляет:
a) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2
b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 4p 6 3d 10 5s 2
c) 1s 2 2s 2 2p 6 3s 2 3п 6 3д 10 4с 2 4п 6 5с 2
г) 1с 2 2s 2 2p 6 3s 2 3p 6 4p 6 4s 2 3d 10 5s 2
e) 1s 2 2s 2 2p 6 3p 6 3s 2 4s 2 4p 6 3d 10 5s 2
а) 1с 2 2с 2 2п 6 3с 2 3п 6 4с 2 3d 10 4п 6 5с 2
3. (IFSP / 2013) Число электронов в валентной оболочке атома кальция (Z = 20) в фундаментальном состоянии равно
Проверьте вестибулярные нарушения с комментариями к разрешению: Упражнения на периодическую таблицу.
Что такое валентный слой?
валентный слой это самый внешний слой (или уровень) (самый дальний от ядра) атома, то есть самый дальний от ядра. Следовательно, он имеет так называемые внешние электроны или валентные электроны.
Количество уровней, которые может иметь атом, варьируется от 1 до 7, которые имеют следующие подуровни (отмечены желтым цветом):
уровень К (1-й слой): подуровень s
уровень L (2-й слой): подуровни s а также п
уровень Q (1-й уровень): подуровни s а также п
На каждом из подуровней находится разное количество электронов. Посмотрите:
подуровень s содержит максимум 2 электрона;
подуровень p содержит максимум 6 электронов;
подуровень d содержит максимум 10 электронов;
подуровень f содержит максимум 14 электронов.
Таким образом, если валентная оболочка определенного атома равна M, максимальное количество электронов, которое может в нем присутствуют 18 (2 электрона с подуровня s + 6 электронов с подуровня p + 10 электронов с подуровня подуровень г).
Определить валентную оболочку атома и количество электронов в ней можно двумя способами, а именно:
→ Определение валентной оболочки и количества электронов в ней по электронному распределению
Представление диаграммы Линуса Полинга
Обычный атомный номер (который указывает количество электронов в атоме), мы делаем электронное распределение. Например, атом с атомным номером 50:
Электронное распределение атома с атомным номером 50
Анализируя приведенное выше распределение, мы видим, что наиболее удаленным от ядра уровнем является 5-й (уровень N), на котором мы имеем присутствие 4 электронов (два на подуровне s и 2 на подуровне p).
→ Определение валентной оболочки и количества электронов в ней по Периодической таблице
Таблица разбита на периоды (горизонтальные столбцы), которые указывают количество уровней атома, и группы или семейства (вертикальные столбцы). Период используется для определения валентный слой, а семейства используются для определения числа электронов.
а) Зная период химического элемента
В Периодической таблице представлено всего семь периодов, количество которых связано с количеством уровней, присутствующих на диаграмме Линуса Полинга. Итак, если мы знаем период, в который химический элемент он находится в таблице, автоматически мы знаем, сколько уровней имеют ваши атомы, причем валентный слой является наиболее удаленным от ядра уровнем.
1-й пример: химический элемент Калий
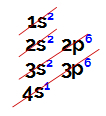
Электронное распределение элемента калия
2-й пример: химический элемент Фтор
Фтор находится во втором периоде Периодической таблицы, поэтому его атом имеет два уровней, вторым уровнем является валентный слой, что подтверждается его распределением электроника.

Электронное распределение элемента фтора
3-й пример: химический элемент индий
Не останавливайся сейчас. После рекламы есть еще кое-что;)
Электронное распределение элемента индия
б) Знание семейства или группы химического элемента
Зная семейство или группу, в которой расположен элемент, мы также знаем количество электронов, присутствующих в валентной оболочке этого элемента.
Элементы семейства А
Элементы семейств A расположены в столбцах 1, 2, 13–18 Периодической таблицы. Каждый из этих столбцов получает число (от 1 до 8, римская цифра), которое указывает точное количество электронов в валентной оболочке этих элементов:
См. Несколько примеров определения количества валентных электронов некоторых элементов семейства A:
Пример 1: химический элемент барий
Барий относится к семейству IIA, поэтому он имеет два электрона в валентной оболочке, что подтверждается его электронным распределением:
Электронное распределение элемента бария
Пример 2: Химический элемент сурьмы
Сурьма относится к семейству VA, поэтому в валентной оболочке у нее пять электронов, что подтверждается ее электронным распределением:
Электронное распределение элемента сурьмы
Пример 3: Ксенон химический элемент
Ксенон относится к семейству VIIIA, поэтому он имеет восемь электронов в валентной оболочке, что подтверждается его электронным распределением.
Электронное распределение ксенонового элемента
Электронное распределение атома гелия
Элементы семейства B
Элементы семейств B расположены в столбцах с 3 по 12 Периодической таблицы. Помимо семейств A, есть также восемь семейств B, которые представлены римскими цифрами. В отличие от семейств A, число семейств B не определяет количество электронов в валентной оболочке.
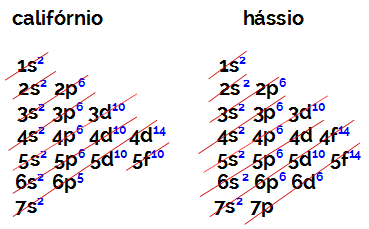
Число электронов в валентной оболочке элемента семейства B всегда равно 2, независимо от атомного номера и положения в таблице. Электронные распределения калифорния (98Cf) и hassius (108hs) докажите это:
Атомы и электроны
Атомно-молекулярное учение
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.
Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Состоит из s-подуровня: одной «s» ячейки (2s 2 ) и p-подуровня: трех «p» ячеек (2p 6 ), на которых помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s 2 ), p-подуровня: трех «p» ячеек (3p 6 ) и d-подуровня: пяти «d» ячеек (3d 10 ), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s 2 ), p-подуровня: трех «p» ячеек (4p 6 ), d-подуровня: пяти «d» ячеек (4d 10 ) и f-подуровня: семи «f» ячеек (4f 14 ), на которых помещается 14 электронов
Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный «рисунок».
Правила заполнения электронных орбиталей и примеры
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
Внешний уровень и валентные электроны
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.
Слой валентности, в чем он состоит, примеры
валентность это тот, чьи электроны ответственны за химические свойства элемента. Электроны в этом слое взаимодействуют с электронами соседнего атома, образуя ковалентные связи (A-B); и если они мигрируют из одного атома в другой более электроотрицательные, ионные связи (A + B-).
Этот слой определяется основным квантовым числом N, который в свою очередь указывает период, когда элемент находится в периодической таблице. При этом упорядочение по группам зависит от количества электронов, вращающихся в валентном слое. Так что для N равно 2, может занимать восемь электронов: восемь групп (1-8).
Что такое слой Валенсия?
Атому нужны электроны, чтобы заполнить все 4n орбиталей. Этот процесс можно наблюдать в электронных конфигурациях элементов в течение определенного периода времени..
черты
Из всего вышесказанного можно суммировать некоторые характеристики валентного слоя для всех атомов:
-Ваш уровень энергии выше; который является тем же самым, более удален от ядра и имеет самую низкую электронную плотность (по сравнению с другими слоями).
-Это неполно Следовательно, он будет по-прежнему заполняться электронами по мере того, как вы проходите период слева направо в периодической таблице..
-Участвует в образовании ковалентных или ионных связей.
Валентный слой 4s не исчез: он пуст только для этих ионов.
примеров
Это потому, что более важными, чем валентный слой, являются его электроны; называется валентными электронами. Когда они представлены в прогрессивной конструкции электронных конфигураций, они определяют электронную структуру атома и, следовательно, его химические свойства..
Исходя из этой информации об атоме A и другом B, структуры их соединений могут быть нарисованы через структуры Льюиса. Также вы можете определить электронные и молекулярные структуры ряда соединений благодаря количеству валентных электронов.
Возможные и самые простые примеры валентных слоев находятся в периодической таблице; в частности, в электронных конфигурациях.
Пример 1
Поскольку X имеет три электрона, а его 5p-орбитали неполные, он находится в p-блоке; более того, в группе IIIA (романская система) или 13 (действующая система нумерации и одобренная IUPAC). Х тогда является индийским элементом, В.
Пример 2
Валентные слои затем могут быть обозначены как nsnp для элемента блока p или s; или (n-1) dns для элемента блока d. Таким образом, таинственный элемент X принадлежит блоку d, потому что его электронная конфигурация имеет тип (n-1) dns (4d). 10 5S 1 ).