Водород и его свойства
Что такое водород
Водород — самый легкий химический элемент, занимающий в периодической таблице Менделеева начальное место.
Его атомный номер — единица. На одноатомную форму водорода приходится около 75% барионной массы, она считается самым распространенным веществом во всей Вселенной. Водородная плазма — основное вещество звезд, за исключением компактных.
У водорода три изотопа:
К общим характеристикам относятся следующие свойства: не имеет цвета запаха, вкуса. Двухатомная форма ( Н 2 ) нетоксична, однако в соединении с воздухом (или О 2 ) пожароопасна и склонна к взрывам. Взрывоопасность также проявляется в присутствии прочих газов-окислителей, например, фтора, хлора.
На Земле водород присутствует в составе молекулярных соединений, например, вода. Его роль в кислотно-основных реакциях трудно переоценить.
Нахождение в природе, изучение его свойств
Звездная температура позволяет существовать водороду в виде плазмы. Это примерно 6000оС. Однако пространство между звездами заполнено отдельными молекулами, атомами и ионами, которые зачастую образовывают молекулярные скопления различных размеров и форм — облака. Плотность вещества при этом не является постоянной величиной, как и его температура.
В коре Земли водород считается десятым по распространенности элементом. Его массовая доля равна 1%. В то же время по числу атомов он достигает 17%. Это второе место после кислорода, доля которого равна 52%. Отсюда и значительная роль водорода в природе, особенно в химических превращениях.
Водород, в отличие от кислорода, не может существовать в свободном состоянии, только в связанном. Исключение составляет атмосфера, в сухом остатке которой 0,00005% простого вещества — водорода.
Все органические вещества включают в свой состав водород. Велика его доля в живых клетках (по количеству атомов его удельный вес достигает 63%).
В составе воды водород имеет большое значение в протекании геохимических процессов. Так, вулканические газы вызывают истечение определенных количестве водорода вдоль разломов (причина — рифтогенез). По этой же причине часто обнаруживают водород в районе угольных месторождений.
Натуральные минералы могут содержать Н2 в виде ионов аммония, гидроксил-ионов и воды.
Причина появления молекул Н2 в атмосфере — разложение формальдегида — участника окисления метана и прочих органических соединений. Кроме того, причина его образования — неполное сгорание топлива и биомассы, фиксация азота некоторыми микроорганизмами, содержащимися в воздухе.
Молекулы водорода легкие, поэтому имеют высокую тепловую скорость. При попадании в верхние слои атмосферы такие молекулы часто улетают в космос, при этом их потери могут достигать 3 кг каждую секунду.
Химические и физические свойства
Начиная говорить о химических свойствах водорода, нужно отметить чрезвычайную прочность его двухатомной молекулы. Для того, чтобы она распалась и атомы могли провзаимодействовать с другими участниками химической реакции, необходима энергия:
Обычные температурные условия обеспечивают протекание реакций только с металлами высокой активности, к примеру, с кальцием:
1 2 C a + H 2 → C a H 2
Исключение составляет реакция с фтором, продуктом которой является фтороводород:
1 2 F 2 + H 2 → 2 H F
Если имеется возможность повышения температуры (либо при другом воздействии, к примеру, освещении), водород может вступать в реакцию с большинством металлов и неметаллов:
1 2 O 2 + 2 H 2 → 2 H 2 O
В реакциях с галогенами образуются галогеноводороды:
1 2 H 2 + F 2 → 2 H F (в темноте происходит взрыв)
1 2 H 2 + C l 2 → 2 H C l (на свету происходит взрыв)
В реакции с оксидами водород проявляет восстановительные свойства:
1 2 C u O + H 2 → H 2 O + C u
Высокая температура делает возможной реакцию с сажей:
1 2 C + 2 H 2 → C H 4
Когда активные металлы соединяются с водородом, образуются гидриды, например гидрид натрия (NaH), гидрид кальция (CaH2), гидрид магния (MgH2). Эти солеобразные твердые, легко гидролизирующиеся вещества:
1 2 C a H 2 + 2 H 2 → C a ( O H ) 2 + 2 H 2
Оксиды металлов, реагируя с водородом, восстанавливаются с выделением воды:
1 2 F e 2 O 3 + 3 H 2 → 2 F e + 3 H 2 O
Благодаря свойствам водорода, он нашел применение для восстановления органических веществ. Протекают реакции с участием катализатора, а также при высоких параметрах давления и температуры. К примеру, насыщенные алканы образуются в результате гидрирования ненасыщенных алкенов и алкинов.
Физические свойства водорода:
Хорошо растворяется в металлах, поэтому способен диффундировать в них. В серебре не растворим.
Получение водорода, как добыть вытеснением из воды
Потребление в мире водорода составляет порядка 75 млн т. Основная масса приходится на нефтепереработку и производство аммиака. Получение водорода для таких промышленных нужд происходит в основном из природного газа (его расход составляет 205 млрд м3). Оставшуюся часть берут из угля. Примерно 100 тыс т вырабатывают с помощью реакции электролиза.
Получение водорода сопровождается поступлением в атмосферу 830 млн т углекислого газа. Стоимость получения водорода из газа составляет от полутора до трех долларов за каждый кг.
Получение водорода методом электролиза в химии выглядит так:
1 2 2 N a C l + 2 H 2 O → 2 N a O H + C l 2 + H 2
Метод конверсии метана при температуре 1000оС с водяными парами:
1 2 C H 4 + H 2 O ↔ C O + 3 H 2
Следующий способ получения — пропускание водяных паров над горящим коксом (температура не менее 1000оС):
1 2 H 2 O + С ↔ С O + H 2
Свободный водород выделяется в результате реакции катализа окислением кислородом:
1 2 2 C H 4 + O 2 ↔ 2 C O + 4 H 2
В промышленности H2 часто получают путем электролиза водных растворов активных металлов:
а также путем крекинга и риформинга углеводородов при переработке нефти.
Существуют способы получения Н2 лабораторными способами:
В промышленности используется очистка водорода из сырья, которое содержит углерод (в частности — водородсодержащий газ ВСГ). Методы следующие:
Получение и собирание водорода в домашних условиях, техника безопасности
Реальным способом получения водорода в домашних условиях является реакция щелочи с алюминием. Газ получается гораздо чище, чем в реакции с кислотой. Схема следующая. В качестве алюминия используют фольгу, щелочного раствора — средство «Крот».
Берем стеклянную емкость, засыпаем в нее немного средства против засора «Крот» и наливаем 100 г воды обычной температуры. Перемешиваем до полного растворения и помещаем сюда же фольгу, скатанную в небольшие шарики. Выделение тепла свидетельствует о начале реакции, после чего ее скорость активируется. Через 20-60 секунд можно добавить новую порцию фольги.
Чтобы образовавшийся водород собрать, можно закрыть банку крышкой, сделав в ней отверстие, в которое вставить трубку. Второй конец трубки закрепить в воздушном шарике.
Поскольку водород является взрывоопасным веществом, делать это нужно крайне осторожно, начиная от момента возможного вытеснения крышки до конца процесса. Попадание водорода в воду приведет к образованию вещества, способного вызвать обморожение.
Особенности применения водорода
Водород используется во многих производственных сферах, что отражено в таблице:
| Применение | Доля |
| Производство аммиака | 54 % |
| Нефтепереработка и химическая промышленность | 35 % |
| Производство электроники | 6 % |
| Металлургия и стекольная промышленность | 3 % |
| Пищевая промышленность | 2 % |
В химической промышленности активный водород идет на производство аммиака (50%), метанола (8%). В нефтеперерабатывающей — для гидрокрекинга и гидроочистки. На эти цели расходуется около 37% всего водорода, что производится.
Пищевая и косметическая промышленность «пользуется» водородом для производства пищевых добавок, а также саломаса, маргарина, мыла, косметических продуктов.
Для химических лабораторий водород — газ-носитель для газовой хроматографии, а для метеорологии — наполнитель оболочек метеозондов.
Водород — ценное ракетное топливо, однако, ввиду незначительного диапазона температур, используется смесь жидкой и твердой фаз.
В электроэнергетике водород применяют для охлаждения электрогенераторов. Его высокая теплопроводность позволяет использовать газ для заполнения сфер гирокомпасов и колб LED-лампочек.
Уголь грядущих веков: когда водород заменит ископаемые энергоносители?
Хотя коронавирус помог человечеству снизить вредные выбросы в атмосферу в I полугодии 2020 на рекордные 9%, экологам праздновать победу рано, потому что, как говорят сантехники, «тут всю систему менять надо» — систему углеродной экономики, построенной на тотальном потреблении ископаемых энергоносителей. И если с новыми источниками мы определились (солнце и ветер), то с носителем их нестабильной энергии ещё нет. На эту роль претендует водород. В этот раз мы расскажем о его перспективах, а также о предсказании Жюля Верна, о ночном кошмаре Илона Маска, о самом большом в мире заводе «зелёного» водорода в Фукусиме и наших шансах на пенсии ездить до дачи на водородных электричках (шансы велики).
Построенное Toshiba предприятие Fukushima Hydrogen Energy Research Field в префектуре Фукусима — самый крупный в мире опытный завод по производству водорода через электролиз. Работы велись в рамках проекта «Hydrogen social construction technical development project/Hydrogen energy system technical development/Technical development concerning business model construction and the large-scale actual proof of a re-energy use hydrogen system» японской Организации по разработке новой энергетической и промышленной технологии (NEDO).

Источник: Toshiba Energy Systems & Solutions Corporation
Жюль Верн в «Таинственном острове» в 1875-м году писал:
— Вода? — переспросил Пенкроф. — Вода будет гореть в топках пароходов, локомотивов, вода будет нагревать воду?
— Да, но вода, разложенная на составные части, — пояснил Сайрес Смит. — Без сомнения, это будет делаться при помощи электричества, которое в руках человека станет могучей силой, ибо все великие открытия — таков непостижимый закон — следуют друг за другом и как бы дополняют друг друга. Да, я уверен, что наступит день, и вода заменит топливо; водород и кислород, из которых она состоит, будут применяться и раздельно; они окажутся неисчерпаемым и таким мощным источником тепла и света, что углю до них далеко! Наступит день, друзья мои, и в трюмы пароходов, в тендеры паровозов станут грузить не уголь, а баллоны с двумя этими сжатыми газами, и они будут сгорать с огромнейшей тепловой отдачей. Следовательно, бояться нечего. Пока землю населяют люди, она их не лишит своих благ, ни света, ни тепла, она отдаст в их распоряжение растения, минералы и животных. Словом, я уверен, когда каменноугольные залежи иссякнут, человек превратит в топливо воду, люди будут обогреваться водой. Вода — это уголь грядущих веков.
— Хотелось бы мне поглядеть на всё это, — заметил моряк.
— Рано ты появился на свет, Пенкроф, — вставил Наб, до тех пор не проронивший ни слова.

Инженер Сайрес Смит (на рисунке в центре) описывает не только водородную экономику. На страницах романа Жюля Верна «Таинственный остров» (1875 г.) он рассказывает, как добывать огонь без спички, определять долготу и широту, строить гончарную печь, делать нитроглицерин и гидроксил, свечи, сооружать гидравлический лифт и т.п. Источник: Rama / Wikimedia Commons
Скептично настроенный моряк из робинзонады Жюля Верна «Таинственный остров» действительно родился слишком рано, чтобы убедиться в точности прогноза Сайреса Смита. Цель превратить водород в «уголь будущих веков» в большинстве программ разных стран должна быть достигнута к 2030-2050 гг. Значит ли это, что человечество уже прошло, скажем, две трети пути к водородной экономике? Попробуем спрогнозировать, но сначала разберёмся с хронологией.
Началось всё в 1776 году с открытия водорода британцем Генри Кавендишем, который реакцией цинка и соляной кислоты получил этот бесцветный газ. В 1800 году его соотечественники Уильям Николсон и Энтони Карлайл впервые провели электролиз — известную всем нам со школы реакцию разложения воды на водород и кислород с применением электричества.
Спустя 30 лет химик из Швейцарии Кристиан Шёнбейн и британец Уильям Грове провели обратный процесс — получили электричество из водорода и кислорода, построив первые в истории топливные элементы на водороде с кислотным электролитом.
В XX веке стало больше прикладных исследований. В 1920-е гг. в немецкий инженер Рудольф Эррен реконструировал двигатели внутреннего сгорания грузовиков, автобусов и подлодок так, чтобы они могли работать на водороде и его смесях. А британец Джон Холдейн впервые предложил использовать энергию ветра для производства водорода электролизом.
Катастрофа дирижабля «Гинденбург» в 1937 году, а затем Вторая Мировая война прервали на время исследования в этой области, хотя водород активно использовался, к примеру, в блокадном Ленинграде.

Когда в Ленинграде закончился бензин, механик Борис Шелищ сумел перевести автомобильные двигатели на отработанный аэростатами водород. Источник: RIA Novosti archive / Wikimedia Commons
В 1970 году химик из США Джон Бокрис ввёл понятие «водородной экономики», предложив питать электросети американских городов энергией солнца, а в качестве её носителя использовать водород.
Все эти годы доступный и практичный газ активно осваивали в промышленности. Правда, о его экологическом потенциале не задумывались, поэтому большинство оставшихся в наследство от индустриальной эпохи способов получения водорода хотя и недорогие, но «грязные». О них далее.
5 оттенков водорода: для чего и как его добывают?
С тех пор как Джон Бокрис предложил превратить водород в энергоноситель, мировой спрос на этот газ увеличился в три раза и достиг 70 млн тонн в год. По разным оценкам, к 2040-м годам показатель возрастет до 100-200 млн тонн в год. По подсчетам Международного энергетического агентства (МЭА), для нефтепереработки вырабатывают 33% этого газа, для получения аммиака и минеральных удобрений — 27%, для синтеза метанола — 11%, а для удовлетворения нужд сталелитейной промышленности — 3%.

Водород бесцветный, не имеющий запаха и вкуса, нетоксичный газ, но в смеси с воздухом или кислородом горюч и опасен. Источник: Toshiba Clip
А откуда берётся водород? Львиная доля добывается из природного газа (76%) и угля (23%). Из-за этого экологически безвредный H2 получается грязным для окружающей среды — его производители выбрасывают в атмосферу столько же углекислого газа, сколько Великобритания и Индонезия вместе взятые. Чтобы раскрыть экологический потенциал водорода, его нужно производить иначе.
В последние годы сложилась «цветовая» классификация водорода по виду источника для его производства:
— серый водород — из природного газа;
— синий водород — из полезных ископаемых, но с применением технологии захвата углекислого газа (Carbon Capture and Storage, CCS), о которой мы рассказывали здесь.
— чёрный водород — из угля;
— коричневый водород — из бурого угля;
— зелёный водород — из возобновляемых источников энергии (ВИЭ).
Теперь посмотрим, как именно производятся «разноцветные водороды» и сколько это стоит.
Легче воздуха, но дороже доллара: сколько стоят разные виды водорода?
Начнём с ископаемых источников. Из природного газа водород производят реформингом — преобразованием CH4 путем эндотермической реакции с использованием водяного пара. Минус этой технологии — выбросы CO2, которые, впрочем, можно уменьшить до 90%, если применять технологии CCS.
Для справки: один кубометр водорода равен 0,08988 килограмма или 1,2699 литра и имеет примерно такую же энергетическую ценность, как треть литра бензина. Это означает, что сжигание 1 килограмма водорода высвобождает такое же количество энергии, как и сжигание 2,75 килограмма бензина.
«Серый» водород пока самый дешёвый. По данным МЭА, стоимость производства одного килограмма водорода 0,90–3,20 долл. США в зависимости от региона и технологии. Самая низкая цена на Ближнем Востоке (0,90 долл./кг), в США (1,00 долл./кг) и России (1,10 долл./кг) — выручают низкие цены на природный газ. В Европе и Китае получается дороже: 1,73 долл./кг 1,78 долл./кг соответственно.
«Синий» водород, вырабатываемый из природного газа с применением захвата CO2, дороже. На Ближнем Востоке он обойдётся 1,45 долл./кг, в США — 1,52 долл./кг, в России — 1,64 долл./кг, в Европе — 2,32 долл./кг, в Китае — 2,38 долл./кг.
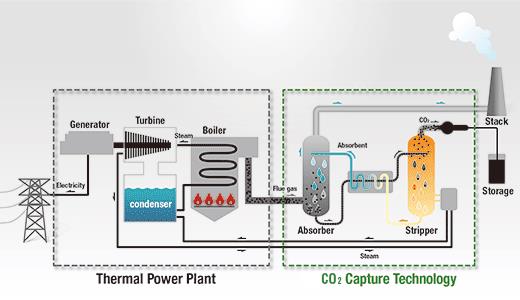
Чтобы снизить «углеродный след» от производства водорода, можно использовать технологии захвата углекислого газа. Принцип CSS — на схеме. Источник: Toshiba Energy Systems & Solutions Corporation
«Чёрный» водород производят методом газификации — переработки твердого или жидкого топлива путем его окисления. Так делают в основном в Китае, где много дешёвого угля. При производстве «чёрного» водорода выбросы CO2 увеличиваются в два раза по сравнению с «серым». Но китайцев привлекает в нём цена — один килограмм «чёрного» водорода стоит 1,10 долл., а с применением захвата CO2 — 1,50 долл.
«Коричневый» водород также можно вырабатывать газификацией, но бурый уголь — пока редкость, поэтому говорить об усредненных ценах рано. Австралийцы хотят его использовать и, по их расчётам, стоимость одного килограмма «коричневого» водорода (с учётом CCS) составит 2,14–2,74 долл.
Конечную цену всех этих видов водорода в основном определяет стоимость сырья, и это главная проблема. Газ и уголь — исчерпаемые ресурсы, их цена волатильна, а «углеродный след» очень заметный. Поэтому с каждым годом всё привлекательнее и для экологов, и для экономистов идея добывать энергоноситель из воды, покрывающей 70% поверхности Земли.
«Зелёный» водород: где его производить и сколько он стоит?
Электролизом пока производится менее 0,1% водорода, но именно этот метод предполагает использование возобновляемых источников энергии.
А энергии нужно много: по подсчетам МЭА, чтобы произвести электролизом текущий годовой объём водорода (70 млн тонн), нужно электричества больше, чем вырабатывает за год Евросоюз (3,60 тыс. ТВт·ч). Поскольку технология получается энергоемкой, стоимость «зеленого» водорода в основном зависит от цен на электричество.
К счастью, они снижаются: по данным Международного агентства по возобновляемой энергии (International Renewable Energy Agency, IRENA), в 2019 году средняя стоимость «солнечного» электричества снизилась на 13% до 0,07 долл./кВт·ч. Энергия морского и сухопутного ветров подешевела на 9% соответственно до 0,05 долл./кВт·ч и 0,12 долл./кВт·ч. Электричество, выработанное из ископаемых источников, в среднем оценивается в 0,066 долл./кВт·ч.
Когда на Земле истощатся запасы воды, на электролиз пойдут запасы виски, пива, энергетиков и газировки. Источник: YouTube-канал Inventor
Со второй составляющей потенциального электролитического чуда (водой) попроще: на один килограмм водорода нужно девять литров воды. Соответственно, чтобы получить годовой объём водорода, понадобятся 617 млн куб. м воды — 1,3% мирового потребления H20 энергетикой. Вода нужна пресная, а морскую воду придётся деминерализовать. Впрочем, к цене одного килограмма водорода это добавляет всего 0,01-0,02 долл.
Сколько в итоге стоит «зелёный» водород? По данным Совета по водородной энергетике (Hydrogen Council), сейчас его цена в среднем равна 6,00 долл. за кг. МЭА даёт такую вилку: 3,00–7,50 долл./кг. Есть факторы, которые сильно влияют на стоимость «зелёного» водорода. Прежде всего, это регион.

Самые перспективные уголки планеты для водорода на возобновляемых источниках энергии — это Патагония, Северная Африка, Ближний Восток, Монголия, Австралия, Китай, США и Новая Зеландия. Здесь стоимость «зеленого» водорода составит 1,60-2,40 долл./кг. Источник: International Energy Agency
Второй фактор — масштаб производства. Чем он больше, тем ниже конечная стоимость «зелёного водорода». И поэтому, хотя Япония небольшая страна, земли для самого большого в мире завода по производству водорода на солнечной энергии компании Toshiba власти префектуры Фукусима не пожалели…
Реально мирный атом: зачем в Фукусиме построили самый большой водородный завод в мире?
По подсчётам Совета по водородной энергетике (Hydrogen Council), чтобы один килограмм «зелёного» водорода стоил 1,00-2,00 долл., к 2030 году, нужно увеличить его производство до 12 млн тонн в год. Чем больше масштаб производства, тем ниже его удельные затраты.
Чтобы понять, как большое производство водорода можно интегрировать в существующую энергосистему, компания Toshiba построила самый крупный в мире опытный завод по производству водорода через электролиз, который питает энергия солнечной электростанции (СЭС). Он называется Fukushima Hydrogen Energy Research Field, FH2R. Завод находится в посёлке Намиэ (преф. Фукусима) и занимает площадь 220 тыс. кв. м. Он состоит из солнечной электростанции мощностью 20 МВт и электролизера с входной мощностью 10 МВт.

Помимо СЭС, завод питает обычная электросеть. ВИЭ могут давать энергию с избытком, и лишний водород можно запасать для поддержания электролиза в периоды минимальной активности солнца или ветра. Но не в столь солнечной стране как Япония Toshiba решила использовать электросеть, чтобы найти экономический баланс между альтернативным традиционным источниками тока. Источник: International Energy Agency
Опытный завод FH2R будет производить до 900 тонн водорода в год для питания машин и автобусов на топливных элементах, а также для собственных нужд. Выработка достигнет 1,20 тыс. куб. м в час, то есть в сутки продукции завода хватит на заправку 560 водородомобилей и энергию для 150 домов.
Кстати, о транспорте. Путь к водородной экономике, скорее всего, лежит через баки личных авто, автобусов и грузовиков, где водород заменит бензин. Как и когда это произойдёт?
Ночной кошмар Илона Маска: победят ли водородомобили «Теслу»?
Машины на топливных элементах — программа минимум водородной революции. Такой транспорт в центре внимания программ большинства принявших их стран.
Водород содержит больше энергии на единицу массы, чем природный газ или бензин, что делает его привлекательным в качестве транспортного топлива. Из плюсов ещё быстрая заправка (в отличие от электрокаров), больший запас хода (около 400 км при средних 250 км у электромобилей), низкий вес сырья, отсутствие выбросов CO2, более экологичная и простая утилизация топливных ячеек по сравнению с батареями электрокаров.
Сейчас по миру ездят более 25 тыс. машин на водороде — в два раза больше чем в 2018. В основном это Toyota Mirai (о которой мы однажды писали здесь, на «Хабре»), Hyundai Nexo и Honda Clarity Fuel Cell, хотя в Китае доминируют автобусы и грузовики. Но водородомобилей гораздо меньше, чем их прямых конкурентов — электрокаров на батареях, число которых приблизилось к 7,2 млн. Почему?
Во-первых, водородные машины дороже. К примеру, Toyota Mirai стоит 58,5 тыс. долларов США, а Tesla Model 3 — 35 тыс. долл. Дорогими выходят два основных компонента водородомобиля — топливные элементы и бак. Однако и эта проблема в перспективе будет решена увеличением масштабов производства. Если сейчас стоимость топливной ячейки для водородной машины составляет 230-180 долл/кВт·ч, то при увеличении их выпуска с 1 тыс. до 500 тыс. единиц в год она снизится до 45 долл/кВт·ч. Цена водородного бака при таком же увеличении масштаба снизится с 23 долл/кВт·ч до 14-18 долл./кВт·ч.

В Toyota Mirai два водородных бака общим весом почти 88 кг. Водород в них хранится под давлением в 70 МПа. Источник: Mariordo / Wikimedia Commons
Во-вторых, есть проблема с заправками: их мало — 25 тыс. водородомобилей заправляются на 470 станциях, большая часть которых находятся в Японии (113), Германии (81) и США (64). Впрочем, со временем проблему решит развитие сети заправок.
Теперь о расходах на топливо. К примеру, в Германии 1 кг водорода на общественных заправках стоит 9,50 евро. Автомобиль на топливных элементах потребляет примерно один килограмм водорода на 100 км. Таким образом, затраты на топливо сопоставимы со средним бензиновым автомобилем, который потребляет 7 литров на 100 км.
В сумме капитальные и текущие затраты на водородомобиль оцениваются экспертами МЭА примерно в 0,65 долл./км, тогда как у электромобилей он составляет порядка 0,58 долл./км., но в перспективе они сравняются. По прогнозу Совета по водородной энергетике, личные авто станут конкурентоспособными к 2030 году при снижении цены водорода до 2,00 долл./кг. А что с другими областями применения водорода?
Резюме: когда начнётся эпоха водорода (и начнётся ли вообще)?
Эксперты Совета по водородной энергетике посчитали, при какой цене за килограмм водород станет конкурентной альтернативой другим энергоносителями с малым «углеродным следом».

Водород уже незаменим в качестве сырья в промышленности, а в будущем его перспективы связаны с транспортом и поставками тепло- и электроэнергии для гражданских и промышленных потребителей. Источник: Path to Hydrogen Competitiveness. A Cost Perspective // 20 January 2020, Hydrogen Council
Когда цена килограмма водорода опустится до 4,00-5,00 долл., конкурентоспособными станут грузовики и автобусы, курсирующие по длинным маршрутам. Причём это может произойти уже через 5 лет. С личными авто и фургонами ситуация иная: даже если цена водорода снизится, их стоимость может остаться высокой относительно электрокаров. Тогда покупать водородомобили будут только автомобилисты с приоритетами быстрой заправки и те, кто использует авто очень интенсивно, например, таксисты. Чтобы превратить маленькие авто в конкурентов Tesla, нужно снизить цену водорода до 1,00-1,50 долл./кг.
А вот электрички на топливных элементах уже вполне могут тягаться с обычными на маршрутах до 50 км с высокой частотой рейсов. Чтобы они сохранили привлекательность, доля расходов на топливо должна упасть с текущих 40-50% до 20-30%, что может произойти при цене 4,5 долл./кг водорода к 2030 году.
Совсем скоро (примерно к 2023 году) могут завоевать мир погрузчики, которые уже сейчас активно используются в Китае при цене 1 кг водорода в 7,00-9,00 долл.
По трубопроводам водород можно подавать в жилые здания. В этом случае он сможет заменить для электричества и отопления домов природный газ с применением технологии захвата углекислого газа. При снижении цены до 3,00-5,40 долл./кг водород становится более выгодным, чем другие системы отопления, скажем, на биометане. Но с природным газом без CCS водород справится только если будет стоить меньше 1,00 долл./кг. В качестве источника электроэнергии топливные ячейки на водороде станут конкурентными при цене 1,90 долл./кг.




