Как и чем можно объяснить образование водородных связей? Объяснение
Содержание:
Молекулы внутри вещества взаимодействуют друг с другом. Это осуществляется с помощью межмолекулярных взаимодействий, возникающих среди нейтральных молекул без образования ковалентных связей. К ним относятся водородные связи, которые также могут быть представителями внутримолекулярных взаимодействий.
Что такое водородные связи?
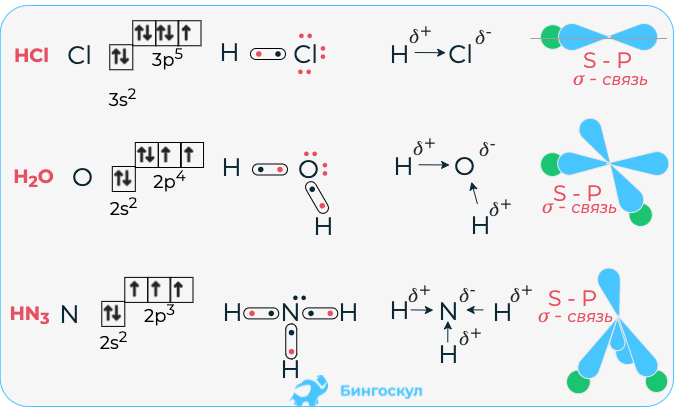
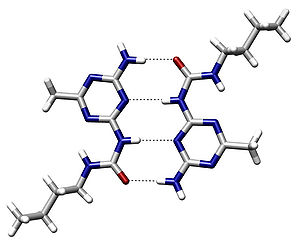
Водородная связь – связь, которая формируется между водородом и молекулами с сильнополярными связями (H-F, H-O, H-N). Она обеспечивает дополнительные межмолекулярные силы притяжения и увеличивает устойчивость вещества. Обозначается точками: Н ··· O.
Создание водородной связи отличается от других связей. Она формируется одновременно по обменному и донорно-акцепторному механизму. Роль донора играет электроотрицательный элемент, а акцептора – водород. Чем выше электроотрицательность, тем больше устойчивость вещества.
Водородная связь свойственна для многих веществ:
Образованием водородных связей можно объяснить изменение свойств веществ. Например, она повышает температуру кипения и плавления.
Биологическая роль водородных связей
Полимерные цепи с помощью водородных связей формируют объемные структуры, которым характерна высокая биологическая активность. Химические взаимодействия возникают из-за электростатических взаимоотношений разноименных зарядов частиц в веществе. Разрыв водородных связей в белках или нуклеиновых кислотах лишает нативных свойств.
Многие полимеры укреплены с помощью водородных связей. В нейлоне они играют главную роль при кристаллизации материала. Также они присутствуют в древесине, хлопке, льне, целлюлозе и других соединениях.
В какой структуре белка появляются водородные связи?
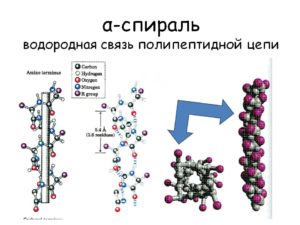
Водородные связи укрепляют белки и нуклеиновые кислоты во вторичной и третичной структурах. Они позволяют макромолекулам принимать определенную форму. Биологическое значение водородной связи заключается в образовании спиральных структур нуклеиновой кислоты ДНК, которая обеспечивается попарным расположением нуклеотидов.
В белках есть два варианта образования связей между:
Водородные связи формируются с помощью ван-дер-ваальсовых сил разноименных полюсов диполя. Первичная структура белков образуется с помощью пептидных связей. Пространственная структура основывается на водородных и ионных связях, ван-дер-ваальсовых силах, гидрофобных взаимодействиях. Водородные связи пептидных групп образуют вторичную структуру белков. Формирование третичной и четвертичной структур осуществляется водородными связями, образующимися между радикалами полярных аминокислот, ионными взаимодействиями, ван-дер-ваальсовыми силами, гидрофобными взаимодействиями.
Образование
Водородные связи в биологии
Водородные связи в биологии
(Здравствуйте уважаемый читатель.Наше настоятельное пожелание-посетите главную страницу сайта.)
Водородную связь относят к числу слабых хим. взаимодействий. Энергия водородной связи как правило лежит в границах от 10 до 30 кДж/моль, но временами она достигает и сотен кДж/моль. Энергии нормальных хим связей (ковалентных и ионных), как правило, сильно превосходят 150 кДж/моль, достигая, к примеру, для молекул азота или же оксида углерода величин 900 кДж/моль и больше [1]. За последние 50 лет было замечено точное осознание исключительной роли слабых взаимодействий, роли водородных связей в стабилизации конденсированных состояний множества несложных молекулярных систем, к примеру воды, фтороводорода, и, что самое значительное, в стабилизации биополимеров (нуклеиновых кислот, белков).
Водородные связи позволяют полимерным цепям соединяться в специфические трехмерные структуры, приобретающие при этом функциональную биологическую активность, структуры, с одной стороны достаточно прочные (за счет образования большого числа водородных связей), а с другой — достаточно чутко реагирующие на изменение внешних условий (например, приближение той или иной молекулы) именно из-за того, что эти взаимодействия являются слабыми.
Разрыв таких связей лишает белки или нуклеиновые кислоты их биологических функций. Отсюда, в частности, видна исключительно важная роль водородных связей, которую они играют в биологических процессах на молекулярном уровне. Понятно и то важное значение исследований и понимания природы водородных связей, которым в последние время было уделено столь пристальное внимание ученых различных направлений.
Общей причиной возникновения водородной связи, как, впрочем, и других выделяемых обычно типов химических связей, является главным образом электростатическое, кулоновское взаимодействие разноименных зарядов тех частиц, которые образуют молекулу. Правда, это взаимодействие отличается от того, которое встречается в классической теории, поскольку оно не определяется только лишь плотностью распределения положительного и отрицательного зарядов, а выражается более сложным образом с помощью волновых функций, определяющих состояния молекулярной системы. Поэтому естественно стремление найти некоторые более простые образы, которые давали бы возможность наглядно представить себе, как же все-таки образуется химическая связь.
Водородная связь по своему происхождению не представляет собой нечто отличающееся от того, что характерно для химических связей вообще. Ее определяют главным образом поляризация электронного распределения в мономерных звеньях (в общем случае в молекулах, образующих такую связь) и отличная от мономерных звеньев динамика колебательного движения атомов в водородно-связанном фрагменте. Пристальное внимание к изучению систем с водородными связями давно уже определяется не спецификой этой связи как таковой, а широкой распространенностью водородных связей, особенно в биологических объектах, и той важной ролью, которую они играют в биополимерах и жизненно важных процессах с их участием.
Примеры соединений с водородной связью
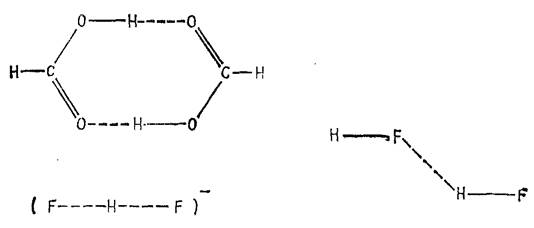
Во многих случаях, когда имеется сильная связь между молекулами или разными группами одной и той же молекулы, эту связь можно приписать атомам водорода, проявляющим двухвалентный характер. Таковы, например, димеры алифатических кислот, ион дифторида 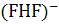
Рисунок 1.1 Некоторые примеры структур с водородной связью
Водород служит в качестве связующего атома в другом важном классе соединений – бороводородах. Простейшим членом этого семейства является диборан (В2 Н6 ). Однако бороводороды обычно не рассматривают в качестве соединений с водородной связью, так как их нельзя разбить на фрагменты, представляющие собой стабильные молекулы. Рассмотрим эти соединения лишь для того, чтобы сопоставить их с комплексами с водородной связью.
Бороводороды были названы электронодефицитнымимолекулами (термин электронодефицитный в применении к бороводородам не совсем оправдан, так как во всех случаях электронов достаточно для заполнения всех связывающих молекулярных орбиталей), так как они не имеют достаточно электронов для образования того количества двухэлектронных связей, которое, по-видимому, подразумевается их молекулярной геометрией. Диборан имеет восемь связей В–Н, но только четырнадцать валентных электронов. Расчеты на основе метода молекулярных орбиталей показывают, что концевые связи представляют собой нормальные двухэлектронные связи, а мостиковые связи следует описывать как трехцентровые двухэлектронные связи.
Можно преобразовать σ g — и σ u -орбитали в эквивалентные орбитали θ1 = σ g + σ u и θ2 = σ g – σ u , локализованные на двух связях F–Н, что демонстрирует отличие от мостиков в бороводородах, орбитали которых не могут быть локализованы на связях.
Ион дифторида не типичен для соединений с водородными связями в том отношении, что атом водорода расположен посредине между двумя тяжелыми атомами. Обычно энергии водородных связей намного меньше, чем для иона дифторида, а водород более тесно связан с одним из атомов, чем с другим, как в димере муравьиной кислоты (рис. 1.1). В действительности геометрия двух компонентов, составляющих комплекс, немного отличается от их геометрии в изолированных состояниях.
Таблица 1.1 Энергии димеризации некоторых газофазных димеров с водородной связью
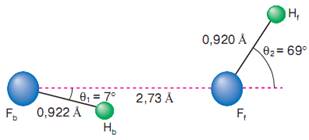
Димер HF
Геометрическая конфигурация, колебания, энергия связи
Рисунок 1.2 Равновесная геометрическая конфигурация комплекса (HF)2
Водородная связь.
Водородная связь – связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы.
Механизм возникновения водородной связи – частично электростатический и частично донорно-акцепторный.
Характерной чертой водородной связи является расстояние между атомом водорода и другим атомом, её образующим. Оно должно быть меньше, чем сумма радиусов этих атомов.
Водородная связь подразделяется:
1. Межмолекулярная водородная связь образуется между молекулами веществ, в состав которых входят водород и сильно электроотрицательный элемент – фтор, кислород, азот, хлор, сера. Сильно смещенная общая электронная пара от водорода к атому отрицательно заряженного элемента, при этом положительный заряд водорода сконцентрирован в малом объеме, приводит взаимодействие протона с неподеленной электронной парой другого атома или иона, обобществляя её.
Водородную связь обозначают точками, указывая, что она намного слабее ковалентной связи (примерно в 15-20 раз).
Межмолекулярная водородная связь: две молекулы воды и две молекулы уксусной кислоты с образованием циклической структуры
2. Внутримолекулярная водородная связь присутствует в многоатомных спиртах, углеводах, белках и других органических веществах.
Молекула салициловой кислоты.
Вещества с водородной связь имеют молекулярные кристаллические решетки, в узлах которой находятся молекулы.
Примеры: вода в виде льда, йод, хлор, бром, «сухой лёд» (твердый диоксид углерода), твёрдый аммиак, а также твёрдые органические вещества (метан, бензол, фенол, нафталин, белки и т.д.).
Физические свойства веществ с водородной связью.
Водородная связь обеспечивает низкомолекулярным веществам способность быть при обычных условиях в жидком агрегатном состоянии (этанол, метанол, вода) или сжижающимися газами (аммиак, фтороводород).
Более высокая температура кипения воды (100 о С) по сравнению с водородными соединениями элементов подгруппы кислорода (Н2S, Н2Sе, Н2Те), так как затрачивается дополнительная энергия на разрушение водородных связей.
Также при плавлении воды её плотность возрастает. Это объясняется тем, что в структуре льда каждый атом кислорода связан через атомы водорода с четырьмя другими атомами кислорода других молекул воды. В результате образуется рыхлая «ажурная» структура.
Водородная связь
Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными. [1]
Содержание
Природа
Часто водородную связь рассматривают как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Тогда об этом говорят как о разновидности донорно-акцепторной связи, невалентном взаимодействии между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR’. Результатом таких взаимодействий являются комплексы RA-H•••BR’ различной степени стабильности, в которых атом водорода выступает в роли «моста», связывающего фрагменты RA и BR’.
История
Свойства
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак.
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от
6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB) ± ; так, для комплекса (H2O•H•OH2) + образованного H2O и H3O + — 132 кДж/моль в газовой фазе.
В воде
Механизм Гротгуса
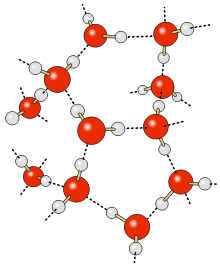
Аномально высокая теплоёмкость воды, а также теплопроводность многоатомных спиртов обеспечивается многочисленными водородными связями. Одна молекула воды может образовать до четырёх классических водородных связей с соседями (с учётом бифуркатных Н-связей до 5-6).
Водородные связи повышают температуру кипения, вязкость и поверхностное натяжение жидкостей. Водородные связи ответственны за многие другие уникальные свойства воды.
Водные кластеры
Согласно современным представлениям, наличие водородных связей между молекулами воды приводит к возникновению так называемых водных кластеров или комплексов. Простейшим примером такого кластера может служить димер воды:
В нуклеиновых кислотах и белках
Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты. В частности, элементы вторичной структуры (например, α-спирали, β-складки) и третичной структуры в молекулах белков, РНК и ДНК стабилизированы водородными связями. В этих макромолекулах, водородные связи сцепляют части той же самой макромолекулы, заставляя её сворачиваться в определенную форму. Например, двойная спиральная структура ДНК, определяется в значительной степени наличием водородных связей, сцепляющих пары нуклеотидов, которые связывают одну комплементарную нить с другой.
В полимерах
Много полимеров усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример — нейлон, где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина, хлопок и лён.
См. также
Примечания
Литература
Полезное
Смотреть что такое «Водородная связь» в других словарях:
ВОДОРОДНАЯ СВЯЗЬ — ВОДОРОДНАЯ СВЯЗЬ, ХИМИЧЕСКАЯ связь, образующаяся между некоторыми молекулами, содержащими водород. Атом водорода должен быть связан с электроотрицательным (отталкивающим электроны) атомом; связь возникает между положительным зарядом атома… … Научно-технический энциклопедический словарь
ВОДОРОДНАЯ СВЯЗЬ — тип связи, промежуточный между ковалентной химической связью и невалентным межат. вз ствием и осуществляющийся с участием атома водорода, расположенного либо между молекулами, либо между атомами внутри молекулы. Примером межмолекулярной В. с. явл … Физическая энциклопедия
ВОДОРОДНАЯ СВЯЗЬ — вид химической связи типа А Н. А ; образуется в результате взаимодействия атома водорода, связанного ковалентной связью с электроотрицательным атомом А (N, O, S и др.), и неподеленной парой электронов другого атома А (обычно O, N). Атомы А и А… … Большой Энциклопедический словарь
водородная связь — – особый вид трехцентровой химической связи X H. Y, в которой центральный атом водорода, соединенный ковалентной связью с электроотрицательным атомом X (C, N, O, S) образует дополнительную связь с атомом Y (N, O, S), имеющим направленную вдоль… … Химические термины
водородная связь — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN hydrogen bond … Справочник технического переводчика
водородная связь — Термин водородная связь Термин на английском hydrogen bond Синонимы Аббревиатуры H bond Связанные термины клатрат, когезия, протеомика, супрамолекулярная химия, нанодиапазон, межмолекулярное взаимодействие Определение притяжение между ковалентно… … Энциклопедический словарь нанотехнологий
водородная связь — вид химической связи типа А Н. А ; образуется в результате взаимодействия атома водорода, связанного ковалентной связью с электроотрицательным атомом A (N, O, S и др.), и неподелённой парой электронов другого атома А (обычно О, N). Атомы А и А… … Энциклопедический словарь
Водородная связь — вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом (А). Группа А Н выступает донором протона (акцептором… … Большая советская энциклопедия
ВОДОРОДНАЯ СВЯЗЬ — невалентное взаимод. между группой АН одной молекулы (RAH) и атомом В другой (BR ). В результате этого взаимод. образуется устойчивый комплекс RAH. BR с межмолекулярной B.C., в к ром атом водорода играет роль мостика, соединяющего фрагменты RA и … Химическая энциклопедия
водородная связь — hydrogen bond водородная связь. Cлабое электростатическое взаимодействие между атомами водорода, связанными с атомами кислорода либо азота; В.с. слабее ковалентной связи; В.с. играет важную роль в образовании структур высшего порядка у… … Молекулярная биология и генетика. Толковый словарь.
водородная связь
Смотреть что такое «водородная связь» в других словарях:
ВОДОРОДНАЯ СВЯЗЬ — ВОДОРОДНАЯ СВЯЗЬ, ХИМИЧЕСКАЯ связь, образующаяся между некоторыми молекулами, содержащими водород. Атом водорода должен быть связан с электроотрицательным (отталкивающим электроны) атомом; связь возникает между положительным зарядом атома… … Научно-технический энциклопедический словарь
ВОДОРОДНАЯ СВЯЗЬ — тип связи, промежуточный между ковалентной химической связью и невалентным межат. вз ствием и осуществляющийся с участием атома водорода, расположенного либо между молекулами, либо между атомами внутри молекулы. Примером межмолекулярной В. с. явл … Физическая энциклопедия
ВОДОРОДНАЯ СВЯЗЬ — вид химической связи типа А Н. А ; образуется в результате взаимодействия атома водорода, связанного ковалентной связью с электроотрицательным атомом А (N, O, S и др.), и неподеленной парой электронов другого атома А (обычно O, N). Атомы А и А… … Большой Энциклопедический словарь
водородная связь — – особый вид трехцентровой химической связи X H. Y, в которой центральный атом водорода, соединенный ковалентной связью с электроотрицательным атомом X (C, N, O, S) образует дополнительную связь с атомом Y (N, O, S), имеющим направленную вдоль… … Химические термины
водородная связь — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN hydrogen bond … Справочник технического переводчика
Водородная связь — Пример межмолекулярных водородных связей Водо … Википедия
водородная связь — Термин водородная связь Термин на английском hydrogen bond Синонимы Аббревиатуры H bond Связанные термины клатрат, когезия, протеомика, супрамолекулярная химия, нанодиапазон, межмолекулярное взаимодействие Определение притяжение между ковалентно… … Энциклопедический словарь нанотехнологий
водородная связь — вид химической связи типа А Н. А ; образуется в результате взаимодействия атома водорода, связанного ковалентной связью с электроотрицательным атомом A (N, O, S и др.), и неподелённой парой электронов другого атома А (обычно О, N). Атомы А и А… … Энциклопедический словарь
Водородная связь — вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом (А). Группа А Н выступает донором протона (акцептором… … Большая советская энциклопедия