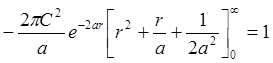1. ОСНОВНЫЕ ПОНЯТИЯ
1.1. Волновая функция.
1. Конечность во всем пространстве. В противном случае невозможно определить параметры системы в тех точках, где волновая функция обращается в бесконечность.
2. Однозначность. В любой точке пространства функция принимает одно единственное значение.
3. Непрерывность. Нет разрывов. Функция определена при любых значения аргументов.
В качестве примера рассмотрим волновую функцию для свободного электрона, которая описывает состояние плоской монохроматической волны, распространяющуюся вдоль координаты X
Y = 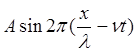
Y= 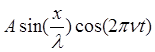
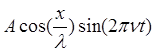
В приведенных записях учитывается как положение в пространстве, так и зависимость от времени. В дальнейшем мы будем иметь дело только с функциями, не зависимыми от времени.
Другим свойством волновой функции является принцип суперпозиции. Если система может находиться в состояниях, описываемых волновыми функциями Y1 и Y2 (решения волнового уравнения), то она может находиться и в состоянии Y = aY1 + bY2. где a и b простые числа (т.е. Y также решение исходного уравнения). Это легко показать подстановкой новой волной функции в исходное волновое уравнение.
Примером принципа суперпозиции является волновая функция свободного электрона
Y = A( 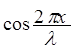
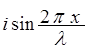
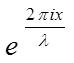
Используя принцип суперпозиции можно получить волновые функции для p-состояния атома (три независимые друг от друга функции).
Y+1 = (x + iy)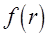
Yo = z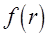
При расчётах в квантовой химии используют нормированные волновые функции. Нормировка волновой функции заключается в определении нормировочного множителя (множителей). Произведём нормировку волновой функции, соответствующей s-электрону в атоме, Y = 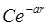
Условие нормировки: 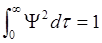
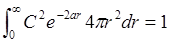
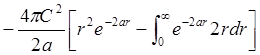
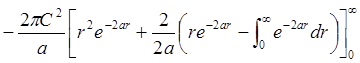
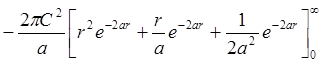
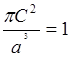
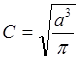
4. Ортогональность волновых функций. Важным свойством волновых функций, используемых в квантовой химии, является их ортогональность.
Условие ортогональности имеет вид:
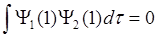
Чтобы распечатать файл, скачайте его (в формате Word).
Волновая функция и волновое уравнение
2.1.3. Волновая функция и волновое уравнение.
Так как электронам присущи волновые свойства и они обладают неопределенностью положения в пространстве, их движение характеризуется при помощи волновой функции и описывается волновым уравнением. Физический смысл волновой функции заключается в том, что ее квадрат 2 пропорционален вероятности нахождении электрона в элементарном объеме атома V с координатами x, y, z.
Значение волновой функции находят при решении волнового уравнения Шредингера:
2 /x 2 + 2 /y 2 + 2 /z 2 +82m/h 2 *(E–U)=0
В этом сложном дифференциальном уравнении с частными производными: Е–полная энергия частицы, U – потенциальная энергия, –волновая функция.
В
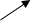

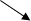
В итоге – значения квантовых чисел есть не что иное как результат решения уравнения Шредингера. Следовательно, при решении уравнения Шредингера получены значения волновой функции и возможные /допустимые/ значения квантовых чисел.
2.1.4. Квантовые числа. Атомные орбитали.
Так как электрон имеет четыре степени свободы, то для характеристики его поведения в атоме требуется четыре квантовых числа.
Главное квантовое число n определяет удаленность атомной орбитали от ядра и характеризует общий запас энергии электрона на данном энергетическом уровне. n принимает целочисленные значения от единицы до бесконечности. В зависимости от цифровых значений главного квантового числа приняты буквенные обозначения квантовых уровней n=1, 2, 3, 4,…
обозначение К, L, M, N,…
Чем больше n, тем слабее электрон связан с ядром и более емким становится квантовый уровень. Числовые значения n определяют также и количество подуровней, содержащееся на данном квантовом уровне /т.е. числовые значения n определяют емкость квантового уровня/. Так, если n=3, то это значит, что имеем третий квантовый уровень, который состоит из трех подуровней.
Орбитальное квантовое число l характеризует момент количества движения электрона относительно центра орбитали. Наличие такого движения приводит к делению квантового уровня на подуровни. Орбитальное квантовое число характеризует так же пространственную форму электронного облака. Это квантовое число предопределяется главным квантовым числом n и принимает ряд целочисленных значений от нуля до n–1. В зависимости от числовых значений l приняты буквенные обозначения подуровней:
обозначение подуровня: s, p, d, f,…
ф
Магнитное квантовое число ml характеризует магнитный момент электрона. Определяет ориентацию квантового подуровня в пространстве. Число проекций подуровня на направление магнитных силовых линий квантуется и оно равно количеству орбиталей на данном подуровне. Можно сказать, что магнитное квантовое число определяет количество орбиталей на подуровне. ml принимает значения от –l через ноль до +l.
Рассмотрим подуровень s. Для него: l=0, ml=0
П
В
С
Для d-подуровня: l=2, ml = –2, –1, 0, +1, +2. Это значит, что согласно квантовой теории d-подуровень состоит из пяти d-орбиталей.
Подуровень f имеет l=3, ml = –3, –2, –1, 0, +1, +2, +3. Следовательно f-подуровень состоит из семи f-орбиталей.
Число орбиталей на подуровне можно определить из выражения ml =2l+1:
значение l: 0, 1, 2, 3, …….
подуровень: s, p, d, f, …….
число орбиталей: 1, 3, 5, 7, …….
Спиновое квантовое число ms характеризует собственный момент количества движения, возникающий как бы из-за «вращения» электрона вокруг собственной оси. Принимает два значения: +1/2 и –1/2, что соответствует двум возможным направлениям вращения электрона.
Оно получено из опытов Штерна и Герлаха.
Рассмотренные квантовые числа определяют энергию электрона, объем и форму пространства, в котором вероятно его пребывание в околоядерном объеме, т.е. размер, форму и ориентацию орбитали в пространстве.
Так как волновая функция является решением уравнения Шредингера при всевозможных значениях квантовых чисел, то можно сказать, что волновая функция является в свою очередь функцией рассмотренных квантовых параметров n, l и ml, где:
Атомные орбитали. Так как вероятность нахождения электрона в пространстве далеком от ядра очень мала, когда говорят об орбиталях, то имеют в виду такую область вокруг ядра атома внутри которой сосредоточено 90–95% электронного заряда. С точки зрения квантовой механики атомные орбитали являются геометрическим изображением волновой функции (n, l, ml).
Z






Y нулю. Имеем только одно значение ml =0. Следовательно,
s-орбиталь имеет максимальную симметричность. У нее
X сферическая форма (рис.2.4.). В этом случае вероятность на–
хождения электрона в околоядерном пространстве определя–
рис.2.4. ется только радиусом-вектором и не зависит от угла координат.
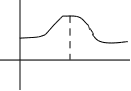
электрона соответствует кривой с максимумом (рис.2.5.).
Максимум распространения вероятности находится на
0 r1 r,A 0 расстоянии от ядра r1, которые соответствует радиусу
рис.2.5. первой боровской орбиты.
р-орбиталь. Существует при l=1. ml = –1, 0, +1.
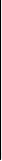
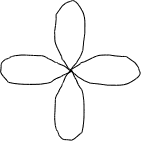

Y не каждого уровне может быть три р-орбитали. р-орбиталь
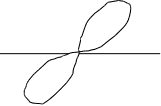
X лагаются в пространстве по направлению координатных
Px осей. Их называют соответственно рх, рy, рz-орбитали
Р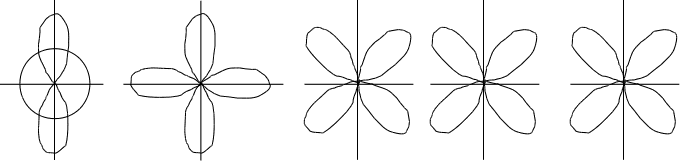
dz 2 dx 2 y 2 dxy dxz dyz
d-орбиталь. Появляется при l=2 на третьем квантовом уровне. На d-подуровне может быть уже пять различных состояний электронов, поэтому на d-подуровне каждого квантового уровня содержится пять d-орбиталей. В этом случае ml принимает пять значений: ml = –2, –1, 0, +1, +2, d-орбитали имеют более сложную форму, чем р-орбитали, они либо в виде четырех лепестков либо в виде гантели с ободком (рис.2.7.).
f-орбиталь. Появляется при значении l=3. f-орбитали могут быть только на четвертом и более отдаленных уровнях. Так как при l=3 ml имеет 7 значений /–3, –2, –1, 0, +1, +2, +3/, то на f-подуровне может быть семь орбиталей. Форма f-орбиталей еще более сложная, чем у d-орбиталей. f-орбитали изображают в виде сложных шестилепестковых фигур.
Форма орбиталей и ее направленность играют существенную роль при образовании химических связей, т.к. эти два фактора определяют характер и степень перекрывания электронных облаков соединяющихся атомов.
Что такое волновая функция в химии
3.1.2 Волновое уравнение. Квантовомеханическое объяснение строения атома
Неопределенность установления положения и скорости электрона столь велика, что необходимо вообще отказаться от анализа траектории его движения. Однако есть возможность вероятностного описания строения атома.
E – полная энергия электрона;
б) Побочное, или орбитальное, квантовое число ( l ). В спектрах многоэлектронных атомов наблюдается мультиплетная структура линий, т.е. линии расщеплены на несколько компонент. Мультиплетность линий означает, что энергетические уровни представляют собой совокупности энергетических подуровней, т.к. любой линии в спектре отвечает переход электрона из одного состояния в другое. Энергетические различия в состоянии электронов в данном уровне связаны с различием в форме электронных облаков.
Рисунок 3.1 – График волновой функции s-электрона в зависимости от расстояния до ядра. Форма s-орбитали
Рисунок 3.2 – График волновой функции p-электрона. Форма p-электронного облака
Знаки “+” и “–” от носятся не к вероятности нахождения электрона (она всегда положительна и равна | Ψ | 2 ), а к волновой функции, которая в разных частях электронного облака имеет различный знак.
в) Магнитное квантовое число ( ml ). Если атом поместить во внешнее магнитное поле, то происходит дальнейшее расщепление спектральных линий. Это означает, что при данных значениях n и l может существовать несколько состояний электрона с одинаковой энергией. Такие энергетические состояния называются вырожденными. Вырождение исчезает при воздействии на атом внешнего магнитного поля, что и приводит к появлению новых линий в спектре.
На рисунке 3.3 показано постепенное усложнение представлений о структуре электронной оболочки атома (от уровней к подуровням и далее к орбиталям ).
Рисунок 3.3 – Эволюция представлений о строении электронной оболочки атома. Энергетическая диаграмма уровней с 1-го по 3-й
Пользуясь принципом Паули, можно подсчитать, какое максимальное число электронов может находиться на каждом подуровне, т.е. определить емкость подуровней:
Здесь электроны на орбиталях изображены стрелками, направленными вверх или вниз в зависимости от знака спинового квантового числа.
Квантовая химия
Содержание
Общие сведения
Основной задачей квантовой химии является решение уравнения Шредингера и его релятивистского варианта (уравнение Дирака) для атомов и молекул. Уравнение Шредингера решается аналитически, учитывая следующие ограничения: жёсткий ротатор, гармонический осциллятор, одноэлектронная система. Но реальные многоатомные системы содержат большое количество взаимодействующих электронов, а для таких систем не существует аналитического решения этих уравнений, и, по всей видимости, оно не будет найдено и в дальнейшем. По этой причине в квантовой химии приходится строить различные приближённые, обычно численные или получисленные решения. Из-за быстрого роста сложности поиска решений с ростом сложности системы и требований к точности расчёта, возможности квантовохимических расчётов сильно ограничиваются текущим развитием вычислительной техники, хотя, наблюдаемые в последние два десятилетия революционные сдвиги в развитии компьютерной техники, приведшие к её заметному удешевлению, заметно стимулируют развитие прикладной квантовой химии. Решение уравнения Шредингера строится на уравнении Хартри-Фока-Рутана итерационным методом (SCF-self consistent field — самосогласованное поле) и состоит в нахождении вида волновой функции. Приближения, используемые в квантовой химии:
1. Приближение Борна — Оппенгеймера (адиабатическое): движение электронов и движение ядер разделено (ядра движутся настолько медленно, что при расчёте движения электронов ядра можно принять за неподвижные объекты). В связи с этим приближением существует так называемый эффект Яна-Теллера. Данное приближение позволяет представить волновую функцию системы как произведение волновой функции ядер и волновой функции электронов.
2. Одноэлектронное приближение (или приближение Хартри): считается, что движение электрона не зависит от движения других электронов системы. В связи с этим в уравнения, используемые в квантовой химии вносятся поправки на взаимное отталкивание электронов. Это позволяет волновую функцию электронов представить в виде суммы волновых функций отдельных электронов.
3. Приближение МО ЛКАО (Молекулярная Орбиталь как Линейная Комбинация Атомных Орбиталей): в данном подходе волновая функция молекулы представляется как сумма атомных орбиталей с коэффициентами: Ψ(r)=c1ψ1+ c2ψ2+…+cnψn, где
Ψ(r) — волновая функция (а точнее — её электронная часть),
c1 — коэффициент при атомной орбитали,
ψ1 — волновая функция атомной орбитали (получается при решении уравнения Шредингера для атома водорода — известно в точном виде). Решение задачи состоит в нахождении коэффициентов С. При учёте всех интегралов — так называемый метод Ab initio — количество вычислений растёт пропорционально количеству электронов в 6-8 степени, при полуэмпирических методах — в 4-5 степени.
Получаемая при решении уравнения волновая функция является математической абстракцией. Имеет определённый физический смысл лишь квадрат её значения, который по мнению Э.Шрёдингера, характеризует вероятность распределения (плотность) отрицательно заряженного электронного облака.
Однако большинство физиков не разделяло убеждений Э.Шрёдингера, так как доказательств существования электрона как отрицательно заряженного облака не существовало на тот момент. Общепринятой точка зрения стала лишь благодаря работам Макса Борна, который обосновал вероятностную трактовку квадрата волновой функции. За фундаментальное исследование в области квантовой механики, особенно за статистическую (вероятностную) интерпретацию волновой функции, М.Борну была присуждена в 1954 году Нобелевская премия по физике.
Строение атома
Волновая функция – математическая абстракция или физическая реальность?
Известно, что квантовые объекты могут вести себя странным образом: как будто они двигаются сразу в нескольких направлениях, находятся одновременно в нескольких местах или вращаются сразу по и против часовой стрелки. На математическом уровне квантовое поведение частиц описывается при помощи так называемой «волновой функции». В зависимости от условий эксперимента она позволяет рассчитать, например, вероятность нахождения электрона в определенном месте. Или предсказать (опять же в терминах вероятности), как будет направлен его спин – вверх или вниз.
Но математика не дает ответа на вопрос о природе этой функции. Является ли она элементом физического мира? Или это всего лишь математический инструмент, позволяющий нам работать в условиях фундаментального непонимания этого мира? И стоит ли вообще задаваться такими вопросами? Физики ставят эксперименты, чтобы понять природу этой загадочной функции, описывающей странности квантового мира.
Если бомбардировать редкими электронами стенку с двумя крошечными дырками, часть электронов проходит сквозь отверстия и каждый из них оставляет точечный след на экране за стенкой. Проводя эксперимент достаточное время, мы могли бы ожидать возникновение на экране двух круглых пятен, однако проявляющаяся картина выглядит более изощрённой и совпадает с картиной интерференции электромагнитных волн. Волновые свойства электрона и других элементарных частиц можно выразить математически через так называемую волновую функцию, определяющую вероятность обнаружить частицу в некоторой области пространства в течение заданного промежутка времени.
Да, наблюдения показывают и теории предсказывают, что квантовые объекты ведут себя странно, но имеет ли смысл думать о том, почему они так делают?
Здесь мнения ученых разделились. Сторонники так называемой «копенгагенской интерпретации» квантовой механики считают, что размышлять об этом не имеет практического смысла. Волновая функция – это работающий инструмент для предсказания результатов наблюдений. Суть этого подхода хлестко изложил Дэвид Мермин: «Заткнись и вычисляй!» И в целом эта позиция оправдана, поскольку привела к огромному прогрессу в ядерной физике и других отраслях.
Однако не всех ученых такой подход устраивает, и они продолжают предлагать свои интерпретации квантовых феноменов. Сторонники так называемой «причинной интерпретации», корни которой уходят к работам Эйнштейна, полагают наличие у квантовых объектов неких «скрытых параметров», знать которые нам пока не дано. Волновая функция отражает, таким образом, наше неведение относительно реального мира. На вопрос, жив или мертв кот Шредингера, сторонники причинной интерпретации отвечают: «Не знаю. Давайте поглядим». Однако есть и другие интерпретации, часть из которых рассматривают волновую функцию как элемент реальности. Одна из философских сложностей здесь состоит в том, что последние считают вышеупомянутого кота «одновременно» и живым, и мертвым, так же, как и приверженцы успешной копенгагенской интерпретации.
Кто же из них прав? На этот вопрос крайне сложно ответить при помощи эксперимента. Однако физику О. Мэруни и его коллегам из Оксфордского университета (Великобритания) удалось придумать эксперимент для проверки реальности волновой функции, а в прошлом году А. Федрицци, А. Уайт и др. (Квинслендский университет, Австралия) смогли реализовать его на практике. Суть эксперимента проста. Представьте две колоды карт – в одной карты только красной масти, а в другой одни тузы. «Вам дают карту и предлагают определить, из какой она колоды», – говорит физик М. Рингбауэр (Квинслендский университет). – «Если это красный туз, то вы имеете перекрывание (совмещение) признаков, и вы не сможете сказать, из какой эта карта колоды». Даже если вы знаете точный состав карт в каждой колоде, то в лучшем случае вы сможете подсчитать лишь вероятность возникновения такой неопределенной ситуации.
Подобная неопределенность присутствует и в квантовых системах. Экспериментаторы измерили поляризацию и другие параметры луча фотонов и обнаружили перекрывание, которое нельзя объяснить при помощи моделей, основанных на причинной интерпретации. Результаты эксперимента свидетельствуют о том, что если объективная реальность существует, то волновая функция реальна. С этим выводом можно спорить, потому что условия эксперимента предполагали существенные допущения. Поэтому ученые планируют в ближайшее время провести аналогичный эксперимент с ионами, которые легче отследить, чем фотоны. «В ближайшие полгода мы надеемся разработать эксперимент, не допускающий двойного толкования», говорит Мэруни.
В конечном счете такие исследования подводят нас вплотную к философскому вопросу о существовании объективной реальности. Хотя никто еще не знает, как это сделать, но, как говорит Уайт, «было бы невероятно интересно разработать эксперимент, чтобы проверить, существует ли на самом деле объективная реальность».
Подготовила Алла Кобкова
Проблема понимания и интерпретации квантового мира привлекает внимание ученых с первых лет развития квантовой механики. Нильс Бор утверждал, что наше сознание и язык не подходят для понимания явлений, происходящих на микро-масштабах. Квантовая механика смогла корректно предсказать исход тысяч экспериментов, что подтверждает ее статус как теории. Однако значительно сложнее проверить надежность ее интерпретаций. Один из наиболее интересных экспериментов в этой области поставил Ален Аспе в 1982 году – этот эксперимент показал отсутствие «скрытых параметров», которые могли бы определить результат квантовомеханических экспериментов, являющихся вероятностными с точки зрения современной физики. Проблема до сих остается скорее предметом философии нежели физики. В 1957 году Хью Эверетт разработал теорию множественности миров, согласно которой все альтернативные результаты измерений являются частью реальности, каждый в своем мире. Последние достижения квантовой оптики и компьютерного моделирования позволяют нам поставить в реальности классические мысленные эксперименты, предложенные Эйнштейном и Шредингером, что повышает интерес к основам квантовой механики.
Исследование «многомировой интерперетации» Эверетта – это важный и интересный шаг в этом направлении.