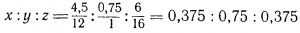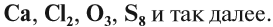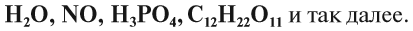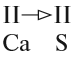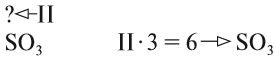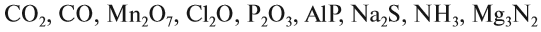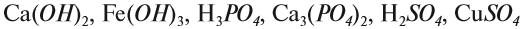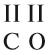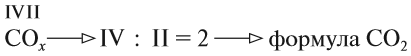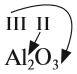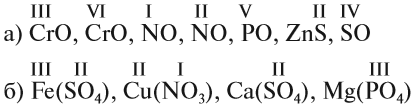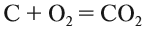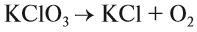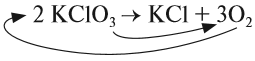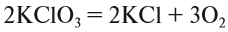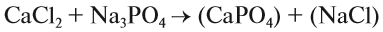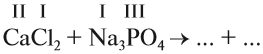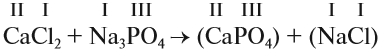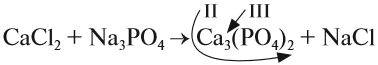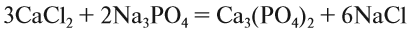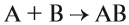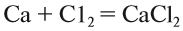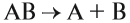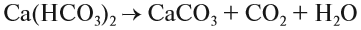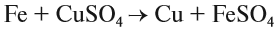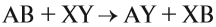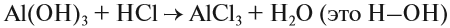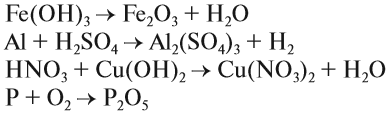Как написать вывод в лабораторной работе?
Лабораторная работа – один из важнейших видов деятельности для учащихся. Школьники сталкиваются с ними в основном на уроках физики, химии и биологии, а студенты – на факультетах естественных и технических наук. Она предусматривает практическое занятие с написанием отчета по результатам. В зависимости от многих факторов можно заказать лабораторную работу в Москве – качественно написанную, с подробным отчетом и выводами.
Лабораторные работы необходимы для закрепления на практике всех полученных теоретических знаний, приобретения навыков. Зачастую они довольно увлекательны, учащиеся с интересом делают их, но, когда приходит время писать отчеты, даже отличники, которые с легкостью оперируют теорией и умело применяют ее, теряются перед написанием сухих выводов.
Что такое вывод?
Вывод по лабораторной работе – это изложение результата практического занятия с их оценкой. Главный вопрос, на который должен отвечать этот пункт отчета – достигнута ли поставленная цель? На нее стоит ориентироваться при подбивании итогов выполненного задания. Что должно быть упомянуто в выводе:
Все это нужно грамотно описать, логически связать. В школе практические занятия носят скорее ознакомительный характер, а вот для студентов они имеют большее значение, ведь являются своеобразной «репетицией» перед уже реальной, не учебной практикой.
Рекомендации по написанию
Даже если написание вывода кажется чем-то чрезвычайно сложным, не стоит отчаиваться и бросать выполненную работу. Если лабораторная была проведена правильно, создание выводов – дело техники. Придерживайтесь следующих рекомендаций:
Цель является основным руководством к написанию вывода, но это не означает, то можно просто переписать ее, и дело сделано. Нужно указать все моменты: какие методы вы применяли, какие возникли непредвиденные ситуации, какие были обнаружены тонкости, и к чему привели все ваши действия. Даже если вам не удалось достичь поставленной цели, это не означает, что лабораторная работа неуспешная, и результат должен быть описан целиком.
Вывод химических формул

Обычно состав сложного вещества выражают в процентах, но он может быть выражен и в любых других числах, указывающих отноше ние между весовыми количествами элементов, образующих данное вещество.
Например, состав окиси алюминия, содержащей 52,94% алюминия и 47,06% кислорода, будет вполне определен, если мы скажем, что алюминий и кислород соединены в весовом отношении 9:8, т. е. что на 9 вес. ч. алюминия приходится 8 вес. ч. кислорода. Понятно, что отношение 9: 8 должно равняться отношению 52,94 : 47,06.
Зная весовой состав сложного вещества и атомные веса образующих его элементов, нетрудно найти относительное число атомов каждого элемента в молекуле взятого вещества и таким образом установить его простейшую формулу.
Пример вывода химических формул
что требуется вывести формулу хлористого кальция, содержащего 36% кальция и 64% хлора. Атомный вес кальция 40, хлора 35,5.
Обозначим число атомов кальция в молекуле хлористого кальция через х, а число атомов хлора через у. Так как атом кальция весит 40, а атом хлора 35,5 кислородных единиц, то общий вес атомов кальция, входящих в состав молекулы хлористого кальция, будет равен 40 х, а вес атомов хлора 35,5 у. Отношение этих чисел, очевидно, должно равняться отношению весовых количеств кальция и хлора в любом количестве хлористого кальция. Но последнее отношение равно 36 : 64.
Приравняв оба отношения, получим:
Затем освободимся от коэффициентов при неизвестных х и у путем деления первых членов пропорции на 40, а вторых на 35,5: 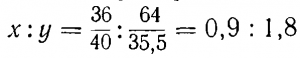
Следовательно, в молекуле хлористого кальция на один атом кальция приходятся два атома хлора. Этому условию удовлетворяет целый ряд формул: СаСl2, Са2Сl4, Са3Сl6 и т. д. Так как у нас нет данных, чтобы судить, какая из написанных формул отвечает действительному атомному составу молекулы хлористого кальция, то мы остановимся на простейшей из них СаСl2, указывающей наименьшее возможное число атомов в молекуле хлористого кальция.
Однако произвол в выборе формулы отпадает, если наряду с весовым составом вещества известен также его молекулярный вес. В этом случае нетрудно вывести формулу, выражающую истинный состав молекулы. Приведем пример.
Путем анализа установлено, что глюкоза содержит на 4,5 вес. ч. углерода 0,75 вес. ч. водорода и 6 вес. ч. кислорода. Молекулярный вес ее был найден равным 180. Требуется вывести формулу глюкозы.
Как и в предыдущем случае, находим сперва отношение между числом атомов углерода (атомный вес 12), водорода и кислорода в молекуле глюкозы. Обозначив число атомов углерода через х, водорода через у и кислорода через z, составляем пропорцию:
2х :у: 16z = 4,5 : 0,75 : 6
Разделив все три члена второй половины равенства на 0,375, получаем:
Следовательно, простейшая формула глюкозы будет СН2O. Но вычисленный по ней молекулярный вес равнялся бы 30, тогда как в действительности молекулярный вес глюкозы 180, т. е. в шесть раз больше. Очевидно, что для глюкозы нужно принять формулу C6H12O6.
Формулы, основанные, кроме данных анализа, также и на определении молекулярного веса и указывающие действительное число атомов в молекуле, называются истинными или молекулярными формулами; формулы же, выведенные только из данных анализа, называются простейшими или эмпирическими.
Познакомившись с выводом химических формул, легко понять, как устанавливаются точные молекулярные веса. Как мы уже упоминали, существующие методы определения молекулярных весов в большинстве случаев не дают вполне точных результатов. Но, зная хотя бы приблизительный молекулярный вес и процентный состав вещества, можно установить его формулу, выражающую атомный состав молекулы.
Так как вес молекулы равняется сумме весов образующих ее атомов, то, сложив веса атомов, входящих в состав молекулы, мы определим ее вес в кислородных единицах, т. е. молекулярный вес вещества. Точность найденного молекулярного веса будет такой же, как и точность атомных весов.
Нахождение формулы химического соединения во многих случаях может быть значительно упрощено, если воспользоваться понятием о валентности элементов.
Напомним, что валентностью элемента называется свойство его атомов присоединять к себе или замещать определенное число атомов другого элемента.
Что такое валентность
Валентность элемента определяется числом, показывающим, сколько атомов водорода (или другого одновалентного элемента) присоединяет или замещает атом данного элемента.
Понятие о валентности распространяется не только на отдельные атомы, но и на целые группы атомов, входящие в состав химических соединений и участвующие как одно целое в химических реакциях. Такие группы атомов получили название радикалов. В неорганической химии наиболее важными радикалами являются: 1) водный остаток, или гидроксил ОН; 2) кислотные остатки; 3) основные остатки.
Водный остаток, или гидроксил, получается, если от молекулы воды отнять один атом водорода. В молекуле воды гидроксил связан с одним атомом водорода, следовательно, группа ОН одновалентна.
Кислотными остатками называются группы атомов (а иногда и один атом), «остающиеся» от молекул кислот, если мысленно отнять от них один или несколько атомов водорода, замещаемых металлом. Валентность этих групп определяется числом отнятых атомов водорода.
Например, серная кислота дает два кислотных остатка — один двухвалентный SO4 и другой одновалентный HSO4,входящий в состав различных кислых солей. Фосфорная кислота Н3РО4 может дать три кислотных остатка: трехвалентный РО4,двухвалентный НРО4 и одновалентный Н2РО4 и т. д.
Основными остатками мы будем называть; атомы или группы атомов, «остающиеся» от молекул оснований, если мысленно отнять от них один или несколько гидроксилов. Например, последовательно отнимая от молекулы Fe(OH)3 гидроксилы, получаем следующие основные остатки: Fe(OH)2, FeOH и Fe. Валентность их определяется числом отнятых гидроксильных групп:Fe(OH)2 — одновалентен; Fe(OH)—двухвалентен; Fe — трехвалентен.
Основные остатки, содержащие гидроксильные группы, входят в состав так называемых основных солей. Последние можно рассматривать как основания, в которых часть гидроксилов замещена кислотными остатками. Так, при замещении двух гидроксилов в Fe(OH)3 кислотным остатком SO4 получается основная соль FeOHSO4, при замещении одного гидроксила в Bi(OH)3 кислотным остатком NO3 получается основная соль Bi(OH)2NO3 и т.д.
Знание валентностей отдельных элементов и радикалов позволяет в простых случаях быстро составлять формулы очень многих химических соединений, что освобождает химика от необходимости механически их заучивать.
Так как составление простейших формул — окислов, оснований и нормальных солей хорошо известно из элементарного курса химии, то мы ограничимся здесь лишь примерами составления формул кислых и основных солей.
Химические формулы
Пример составления химической формулы
Составить формулу гидрокарбоната кальция — кислой соли угольной кислоты.
В состав этой соли должны входить атомы кальция и одновалентные кислотные остатки НСО3. Так как кальций двухвалентен, то на один атом кальция надо взять два кислотных остатка. Следовательно, формула соли будет Са(НСО3)г.
Промер 2. Составить формулу основного карбоната меди — основной медной соли угольной кислоты.
Эта соль должна состоять из одновалентных основных остатков СuОН и двухвалентных кислотных остатков СО3. Поэтому формула соли будет (СuОН)2СО3 или Сu2(ОН)2СО3.
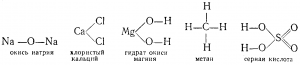
Правило составления формул по валентности приобретает большую наглядность, если изображать состав молекул так называемыми структурными формулами. Примерами структурных формул некоторых простейших соединений могут служить следующие:
Похожие страницы:
Понравилась статья поделись ей
Как выполнить лабораторную работу по химии: подготовка, структура и написание вывода
Без практики на специальностях, связанных с химией, не обойтись. И лучший способ проверить приобретенные знания и закрепить навыки — выполнение лабораторной работы.
В статье я расскажу, как успешно справиться с лабораторной даже первокурснику.
Подготовка к выполнению лабораторной
Поскольку работа по химии довольно специфична, то вначале нужно:
Эти четыре простых правила подготовки существенно облегчат процесс выполнения работы и обеспечат качество результатов.
Ведение лабораторного журнала и структура
Перед написанием работы заведите лабораторный журнал: без него хорошо выполнить практикум у вас не выйдет. В журнале нужно фиксировать все, что вы делаете. Потом на основе записей журнала вам нужно будет написать конспект.
Он же помогает заполнить все структурные элементы работы, к которым относятся:
Как написать вывод к лабораторной
Вывод в лабораторной — итог всего практического исследования. Если вы ищете ответ на вопрос как сделать лабораторную по химии и получить «отлично», то первым делом нужно сконцентрироваться на выводах.
Обратите внимание на цели исследования — на основании их формулируются выводы. Важно не копировать цели из введения, а дополнить их и развивать.
При этом держите в уме короткий и емкий вывод: 2-3 предложения будет достаточно.
В статье о лабораторной по физике мы приводили образец оформления. Он почти ничем не отличается от того, что требуется в практикуме по химии. Поэтому можете смело на него ориентироваться.
Урок 1. Основные понятия и законы предмета «Химия»
Простейшие понятия: вещество, молекула, атом, химический элемент
Что такое химия? Где мы встречаемся с химическими явлениями? Везде. Сама жизнь — это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов…
Что изучает химия? Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество — понятно: это то, из чего состоит окружающий нас мир и мы сами. Но что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество. Изменились молекулы — изменилось вещество (оно стало другим!), — изменились его свойства:
Все эти изменения — следствие сложных и многообразных химических процессов. Итак,
химия — это наука о веществах и их превращениях.
При этом исследуются не всякие превращения, а только такие, при которых
В этом определении встречаются такие понятия, как «вещество», «молекула», «атом». Разберём их подробнее.
Вещество — это то, из чего состоят окружающие нас предметы. Каждому абсолютно чистому веществу (таких в природе, кстати, не существует) приписывают определённую химическую формулу, которая отражает его состав, например:
Выше приведены молекулярные формулы двух веществ. Следует отметить, что далеко не все вещества состоят из молекул, так как существуют вещества, которые состоят из атомов или ионов. Например, алмаз состоит из атомов углерода, а обычная поваренная соль — из ионов Na + и ионов Cl – (условная «молекула» — NaСl).
Наименьшая частица вещества, которая отражает его качественный и количественный состав, называется молекулой.
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака):
Число атомов в молекуле обозначают при помощи индекса:
Но! Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента:
Аналогично изображают число молекул:
Почему атомы водорода и кислорода имеют разное название, разный символ? Потому что это атомы разных химических элементов.
Химический элемент — это частицы с одинаковым зарядом ядер их атомов.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях? Из чего состоит атом*?
* Подробнее о строении атома будет рассказано в уроке 3.
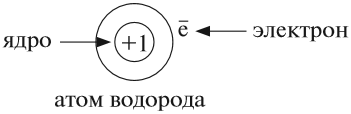
Атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:
В ходе химических реакций число электронов любого атома может изменяться, но заряд ядра атома в химических реакциях НЕ МЕНЯЕТСЯ!
Поэтому заряд ядра атома — своеобразный «паспорт» химического элемента. Все атомы с зарядом ядра +1 принадлежат химическому элементу под названием «водород». Атомы с зарядом ядра +8 составляют химический элемент «кислород».
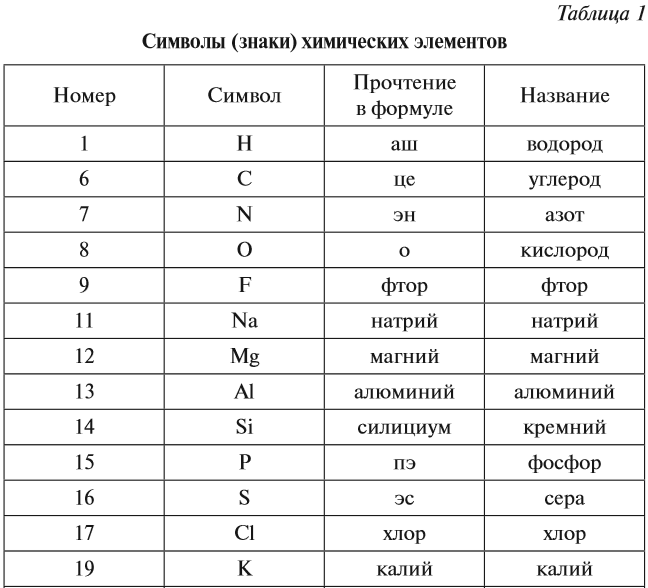
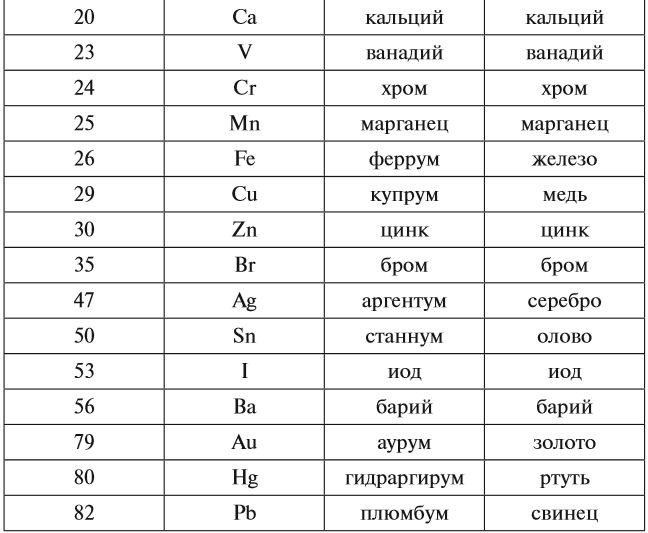
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Менделеева (порядковый номер равен заряду ядра атома); определённое название и, для некоторых химических элементов, особое прочтение символа в химической формуле (табл. 1).
Подведём итог. Вещества состоят из молекул, молекулы состоят из атомов, атомы с одинаковым зарядом ядра относятся к одному и тому же химическому элементу.
Но, если вещество состоит из молекул, то любое изменение состава или строения молекулы приводит к изменению самого вещества, его свойств.
Вопрос. Чем отличаются химические формулы веществ: Н2О и Н2О2?
Хотя по составу молекулы этих веществ отличаются на один атом кислорода, сами вещества по свойствам сильно отличаются друг от друга. Воду Н2О мы пьём и жить без неё не можем, а Н2О2 — перекись водорода, пить нельзя, а в быту её используют для обесцвечивания волос.
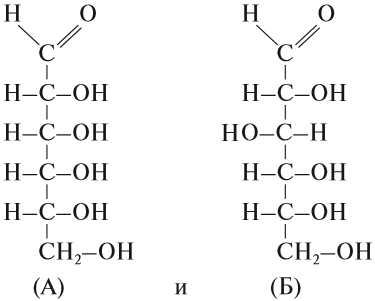
Вопрос. А чем отличаются химические формулы веществ:
Состав этих веществ — аллозы (А) и глюкозы (Б) — одинаков — С6Н12О6. Отличаются они строением молекул, в данном случае — расположением групп ОН в пространстве. Глюкоза — универсальный источник энергии для большинства живых организмов, а аллоза практически не встречается в природе и не может быть источником энергии.
Простые и сложные вещества. Валентность
Вещества бывают простые и сложные. Если молекула состоит из атомов одного химического элемента, — это простое вещество:
Если в состав вещества входят атомы только одного химического элемента — это простое вещество. Причём некоторые химические элементы образуют несколько простых веществ. Так, химический элемент кислород образует простое вещество «кислород» О2 и простое вещество «озон» О3*.
* В 2002 г. появилось сообщение о существовании ещё одного простого вещества кислорода — O4.
А химический элемент углерод образует четыре простых вещества, причём ни одно из них не называется «углерод». Эти вещества отличаются пространственным расположением атомов:
В четвертой модификации «углерода» — фуллерене — атомы углерода образуют сферу, т. е. молекулы фуллерена напоминают мячик.
Существование элемента в виде нескольких простых веществ называется аллотропией. Алмаз, графит, карбин, фуллерен — аллотропные модификации элемента «углерод», а кислород и озон — аллотропные модификации элемента «кислород».
Таким образом, не следует путать эти понятия: «химический элемент» и «простое вещество», а также «молекула» и «атом».
Очень часто в письменных записях слова «молекула» или «атом» заменяют соответствующими символами, но не всегда правильно. Так, нельзя писать: «В состав воды входит Н2», так как речь здесь идёт о химическом элементе водороде — Н. Нужно писать: «В состав воды входит (Н)». Аналогично, правильной будет запись: «При действии металла на раствор кислоты выделится Н2», т. е. вещество водород, молекула которого двухатомна.
Молекулы сложных веществ состоят из атомов разных химических элементов:
Как известно, в состав сложных веществ входят атомы разных химических элементов. Эти атомы соединяются между собой химическими связями: ковалентными, ионными, металлическими.
Способность атома образовывать определённое число ковалентных химических связей называется валентностью. (Подробнее см. урок 4 «Химическая связь».) Правильнее всего определять валентность по графическим или структурным формулам:
В таких формулах одна чёрточка обозначает одну ковалентную связь, т. е. «одну валентность». На практике чаще всего валентность определяют по молекулярной формуле, хотя здесь правильнее говорить о степени окисления элемента (см. урок 7). Иногда результат определения степени окисления соответствует реальному значению валентности, но бывают и неодинаковые результаты.
Задание 1.1. Определите «валентность» (степени окисления) атомов кальция и углерода по формуле СаС2. Совпадает ли полученный результат с реальным значением валентности?
В устойчивой молекуле не может быть «свободных», «лишних» валентностей! Поэтому для двухэлементной молекулы число химических связей (валентностей) атомов одного элемента равно общему числу химических связей атомов другого элемента.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Для других атомов валентность можно определить (вычислить) из химической формулы вещества.
Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. урок 7). Но поскольку в некоторых соединениях числовые значения этих понятий совпадают, то иногда по формуле можно определять и валентность.
При этом следует учитывать изложенное выше правило о химической связи.
Сделаем практические выводы.
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
4. В остальных случаях ставьте валентности «крест-накрест», т. е. валентность первого атома равна числу атомов второго элемента и наоборот:
Задание 1.2. Определите валентности элементов в соединениях:
Вначале укажите валентности атомов, у которых она постоянна! Аналогично определяется валентность атомных групп (ОН), (РО4), (SО4) и так далее.
Задание 1.3. Определите валентности атомных групп (в формулах выделены курсивом):
Обратите внимание! Одинаковые группы атомов (OH), (РО4), (SO4) имеют одинаковые валентности во всех соединениях.
Зная валентности атома или группы атомов можно составить формулу соединения. Для этого пользуются правилами:
Задание 1.4. Составьте химические формулы соединений:
Уравнения химических реакций
Вещества, состав которых отражают химические формулы, могут участвовать в химических процессах (реакциях). Графическая запись, соответствующая данной химической реакции, называется уравнением химической реакции. Например, при сгорании (взаимодействии с кислородом) угля происходит химическая реакция:
Запись показывает, что один атом углерода С, соединяясь с одной молекулой кислорода O2, образует одну молекулу углекислого газа СО2. Число атомов каждого химического элемента до и после реакции должно быть одинаково! Это правило — следствие Закона сохранения массы вещества: масса исходных веществ равна массе продуктов реакции. Закон был открыт в 18-м веке М. В. Ломоносовым и, независимо от него, А. Л. Лавуазье.
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли КClO3, получается соль КСl и кислород О2:
Число атомов калия и хлора одинаково, а кислорода — разное. Уравняем их:
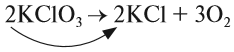
Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
Теперь между правой и левой частями уравнения можно поставить знак равенства:
Полученная запись показывает, что при разложении двух молекул КClO3 получается две молекулы КСl и три молекулы кислорода O2. Число молекул показывают при помощи коэффициентов.
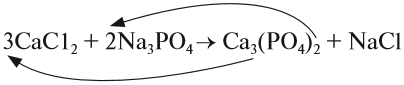
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым:
Последовательность действий такова:
1. Определим валентность исходных атомов и группы PO4:
2. Перенесём эти числа в правую часть уравнения:
3. Составим химические формулы полученных веществ по валентностям составных частей:
4. Обратим внимание на состав «самого сложного» соединения: Ca3(PO4)2 и уравняем число атомов кальция (их три) и число групп РО4 (их две):
5. Число атомов натрия и хлора до реакции теперь стало равным шести; доставим соответствующий коэффициент:
Эти правила образуют Алгоритм составления уравнений химических реакций обмена, так как, пользуясь этой последовательностью, можно уравнять схемы многих химических реакций, за исключением более сложных окислительно-восстановительных реакций (см. урок 7).
Химические реакции бывают разных типов. Основными являются:
1. Реакции соединения:
Здесь из двух и более веществ образуется одно вещество:
2. Реакции разложения:
Здесь из одного вещества получаются два вещества и более веществ:
3. Реакции замещения:
Здесь реагируют простое и сложное вещества, образуются также простое и сложное вещества, причём простое вещество замещает часть атомов сложного вещества:
4. Реакции обмена:
Здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
Существуют и другие типы химических реакций.
Задание 1.5. Расставьте коэффициенты в предложенных выше примерах.
Задание 1.6. Расставьте коэффициенты и определите тип химической реакции:
Выводы
Вещества бывают простые и сложные. Состав веществ показывают при помощи химических формул. Формулы веществ составляют, учитывая валентности составных частей этих веществ. Запись химического процесса при помощи формул называется уравнением химической реакции. Химические реакции бывают разных типов: обмена, замещения, разложения, соединения и другие.