Геморрагический синдром
Клиническая характеристика геморрагического синдрома
| I.Гематомный тип (нарушение внутреннего пути свертывания коагуляционного гемостаза) | II.Петехиально-пятнистый (микроциркуляторный) тип (нарушение тромбоцитаного звена гемостаза, внешнего пути свертывания коагуляционного гемостаза) | III.Смешанный (синячково-гематомный) тип (сочетанное нарушение и тромбоцитарного и коагуляционного звена гемостаза) |
(патология микрососудистого русла)
(локальная сосудистая патология)
Симптомы геморрагического синдрома
Характер и локализация кожных высыпаний при геморрагическом синдроме определяют симптоматику данной патологии.
Основной симптом – длительные кровотечения, возникающие как следствие травмы или изнуряющей физической нагрузки, сильного перенапряжения, переохлаждения или перегревания, которые могут также происходить самопроизвольно.
В каждом пятом случае патологии наблюдается сыпь различного характера, могут появляться как мелкие петехии, так и крупные гематомы некротических форм, возможно возникновение ангиэктазий.
Геморрагический синдром может стать следствием приема лекарственных препаратов, которые влияют на естественные процессы тромбоцитов и понижают свертываемость крови. Кроме того, у пациентов, страдающих болезнью Верльгофа, гемофилией и дефицитом протромбина также может наблюдаться данная патология.
Проявления геморрагического синдрома
Разновидности геморрагического синдрома
Нарушение внутреннего пути свертывания коагуляционного гемостаза (гематомный тип кровоточивости)
Врожденная и приобретенная афибриногенемия
Нарушение тромбоцитарного звена гемостаза, внешнего пути свертывания коагуляционного гемостаза (петехиально-пятнистый тип кровоточивости)
Тромбоцитопения
Тромбоцитопатия
Дефицит факторов II,V,VII,XI
Cочетанное нарушение тромбоцитарного и коагуляционного звена гемостаза (смешанный (синячково-гематомный) тип кровоточивости)
Диссеминированное внутрисосудистое свёртывание
Болезнь Виллебранда
Патология микрососудистого русла (васкулитно-пурпурный тип кровоточивости)
Кровоточивость петехиальная с эксудативно-воспалительными явлениями, очагами некроза, гематурия, артралгия, кровоточивость слизистых.
Геморрагический васкулит
Ангиоматозные кровотечения
Диагностика геморрагического синдрома
Вовремя установленный диагноз поможет специалисту назначить эффективное лечение, а вам – сделать свои сосуды здоровыми раз и навсегда. Подтвердить или опровергнуть диагноз можно, сдав ряд лабораторных анализов, направленных на получение детальной информации о состоянии крови. Также понадобится провести коагуляционные тесты, во время спорных ситуаций врач-диагност может взять стернальную пункцию для углубленной диагностики.
После получения полной картины заболевания, определения ее стадии, причин и степени тяжести геморрагического синдрома, будет назначено лечение.
Лечение геморрагического синдрома
Основой выбора метода лечения геморрагического синдрома является определение причины заболевания, однако существуют следующие ключевые принципы:
Профилактика геморрагического синдрома
Важнейшей и основополагающей частью предупреждения геморрагического синдрома является полное медицинское обследование для своевременного установления и устранения его возможных причин.
Новорожденным недоношенным детям необходимо введение подкожно витамина К и прикладывание ребенка к груди как можно скорее после рождения.
Диетическое питание пациентов, склонных в данной патологии, должно быть основано на усиленном потреблении витамина К, а также белков, овощей и фруктов. Кроме того, таким людям необходимо избегать физической активности, приводящей к возникновению травм и ранений.
Что такое геморрагические осложнения
Данковцева Е.Н., Архипов С.Л., Затейщиков Д.А.
По данным FDA (Food and Drug Administration), непрямые антикоагулянты (НАК) входят в десятку препаратов, наиболее часто вызывающих осложнения. При этом кровотечения – пожалуй, самое частое и опасное из них. Частота их развития в различных клинических исследованиях с применением НАК составляла примерно 2,0 % (от 1,0 до 7,4 %).
Все кровотечения, осложняющие терапию НАК, принято разделять на три категории:
2) тяжелые (требующие для их остановки хирургического вмешательства, переливания эритроцитарной массы или сопровождающиеся снижением систолического артериального давления (АД) ниже 90 мм рт. ст. с олигурией или падением уровня гемоглобина более чем на 2 г/л);
3) нетяжелые кровотечения (все остальные).
Внутричерепные кровоизлияния (ВЧК) – наиболее опасные из всех геморрагических осложнений терапии НАК. Считается, что прием варфарина увеличивает риск ВЧК в 8–10 раз [1, 2]. Их частота, по данным разных авторов, составляет около 0,3–1,0 % в год, а доля среди всех ВЧК – от 6 до 24 % [3–5]. На внутримозговые кровоизлияния приходится 70 % от всех варфарин-ассоциированных ВЧК, оставшиеся 30 % – это субдуральные и субарахноидальные кровоизлияния [1]. Хотя риск возрастает с увеличением международного нормализованного отношения (МНО), большая часть варфарин-ассоциированных ВЧК отмечается в период, когда МНО находится в пределах терапевтического диапазона [6–9]. ВЧК на фоне терапии варфарином встречаются несколько чаще и при меньшей степени гипокоагуляции у азиатов, африканцев и испанцев, чем у лиц белой расы [10, 11].
При варфарин-ассоциированных ВЧК смертность достигает 67 %, что приблизительно в 2 раза выше, чем у больных, у которых кровоизлияние возникло без участия антикоагулянтов [1, 9, 12]. На варфарин-ассоциированные ВЧК приходится до 90 % смертности от всех варфарин-ассоциированных кровотечений. M.C. Fang и соавт. [13] проанализировали данные 13 559 взрослых пациентов с мерцательной аритмией (МА) неревматического генеза. Было выявлено 72 случая ВЧК и 98 тяжелых экстракраниальных кровотечений. На момент выписки 76 % больных ВЧК имели тяжелую степень инвалидности или умерли.
Оценка риска развития ВЧК
Следует помнить, что риск геморрагических осложнений при лечении НАК есть у всех больных, но также совершенно очевидно, что степень риска у них различна. И самое сложное – это учет всех фактов ‘за” и “против” назначения НАК, т. е. принятие в конечном счете решения по поводу соотношения риска и пользы лечения. Для решения вопроса о целесообразности и безопасности терапии антикоагулянтами для конкретного больного необходимо оценить риск геморрагических осложнений. В настоящее время наиболее часто используются шкалы HEMORR2HAGES и HASBLED (табл. 1, 2).
Примечание. АЛТ – аланинаминотрансфераза, АСТ – аспартатаминотрансфераза, ВГН – верхняя граница нормы, НПВС – нестероидные противовоспалительные средства, АГ – артериальная гипертензия.
Примечание. АЛТ – аланинаминотрансфераза, АСТ – аспартатаминотрансфераза, ВГН – верхняя граница нормы; ЩФ – щелочная фосфатаза, АГ – артериальная гипертензия.
Шкала HEMORR2HAGES предложена коллективом из Вашингтонского университета для оценки риска тяжелых кровотечений [14]. Она составлена на основании анализа результатов NRAF (National Registiy of Atrial Fibrillation). В анализ вошли результаты обследования 3971 больного МА. За год наблюдения тяжелые кровотечения возникли у 162 из 3138 больных, из них у 67,3 % отмечены желудочно-кишечные, у 15,4 % – ВЧК и у 17,3 % – кровотечения другой локализации. В шкалу HEMORR2HAGES помимо используемых ранее факторов риска были добавлены генетические факторы. Риск геморрагических осложнений существенно возрастал при увеличении числа баллов всего на одну единицу: 1 балл – 2,2 % в год, 2 балла – 4,4 %, 5 баллов и более – 12,3 %. Сравнение с предлагавшимися ранее шкалами оценки риска геморрагических осложнений показало преимущество шкалы HEMORR2HAGES.
Позднее на основании анализа данных того же регистра больных (NRAF) разработана еще одна шкала оценки риска геморрагических осложнений у больных, получающих антитромботическую терапию по поводу мерцательной аритмии, – HAS-BLED [15]. Данная шкала выгодно отличается от HEMORR2HAGES своей простотой. Каждый фактор дает 1 балл, за исключением некоторых. Максимальная сумма баллов – 9. Согласно шкале HAS-BLED, так же как и HEMORR2HAGES, риск геморрагических осложнений существенно возрастает при увеличении числа баллов: 1 балл – 1,02 % в год, 2 балла – 1,88 %, 3 балла – 3,74 %, 4 балла – 8,70 %, 5 баллов и более – 12,5 %. Предсказательная ценность этих двух шкал у больных, принимающих НАК, оказалась сходной. Шкала HAS-BLED вошла в официальные рекомендации Европейского общества кардиологов по ведению больных мерцательной аритмией в качестве основной для оценки риска развития геморрагических осложнений на фоне терапии антикоагулянтами [16].
Расчет риска кровотечения при помощи описанных шкал и сравнение его с риском тромбоэмболических осложнений (ТЭО) позволяют принимать взвешенное решение о целесообразности назначения антикоагулянтов каждому конкретному больному. К сожалению, специфических шкал для оценки риска именно ВЧК на фоне терапии варфарином или другими НАК в настоящее время не существует.
Диагноз ВЧК
Появление у больного, получающего НАК, резкой головной боли преимущественно в затылочной области, тошноты, рвоты, не приносящей облегчения, несистемного головокружения, а также оглушенного сознания является основанием для немедленного исключения диагноза ВЧК. Симптомы кровоизлияния обычно развиваются внезапно [3, 7, 17–19], причем в первую очередь могут развиться менингеальный синдром и субфебрилитет. Уже в первые часы признаки ВЧК можно определить с помощью компьютерной или магнитно-резонансной томографии (МРТ). Высокочувствительной методикой является МРТ с использованием градиентного эхо [1, 20, 21].
Патофизиология
R.G. Hart и соавт. [22] высказали гипотезу о том, что использование НАК всего лишь демаскирует ВЧК, которые в другом случае остались бы бессимптомными, особенно у больных АГ или цереброваскулярной болезнью; несколько обсервационных исследований подтверждают это предположение. Во-первых, МРТ в режиме градиентного эхо показывает, что микрокровоизлияния, являющиеся одним из факторов риска ВЧК на фоне применения антитромботических препаратов [23, 24], могут выявляться даже у лиц без острой неврологической симптоматики – как правило, пожилых и страдающих АГ [25].
Во-вторых, церебральная амилоидная ангиопатия, которая наиболее часто обнаруживается у людей старше 65 лет, наряду с возрастом является одним из факторов риска и спонтанных, и варфарин-ассоциированных ВЧК [26, 27].
В-третьих, данные исследований SPIRIT (Stroke Prevention in Reversible Ischemia Trial) и EAFT (European Atrial Fibrillation Trial) показывают, что пациенты с уже имеющейся цереброваскулярной болезнью имеют значительно более высокий риск варфарин-ассоциированных ВЧК [28, 29], а наличие очаговых или диффузных гиподенсивных изменений в глубоких слоях белого вещества (т. н. лейкоареозис) является независимым предиктором варфарин-ассоциированных ВЧК [30]. Кроме того, локализация спонтанных и варфарин-ассоциированных ВЧК совпадает [4, 12]. Таким образом, причины, лежащие в основе обоих вариантов кровоизлияний, могут бытьодними и теми же, а использование НАК действует лишь как усугубляющий фактор.
По данным J.J. Flibotte и соавт. [19], связи между исходным размером гематомы и приемом варфарина не обнаружено. Предикторами большего исходного объема гематомы являются гипергликемия (p 6 – 50 МЕ/кг [50]. После начальной в/в инфузии 500–1000 МЕ со скоростью 100 МЕ/мин ее продолжают со скоростью 25 МЕ/мин или ниже. МНО необходимо измерить через 30 минут после начала инфузии, чтобы убедиться, что оно нормализовалось; в противном случае должен быть рассмотрен вопрос о продлении инфузии. Фитоменадион (10 мг в/в) должен применяться одновременно с КПК [34, 44, 47]. В отсутствие фитоменадиона вводят менадион (викасол) 15 мг в/м.
Некоторые авторы рекомендуют одновременно использовать низкие дозы нефракционированного гепарина или низкомолекулярных гепаринов для снижения риска тромбозов [38]. Эптаког альфа (активированный; рекомбинантный фактор VIIa – rVIIa), одобренный для лечения геморрагических осложнений у больных гемофилией, в отдельных случаях может также использоваться для лечения больных ВЧК, связанными с варфарином [51–55]. В нашей стране rVIIa зарегистрирован как Коагил-VII (Лекко) и НовоСэвен (Ново Нордиск). Быстрая коррекция МНО продемонстрирована в двух небольших наблюдениях, включивших семь человек с варфарин-ассоциированными ВЧК, которые одновременно получали rVIIa, СЗП и фитоменадион [53, 54].
Остается неясным, насколько точно уровень МНО отражает коагуляционный статус после введения рекомбинантного фактора VIIa. Дело в том, что фактор VIIa временно корректирует дефицит только фактора VII, но не возмещает дефицит других витамин-K-зависимых факторов свертывания. Повторное введение rVIIа необходимо, если одновременно не вводят препараты витамина K или СЗП. В настоящее время Американское общество гематологов (American Society of Hematology) не рекомендует рутинно использовать rVIIа для устранения эффектов варфарина [56]. Кроме того, следует помнить, что редкими, но серьезными осложнениями терапии rVIIа также являются тромбоэмболии [34] и этот факт может осложнять его применение у больных высокого риска ТЭО.
D.K. Nishijima и соавт. [57] сравнивали прогноз у больных, постоянно принимавших варфарин и поступивших в отделение неотложной помощи в связи с травматическим ВЧК, в зависимости от факта применения rFVIIa (n = 40, по 20 в каждой группе). Формально статистически значимых различий в частоте развития ТЭО не было, однако в группе стандартного лечения был зарегистрирован 1 (5,0 %) тромбоэмболический эпизод на 20 больных, а в rVIIа – 4 (20,0 %). Время до нормализации МНО было меньше в группе rFVIIa (4,8 против 17,5 часа в группе стандартного лечения, p 200 мм рт. ст. или среднее АД > 150 мм рт. ст., обоснованно агрессивное снижение АД путем в/в инфузии антигипертензивных препаратов с частым (каждые 5 минут) мониторированием уровня АД. Если систолическое АД > 180 мм рт. ст. или среднее АД > 130 мм рт. ст. и есть вероятность повышенного внутричерепного давления, рекомендуется мониторинг внутричерепного давления и снижение АД с использованием прерывистой или постоянной в/в инфузии антигипертензивных препаратов для поддержания церебрального перфузионного давления на уровне ≥ 60 мм рт. ст. Если внутричерепное давление не повышено, рекомендуется более медленное снижение АД (цель – АД 160/90 мм рт. ст. или среднее АД 110 мм рт. ст.) [39].
Прогноз при ВЧК
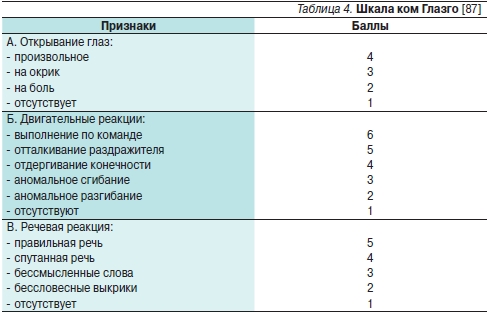
Чем выше уровень МНО в момент госпитализации, тем больше вероятность увеличения размера гематомы, остаточного неврологического дефицита и смерти [3, 17, 46, 65, 66]. Летальный исход отмечается у 2/3 больных ВЧК, если МНО в момент госпитализации превышает 3 [65]. С плохим прогнозом также ассоциируются большой объем гематомы (> 50 мл), распространение кровоизлияния в желудочке (intraventricular extension), а также смещение срединных структур мозга [3, 6, 7]. По данным A.Y. Zubkov и соавт. [67], прогностически неблагоприятными факторами являются низкая сумма баллов по шкале Глазго (табл. 4) в момент поступления и большой изначальный объем гематомы. Развитие неврологического дефицита никак не зависит от уровня МНО при поступлении.
Возобновление антикоагулянтной терапии
Описанные выше меры по коррекции уровня коагуляции могут быть весьма эффективными, но как только кровотечение остановлено, на первое место вновь выходит вопрос риска развития тромбоэмболий. Мнения экспертов о том, когда следует возобновлять антикоагулянтную терапию и следует ли ее возобновлять вообще, расходятся.
Риск повторного ВЧК в течение первых 3 месяцев составляет 1 %, а в дальнейшем – 2–4 % в год, но у больных, продолжающих получать варфарин, риск, вероятно, выше [68–71]. Несколько небольших работ было посвящено риску ТЭО и повторных ВЧК в случае возобновления или полной отмены варфарина [3, 72–76].
По-видимому, решение о возобновлении приема НАК должно основываться на индивидуальной оценке соотношения риска ТЭО и повторных кровоизлияний. Наличие церебральной амилоидной ангиопатии и признаков микрокровоизлияний (по данным МРТ) увеличивает риск повторных геморрагических эпизодов [77].
В случае применения варфарина с целью первичной профилактики ишемического инсульта у пожилых пациентов с МА риск повторных ВЧК может превысить пользу, поэтому мнение больного является немаловажным фактором в принятии решения о продолжении антикоагулянтной терапии. У больных с исходно низким риском ТЭО, которым не требуется возобновления антикоагулянтной терапии, после перенесенного ВЧК рекомендуется ношение эластичных чулок или перемежающаяся пневматическая компрессия ног [39, 78].
У больных с высоким риском ТЭО (протезированные клапаны сердца, МА, ишемический инсульт в анамнезе и др.) риск ТЭО без антикоагулянтной терапии гораздо выше, поэтому лечение НАК следует возобновлять. После нормализации МНО на фоне лечения КПК многие эксперты для профилактики тромбоза глубоких вен нижних конечностей предлагают начинать подкожное введение низких доз нефракционированного гепарина (5000 МЕ 2 раза в сутки) либо низкомолекулярных гепаринов (эноксапарин 40 мг 1 раз в сутки или дальтепарин 5000 МЕ 1 раз в сутки) уже через 48 часов после развития ВЧК, а через несколько дней увеличивать дозу прямых антикоагулянтов до лечебной [77]. Европейский комитет по инсульту рекомендует больным со строгими показаниями к антикоагулянтной терапии возобновлять прием варфарина через 10–14 дней [79], а Американская кардиологическая ассоциация допускает возобновление его приема у лиц с очень высоким риском тромбоэмболий уже через 7–10 дней от развития кровоизлияния [71, 80].
Однако ряд экспертов считают неоправданным использование антикоагулянтного мостика, аргументируя это тем, что ежедневный риск ТЭО у лиц с протезированными клапанами непосредственно после ВЧК достаточно низок – 0,016 % [75].
При особенно высоком риске повторных ВЧК у лиц с МА неклапанного генеза альтернативой может быть прием антиагрегантов [81]. Использование их в сочетании с варфарином вероятнее всего увеличивает риск повторных ВЧК, и эту комбинацию не следует назначать рутинно [82–84].
Интересным представляется анализ, выполненный А. Majeed и соавт. [85]. Проведена оценка истории болезней 2869 пациентов, последовательно госпитализированных в связи с ВЧК. С использованием модели Кокса был подсчитан ежедневный суммарный риск ВЧК и ишемического инсульта при возобновлении терапии варфарином и отказе от него. Отношение шансов развития повторных ВЧК при возобновлении приема варфарина составило 5,6 (95 % доверительный интервал [ДИ] – 1,8–17,2), для ишемического инсульта – 0,11 (95 % ДИ – 0,014–0,890). Суммарный риск обоих состояний был наиболее низким, если прием варфарина возобновляли в период между 10-й и 30-й неделями от перенесенного ВЧК.
Таким образом, в настоящее время трудно говорить о наличии четких рекомендаций по возобновлению терапии варфарином после ВЧК. Слишком много факторов может определять индивидуальный риск повторных кровотечений или тромбоэмболий, и не все они хорошо изучены. Представляется, что все-таки большая часть больных высокого риска по развитию ТЭО получит большую пользу от возобновления терапии варфарином, чем наоборот.
Литература
1. Hart RG, Boop BS, Anderson DC. Oral anticoagulants and intracranial hemorrhage: facts and hypotheses. Stroke 1995;26:1471—77.
2. Go AS, Hylek EM, Chang Y, et al. Anticoagulation therapy for stroke prevention in atrial fibrillation: how well do randomized trials translate into clinical practice? JAMA 2003;290:2685–92.
3. Berwaerts J, Robb OJ, Jeffers TA, Webster J. Intracerebral haemorrhages and oral anticoagulation in the north of Scotland. Scott Med J2000;45:101–04.
4. Nilsson OG, Lindgren A, Stahl N, et al. Incidence of intracerebral and subarachnoid haemorrhage in southern Sweden. J Neurol NeurosurgPsychiatry 2000;69:601–07.
5. Woo D, Sauerbeck LR, Kissela BM et al. Genetic and environmental risk factors for intracerebral hemorrhage: preliminary results of a populationbased study. Stroke 2002;33:1190–95.
6. Neau JP, Couderq C, Ingrand P, et al. Intracranial hemorrhage and oral anticoagulant treatment. Cerebrovasc Dis 2001;11:195–200.
7. Sjoblom L, Hardemark HG, Lindgren A, et al. Management and prognostic features of intracerebral hemorrhage during anticoagulant therapy: a Swedish multicenter study. Stroke.2001;32:2567–74.
8. Punthakee X, Doobay J, Anand SS. Oralanticoagulant-related intracerebral hemorrhage. Thromb Res 2002;108:31–36.
9. Hylek EM, Go AS, Chang Y, et al. Effect of intensity of oral anticoagulation on stroke severity and mortality in atrial fibrillation. N Engl J Med2003;349:1019–26.
10. Mok V, Wong KS, Lam W, et al. Warfarinassociated intracerebral hemorrhage occurs with lower intensification of anticoagulation in Chinese. Neurol J Southeast Asia. 2001;6:107–11.
11. Shen AY, Yao JF, Brar SS, et al. Racial/Ethnic Differences in the Risk of Intracranial Hemorrhage Among Patients With Atrial Fibrillation. Stroke2008;39:2736–43.
12. Rosand J, Eckman MH, Knudsen KA, et al. The effect of warfarin and intensity of anticoagulation on outcome of intracerebral hemorrhage. Arch Inter Med 2004;164:880–84.
13. Fang MC, Go AS, Chang Y, et al. Death and disability from warfarin-associated intracranial and extracranial hemorrhages. Am J Med2007;120(8):700–05.
14. Gage BF. Clinical classification schemes for predicting hemorrhage: Results from the National Registry of Atrial Fibrillation (NRAF). Am Heart J2006;151:713–19.
15. Pisters R, Lane DA, Nieuwlaat R, et al. A novel user-friendly score (HAS-BLED) to assess oneyear risk of major bleeding in atrial fibrillation patients: The Euro Heart Survey. Chest2010;138:1093–100.
16. Camm AJ, Kirchhof P, Lip GYH, et al. Guidelines for the management of atrial fibrillation. The Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). EurHeart J 2010;31(19):2369–429.
17. Yasaka M, Oomura M, Ikeno, K et al. Effect of prothrombin complex concentrate on INR and blood coagulation system in emergency patients treated with warfarin overdose. Ann Hematol 2003; 82:121–23.
18. Yasaka M, Minematsu K, Naritomi H, et al. Predisposing factors for enlargement of intracerebral hemorrhage in patients treated with warfarin. Thromb Haemost 2003;89:278–83.
19. Flibotte JJ, Hagan N, O’Donnell J, et al. Warfarin, hematoma expansion, and outcome of intracerebral hemorrhage. Neurology 2004;63:1059–64.
20. Ichikawa K, Yanagihara C. Sedimentation level in acute intracerebral hematoma in a patient receiving anticoagulation therapy: an autopsy study. Neuroradiology 1998;40:380–82.
21. Kidwell CS, Chalela JA, Saver JL, et al. Comparison of MRI and CT for detection of acute intracerebral hemorrhage. JAMA 2004;292:1823–30.
22. Hart RG. What causes intracerebral hemorrhage during warfarin therapy? Neurology 2000;55:907–08.
23. Lee S, Ryu W, Roh J. Cerebral microbleeds are a risk factor for warfarin-related intracerebral hemorrhage. Neurology 2009;72:171–76.
24. Lovelock CE, Cordonnier C, Naka H, et al. Antithrombotic Drug Use, Cerebral Microbleeds, and Intracerebral Hemorrhage. Stroke2010;41:1222–28.
25. Roob G, Schmidt R, Kapeller P, et al. MRI evidence of past cerebral microbleeds in a healthy elderly population. Neurology 1999;52:991–94.
26. Rosand J, Hylek EM, O’Donnell HC, Greenberg SM. Warfarin-associated hemorrhage and cerebral amyloid angiopathy: a genetic and pathologic study. Neurology 2000;55:947–51.
27. Yasaka M, Minematsu K, Yamaguchi T. Optimal intensity of international normalized ratio in warfarin therapy for secondary prevention of stroke in patients with non-valvular atrial fibrillation. Intern Med 2001;40:1183–88.
28. The Stroke Prevention in Reversible Ischemia Trial (SPIRIT) Study Group. A randomized trial of anticoagulants versus aspirin after cerebral ischemia of presumed arterial origin. Ann Neurol1997;42:857–65.
29. Gorter JW. Major bleeding during anticoagulation after cerebral ischemia: patterns and risk factors. Stroke Prevention In Reversible Ischemia Trial (SPIRIT). European Atrial Fibrillation Trial (EAFT) study groups. Neurology 1999;53:1319–27.
30. Smith EE, Rosand J, Knudsen KA, et al. Leukoaraiosis is associated with warfarinrelated hemorrhage following ischemic stroke. Neurology 2002;59:193–97.
31. Kazui S, Naritomi H, Yamamoto H, et al. Enlargement of spontaneous intracerebral hemorrhage. Incidence and time course. Stroke1996;27:1783–87.
32. Brott T, Broderick J, Kothari R, et al. Early hemorrhage growth in patients with intracerebral hemorrhage. Stroke 1997;28:1–5.
33. Becker KJ, Baxter AB, Bybee HM, et al. Extravasation of radiographic contrast is an independent predictor of death in primary intracerebral hemorrhage. Stroke 1999;30:2025–32.
34. Mayer SA, Brun NC, Begtrup K, et al. Recombinant Activated Factor VII for acute intracerebral hemorrhage. N Engl J Med 2005;352:777–85.
35. Mayer SA, Rincon F. Ultra-early hemostatic therapy for acute intracerebral hemorrhage. Semin Hematol 2006; 43(1):S70–76.
36. Goldstein JN, Thomas SH, Frontiero V, et al. Timing of fresh frozen plasma administration and rapid correction of coagulopathy in warfarin-related intracerebral hemorrhage. Stroke 2006;37:151–55.
37. Hellstern P, Halbmayer WM, Kohler M, et al. Prothrombin complex concentrates: indications, contraindications, and risks: a task force summary. Thromb Res 1999;95(4, suppl 1):S3–S6.
38. Yasaka M, Sakata T, Minematsu K, Naritomi H. Correction of INR by prothrombin complex concentrate and vitamin K in patients with warfarin related hemorrhagic complication. Thromb Res 2002;108:25–30.
39. Morgenstern LB, Hemphill JC, Anderson C, et al. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke 2010;41:2108–29.
40. Bianco C. Choice of human plasma preparations for transfusion. Transfus Med Rev 1999; 13:84–88.
41. Fiore LD, Scola MA, Cantillon CE, Brophy MT. Anaphylactoid reactions to vitamin K. J Thromb Thrombolysis 2001;11:175–83.
42. Steiner T, Rosand J, Diringer M. Intracerebral Hemorrhage Associated With Oral Anticoagulant Therapy: Current Practices and Unresolved Questions. Stroke 2006;37:256–62.
43. Hellstern P, Muntean W, Schramm W, et al. Practical guidelines for the clinical use of plasma. Thromb Res 2002;107(1):S53–57.
44. Yasaka M, Sakata T, Naritomi H, et al. Optimal dose of prothrombin complex concentrate for acute reversal of oral anticoagulation. ThrombRes 2005;115:455–59.
45. Hart RG. Management of warfarin-associated intracerebral hemorrhage. UpToDate Online. Last literature review version 18.2: May 2010. Last updated: JUN15, 2010.
46. Aguilar MI, Hart RG, Kase CS, et al. Treatment of Warfarin-Associated Intracerebral Hemorrhage: Literature Review and Expert Opinion. Mayo Clin Proc 2007;82(1):82–92.
47. Fredriksson K, Norrving B, Stromblad LG. Emergency reversal of anticoagulation after intracerebral hemorrhage. Stroke 1992;23:972–77.
48. Bertram M, Bonsanto M, Hacke W, et al. Managing the therapeutic dilemma: patients with spontaneous intracerebral hemorrhage and urgent need for anticoagulation. J Neurol2000;247:209–14.
49. Preston FE, Laidlaw ST, Sampson B, et al. Rapid reversal of oral anticoagulation with warfarin by a prothrombin complex concentrate (Beriplex): efficacy and safety in 42 patients. Br J Haematol 2002;116:619–24.
50. Noakes T. Derriford Hospital guideline for reversal of anticoagulation. 2003.
51. Deveras RA, Kessler CM. Reversal of warfarininduced excessive anticoagulation with recombinant human factor VIIa concentrate. Ann InternMed 2002;137:884–88.
52. Veshchev I, Elran H, Salame K, et al. Recombinant coagulation factor VIIa for rapid preoperative correction of warfarin-related coagulopathy in patients with acute subdural hematoma. Med Sci Monit 2002;8:CS98–100.
53. Sorensen B, Johansen P, Nielsen GL, et al. Reversal of the International Normalized Ratio with recombinant activated factor VII in central nervous system bleeding during warfarin thromboprophylaxis: clinical and biochemical aspects. Blood Coagul Fibrinolysis 2003;14:469–77.
54. Freeman WD, Brott TG, Barrett KM, et al. Recombinant factor VIIa for rapid reversal of warfarin anticoagulation in acute intracranial hemorrhage. Mayo Clin Proc 2004; 79:1495–500.
55. Brody DL, Aiyagari V, Shackleford AM, Diringer MN. Use of recombinant factor VIIa in patients with warfarin-associated intracranial hemorrhage. Neurocrit Care 2005; 2:263–67.
56. Rosovsky RP, Crowther MA. What Is the Evidence for the Off-label Use of Recombinant Factor VIIa (rFVIIa) in the Acute Reversal of Warfarin? Hematol Am Soc Hematol Educ Program2008:36–38.
57. Nishijima DK, Dager WE, Schrot RJ, et al. The efficacy of factor VIIa in emergency department patients with warfarin use and traumatic intracranial hemorrhage. Acad Emerg Med 2010;17(3):244–51.
58. Makris M, Greaves M, Phillips WS, et al. Emergency oral anticoagulant reversal: the relative efficacy of infusions of fresh frozen plasma and clotting factor concentrate on correction of the coagulopathy. Thromb Haemost 1997;77:477–80.
59. O’Shaughnessy DF, Atterbury C, Bolton Maggs P, et al. Guidelines for the use of fresh-frozen plasma, cryoprecipitate and cryosupernatant. BrJ Haematol 2004;126:11–28.
60. Jackson CM, Esnouf MP, Lindahl TL. A critical evaluation of the prothrombin time for monitoring oral anticoagulant therapy. PathophysiolHaemost Thromb 2003;33:43–51.
61. Pindur G, Morsdorf S, Schenk JF, et al. The overdosed patient and bleedings with oral anticoagulation. Semin Thromb Hemost 1999;25:85–88.
62. Hacke W. The dilemma of anticoagulation for patients with intracranial hemorrhage or how wide is the strait between Skylla and Karybdis? Neurology 2000;57:1682–84.
63. Sorensen B, Johansen P, Christiansen K, et al. Whole blood coagulation thrombelastographic profiles employing minimal tissue factor activation. J Thromb Haemost 2003;1:551–58.
64. Powers WJ, Zazulia AR, Videen TO, et al. Autoregulation of cerebral blood flow surrounding acute (6 to 22 hours) intracerebral hemorrhage. Neurology 2001;57:18–24.
65. Eckman MH, Rosand J, Knudsen KA, et al. Can patients be anticoagulated after intracerebral hemorrhage? A decision analysis. Stroke 2003;34(7):1710–16.
66. Huttner HB, Schellinger PD, Hartmann M, et al. Hematoma growth and outcome in treated neurocritical care patients with intracerebral hemorrhage related to oral anticoagulant therapy: comparison of acute treatment strategies using vitamin K, fresh frozen plasma, and prothrombin complex concentrates. Stroke 2006; 37:1465–70.
67. Zubkov AY, Mandrekar JN, Claassen DO. Predictors of Outcome in Warfarin-Related Intracerebral Hemorrhage. Arch Neurol2008;65(10):1320–25.
68. Bailey RD, Hart RG, Benavente O, et al. Recurrent brain hemorrhage is more frequent than ischemic stroke after intracranial hemorrhage. Neurology2001;56:773–77.
69. Vermeer SE, Algra A, Franke CL, et al. Longterm prognosis after recovery from primary intracerebral hemorrhage. Neurology 2002;59:205–09.
70. Viswanathan A, Rakich SM, EngelC, et al. Antiplatelet use after intracerebral hemorrhage. Neurology 2006;66:206–09.
71. Broderick J, Connolly S, Feldmann E, et al. American Heart Association; American Stroke Association Stroke Council; High Blood Pressure Research Council; Quality of Care and Outcomes in Research Interdisciplinary Working Group. Guidelines for the management of spontaneous intracerebral hemorrhage in adults: 2007 update: a guideline from the American Heart Association/American Stroke Association Stroke Council, High Blood Pressure Research Council, and the Quality of Care and Outcomes in Research Interdisciplinary Working Group. Stroke 2007;38:2001–23.
72. Butler AC, Tait RC. Restarting anticoagulation in prosthetic heart valve patients after intracranial haemorrhage: a 2 year follow up. Br J Haematol1998;103:1064–66.
73. Phan TG, Koh M, Wijdicks EF, et al. Safety of discontinuation of anticoagulation in patients with intracranial hemorrhage at high thromboembolic risk. Arch Neurol 2000;57:1710–13.
74. Ananthasubramaniam K, Beattie JN, Rosman HS, et al. How Safely and for How Long Can Warfarin Therapy Be Withheld in Prosthetic Heart Valve Patients Hospitalized With a Major Hemorrhage? Chest 2001;119:478–84.
75. De Vleeschouwer S, Van Calenbergh F, van Loon J, et al. Risk analysis of thrombo-embolic and recurrent bleeding events in the management of intracranial haemorrhage due to oral anticoagulation. Acta Chir Belg 2005;105:268–74.
76. Claassen DO, Kazemi N, Zubkov AY, et al. Restarting anticoagulation therapy after warfarin-associated intracerebral hemorrhage. ArchNeurol 2008;65:1313–18.
77. Goldstein JN, Greenberg SM. Should anticoagulation be resumed after intracerebral hemorrhage? Cleveland Clin J Med 2010;77(11):791–99.
78. Lacut K, Bressollette L, Le Gal G, et al. VICTORIAh (Venous Intermittent Compression and Thrombosis Occurrence Related to Intracerebral Acute hemorrhage) Investigators. Prevention of venous thrombosis in patients with acute intracerebral hemorrhage. Neurology 2005;65:865–69.
80. Furie KL, Kasner SE, Adams RJ, et al. Guidelines for the Prevention of Stroke in Patients With Stroke or Transient Ischemic Attack. A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke 2011;42:227–76.
81. Singer DE, Albers GW, Dalen JE, et al. American College of Chest Physicians. Antithrombotic therapy in atrial fibrillation: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008;133(suppl 6):546S–92S.
82. Hart RG, Benavente O, Pearce LA, et al. Increased risk of intracranial hemorrhage when aspirin is combined with warfarin: a meta-analysis and hypothesis. Cerebrovasc Dis 1999; 9:215–17.
83. Shireman TI, Howard PA, Kresowik TF, et al. Combined anticoagulant-antiplatelet use and major bleeding events in elderly atrial fibrillation patients. Stroke 2004;35:2362–67.
84. Gasse C, Hollowell J, Meier CR, et al. Drug interactions and risk of acute bleeding leading to hospitalisation or death in patients with chronic atrial fibrillation treated with warfarin. ThrombHaemost 2005;94:537–43.
85. Majeed A, Kim Y, Roberts RS, et al. Optimal Timing of Resumption of Warfarin After Intracranial Hemorrhage. Stroke 2010;41:2860.