Фокальная нодулярная гиперплазия
Фокальная нодулярная гиперплазия (ФНГ) является второй по частоте (после гемангиомы) доброкачественной опухолью печени. Частота ФНГ достигает 25% среди доброкачественных и 8% среди всех первичных новообразований печени. Опухоль встречается в любом возрасте, но чаще всего у женщин 30—40 лет (80—95%).
Причины возникновения
Однозначного мнения о причинах возникновения ФНГ не существует. Преобладание женщин, а также большая доля женщин (до 85%), употреблявших гормональные контрацептивы, долгое время поддерживали гипотезу о том, что данные препараты являются причиной заболевания. Однако обследование 216 женщин во Франции показало, что гормональные контрацептивы не оказывают влияния на частоту возникновения и размеры опухоли. В настоящее время считают, что ФНГ является реакцией гепатоцитов на локальные сосудистые мальформации (врожденные или приобретенные). Местные изменения кровотока ведут к появлению участков паренхимы с повышенным артериальным кровоснабжением и гиперплазии клеток печени. В пользу сосудистого генеза свидетельствует частое сочетание ФНГ с гемангиомами печени (до 23%) и различными сосудистыми аномалиями. Также отмечено появление ФНГ после травмы живота и химиотерапии, что связывают с повреждением внутрипеченочных сосудов.
ФНГ не трансформируется в злокачественную опухоль. Осложнения возникают крайне редко. В связи с доброкачественным характером и благоприятным прогнозом новообразования активного лечения не требуется. Необходимость в операции может возникнуть при увеличении размера, появлении симптомов или осложнений, а также при трудностях дифференциальной диагностики ФНГ и злокачественных опухолей печени.
Классификация
В гастроэнтерологии выделяют два типа нодулярной гиперплазии печени: классический (диагностируется в 80% случаев) и неклассический. Классический тип характеризуется наличием трех признаков: аномальной структуры дольки, извилистых толстостенных сосудов и гиперплазии желчных протоков; в 60% наблюдений обнаруживается центральный рубец с измененными сосудами разного калибра. При неклассическом типе всегда есть гиперплазия протоков, а один из оставшихся признаков (измененные сосуды или аномальная узловая архитектура) может отсутствовать. Неклассический тип подразделяют на три подтипа: аденоматозный гиперпластический, телеангиэктатический и нодулярную гиперплазию печени с клеточной атипией.
Что такое гиперплазия печени
Еще сравнительно недавно ФНГ относили к числу редких (3%) объемных поражений печени (ОПП) [2, 5, 6]. В настоящее время вследствие активного применения современных методов визуализации печени количество выявленных больных с ФНГ (как и очаговых заболеваний печени в целом) возросло [3, 12]. По данным литературы, ФНГ в структуре очаговых заболеваний печени занимает третье место среди доброкачественных ОПП после гемангиомы и аденомы [4, 8]. Этиология и патогенез ФНГ остаются неясными [11]. Теория об участии в развитии ФНГ гормональных контрацептивов не получила подтверждения, и в настоящее время большинство исследователей считают, что ФНГ является итогом прогрессирования врожденных или приобретенных сосудистых мальформаций, приводящих к гиперплазии гепатоцитов [8, 9, 14]. Макроскопически ФНГ чаще всего определяется в виде хорошо отграниченного от ткани печени, мягкоэластического образования, иногда плотного, желтого, вишневого, белесоватого, светло-коричневого или розоватого цвета, дольчатой структуры с наличием фиброзных прослоек, отходящих, как правило, от центрально расположенного рубца.
Микроскопическая картина схожа с таковой при истинном крупноузловом циррозе печени. Отмечается гиперплазия печеночной паренхимы, разделенной на узлы фиброзными прослойками; последние образуют рубцы звездчатой формы. Гепатоциты содержат избыточное количество гликогена и жира. В фиброзных прослойках имеются мелкие желчные протоки, иногда определяется воспалительная инфильтрация. Наблюдаются аномальные сосуды с утолщенными стенками. Процесс имеет очаговый характер, ткань печени вне очага выглядит неизмененной [8, 11].
Заболевание нередко протекает бессимптомно и является случайной находкой при УЗИ печени, выполненном по другому поводу. Клинические проявления (дискомфорт, чувство тяжести) обусловлены «масс-эффектом» и мало отличаются от таковых при иных ОПП. Специфическая лабораторная симптоматика отсутствует. ФНГ не озлокачествляется и крайне редко вызывает осложнения в виде внутрибрюшного кровотечения [13]. Описаны случаи регрессии опухоли вплоть до полного ее исчезновения [10]. При подтверждении диагноза ФНГ и отсутствии осложнений ряд авторов рекомендуют динамическое наблюдение, хотя подобная тактика дискутабельна [7, 9, 10]. Лечебная тактика при ФНГ остается спорной и, кроме того, в доступной литературе нами не обнаружено сообщений о попытках проследить «естественное» течение заболевания при отказе от операции. Это побудило нас поделиться собственным опытом лечения этого заболевания.
Материал и методы
Результаты и обсуждение
Ретроспективный анализ историй болезни с 1996 г. позволил выделить два периода, на протяжении которых тактические подходы к ведению больных с ФНГ претерпели некоторые изменения. Период с 1996 по 2005 г. характеризовался преимущественным применением УЗИ в качестве основного средства диагностики очагового заболевания печени, при этом ФНГ фигурировала в качестве «редкого» заболевания печени. Эхосемиотика ФНГ была разработана слабо, «осознанной» диагностической и лечебной тактики не было. В этих условиях сам факт обнаружения ОПП неясной этиологии определял показания к оперативному лечению, а точный морфологический диагноз ФНГ устанавливали после операции. В этот период оперированы 22 больных, причем в 3 наблюдениях выполнена эксплоративная лапаротомия. Показания к оперативному лечению выставляли довольно широко, но от удаления опухоли при подтверждении ее доброкачественного характера при предполагаемом вмешательстве большого объема воздерживались. Это дало возможность проследить «естественное» течение ФНГ. Выяснилось, что тезис о «безобидности» течения ФНГ сомнителен. Подтверждением служат два наших наблюдения, опубликованные в журнале «Хирургия» за 2005 г. [7].
Выполнена левосторонняя расширенная гемигепатэктомия, холецистэктомия. Гистологическое заключение: фибронодулярная гиперплазия печени (рис. 2). 
В практике хирургов-гепатологов ФНГ встречается не так редко. Следует заметить, что хирурги других специальностей, а также врачи-«визуалисты» недостаточно хорошо знакомы с этим заболеванием. На этапе амбулаторного обследования диагноз ФНГ был установлен только в 16 (30,7%) наблюдениях, что отражает как недостаточную осведомленность врачей-«визуалистов» об этом заболевании, так и объективные трудности диагностики, обусловленные вариабельностью соотношения в узле стромального, паренхиматозного и сосудистого компонентов. Чаще всего образование в печени на дооперационном этапе трактовали как гемангиому, рак печени, «объемное поражение печени неясного генеза». Исключить злокачественный характер патологического очага без операции далеко не всегда возможно, поэтому целесообразность лапаротомии как завершающего этапа диагностики в ряде наблюдений не вызывает сомнений. Целесообразность выполнения у всех больных предоперационной пункционной биопсии под контролем УЗИ или КТ представляется спорной. Часто приходится дифференцировать ФНГ со злокачественной опухолью печени, в частности гепатоцеллюлярным раком. Пункционная биопсия очага далеко не всегда информативна (репрезентативность биоптата) и окончательность гистологического заключения в таких ситуациях сомнительна. Кроме того, биопсия при раке чревата опасностью диссеминации либо имплантационного метастазирования. Мы согласны с мнением авторов, призывающих не выполнять предоперационную биопсию при подозрении на рак, поскольку этот фактор ухудшает прогноз заболевания [15]. При подозрении на гемангиому такая манипуляция в принципе противопоказана из-за угрозы внутрибрюшного кровотечения.
Исходя из нашего опыта, в настоящее время к длительному динамическому наблюдению больных даже с установленным и подтвержденным гистологически диагнозом ФНГ относимся с осторожностью. Обязательными условиями для этого следует считать возможность регулярного УЗ-мониторинга (1 раз в 6-8 мес) и достаточного комплайенса со стороны больного. Как и при большинстве ОПП, «выход» очага за пределы легкой операбельности чреват интраоперационными проблемами и тяжелым течением послеоперационного периода [6].
Комментарий от редколлегии
Широкое распространение и доступность современных неинвазивных методов диагностики (КТ, МРТ), а также увеличение их разрешающей способности привели к возрастанию частоты выявления бессимптомных очаговых образований печени. Подавляющее большинство из них являются доброкачественными, тем не менее перед врачом нередко встает вопрос о тактике ведения таких пациентов. Статья, посвященная фокальной нодулярной гиперплазии, одной из наиболее частых доброкачественных опухолей печени, безусловно, будет интересна хирургам-гепатологам, тем более, что русскоязычные публикации на эту тему единичны.
Для начала необходимо определиться с терминологией. В начале статьи авторы предлагают использовать термин «фибронодулярная гиперплазия». С этим можно соглашаться или нет, но для того, чтобы избежать путаницы и непонимания, лучше придерживаться международной терминологии, предложенной исследовательской группой в 1995 г. (Terminology of Nodular Hepatocellular Lesions. International Working Party. Hepatology, 1995), в которой данное образование определено как фокальная нодулярная гиперплазия (focal nodular hyperplasia) и предложены критерии, по которым его можно отличить от других регенераторных образований.
Неинвазивные методы играют главенствующую роль в диагностике ФНГ. МРТ и КТ обладают высокой чувствительностью и специфичностью, однако у ряда пациентов диагноз может оставаться сомнительным, и в этом случае оправдано выполнение биопсии, тем более, что предложены «большие» и «малые» критерии для интерпретации полученного при биопсии материала (A. Fabre и соавт., 2002). Авторы настороженно относятся к биопсии, опасаясь осложнений и имплантационного метастазирования в случае злокачественной опухоли, однако мы считаем, что для установления диагноза необходимо использовать весь арсенал имеющихся средств, и только при остающихся сомнениях прибегать к лапаротомии и резекции образования. Риски биопсии при соблюдении ряда правил считаем преувеличенными.
Мы придерживаемся сдержанной тактики ведения ФНГ, так как прогноз благоприятный: не зафиксировано случаев малигнизации, осложнения редки (описано всего несколько наблюдений разрыва опухоли с кровотечением), большинство опухолей бессимптомны, а размеры остаются стабильными в течение длительных сроков.
В связи с этим мы поддерживаем приведенные в статье показания для хирургического лечения: симптомная опухоль, ее рост, невозможность исключить злокачественное образование после всестороннего обследования. Важно отметить также, что симптомы ФНГ неспецифичны, поэтому исключение сопутствующей патологии органов брюшной полости, которая может обусловливать клиническую картину, является необходимым. Что касается рекомендации удалять образования, размер которых превышает 5 см, с этим можно не согласиться, так как на наличие симптомов влияет не только размер образования, но и его локализация и соседство окружающих органов. Кроме того, имеют значения размеры самого пациента и его органов. Например, ФНГ размером 10 см у крупного человека, расположенная интрапаренхиматозно, может никак себя не проявлять, в связи с чем необходимость резекции печени у него будет сомнительна.
Таким образом, при выборе тактики ведения у конкретного пациента следует ориентироваться на комплекс факторов, не подвергая его необоснованному риску хирургического вмешательства, так как летальность в группе пациентов с доброкачественными образованиями печени недопустима.
Некоторые аспекты диагностики фокальной нодулярной гиперплазии печени (фибронодулярной гиперплазии)
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Еще сравнительно недавно фокальная нодулярная гиперплазия печени (ФНГ) относилась к редким (3%) объемным образованиям печени. Однако, учитывая применение современных методов визуализации, в настоящее время ФНГ занимает 3-е место среди доброкачественных образований печени после гемангиомы и аденомы [8, 10, 14].
Согласно морфологической классификации опухолей печени, ФНГ относится к опухолеподобным процессам и характеризуется гиперплазией печеночной паренхимы, разделенной на узлы фиброзными прослойками в виде звездчатого рубца [14]. Гиперпластические узлы без четких границ переходят в окружающую ткань, не сдавливая ее. Опухоль состоит из гепатоцитов, элементов желчных протоков, купферовских клеток и фиброзной ткани.
ФНГ развивается в любом возрасте, одинаково часто у лиц разного пола. В то же время имеются данные о том, что подобные новообразования чаще диагностируются у женщин (в 82,2% случаев) [10, 17].
Макроскопически очаговая узловая гиперплазия представляет собой мягкоэластичный, четко ограниченный, иногда инкапсулированный узел серовато-коричневого цвета размером от 0,5 до 6 см. Узлы могут быть как одиночными, так и множественными и располагаться в периферических отделах правой (чаще) и левой доли. Иногда узлы заметно выбухают на поверхности печени, в редких случаях они имеют ножку. Узлы имеют дольчатую структуру с наличием фиброзных прослоек, отходящих, как правило, от центрально расположенного рубца.
При микроскопическом исследовании узлов определяют нормальные гепатоциты, содержащие гликоген и формирующие трабекулярные структуры. Местами наблюдается полиморфизм величины и формы зрелых гепатоцитов, они образуют синцитий. В центре печеночной доли, как правило, располагается центральная вена, имеются синусоиды, выстланные купферовскими клетками (звездчатые ретикулоэндотелиоциты). Портальные прослойки сформированы правильно, достаточно деликатны. В зоне звездчатого рубца и по ходу стромы располагаются сосуды. Сосу дис тый компонент весьма разнообразен как по содержанию (венозные, толстостенные артериальные сосуды с миксоматозной дегенерацией среднего слоя), так и по форме (гемангиоматоз). По ходу портальных септ определяются пролиферирующие желчные протоки, единичные мелкие узлы регенерации и лимфоплазмоцитарные инфильтраты. Эти признаки служат основными дифференциально-диагностическими критериями, позволяющими отличить ФНГ от печеночно-клеточной аденомы [17].
Выделяют 2 типа ФНГ: классическая и неклассическая. При классическом типе выделяют все 3 признака: аномальная нодулярная структура, извилистые толстостенные сосуды, гиперплазия желчных протоков. Центральный рубец присутствует в 65% наблюдений. Он всегда содержит измененные сосуды разного калибра: большие извилистые артерии с гипертрофией интимы и медии, крупные и мелкие вены, капилляры. При неклассическом типе отсутствует один из двух признаков (нодулярная структура или измененные сосуды), но гиперплазия протоков есть всегда. Централь ный рубец отсутствует. В свою очередь неклассический тип делится на 3 подтипа: телеангиэктатический (склонный к кровотечениям), аденоматозный и ФНГ с клеточной атипией.
Опухоль в большинстве случаев (66,7-80,8% пациентов) не проявляет себя клинически и может быть случайно обнаружена при проведении ультразвукового исследования (УЗИ) по иному поводу [18]. Специфичные лабораторные симптомы отсутствуют. ФНГ не озлокачествляется и край не редко вызывает осложнения в виде внутрибрюшного кровотечения.
Ультразвуковая картина ФНГ
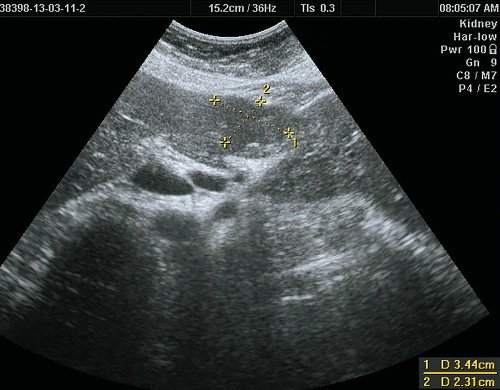
Так, при УЗИ в В-режиме вид ФНГ неспецифичен и вариабелен. Чаще всего ФНГ печени выглядит как единичное очаговое образование с нечеткими или четкими, ровными или неровными контурами, несколько неоднородное по своей внутренней структуре, без капсулы. В 80% случаев (рис. 1) очаг изоэхогенный или гипоэхогенный [3, 8, 9, 11-14].
а) В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
Доброкачественные образования печени
Болезни печени являются одними из самых распространенных заболеваний пищеварительной системы, неуклонный рост которых называют «второй эпидемией нашего века». Особое место среди них занимают различные опухоли и опухолеподобные поражения. За последние годы, благодаря внедрению в клиническую практику более совершенной диагностической аппаратуры и достаточно широкому применению различных контрастных препаратов при исследованиях брюшной полости с помощью ультразвукового исследования, рентгеновской компьютерной и магнитно-резонансной томографии значительно повысились возможности корректной диагностики различных очаговых поражений печени. Кроме того, чувствительность и специфичность различных методов диагностики новообразований печени достигает 88-97%.
По мнению многих авторов, доброкачественные опухоли не имеют клинических симптомов и проявляются в основном в виде очаговых образований печени. В клинической практике по мере выявления очаговых образований печени остро встает вопрос о топическом диагнозе и исключении злокачественности процесса
К доброкачественным образованиям печени относят:
Гемангиома
Гемангиомы многими авторами считаются самыми частыми доброкачественными сосудистыми опухолями печени мезенхимального происхождения, встречающимися в различных возрастных группах. Капиллярная гемангиома состоит из сплетения большого количества ветвящихся сосудов капиллярного типа с узким просветом и не обладающих направленным или с очень медленным кровотоком, 90% площади сосудистого русла составляют венозные каверны. Кавернозные гемангиомы встречаются чаще, чем капиллярные, в ряде случаев имеет место смешанный тип. По мнению большинства авторов, гемангиомы обычно не проявляются клинически и относительно чаще выявляются у женщин.
При УЗИ небольшие (до 3,0 см) гемангиомы выглядят как однородные гиперэхогенные образования с четкими контурами. В ряде случаев эхогенность гемангиом может быть снижена, а контуры выглядеть размыто. В некоторых гемангиомах может отчетливо визуализироваться псевдокапсула в виде гипоэхогенного ободка, что затрудняет их дифференциальную диагностику с метастазами. Перспективу улучшения диагностики многие исследователи проблемы связывают с применением внутривенного контрастирования специальными эхоконтрастными препаратами.
Капиллярная гемангиома печени — однородный гиперэхогенный очаг менее 3 см с четкими границами.
Две кавернозных гемангиомы печени.
Фокальная узловая гиперплазия (ФУГ)
Фокальная узловая гиперплазия (ФУГ) считается вторым (после гемангиом) наиболее распространенным доброкачественным новообразованием печени. По данным ряда авторов, ФУГ встречается у 0,9-5% населения, в 5-20% случаев может сочетаться с кистами и гемангиомами. Согласно литературным данным, ФУГ, не имея признаки опухоли, входит в группу доброкачественных гепатоцеллюлярных опухолей эпителиальной природы. Это одиночное, округлое, неинкапсулированное образование с нарушенной печеночной архитектоникой, разделенное септами, достигающими центрального рубца. Средние размеры очага – 5,7 см (от 1,5 до 12,0 см). Установлено, что ФУГ не склонна к кровоизлияниям и не имеет злокачественного потенциала. Обычно опухоль является случайной находкой при диагностических исследованиях. Узлы малых размеров, как правило, бессимптомны. Крупные опухоли могут вызывать боли в животе.
При нативном УЗИ в большинстве случаев ФУГ визуализируются с трудом, отображаясь в виде участка округлой формы с четкими контурами, изоэхогенной или незначительно гипо- или гиперэхогенной структуры. По мнению некоторых авторов, в диагностике ФУГ контрастное УЗИ является более информативной в отличие от других методов диагностики. Появление эхоконтрастных препаратов второго поколения значительно расширило возможности метода. Это позволяет дифференцировать различные типы опухолей, учитывая их характер васкуляризации, имеющего важное значение в дифференциальной диагностике очаговых образований печени. Повышенная васкуляризация опухоли в сочетании с характерным рисунком «колеса со спицами» является патогномоничным признаком ФУГ (71,4%). При этом частота обнаружения «питающей» артерии опухоли увеличивается до 98%. Чувствительность и специфичность УЗИ с применением внутривенного контрастирования в диагностике ФУГ достигают 83 и 98% соответственно.
Гипоэхогенное образование в печени — доброкачественная фокальная нодулярная гиперплазия. В литературе описывают, что для нее характерен центральный рубец (белая стрелка).
В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
Гепатоцеллюлярная аденома (ГЦА)
Гепатоцеллюлярная аденома (ГЦА). ГЦА считается редко встречающейся доброкачественной опухолью, происходящей из гепатоцитов. Имеются предположения о влиянии на развитие и рост опухоли пероральных контрацептивов, экзогенных андрогенов, беременности и дисбаланса эндогенных половых гормонов. Приводятся противоречивые данные по размерам аденом – указываются цифры от 1 до 19 см, составляя в среднем 5,4 см. В некоторых случаях у пациентов отмечаются множественные аденомы. Образования хорошо очерчены. Ряд авторов отмечает характерные отличительные признаки аденом – в отличие от гемангиом они не располагаются рядом с печеночными сосудами, не занимают целую долю. Течение ГЦА в большинстве случаев бессимптомное. При размерах опухоли от 5 см и более или субкапсулярным ее расположении риск кровотечения увеличивается. Авторы подчеркивают практическую важность диагностики аденомы из-за высокого риска развития кровотечения, разрыва, малигнизации и необходимости выполнения хирургического вмешательства.
При УЗИ ГЦА обычно выглядит как солитарное гетерогенное образование с четкими контурами различной степени эхогенности: 20-40% аденом представляются гипоэхогенными, 30% – гиперэхогенными, что обусловлено наличием жировых включений в тканях опухоли. По мнению ряда авторов, при использовании ЦДК в ряде случаев выявляются периферические пери- и интратуморальные сосуды.
Таким образом, УЗИ органов брюшной полости в настоящее время является скрининговым методом выявления опухолей и опухолеподобных процессов печени. Благодаря достаточно высокой информативности и доступности УЗИ выполняется на первом этапе диагностики при подозрении на новообразование печени. УЗИ позволяет не только выявить опухоль в печени, но и судить о ее размерах, топографии, операбельности процесса. Интраоперационное УЗИ информативно для диагностики внутрипеченочных опухолей, поскольку во время операции другие методы исследования мало применимы.
УЗИ в режиме «серой шкалы» позволяет выявить различные изменения в паренхиме. Однако в ряде случаев провести дифференциальную диагностику между диффузными заболеваниями не представляется возможным из-за схожести эхографических признаков.
Эхография в В-режиме с допплерографией сосудистой системы печени с оценкой состояния гемодинамики позволяет уточнить характер патологического процесса. Однако, несмотря на высокую специфичность (97%), чувствительность метода в выявлении опухолей печени остается достаточно низкой (60%), что позволяет отдавать предпочтение динамическим методикам РКТ или МРТ. Кроме того, по мнению отдельных исследователей, информативность диагностического заключения УЗИ, как субъективного метода исследования, зависит от опыта и квалификации врача УЗ диагностики.