Геморрагическая лихорадка с почечным синдромом
Что провоцирует / Причины Геморрагической лихорадки с почечным синдромом:
В 1938-1940 гг. на Дальнем Востоке России проведены комплексные исследования, в результате которых установлены вирусная природа заболевания, его основные эпидемиологические и клинические закономерности. (Чумаков А.А., Смородинцев М.П.). Заболевание получило название дальневосточного геморрагического нефрозонефрита. Одновременно в Северной Манчжурии среди личного состава японской Квантунской армии было зарегистрировано сходное заболевание, получившее название болезни Сонго. Несколько позже случаи заболевания были отмечены в Тульской области, Швеции, Норвегии и Финляндии, Южной Корее (более 2000 больных во время корейско-американской войны 1951-1953 гг.). В дальнейшем природные очаги выявлены во многих областях Российской Федерации (особенно на Урале и в Среднем Поволжье), на Украине, в Молдавии, Белоруссии, Югославии, Румынии, Венгрии, Чехии, Словакии, Болгарии. В 1976-1978 гг. возбудитель выделен сначала у грызунов, а затем у больного человека. Общее название для различных вариантов болезни «геморрагическая лихорадка с почечным синдромом» введено по решению научной группы ВОЗ в 1982 г.
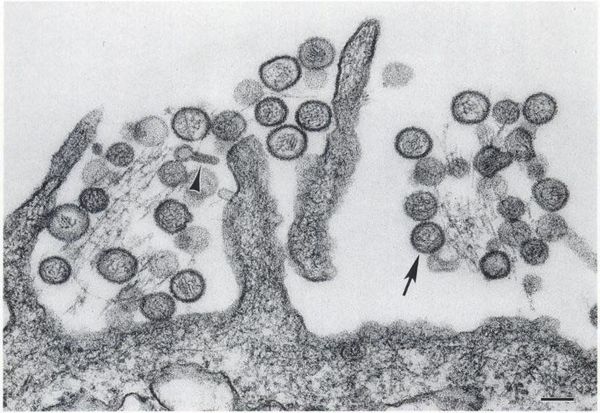
В настоящее время возбудитель геморрагической лихорадки с почечным синдромом относится к семейству буньявирусов (Bunyaviridae) и выделен в отдельный род Hantavirus, который включает вирус Hantaan (корейская геморрагическая лихорадка), вирус Puumala (эпидемическая нефропатия) и два вируса: Prospect Hill, Tchoupitoulast, которые непатогенны для человека.
Патогенез (что происходит?) во время Геморрагической лихорадки с почечным синдромом:
Симптомы Геморрагической лихорадки с почечным синдромом:
Инкубационный период продолжается от 7 до 46 дней (чаще всего от 21 до 25 дней). В течение болезни выделяют следующие периоды: начальный, олигоурический (период почечных и геморрагических проявлений), полиурический и реконвалесценции.
Начальный период (период продромальных явлений) продолжается от 1 до 3 дней и характеризуется острым началом, повышением температуры тела до 38-40°С, которое иногда сопровождается ознобом. Появляется сильная головная боль (но нет болей в надбровных дугах и глазных яблоках), слабость, сухость во рту, признаков воспаления верхних дыхательных путей не отмечается. При осмотре больных отмечается гиперемия кожи лица, шеи, верхних отделов груди (симптом «капюшона»). Слизистая оболочка зева гиперемирована, сосуды склер инъецированы, на фоне гиперемированных конъюнктив иногда можно заметить геморрагическую сыпь. У отдельных больных начало болезни может быть постепенным, а за 2-3 дня до болезни могут быть продромальные явления (слабость, недомогание, катаральные явления со стороны верхних дыхательных путей). Со стороны внутренних органов в начальном периоде особых изменений выявить не удается. Возможна умеренная брадикардия, у некоторых больных тупые боли в пояснице, положительный симптом Пастернацкого. Относительно редко при тяжелых формах могут быть явления менингизма.
Олигурический период (лихорадочный) (со 2-4-го по 8-11-й день болезни). Температура тела остается на уровне 38-40°С и держится до 4-7-го дня болезни, однако снижение температуры тела не сопровождается улучшением состояния больного, чаще оно даже ухудшается. Наиболее типичным проявлением олигоурического периода являются боли в пояснице различной выраженности (иногда они начинаются в конце начального периода). Отсутствие болей позже 5-го дня болезни при выраженности лихорадки и симптомов интоксикации заставляет сомневаться в диагнозе ГЛПС. У большинства больных через 1-2 дня после появления болей в пояснице возникает рвота до 6-8 раз в сутки и больше. Она не связана с приемом пищи или лекарств. В эти же сроки появляются боли в животе, часто отмечается вздутие живота.
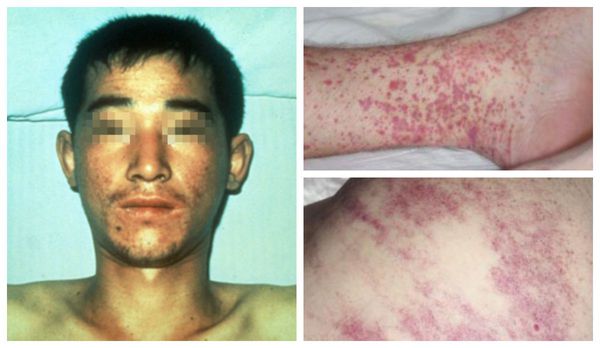
При осмотре в этот период кожа сухая, лицо и шея гиперемированы, сохраняется гиперемия слизистых оболочек зева и конъюнктив, может быть небольшая отечность верхнего века, сосуды склер инъецированы. Появляются геморрагические симптомы.
Тромбогеморрагический синдром разной выраженности развивается лишь у половины больных с более тяжелым течением ГЛПС. Прежде всего и чаще всего отмечается повышенная ломкость сосудов (проба жгута, более объективные данные можно получить при определении резистентности сосудов по Нестерову), далее идет появление петехий (у 10-15% больных), макрогематурия (у 7-8%), кишечные кровотечения (около 5%), кровоподтеки в местах инъекций, носовые кровотечения, кровоизлияния в склеру, очень редко примесь крови отмечается в рвотных массах и мокроте. Не характерны кровотечения из десен и маточные кровотечения. Частота геморрагических проявлений зависит от тяжести болезни, чаще они наблюдаются при тяжелой форме (50-70%), реже при среднетяжелой (30-40%) и легкой (20-25%). Во время эпидемических вспышек геморрагические признаки наблюдаются чаще и выражены более резко. В Скандинавских странах ГЛПС протекает более легко («эпидемическая нефропатия»), чем заболевания, обусловленные восточным вариантом вируса, например при заболевании 2070 военнослужащих США в Корее.
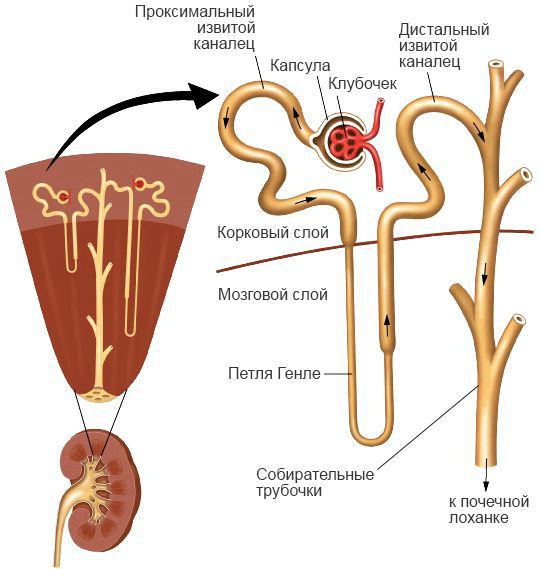
К характерным проявлениям болезни относится поражение почек. Оно проявляется в одутловатости лица, пастозности век, положительном симптоме Пастернацкого (проверять осторожно, так как энергичное поколачивание, также как и неосторожная транспортировка больных может приводить к разрыву почек). Олигоурия развивается со 2-4-го дня, в тяжелых случаях может доходить до анурии. Значительно повышается содержание белка в моче (до 60 г/л), в начале олигоурического периода может быть микрогематурия, в осадке обнаруживают гиалиновые и зернистые цилиндры, иногда появляются длинные грубые «фибринные» цилиндры Дунаевского. Нарастает остаточный азот. Наиболее выраженной азотемия бывает к 7-10-му дню болезни. Нормализация содержания остаточного азота наступает через 2-3 нед.
В результате распада тканевых белков в очагах некробиоза и нарушения азото-выделительной функции почек в крови прогрессивно нарастает уровень азотистых шлаков. Развивается олиго- или анурия. Количество выделяемой суточной мочи соответствует тяжести болезни: незначительное его снижение при лёгких формах, 300-900 мл/сут при среднетяжёлых и менее 300 мл при тяжёлых случаях заболевания.
Резко снижается относительная плотность мочи; в дальнейшем у большинства больных развивается изогипостенурия. В моче увеличивается количество белка, обнаруживают свежие эритроциты, гиалиновые и зернистые цилиндры, вакуолизированные клетки почечного эпителия (клетки Дунаевского).
В крови как следствие органных поражений нарастает лейкоцитоз и начинает повышаться СОЭ.
Полиурический период наступает с 9-13-го дня болезни. Прекращается рвота, постепенно исчезают боли в пояснице и животе, нормализуются сон и аппетит, увеличивается суточное количество мочи (до 3-5 л), сохраняется слабость, сухость во рту, постепенно (с 20-25 дня) наступает период выздоровления.
Период реконвалесценции. Продолжается от 3 до 12 мес. В течение длительного времени остаются выраженная астенизация, патология со стороны почек, особенно в случаях развившегося острого или хронического пиелонефрита. При стойком сохранении (более 6 мес) полиурии, жажды и сухости во рту следует думать о хронической тубулоинтерстициальной нефропатии с нарушением экскреторно-секреторной функции канальцев и повышением суточной экскреции электролитов. Состояние может сохраняться до 10 лет, однако исходов в хроническую почечную недостаточность не наблюдают.
Описанные клинические этапы заболевания могут не иметь чётких переходных границ между собой или проявляться одновременно.
Осложнения обусловлены развитием инфекционно-токсического шока, острой почечной недостаточностью, отёка лёгких, органных кровоизлияний и кровотечений, разрывов почки. В редких случаях наблюдают эклампсию с артериальной гипертензией, тоническими и клоническими судорогами, тризмом, потерей сознания, расширением зрачков, замедлением пульса и дыхания. Возможны субарахноидальные кровоизлияния. В Китае (1988) описаны случаи энцефалитов при геморрагической лихорадке с почечным синдромом.
При развитии уремии как терминальной стадии острой почечной недостаточности усиливаются тошнота и рвота, появляется икота, затем прогрессируют сонливость, непроизвольные подёргивания отдельных групп мышц (мимических, мышц рук) и другая мозговая симптоматика. Значительно нарастает уровень мочевины и креатинина в крови.
Диагностика Геморрагической лихорадки с почечным синдромом:
Помимо общих клинических и биохимических анализов, применяют РНИФ с исследованием сыворотки крови, взятой в максимально ранний период заболевания и затем повторно через 5 дней. Подтверждением диагноза является нарастание титро антител не менее чем в 4 раза. В крови перенёсших геморрагическую лихорадку с почечным синдромом антитела сохраняются в течение многих лет.
Геморрагическую лихорадку с почечным синдромом следует отличать от лептоспирозов, гриппа, энтеровирусной инфекции, пиелонефрита и острого гломерулонефрита, различных видов прочих геморрагических лихорадок.
Лечение Геморрагической лихорадки с почечным синдромом:
Поскольку больные геморрагической лихорадкой с почечным синдромом неконтагиозны, они могут быть госпитализированы в любой стационар, оснащённый соответствующей лабораторной службой, позволяющей организовать систематический контроль функции почек. Транспортировка больных производится на носилках с матрацем с соблюдением максимальной осторожности из-за опасности разрыва почечной капсулы.
Режим строгий постельный, включая первые дни полиурии. Необходимы тщательный уход, туалет полости рта, контроль диуреза и опорожнения кишечника.
Диета № 4 без ограничений белка и соли. При тяжёлом течении временно ограничивают потребление продуктов, содержащих большое количество белка и калия (так как у больных развивается гиперкалиемия). Назначают обильное питьё, в том числе минеральных вод (Боржоми, Ессентуки № 4 и др.).
Этиотропная терапия эффективна в первые 3-4 дня болезни. Рекомендован виразол внутривенно или рибамидил в таблетках по 15 мг/кг/сут в течение 5 дней.
Патогенетическое лечение проводят с учётом тяжести течения болезни и ведущих клинических синдромов. В лёгких случаях назначают рутин, аскорбиновую кислоту, глюконат кальция, димедрол, салицилаты до 1,5 г/сут.
Показаниями к применению глюкокортикоидов являются угроза развития выраженной почечной недостаточности (анурия, многократная рвота), олигурия в течение 2 нед и более, развитие менингоэнцефалита. В этих случаях применяют преднизолон парентерально в суточной дозе от 1 до 2 мг/кг курсом на 3-6 дней. При развитии инфекционно-токсического шока или острой сосудистой недостаточности суточную дозу преднизолона увеличивают до 10-12 мг/кг.
Показаны антигистаминные препараты, ингибиторы протеаз (трасилол, контрикал в/в до 50 тыс. ЕД), препараты антибрадикининового действия, улучшающие микроциркуляцию (продектин по 0,25 г 4 раза в сутки).
Для улучшения диуреза применяют 5-10 мл 2,4% раствора эуфиллина (добавляют в капельницу). Лазикс малоэффективен, маннитол не показан.
В случае отсутствия клинического эффекта от проводимой терапии в течение 2-4 дней и нарастания признаков острой почечной недостаточности (мочевина более 30 ммоль/л и креатинин более 600 мкмоль/л), а также при развитии почечной эклампсии или менингоэнцефалита больных переводят на гемодиализ.
При выраженных геморрагических проявлениях показаны дицинон, аминокапроновая кислота, замещающие дозы крови. При сильных почечных болях применяют промедол, аминазин, димедрол, дроперидол, седуксен в виде литических смесей. В случаях развития сердечно-сосудистой недостаточности внутривенно вводят коргликон, строфантин.
Для профилактики вторичной бактериальной инфекции мочевыводящих путей применяют нитрофураны, нитроксолин (после восстановления диуреза). В полиурический период постепенно отменяют медикаментозную терапию, продолжая внутривенное введение изотонического раствора натрия хлорида.
Выписку больных проводят при клиническом выздоровлении; при этом возможны остаточные полиурия и изогипостенурия.
После выписки реконвалесценты нетрудоспособны в течение 1-4 нед. В дальнейшем их освобождают от тяжёлой физической работы, занятий спортом на 6-12 мес. В восстановительный период рекомендуют полноценное питание, обильное питьё (щелочные минеральные воды, настои шиповника и трав с мочегонным действием), применение витаминных препаратов, физиотерапевтических процедур (диатермия, электрофорез), массажа и лечебной физкультуры.
Профилактика Геморрагической лихорадки с почечным синдромом:
Профилактические мероприятия включают благоустройство лесопарковой территории, барьерной и домовой дератизации на территории природных очагов и санитарно-просветительную работу среди населения. Специфическая профилактика не разработана.
К каким докторам следует обращаться если у Вас Геморрагическая лихорадка с почечным синдромом:
Геморрагическая лихорадка с почечным синдромом
МКБ-10
Общие сведения
Причины ГЛПС
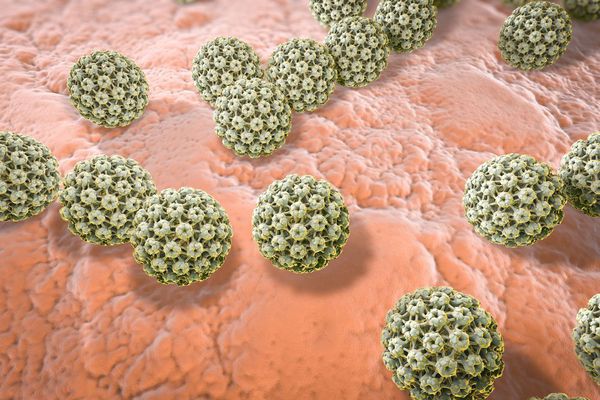
Возбудителями болезни являются РНК-содержащие вирусные агенты рода Hantavirus (хантавирусы), относящиеся к семейству Bunyaviridae. Для человека патогенны 4 серотипа хантавирусов: Hantaan, Dubrava, Puumala, Seoul. Во внешней среде вирусы относительно долго сохраняют стабильность при отрицательной температуре и малоустойчивы при температуре 37°C. Вирусы имеют сферическую или спиральную форму, диаметр 80-120 нм; содержат одноцепочечную РНК. Хантавирусы обладают тропностью к моноцитам, клеткам почек, легких, печени, слюнных желез и размножаются в цитоплазме инфицированных клеток.
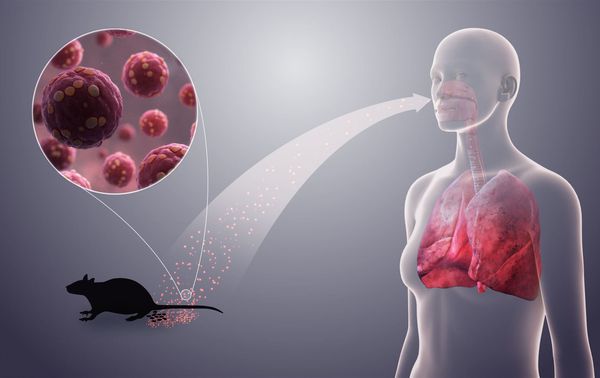
Переносчиками возбудителей геморрагической лихорадки с почечным синдромом служат грызуны: полевые и лесные мыши, полевки, домовые крысы, которые инфицируются друг от друга через укусы клещей и блох. Грызуны переносят инфекцию в форме латентного вирусоносительства, выделяя возбудителей во внешнюю среду со слюной, фекалиями и мочой. Попадание инфицированного выделениями грызунов материала в организм человека может происходить аспирационным (при вдыхании), контактным (при попадании на кожу) или алиментарным (при употреблении пищи) путем.
К группе повышенного риска по заболеваемости геморрагической лихорадкой с почечным синдромом относятся сельскохозяйственные и промышленные рабочие, трактористы, водители, активно контактирующие с объектами внешней среды. Заболеваемость человека напрямую зависит от численности инфицированных грызунов на данной территории. ГЛПС регистрируется преимущественно в виде спорадических случаев; реже – в виде локальных эпидемических вспышек. После перенесенной инфекции остается стойкий пожизненный иммунитет; случаи повторной заболеваемости единичны.
Патогенез
Патогенетическую сущность геморрагической лихорадки с почечным синдромом составляют некротизирующий панваскулит, ДВС-синдром и острая почечная недостаточность. После заражения первичная репликация вируса происходит в эндотелии сосудов и эпителиальных клетках внутренних органов. Вслед за накоплением вирусов наступает вирусемия и генерализация инфекции, которые клинически проявляются общетоксическими симптомами.
В патогенезе геморрагической лихорадки с почечным синдромом большую роль играют образующиеся аутоантитела, аутоантигены, ЦИК, оказывающие капилляротоксическое действие, вызывающие повреждение стенок сосудов, нарушение свертываемости крови, развитие тромбогеморрагического синдрома с повреждением почек и других паренхиматозных органов (печени, поджелудочной железы, надпочечников, миокарда), ЦНС. Почечный синдром характеризуется массивной протеинурией, олигоанурией, азотемией, нарушением КОС.
Симптомы ГЛПС
Геморрагическая лихорадка с почечным синдромом характеризуется циклическим течением с последовательной сменой нескольких периодов:
В зависимости от выраженности симптомов, тяжести инфекционно-токсического, геморрагического и почечного синдромов различают типичные, стертые и субклинические варианты; легкие, среднетяжелые и тяжелые формы геморрагической лихорадки с почечным синдромом.
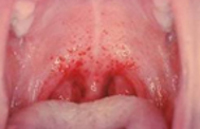
По истечении инкубационного периода наступает короткий продромальный период, во время которого отмечаются утомляемость, недомогание, головные боли, миалгии, субфебрилитет. Лихорадочный период развивается остро, с повышения температуры тела до 39-41°С, озноба и общетоксических симптомов (слабости, головной боли, тошноты, рвоты, расстройства сна, артралгии, ломоты в теле). Характерны боли в глазных яблоках, затуманенное зрение, мелькание «мушек», видение предметов в красном цвете. В разгар лихорадочного периода появляются геморрагические высыпания на слизистых оболочках полости рта, коже грудной клетки, подмышечных областей, шеи. При объективном осмотре выявляется гиперемия и одутловатость лица, инъекция сосудов конъюнктив и склер, брадикардия и артериальная гипотония вплоть до коллапса.
У большинства больных отмечается неукротимая рвота и диарея. Геморрагический синдром может быть выражен в различной степени и включать в себя макрогематурию, кровотечения из мест инъекций, носовые, маточные, желудочно-кишечные кровотечения. В олигоурический период могут развиваться тяжелые осложнения (кровоизлияния в головной мозг, гипофиз, надпочечники), служащие причиной летального исхода.
Переход геморрагической лихорадки с почечным синдромом в полиурическую стадию знаменуется субъективными и объективными улучшениями: нормализацией сна и аппетита, прекращением рвоты, исчезновением боле в пояснице и т. д. Характерными признаками данного периода служит увеличение суточного диуреза до 3-5 л и изогипостенурия. В период полиурии сохраняется сухость во рту и жажда.
Период реконвалесценции при геморрагической лихорадке с почечным синдромом может затягиваться на несколько месяцев и даже лет. У больных долго сохраняется постинфекционная астения, характеризующаяся общей слабостью, снижением работоспособности, быстрой утомляемостью, эмоциональной лабильностью. Синдром вегетативной дистонии выражается гипотонией, инсомнией, одышкой при минимальной нагрузке, повышенной потливостью.
Осложнения
Специфическими осложнениями тяжелых клинических вариантов ГЛПС могут являться инфекционно-токсический шок, кровоизлияния в паренхиматозные органы, отек легких и головного мозга, кровотечения, миокардит, менингоэнцефалит, уремия и др. При присоединении бактериальной инфекции возможно развитие пневмонии, пиелонефрита, гнойных отитов, абсцессов, флегмон, сепсиса.
Диагностика
Клиническая диагностика ГЛПС основывается на цикличности течения инфекции и характерной смене периодов. При сборе эпидемиологического анамнеза обращается внимание на пребывание пациента в эндемичной местности, возможный прямой или косвенный контакт с грызунами. При проведении неспецифического обследования учитывается динамика изменения показателей общего и биохимического анализа мочи, электролитов, биохимических проб крови, КОС, коагулограммы и др. С целью оценки тяжести течения и прогноза заболевания выполняется УЗИ почек, ФГДС, рентгенография органов грудной клетки, ЭКГ и др.
Специфическая лабораторная диагностика геморрагической лихорадки с почечным синдромом проводится с помощью серологических методов (ИФА, РНИФ, РИА) в динамике. Антитела в сыворотке крови появляются в конце 1-ой недели болезни, к концу 2-й недели достигают максимальной концентрации и сохраняются в крови 5–7 лет. РНК вируса может быть выделена с помощью ПЦР-исследования. ГЛПС дифференцируют с лептоспирозом, острым гломерулонефритом, пиелонефритом и энтеровирусной инфекцией, прочими геморрагическими лихорадками.
Лечение ГЛПС
Больные геморрагической лихорадкой с почечным синдромом госпитализируются в инфекционный стационар. Им назначается строгий постельный режим и диета №4; проводится контроль водного баланса, гемодинамики, показателей функционирования сердечно-сосудистой системы и почек. Этиотропная терапия геморрагической лихорадки с почечным синдромом наиболее эффективна в первые 3-5 суток от начала заболевания и включает введение донорского специфического иммуноглобулина против ГЛПС, назначение препаратов интерферона, противовирусных химиопрепаратов (рибавирина).
В лихорадочном периоде проводится инфузионная дезинтоксикационная терапия (внутривенные вливания глюкозы и солевых растворов); профилактика ДВС-синдрома (введение препаратов-дезагрегантов и ангиопротекторов); в тяжелых случаях применяются глюкокортикостероиды. В олигурическом периоде осуществляется стимуляция диуреза (введение ударных доз фуросемида), коррекция ацидоза и гиперкалиемии, профилактика кровотечений. При нарастающей ОПН показано переведение пациента на экстракорпоральный гемодиализ.
При наличии бактериальных осложнений назначается антибиотикотерапия. В полиурическую стадию основной задачей является проведение оральной и парентеральной регидратации. В период реконвалесценции проводится общеукрепляющая и метаболическая терапия; рекомендуется полноценное питание, физиотерапия (диатермия, электрофорез), массаж и ЛФК.
Прогноз и профилактика
Легкие и среднетяжелые формы геморрагической лихорадки с почечным синдромом в большинстве случаев заканчиваются выздоровлением. Резидуальные явления (постинфекционная астения, боли в пояснице, кардиомиопатия, моно- и полиневриты) длительно наблюдаются у половины переболевших. Реконвалесценты нуждаются в ежеквартальном диспансерном наблюдении инфекциониста, нефролога и окулиста на протяжении года. Тяжелое течение сопряжено с высоким риском осложнений; смертность от ГЛПС колеблется в пределах 7-10%.
Профилактика геморрагической лихорадки с почечным синдромом заключается в уничтожении мышевидных грызунов в природных очагах инфекции, предупреждении загрязнения жилищ, водоисточников и продуктов питания выделениями грызунов, дератизации жилых и производственных помещений. Специфической вакцинации против ГЛПС не разработано.
Что такое геморрагическая лихорадка с почечным синдромом (ГЛПС)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
Геморрагическая лихорадка с почечным синдромом (ГЛПС) — это группа острых инфекционных заболеваний, вызываемых хантавирусами из семейства Bunyaviridae, которые поражают мелкие сосуды всего организма, вызывают расстройства свёртывающей системы, нарушают кровообращение и работу почек. Клинически проявляется в виде общей инфекционной интоксикации, воспаления соединительной ткани почек, не поддающегося лечению антибиотиками, и геморрагического диатеза (повышенной кровоточивости тканей). В зависимости от формы заболевания летальность колеблется от 1 % до 15 %.
Синонимы: дальневосточная или корейская геморрагическая лихорадка, геморрагический нефрозонефрит, скандинавская эпидемическая нефропатия и др.
Этиология
Таксономия возбудителя болезни:
Определение ГЛПС как вирусной болезни было предложено советским бактериологом, вирусологом и иммунологом А. А. Смородинцевым в 1944 году. Сам вирус был выделен от животных южно-корейским учёным Н. W. Lee в 1976 году, от человека — в 1978 году.
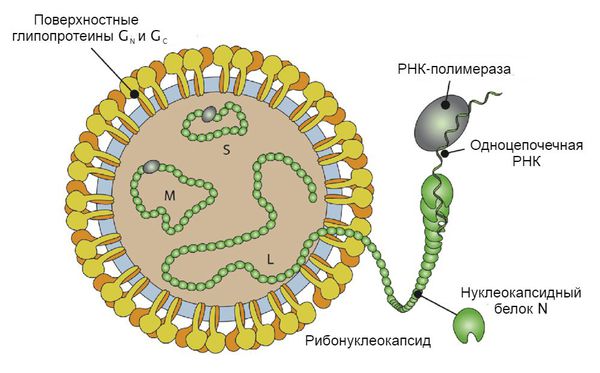
Вирусные частицы представляют собой образования округлой формы диаметром 90-130 нм. Они имеют липидную оболочку с выступами (гликопротеиновыми шипами), содержат одноцепочечную РНК. Геномом кодируются: РНК-зависимая РНК-полимераза, нуклеокапсидный белок N, поверхностные глипопротеины GN GC. В зависимости от вида вируса имеется различное количество открытых рамок считывания, кодирующих неструктурные белки. Проникновение вируса в клетку хозяина осуществляется путём прикрепления к её поверхности с помощью специфических белков G.
Интересен тот факт, что мутации хантавирусов при репликации проходят параллельно с эволюционными изменениями их природных носителей (грызунов).
Эпидемиология
Все перечисленные возбудители также могут циркулировать повсеместно в незначительной концентрации.
Заболевание является природно-очаговым зоонозом, т. е. встречается на определённых территориях, где есть основной источник инфекции — дикие мышевидные грызуны:
В городах незначительная роль отводится домовым мышам и крысам. Сами грызуны, как правило, являются бессимптомными вирусоносителями (вирусные частицы выявляются у них во всех средах организма, но больше — в лёгких).
Заражение грызунов происходит при контакте между собой, в основном через слюну воздушно-капельным путём. Человек в основном заражается через мочу и фекалии грызунов, содержащие вирус.
Механизмы передачи вируса :
Человек обычно не является источником инфекции, для окружающих не заразен (случаи заражения крайне редки и наблюдаются только в лаборатории).
К заболеванию восприимчивы все люди, чаще всего болеют мужчины активного возраста, связанные с определёнными профессиями или образом жизни (фермеры, ассенизаторы, трактористы, лесники, геологи, дачники, работники промышленных предприятий). Дети, женщины и пожилые люди болеют значительно реже в связи с меньшим контактом с источниками вируса в природной среде и особенностями иммунитета (если человек уже контактировал с вирусом).
Сезонность — летне-осенняя, раз в 3-4 года заболеваемость увеличивается из-за активизация грызунов, обитающих рядом с людьми.
Симптомы геморрагической лихорадки с почечным синдромом
Инкубационный период составляет от 4 до 49 дней. В среднем он длится 2-3 недели. Его продолжительность зависит от вида возбудителя, дозы попавшего в организм патогена, места проникновения, иммунореактивности организма и др.
Подавляющее большинство случаев протекает под маской лёгкого и среднетяжёлого ОРЗ в виде непродолжительной остролихорадочной формы и, как правило, не распознаются.
Начало заболевания (лихорадочный период) обычно острое, иногда наблюдается небольшая продрома в виде познабливания, ломоты в теле, повышения температуры тела до 37,5-38°С. Появляется лихорадка с быстрым нарастанием температурной реакции до максимальных цифр (38-40°С), которые держатся в течение 5-11 дней. Колебания температурной кривой не имеют каких-либо особенностей. Больных беспокоит озноб, выраженная головная боль, ломота и боли в мышцах и суставах, сухость во рту и жажда. Быстро нарастает слабость, потливость, адинамия. Может возникнуть небольшой кашель.
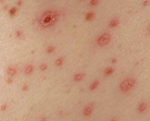
Внешний вид больных : гиперемированная (покрасневшая) верхняя половина тела, инъецированные красноватые склеры (белки глаз), возможна пятнистая энантема мягкого нёба (появление мелких пятен). При прогрессировании болезни появляется петехиальная сыпь (мелкие кровоизлияния) в области туловища, внутренней поверхности плеч и местах уколов, возможны небольшие носовые кровотечения. При сдавливании тканей и щипках в этих местах появляется геморрагическая сыпь.
Со стороны сердца отмечается относительная брадикардия, артериальное давление немного снижено. У чувствительных людей может возникнуть дискомфорт в поясничной области. К концу лихорадочного периода начинает снижаться количество отделяемой мочи (диурез) и частота мочеиспускания.
Внешний вид пациента изменяется : гиперемия лица и верхней части туловища сменяется бледностью, нарастает геморрагический синдром: возникают массивные кровоизлияния в склеры, длительные носовые кровотечения, любое прижатие ткани вызывает выраженную геморрагическую сыпь. Возможно развитие кишечного кровотечения.
Ведущим расстройством олигурической стадии является прогрессирующее снижение количества отделяемой мочи вплоть до анурии (полного её отсутствия). В это время наиболее часто развиваются осложнения и летальные исходы.
Признаки потенциального развития тяжёлой формы болезни :
ГЛПС у беременных
Заболевание протекает несколько тяжелее, чаще переходит в тяжёлую стадию и повышает риск осложнений. Оно способно привести к развитию дистресс-синдрома лёгких, тромбоцитопении и повышению уровня печёночных трансаминаз.
Патогенез геморрагической лихорадки с почечным синдромом
Входные ворота — эпителий дыхательных путей, желудочно-кишечный тракт и повреждённая кожа. В месте проникновения вируса никаких изменений не наблюдается. По кровеносным сосудам патоген распространяется в организме, накапливаясь в клетках макрофагальной ткани, не вызывая при этом никаких симптомов.
По истечению скрытого периода заболевания происходит массивная вирусемия — выход и циркуляция вируса в крови. Она сопровождается активацией иммунной и гормональной систем, которые запускают синтез провоспалительных цитокинов. В результате прямого повреждающего воздействия вируса и иммунопатологических сдвигов повреждается внутренний слой мелких сосудов («излюбленное» место поражения вируса), развивается повышенное слипание тромбоцитов и клеточных элементов, вследствие чего нарушается текучесть крови. Такие изменения приводят к нарушению микроциркуляции, спазму мелких сосудов и нарушению работы органов. Одновременно с этим начинается образование патологических иммунных клеток (аутоиммунная агрессия).
При прогрессировании болезни расстройства микроциркуляции усиливаются, что приводит к системному расстройству гемодинамики, нарушается кровоснабжение органов, нарастает гипоксия, увеличивается кислотность (ацидоз), повреждается структура и функции жизненно важных органов (отёки, кровоизлияния, дистрофия, некроз).
Наиболее выраженные поражения наблюдаются в почках — нарушается микроциркуляция, повышается проницаемость стенки сосудов, на базальной мембране клубочков осаждаются патологические иммунные комплексы. Это ведёт к отёку промежуточного вещества, дистрофии, пропотеванию фибрина и белка в просвет канальцев почек и их обтурацией (закупоркой) — нарушается фильтрация, нарастает ишемия ткани почек и возникает некроз. Это приводит к уменьшению количества отделяемой мочи, нарушению водно-электролитного баланса, уремической интоксикации и ацидозу. Чем тяжелее процесс, тем больше объёмы поражения, что может привести к летальному исходу.
Классификация и стадии развития геморрагической лихорадки с почечным синдромом
В Международной классификации болезней (МКБ-10), заболеванию присвоен код A 98.5.
Выделяют три степени тяжести:
Осложнения геморрагической лихорадки с почечным синдромом
Специфические осложнения ГЛПС :
Неспецифические осложнения ГЛПС — воспалительно-гнойные процессы:
Диагностика геморрагической лихорадки с почечным синдромом
К методам диагностики ГЛПС относятся:
Дифференциальная диагностика
Большинство случаев болезни проходят в лёгкой и среднетяжёлой форме, поэтому, как правило, не распознаются, ошибочно принимаясь за начальный период ОРЗ. Также ГЛПС можно спутать с другими заболеваниями:
Лечение геморрагической лихорадки с почечным синдромом
Лёгкие и многие формы среднетяжёлых случаев болезни лечат дома или в отделении ОРЗ стационаров как нераспознанные случаи. Часть среднетяжёлых и тяжёлых случаев подлежат госпитализации в инфекционные стационары с наличием отделения реанимации и интенсивной терапии (ОРИТ), при отсутствии инфекционного стационара — в общетерапевтический. Транспортировка должна осуществляться без тряски, так как есть риск разрыва почек.
Режим — постельный, до прекращения выраженной полиурии:
Показана механически и химически щадящая диета с достаточным количеством соли. Наиболее подходит диета № 4 по Певзнеру. Необходимо контролировать уровень потребляемой жидкости. В начале болезни, когда функция почек сохранена, показано обильное питьё. В фазу олигоанурии нужно строго следить, чтобы количество потреблённой жидкости не превышало объёма выведенной более чем на 700 мл. В разгар болезни нужно исключить продукты, богатые белком (мясо, рыбу, бобовые) и калием (овощи, фрукты, сухофрукты, картофель). В период выздоровления их нужно включить в рацион. Голодать нельзя, так как оно усиливает распада белка и увеличивает уровень мочевины в крови (азотемия).
Специфической противовирусной терапии прямого действия на сегодняшний день нет. В ранние сроки болезни при среднетяжёлых и тяжёлых формах возможно применение препарата общевирусного действия ( рибавирина ) коротким курсом.
В период выздоровления показано использование общеукрепляющих средств и адаптогенов: минеральных препаратов (например глюконат кальция ), витаминных комплексов и растительных экстрактов (например элеутерококка ).
Сроки выписки пациентов :
Прогноз. Профилактика
При лёгких формах и большей части среднетяжёлых форм прогноз благоприятный: через 3-6 недель наблюдается полное выздоровление. При части среднетяжёлых и тяжёлых формах процесс восстановления может занять месяцы, иногда годы, возможно стойкое нарушение функции некоторых органов (в основном почек). При развитии осложнений нередки летальные исходы (в основном при ГЛПС, вызванной вирусом Хантаан).
Профилактика ГЛПС на современном этапе включает в основном неспецифические мероприятия: