Венозная недостаточность или несостоятельность перфорантных вен
Что такое варикозное расширение вен, знают все. Но далеко не все знают, что такое венозная недостаточность. А ведь именно она является предшественником варикоза. Своевременное распознавание и лечение венозной недостаточности может предотвратить развитие варикозной болезни.
Каковы причины венозной недостаточности
Венозная недостаточность развивается вследствие первичной несостоятельности венозных клапанов или из-за гипертензии в поверхностных венах. В последнем случае кровоток по перфорантным венам резко увеличивается и становится ретроградным, образно говоря, «извращенным»: с преимущественным обратным током из глубоких вен в поверхностные. Так формируется порочный круг: мышечно-венозная помпа голени перегружается, становится несостоятельной и еще больше увеличивает гипертензию в поверхностных венах.
Последствия венозной недостаточности
Венозная недостаточность диагностируется при физикальном обследовании с использованием функциональных проб и ультразвукового исследования (УЗИ), реже – при рентгеноконтрастной флебографии.
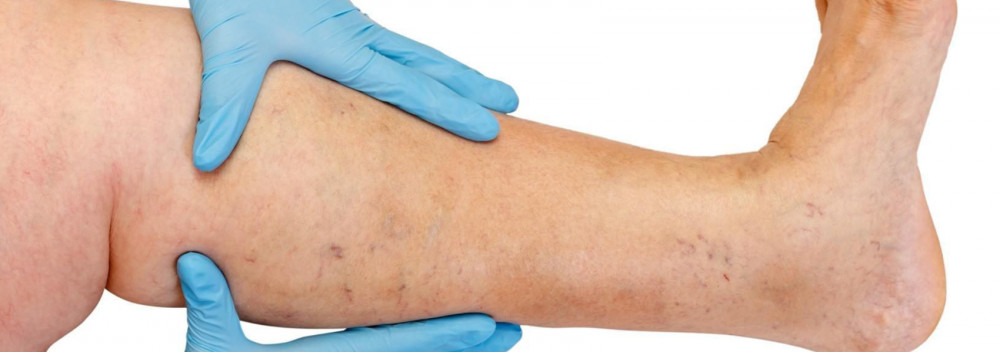
Венозная недостаточность может быть обнаружена при осмотре ноги — по наличию несостоятельных перфорантных вен в проекции наиболее вовлеченных в процесс подкожных вен. При невыраженной подкожной клетчатке и большом диаметре перфорантных вен их локализация определяется пальпаторно по дефекту в фасции.
Доказано, что венозная недостаточность играет большую роль в развитии варикозной болезни. Поэтому при недостаточности вен необходимо ликвидировать ретроградный кровоток. Это достигается хирургическим путем – методами пересечения, перевязки, коагуляции, клипирования либо склерозирования.
Что такое несостоятельные перфорантные вены голени
Кафедра факультетской хирургии лечебного факультета Российского государственного медицинского университета, Москва
Кафедра факультетской хирургии лечебного факультета Российского государственного медицинского университета, Москва
ГКБ №1 им Н. И. Пирогова, Москва, Россия
ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, Москва, Россия
Недостаточность перфорантных вен при варикозной болезни: патогенетическое значение и методы коррекции
Журнал: Флебология. 2010;4(4): 29-36
Ярич А. Н., Брюшков А. Ю., Каралкин А. В., Золотухин И. А. Недостаточность перфорантных вен при варикозной болезни: патогенетическое значение и методы коррекции. Флебология. 2010;4(4):29-36.
Iarich A N, Briushkov A Iu, Karalkin A V, Zolotukhin I A. Incompetence of perforating veins in patients with primary varicosis: role in the pathogenesis and methods of correction. Flebologiya. 2010;4(4):29-36.
Кафедра факультетской хирургии лечебного факультета Российского государственного медицинского университета, Москва
Представлен обзор данных литературы, посвященных недостаточности перфорантных вен при варикозной болезни. Помимо обсуждения общеизвестных и хорошо документированных фактов относительно анатомии и физиологии перфорантных вен авторы уделяют значительное внимание спорным вопросам, касающимся патогенетического значения рефлюкса крови по этим сосудам. Приведены и подвергнуты обсуждению аргументы, позволяющие предполагать отсутствие существенной роли перфорантного сброса в патогенезе варикозной болезни.
Кафедра факультетской хирургии лечебного факультета Российского государственного медицинского университета, Москва
Кафедра факультетской хирургии лечебного факультета Российского государственного медицинского университета, Москва
ГКБ №1 им Н. И. Пирогова, Москва, Россия
ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, Москва, Россия
Вместе с тем в описанной выше общей схеме патогенеза можно обнаружить весьма существенный недостаток. Внимательный, непредвзятый взгляд на роль перфорантного рефлюкса в патогенезе показывает, что неоспоримых доказательств значения несостоятельности ПВ практически нет. Мы хотим представить и проанализировать как хорошо известные, так и относительно недавно опубликованные данные, касающиеся этой проблемы.
История изучения, анатомические и функциональные особенности перфорантных вен
Первым ученым, продемонстрировавшим наличие ПВ на нижних конечностях, был Х.И. Лодер, российский анатом [17]. Вслед за ним на протяжении полутора столетий изучением анатомии ПВ занимались десятки исследователей, подробно описавших их морфологические характеристики 23. ПВ соединяют поверхностные и глубокие вены нижних конечностей и в норме направляют ток крови из первых в последние. Они называются перфорантными, так как перфорируют мышечную фасцию. ПВ часто дублируются. Параллельно с ПВ проходит маленькая артерия [25]. Перфоранты обладают клапанами (от 1 до 4), которые располагаются главным образом в субфасциальном отрезке сосуда [22]. Количество перфорантов на каждой нижней конечности весьма велико. Одной из первых и наиболее полных работ по этой проблеме является исследование, проведенное отечественным хирургом И.А. Костромовым [26]. Он обнаруживал до 112 перфорантов на одной нижней конечности. Эти данные были подтверждены и другими работами [27].
Локализация ПВ является достаточно постоянной, что нашло свое отражение в длительно существовавших наименованиях наиболее значимых из них по именам авторов, подробно описавших их месторасположение. Вместе с тем современными согласительными документами не рекомендовано использование в практике именных названий этих сосудов [28]. В основу нынешней классификации ПВ положен территориально-анатомический принцип. Согласно ему, ПВ нижних конечностей могут быть разделены на шесть групп: ПВ стопы, области голеностопного сустава, голени, области коленного сустава, бедра и околоягодичной зоны [29].
С клинической точки зрения наибольшее значение имеют перфоранты, располагающиеся на голени, в подколенной ямке и на бедре [30]. Самыми известными для клиницистов являются ПВ медиального отдела голени, которые долгие годы называли перфорантами Коккетта. К ним относят четыре вены, имеющие весьма постоянную локализацию и соединяющие притоки большой подкожной вены (БПВ) с задними большеберцовыми венами. Именно рефлюкс по данным ПВ традиционно признается одной из основных причин варикозного расширения вен и последующих трофических расстройств, в связи с чем большинство хирургических методик предназначено для ликвидации этих сосудов [20].
В верхней трети голени по медиальной поверхности расположены паратибиальные ПВ, также называемые венами Шермана и Бойда. Они соединяют БПВ с задними большеберцовыми венами. Появление в этой зоне варикозно-расширенных вен также зачастую связывают с перфорантным рефлюксом [30].
На бедре с клинической точки зрения интересны прежде всего перфоранты бедренного канала (также называемые ПВ Додда или Хантера), соединяющие БПВ с поверхностной бедренной веной. У некоторых пациентов эти ПВ не имеют связи с БПВ [31].
В функциональном отношении ПВ играют важную роль в направлении крови из поверхностной венозной сети в глубокие вены с помощью своих клапанов [32]. При сокращении мышц (мышечная систола), когда происходит быстрое значительное увеличение давления, клапаны в ПВ закрываются, что предотвращает ток крови из глубокой в поверхностную систему. Во время мышечного расслабления (диастола) давление снижается и клапаны в ПВ открываются, обеспечивая дренаж крови из поверхностной в глубокую систему. Ток крови в интактной ПВ в направлении от поверхностных вен к глубоким долгое время считался аксиомой. И.А. Костромов в 1951 г. сообщил о том, что от 3 до 10% исследованных им интактных ПВ на бедре и голени были бесклапанными, а значит кровоток по ним мог осуществляться в обоих направлениях. Вместе с тем автор [26] также отметил, что при наличии клапанов в ПВ они всегда были ориентированы таким образом, чтобы ток крови происходил в направлении глубоких вен. В исследованиях R. Bjordal [33, 34] также продемонстрировано наличие двунаправленного тока крови в ПВ, но уже у пациентов с первичным варикозным расширением вен. Появление в клинической практике ультразвуковой визуализации позволило наблюдать двунаправленный ток крови по ПВ в реальном масштабе времени как у пациентов с венозной патологией [35, 36], так и у здоровых лиц [36, 37]. Тем не менее есть исследователи, которые не считают возможным существование подобного кровотока по перфорантам в норме [35].
Недостаточность перфорантных вен
Первым ученым, высказавшим мнение о патогенетическом значении недостаточности перфорантных вен, по-видимому, стал R. Linton [23]. Он обследовал больных с трофическими расстройствами и сделал вывод, что в их развитии важная роль принадлежит горизонтальному венозному рефлюксу. Следует сказать, что исследования R. Linton были посвящены посттромботической болезни. Тем не менее идея была подхвачена специалистами из многих стран мира и в результате перфорантный рефлюкс был признан причиной не только трофических расстройств при посттромботической болезни, но и первичного варикозного расширения вен [12, 26, 38, 39]. Опубликованы десятки работ, посвященные перфорантному рефлюксу. Основными проблемами, интересовавшими специалистов, стали методы выявления и критерии несостоятельности ПВ, а также поиск эффективных способов ликвидации перфорантного сброса.
Клиническая диагностика несостоятельности ПВ. Патогномоничных клинических признаков, позволяющих установить факт рефлюкса по ПВ и точно ее локализовать, не найдено. Ориентация на расположение конгломератов расширенных вен и данные функциональных проб (трехжгутовая Шейниса, Тальмана, Пратта-2) [40] долгое время были основными диагностическими критериями, но, с позиций современных требований к научным данным, эти способы не имеют доказательной базы.
Еще одним методом выявления перфорантного рефлюкса служила пальпация дефектов фасции голени, сопровождающаяся болезненными для пациента ощущениями при наличии недостаточной ПВ [14, 26, 41]. Вместе с тем доказательств точности этого способа также не существует [42, 43], в частности не было проведено сравнительных исследований с наиболее точным способом локализации ПВ, которым служит ультразвуковое сканирование.
Рентгеноконтрастная флебография в диагностике несостоятельности ПВ. Восходящая флебография и варикография были первыми инструментальными методами обнаружения перфорантного рефлюкса, который проявляется проникновением контраста из глубокой системы в поверхностную. По данным ряда авторов 47, с помощью рентгеноконтрастного исследования можно выявить от 65 до 90% имеющихся несостоятельных ПВ.
Ультразвуковое ангиосканирование в диагностике несостоятельности ПВ. В последние годы этот метод стал ведущим в диагностике перфорантного рефлюкса. С его помощью могут быть визуализированы ПВ, измерен диаметр вен и описано направление кровотока [36]. Единственные затруднения возникают при визуализации и определении тока крови в ПВ диаметром менее 1 мм, хотя до конца неизвестно, являются ли ПВ этого размера клинически или гемодинамически значимыми. Точность диагностики перфорантного рефлюкса по наиболее гемодинамически значимым ПВ медиальной группы соизмерима с флебографией [48]. E. Pierik и соавт. [49] обследовали 42 пациента с венозными язвами и сообщили о 100% специфичности и 79% чувствительности дуплексного исследования.
Критерии несостоятельности ПВ. Этот вопрос во многом является ключевым, поскольку имеет непосредственное влияние как на формирование взглядов на развитие варикозной болезни, так и на хирургическую тактику. В доультразвуковую эру, когда ведущим диагностическим методом была рентгеновская флебография, критерием считали визуализацию ПВ и связанное с движением крови по ним контрастирование подкожных вен. Аналогичный критерий используют и при проведении радиоизотопной флебографии [51]. Значительные надежды возлагались на появившееся в арсенале флебологов в конце 80-х годов прошлого столетия ультразвуковое ангиосканирование, которое позволяет визуализировать ПВ и определить направление движения крови по ней. Тем не менее, несмотря на многолетнюю историю изучения анатомии и функции ПВ, ученым так и не удалось прийти к общему мнению о том, на основании каких признаков можно считать несостоятельной ПВ [36, 37, 52-54].
Наличие рефлюкса, на первый взгляд, является наиболее достоверным критерием недостаточности ПВ. Показано, что количество ПВ с рефлюксом увеличивается при прогрессировании хронического заболевания вен [35, 37, 55].
Продолжительность рефлюкса как критерий недостаточности варьирует от 0,3 с [56] до 1 с [57], однако большинство авторов [55, 58-61] считают признаком несостоятельности ПВ рефлюкс более 0,5 с.
Что касается диаметра, то некоторые авторы [23, 36, 37, 53, 59] считают определенный диаметр признаком несостоятельности ПВ. К тому же в ряде исследований [35, 55, 59] показано, что несостоятельные ПВ имеют больший диаметр по сравнению с интактными сосудами. Вместе с тем многие специалисты [57, 62] обоснованно полагают, что диаметр не может служить критерием несостоятельности ПВ, указывая как на определенную субъективность оценки диаметра вены, так и на тот факт, что ПВ большого диаметра (0,6-0,7 см) зачастую компетентны, а вены небольшого диаметра (0,2-0,3 см) могут быть недостаточными.
Предложены также другие критерии, характеризующие недостаточность ПВ: в проспективном исследовании 265 ПВ на 90 конечностях с помощью ультразвукового дуплексного сканирования K. Delis [55] заключил, что критериями определения недостаточности перфорантов являются не только диаметр и наличие рефлюкса, но и максимальная и средняя скорость, объем потока, время до достижения максимальной скорости и венозный объем, перемещенный в поверхностную систему. Подобные критерии не нашли сторонников в силу громоздкости и заметной субъективности такой оценки.
Исследования [35, 37, 55] последних лет продемонстрировали, что с нарастанием тяжести заболевания увеличивается и частота выявления недостаточных ПВ. По данным Ю.А. Белькова и соавт. [64], частота гемодинамически значимого рефлюкса в ПВ при различных клинических классах хронических заболеваний вен составляет от 33 до 85%. Исследование, проведенное сотрудниками клиники В.С. Савельева [62], показало, что у пациентов с трофическими расстройствами (классы С4-С5) при ВБНК частота выявления несостоятельных ПВ достигает 100%, но, с другой стороны, при неосложненном течении заболевания (класс С2) перфорантный рефлюкс фиксируется только в 28% случаев.
Недостатки и ограничения инструментальных методов диагностики несостоятельности ПВ. Нельзя не упомянуть о принципиальных недостатках ультразвукового ангиосканирования, которые имеют существенное значение при оценке состояния ПВ. При исследовании проводится оценка кровотока лишь на небольшом отрезке венозного русла и на протяжении незначительного промежутка времени [62]. Таким образом, при получении достаточно детальной анатомической информации о ПВ интегративная оценка ее функции практически невозможна. Предлагаемая техника сканирования ПВ в вертикальном положении пациента во время сокращения-расслабления им икроножных мышц (имитация ходьбы) в некоторой степени нивелирует указанный недостаток ультразвукового сканирования [62, 65], и все же при этом более точно фиксируется лишь факт двунаправленного кровотока по ПВ. Гемодинамическое значение же перфорантного рефлюкса с помощью ультразвукового ангиосканирования установить невозможно.
Методы коррекции недостаточности перфорантных вен
Разработка методов хирургической коррекции несостоятельности ПВ связана с именем R. Linton [23], который предложил проводить их диссекцию через продольный разрез большой длины по медиальной поверхности голени. Это вмешательство получило его имя [14, 66-68]. D. Felder и соавт. [69] в 1955 г. модифицировали вмешательство, предложив выполнять перевязку ПВ из доступа по задней поверхности голени. Этот вариант за счет удаления разреза от трофически измененных тканей позволил уменьшить частоту гнойно-некротических осложнений [66]. Операция Линтона в модификации Фельдера широко применялась во многих флебологических и хирургических центрах мира и стала одной из самых известных во флебохирургии [14, 68]. Вместе с тем высокая частота тяжелых гнойно-некротических осложнений привела к постепенному отказу от ее применения [70].
F. Cockett [20] предложил выполнять не суб-, а надфасциальную перевязку ПВ в нижней и средней трети голени по внутренней поверхности. Однако поиск ПВ в подкожной клетчатке при выраженных трофических изменениях травматичен, вызывает значительные технические трудности, поэтому нередко сопровождался послеоперационным некрозом краев раны и ее нагноением [9, 66], в связи с чем от применения этого вмешательства также пришлось отказаться. Тем не менее, претерпев определенную трансформацию, оно осталось в хирургической практике в виде надфасциального лигирования перфорантов из отдельных небольших разрезов и по-прежнему используется многими врачами. Именно такой вариант известен отечественным хирургам как операция Коккетта, хотя это и не совсем точное наименование.
В 1985 г. G. Hauer [71] впервые опубликовал работу, посвященную эндоскопической диссекции ПВ. Он использовал медиастиноскоп или жесткий проктоскоп для введения инструментов под собственную фасцию голени. Позднее методика была усовершенствована, разработаны специальные эндоскопы и инструменты для выделения и пересечения ПВ [72, 73]. Преимуществами способа являются значимо меньшее количество осложнений, рубцы небольшого размера и более короткий период пребывания больного в стационаре [56, 58, 74, 75]. Частота раневых осложнений составляет 4-26% [76, 77]. Послеоперационный тромбоз глубоких вен возникает редко [74]. Могут также развиться боль (1,5%) и парестезии (6%) после операции, особенно при использовании электрокоагуляции в субфасциальном пространстве [78]. Сообщалось о единичных случаях ятрогенных язв [79] и артериовенозных фистул [80].
Эндоскопическая диссекция ПВ считается эффективной у больных с венозными трофическими язвами (от 84 до 100% заживления язв и 0-22% рецидивов в течение 2 лет) [56, 81-84].
Методы эндовазальной лазерной и радиочастотной облитерации появились в клинической практике в конце 90-х годов прошлого века. Они представляют собой миниинвазивные амбулаторные процедуры, требующие только местной анестезии. Первоначальной областью их применения стало устранение рефлюкса по большой или малой подкожным венам 88.
Флебосклерозирование давно используют многие врачи для ликвидации несостоятельных ПВ [31, 91-93], но к настоящему времени отсутствует общая точка зрения на эффективность и роль этой методики 93.
Оценивая эффективность склерозирования ПВ, нужно признать, что качественных исследований [28, 61, 97], посвященных этой проблеме, крайне мало. Было проведено два проспективных исследования склеротерапии несостоятельных ПВ под ультразвуковым контролем. P. Thibault и W. Lewis [98] склерозировали ПВ у 36 пациентов 0,5-1,0 мл 3% тетрадецилсульфата натрия. В 15% случаев возникла необходимость в проведении повторных инъекций. Компрессию применяли в течение 4 нед. Через 6 мес от 73 до 100% перфорантов были облитерированы. Наилучшие результаты были достигнуты при инъекции в недостаточные ПВ голени. Авторы сделали вывод, что требуются дальнейшее усовершенствование технически сложной процедуры и разработка устройства для игольного проводникового зонда, позволяющего достичь точной локализации конца иглы на глубине от 0,5 до 3 см. Осложнений (тромбоз глубоких вен, легочная эмболия или внутриартериальное введение) не отметили.
В другом открытом проспективном исследовании, выполненном M. Schadeck [99], 3% тетрадецилсульфат натрия использовали у 51 пациента. В первую очередь склерозировали подкожные вены. Наблюдение в срок от 1 до 7 мес показало 92% благоприятных исходов при одном проведенном сеансе. Компрессию не применяли. В 40% случаев наблюдали такие осложнения, как покраснение, боль или уплотнение. Не отмечено ни одной интраартериальной инъекции, венозного тромбоза или повреждений нервов.
J.-J. Guex [100] сообщил о достижении окклюзии ПВ в 90% случаев при трех или менее сеансах терапии. Вены с диаметром более 8 мм, по его мнению, устойчивы к склерозирующему воздействию. По мнению J.-J. Guex, дальнейшие исследования должны включать измерения диаметра и длительности рефлюкса до и после процедуры, плетизмографическую оценку терапии.
Осложнения склеротерапии ПВ идентичны таковым при облитерации подкожных вен: гиперпигментация, флебит, некроз, аллергические реакции, интраартериальные инъекции [101]. Вопреки упоминаемой многими авторами [102] опасности попадания в сопровождающую перфорант артерию такие осложнения при склерозировании ПВ более редки.
Очевидно, что возможности склерозирования ПВ нуждаются в тщательном дальнейшем изучении. Неизвестны отдаленные результаты этих манипуляций [100], поскольку большинство исследователей [103] сообщают лишь о коротких периодах наблюдения.
Подобные наблюдения заставляют задуматься, во-первых, о возможностях хирургического устранения ПВ, а, во-вторых, о патогенетической обоснованности и целесообразности этих вмешательств.
Противоречия в теории патогенетического значения перфорантного сброса при варикозной болезни
Безусловно, все приведенные аргументы могут служить лишь косвенным свидетельством того, что несостоятельность ПВ при варикозной болезни не имеет того значения, которое ей принято придавать. Тем не менее эти данные нельзя игнорировать.
Варикозная болезнь ног: анатомия, клиника, диагностика и методы лечения
Анатомия вен ног человека
Анатомическое строение венозной системы нижних конечностей отличается большой вариабельностью. Знание индивидуальных особенностей строения венозной системы играет большую роль в оценке данных инструментального обследования в выборе правильного метода лечения.
Глубокие вены тыла стопы начинаются тыльными плюсневыми венами стопы, впадающими в тыльную венозную дугу стопы, откуда кровь оттекает в передние большеберцовые вены. На уровне верхней трети голени передние и задние большеберцовые вены сливаясь образуют подколенную вену, которая располагается латеральнее и несколько сзади от одноименной артерии. В области подколенной ямки в подколенную вену впадают малая подкожная вена, вены коленного сустава. Глубокая вена бедра обычно впадает в бедренную на 6-8см ниже паховой складки. Выше паховой связки этот сосуд принимает эпигастральную вену, глубокую вену окружающую подвзошную кость и переходит в наружную подвздошную вену, которая у крестцово-подвздошного сочленения сливается с внутренней подвздошной веной. Парная общая подвздошная вена начинается после слияния наружной и внутренней подвзошных вен. Правая и левая общие подвздошные вены сливаются, образуя нижнюю полую вену. Она представляет собой крупный сосуд, не имеющий клапанов длинной 19-20см и диаметром 0,2-0,4см. Нижняя полая вена имеет париетальные и висцеральные ветви, по которым поступает кровь от нижних конечностей, нижней части туловища, органов брюшной полости, малого таза.
Перфорантные (коммуникантные) вены соединяют глубокие вены с поверхностными. Большинство из них имеют клапаны, расположенные надфасциально и благодаря которым кровь движется из поверхностных вен в глубокие. Различают прямые и непрямые перфорантные вены. Прямые непосредственно соединяют глубокую и поверхностные венозные сети, непрямые соединяют опосредованно, то есть сначала впадают в мышечную вену, которая затем впадает в глубокую.
Клиническое течение заболевания
Диагностика варикозной болезни
Особенно трудно диагностировать доклиническую стадию варикозной болезни, поскольку у такого больного может и не быть варикозных вен на ногах.
У таких пациентов ошибочно отвергается диагноз варикозного расширения вен ног, хотя имеется симптоматика варикоза, указания на наличие у пациента родственников, страдающих этим недугом (наследственная предрасположенность), данные ультразвукового исследования о начальных патологических изменениях в венозной системе.
Все это может привести к упущению сроков для оптимального начала лечения, формированию необратимых изменений венозной стенки и развитию весьма серьезных и опасных осложнений варикоза. Только при распознавании болезни на ранней доклинической стадии появляется возможность предупредить патологические изменения в венозной системе ног путем минимального лечебного воздействия на варикозную болезнь.
Избежать разного рода диагностических ошибок и поставить правильный диагноз возможно только после тщательного осмотра пациента опытным специалистом, правильная интерпретация всех его жалоб, подробнейший анализ истории заболевания и полученной на самом современном оборудовании максимально возможной информации о состоянии венозной системы ног (инструментальные методы диагностики).
Дуплексное сканирование иногда проводят для определения точной локализации перфорантных вен, выяснения вено-венозных рефлюксов в цветовом коде. В случае недостаточности клапанов их створки перестают полностью смыкаться при проведении пробы Вальсавы или компрессионных пробах. Недостаточность клапанов приводит к появлению вено-венозного рефлюкса, высокого, через несостоятельное сафено-феморальное соустье, и низкого, через несостоятельные перфорантные вены голени. С помощью этого метода можно зарегистрировать обратный ток крови через пролабирующие створки несостоятельного клапана. Именно поэтому диагностика у нас носит многоступенчатый или многоуровневый характер. В обычной ситуации диагноз ставится после УЗИ-диагностики и осмотра врача-флеболога. Однако в особо трудных случаях обследование приходится выполнять поэтапно.
Лечение
Больным рекомендуется ограничивать прием воды и соли, нормализовать массу тела, периодически принимать диуретики, препараты улучшающие тонус вен (детралекс, гинкор-форт, троксевазин, венорутон, анавеол, эскузан и др.). По показаниям назначают препараты улучшающие микроциркуляцию в тканях (пентоксифиллин, аспирин и упомянутые выше препараты). Для лечения рекомендуем применять нестероидные противовоспалительные средства.
Существенную роль в предупреждении варикозного расширения вен принадлежит лечебной физкультуре. При неосложненных формах полезны водные процедуры, особенно плавание, теплые (не выше 35°) ножные ванны с 5-10 % раствором пищевой соли.
Компрессионная склеротерапия
Чрескожная лазерная коагуляция (ЧЛК)
Эффективность ЧЛК напрямую зависит от глубины проникновения лазерного излучения: чем глубже находится сосуд, тем больше должна быть длина волны, тем самым ЧЛК имеет достаточно ограниченные показания. Для сосудов с диаметром, превышающим 1,0-1,5 мм наиболее эффективной является микросклеротерапия. Учитывая протяженное и ветвистое распространение сосудистых звездочек на ногах, вариабельный диаметр сосудов, в настоящее время активно используется комбинированный метод лечения : на первом этапе проводится склеротерапия вен диаметром более 0,5 мм, затем для удаления оставшихся «звездочек» меньшего диаметра используют лазер.
Процедура практически безболезненна и безопасна (охлаждение кожи и анестетики не применяются), поскольку свет аппарата Ellipse относится к видимой части спектра, а длина световой волны рассчитана так, чтобы вода в тканях не закипала, и пациент не получил ожоги. Пациентам с высокой болевой чувствительностью рекомендовано предварительное нанесение крема «ЭМЛА», обладающего местноанестезирующим действием. Эритема и отеки спадают через 1-2 дня. После курса, примерно в течение двух недель, у некоторых пациентов может наблюдаться потемнение или осветление обработанного участка кожи, которое затем исчезает. У людей со светлой кожей изменения практически незаметны, а вот у пациентов со смуглой кожей или сильным загаром, риск такой временной пигментации достаточно высок.
Хирургическое лечение
Хирургическое вмешательство является единственным радикальным методом лечения больных с варикозно расширенными венами нижней конечности. Целью операции является устранение патогенетических механизмов (вено-венозных рефлюксов). Это достигается путем удаления основных стволов большой и малой подкожной вены и лигированием несостоятельных коммуникантных вен.
Лечение варикоза оперативным путем имеет столетнюю историю. Ранее, а многими хирургами и сейчас, применялись большие разрезы по ходу варикозных вен, общая или спинномозговая анестезия. Следы после такой «минифлебэктомии» остаются пожизненным напоминанием о перенесенной операции. Первые операции на венах (по Шаде, по Маделунгу) были настолько травматичными, что вред от них превышал вред от варикозной болезни.
Флебологами нашей сети клиник разработана уникальная технология лечения варикозной болезни за один день. Сложные случаи оперируются с применением комбинированной техники. Основные крупные варикозные стволы удаляются инверсионным стриппингом, который подразумевает минимальное вмешательство через миниразрезы (от 2 до 7мм) кожи, которые практически не оставляют рубцов. Использование миниинвазивной техники предполагает минимальную травму тканей. Результатом нашей операции является устранение варикозной болезни с отличным эстетическим результатом. Комбинированное оперативное лечение мы проводим под тотальной внутривенной или спинальной анестезией, а максимальными сроками госпитализации до 1 суток.
Оперативное лечение включает в себя:
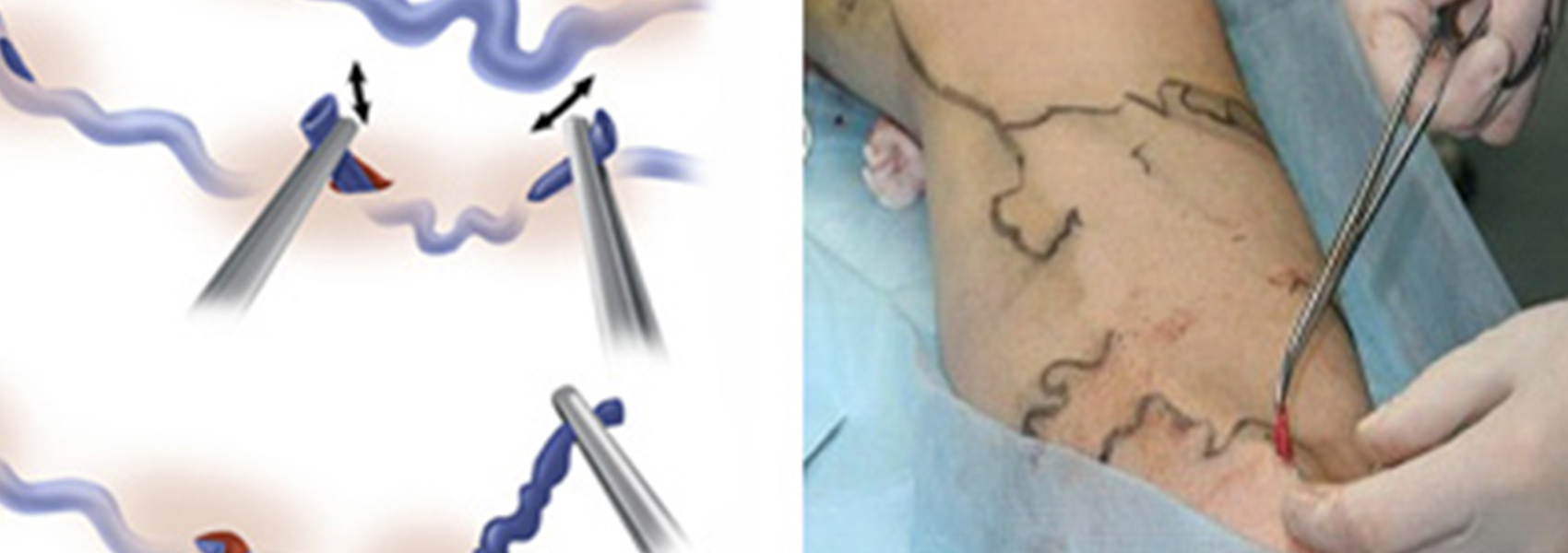
Собственно минифлебэктомия пришла на смену методике удаления варикозно расширенных притоков магистральных вен по Нарату. Раньше по ходу вариксов выполнялись разрезы кожи от 1-2 до 5-6 см, через которые вены выделялись и удалялись. Стремление улучшить косметический результат вмешательства и получить возможность удалять вены не через традиционные разрезы, а через миниразрезы (проколы), заставило врачей разработать инструменты, позволяющие делать практически то же самое через минимальный дефект кожи. Так появились наборы флебэктомических «крючков» различных размеров и конфигурации и специальные шпатели. А вместо обычного скальпеля для прокола кожи стали использовать скальпели с очень узким лезвием или иглы достаточно большого диаметра (например, игла, использующаяся для взятия венозной крови на анализ диаметром 18G). В идеале, след от прокола такой иглой через некоторое время практически не виден.
При некоторых формах варикозной болезни мы проводим лечение в амбулаторных условиях под местной анестезией. Минимальная травма при минифлебэктомии, а так же небольшой риск вмешательства, позволяют проводить эту операцию в условиях дневного стационара. После минимального наблюдения в клинике после операции, пациент может быть отпущен домой своим ходом. В послеоперационном периоде сохраняется активный образ жизни, приветствуется активная ходьба. Временная нетрудоспособность составляет обычно не более 7 дней, затем возможно приступить к труду.
Когда применяется микрофлебэктомия?
Она может быть самостоятельной операцией или являться компонентом комбинированного лечения варикоза, сочетаясь с лазерным лечением вен и склеротерапией. Тактика применения определяется индивидуально, обязательно с учетом результатов ультразвукового дуплексного сканирования венозной системы пациента. Микрофлебэтомия применяется для удаления измененных по разным причинам вен самой разной локализации, в том числе и на лице. Профессор Варади из Франкфурта разработал свои удобные инструменты и сформулировал основные постулаты современной микрофлебэктомии. Метод флебэктомии по Варади даёт превосходный косметический результат без боли и госпитализации. Это очень кропотливая, почти ювелирная работа.
После операции на венах
Послеоперационный период после обычной «классической» флебэктомии достаточно болезненный. Иногда беспокоят крупные гематомы, бывает отек. Заживление ран зависит от хирургической техники флеболога, иногда бывает истечение лимфы и длительное формирование заметных рубцов, нередко после большой флебэктомии остается нарушение чувствительности в области пятки.
В противоположность этому после минифлебэктомии раны не требуют зашивания, так как это только проколы, болевых ощущений не бывает, повреждения кожных нервов в нашей практике не наблюдалось. Однако такие результаты флебэктомии достигаются только у очень опытных флебологов.
Запись на прием к врачу флебологу
Обязательно пройдите консультацию квалифицированного специалиста в области заболеваний сосудов в клинике «Семейная».