Что такое отек мозга после операции
Быстро возникающий интраоперационный отек мозга создает нейроанестезиологу множество проблем. В тяжелых (экстренных) случаях может возникать опасность для жизни при острой мозговой грыже. При меньшей степени набухания, необходимо принять меры для уменьшения напряжения мозговой ткани, для улучшения хирургического доступа.
Чаще всего отек наблюдается после удаления посттравматических внутричерепных гематом, но может развиваться и при плановых операциях в результате острого кровотечения. Механизмы, лежащие в основе развития интраоперационного отека, окончательно не ясны, но доказана роль острой церебральной гиперемия или отека мозговой ткани.
Клиническая картина отека мозга во время операции. Обычно первым признаки отека замечает оперирующий хирург, но если причиной является скрытое кровотечение, возникшее пне операционного gоля, то сердечно-сосудистые изменения, такие как гипертензия или брадикардия, отек первым замечает анестезиолог.
Лечение интраоперационного отека мозга
Принципы лечения отека мозга одинаковы и при открытом и при закрытом черепе.
• Обсудить с хирургом:
— Имеется ли кровотечение или гидроцефалия?
— Где находятся хирургические ретракторы?
• Исключить нарушение венозного оттока:
— правильно ли уложена голова пациента на столе?
— не пережимаются ли вены шейным воротником или фиксатором интубационной трубки?
— также можно приподнять головной конец на 15-20°.
• Убедиться в достаточной оксигенации.
• Убедиться, что уровень РаСО2 находится в пределах 4,5-5,0 кПа:
— если это так, провести транзиторную гипервентиляцию;
— проверить газы артериальной крови.
• Минимизировать потребление кислорода мозгом:
— убедиться в адекватной миорелаксации, анальгезии и анестезии;
— болюсно ввести пропофол или тиопентал.
• Диуретики:
— маннитол 0,25-1,0 г/кг.
• Стероиды: несмотря на то, что у пациентов с ЧМТ не доказан положительный эффект от стероидов, (дополнительная) доза дексаметазона часто запрашивается хирургом во время резекции опухоли. Эффект стероидов развивается недостаточно быстро для эффективного купирования интраоперационного отека мозга.
Советы по ведению пациента с интраоперационным отеком мозга:
• Быстро развивающийся острый интраоперационный отек мозга связывают со скрытым кровотечением, пока не доказана другая причина. Терапевтические меры, направленные на снижение ВЧД, не смогут остановить кровотечение.
• Снижение САД может уменьшить церебральную гиперемию, но при этом создает дополнительный риск ишемии.
• Парциальное давление СО2 в конце выдоха не может использоваться для оценки его содержания в артериальной крови. При остром отеке мозга всегда проводят анализ газов артериальной крови.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отек мозга
Отек мозга характеризуется накоплением воды в ткани мозга, увеличением его объема и массы, а также повышением внутричерепного давления. Причины набухания мозга разнообразны: травма мозга, нарушение мозгового кровообращения (в частности, гипертонический криз, острая гипертоническая энцефалопатия), геморрагический инсульт, инфаркт мозга, опухоль мозга, менингоэнцефалит, энцефалит, гипоксия мозга, интоксикации, облучение мозга, эпилептический статус. В зависимости от конкретных механизмов развития различают следующие варианты отека мозга.
1) Вазогенный отек. Возникает в результате значительного повышения давления в капиллярах мозга и расширения в них межклеточных щелей. Обычно развивается при остром нарушении мозгового кровообращения, энцефалите, опухоли из клеток нейроглии.
2) Цитотоксический отек. Возникает при экзогенной, а в случае опухоли мозга и эндогенной интоксикации промежуточными продуктами обмена при нарушении клеточного метаболизма. Определенную роль могут играть продукты распада злокачественных опухолей мозга. К цитотоксическому относят и отек, развивающийся вследствие ишемии мозга.
3) Осмотический отек. Развивается при нарушении существующего в норме небольшого осмотического градиента между осмолярностью ткани мозга (она выше) и осмолярностью плазмы. Этот градиент возрастает при нарушениях клеточного метаболизма и дисфункции клеточных мембран, ведущей к накоплению в клетках продуктов метаболизма. Отек возрастает, если искусственно снижается осмолярность плазмы, например путем в/в введения низкоосмолярных растворов.
4) Гидростатический отек. Развивается на фоне повышенного ликворного давления, когда затрудняется фильтрация жидкости из межклеточных пространств в ликвор.
Отек мозга может быть ограниченным, очаговым или диффузным, разлитым. Диагностика достаточно сложна, поскольку прямых методов его распознавания в настоящее время не существует. Ныне единственной возможностью идентифицировать отек мозга инструментальными методами исследования являются проводимые в динамике КТ и МРТ, показывающие возрастающее понижение плотности мозговой ткани.
Отек мозга приводит к морфологическим изменениям нервной ткани, таким как: 1) расширение межклеточных и околососудистых щелей; 2) изменения эндотелия капилляров; 3) увеличение объема нейронов и особенно глиальных клеток, астроцитов и олигодендроцитов, которые набухают, как и нейроны; 4) нарушение структуры миелиновой оболочки; 5) длительный отек влечет гибель нейронов, в меньшей степени – глиальных элементов. Разрушение нейронов во многом определяет прогноз даже при адекватном, но несвоевременном начале лечения.
Другая опасность диффузного набухания мозга состоит в высоком риске вклинения мозговых структур в щели твердой мозговой оболочки. Вклинения обычно сопровождаются смещением и сдавлением артерий и вен, черепных нервов, нарушением ликвородинамики, что, в свою очередь, приводит к дальнейшему нарастанию отека.
В лечении отека мозга главным является устранение его причины. Кроме того, назначаются осмотические диуретики (чаще используется в/в капельное введение маннитола, реже – менее эффективного глицерола), салуретики (чаще фуросемид или лазикс), диакарб (фонурит, ацетазоламид), кортикостероиды в достаточных дозировках (обычно дексаметазон, преднизолон), средства симптоматической терапии.
Отек головного мозга
Почему возникает отек головного мозга, чем он грозит и как его предотвратить.
Мозг отвечает за все функции организма, поэтому, если он «выходит из строя», это влечет за собой множество проблем со здоровьем.
Что такое отек головного мозга?
Отек мозга – это ответная реакция организма на чрезмерные нагрузки или инфекцию. Обычно отек развивается очень быстро, однако так же быстро исчезает, если вовремя наложить лед или удалить избыточное количество жидкости. Если же отек мозга является результатом травмы или заболевания, вылечить его гораздо сложнее.
Для описания этого состояния также используется термин «повышенное внутричерепное давление», а также «церебральная эдема». Его суть заключается в том, что внутри черепной коробки повышается давление, в ответ на это нарушается мозговое кровообращение, а это, в свою очередь, приводит к отмиранию клеток мозга.
Причины отека головного мозга
Травма, болезнь, инфекция и даже перепад высот – любая из этих причин может привести к отеку мозга.
Черепно-мозговая травма (ЧМТ) – механическое повреждение внутричерепных структур. Возникает вследствие удара, падения, аварии. Зачастую ЧМТ осложняется ранением мозга отломками кости. Слишком сильный отек, в свою очередь, препятствует оттоку жидкости из ткани мозга.
Ишемический инсульт – наиболее распространенный тип нарушения мозгового кровообращения в результате образования тромба. В этом случае клетки мозга, не получая должного количества кислорода, начинают отмирать, и развивается отек.
Геморрагический инсульт – результат повреждения кровеносных сосудов мозга. Возникшее внутримозговое кровоизлияние приводит к повышению внутричерепного давления. Чаще всего геморрагический инсульт развивается из-за повышенного артериального давления, среди других причин – травма головы, прием некоторых лекарственных препаратов, а также врожденные пороки развития.
Инфекционные заболевания:
• Менингит – воспаление оболочки головного мозга, вызванное бактериями, вирусами и другими микроорганизмами, а также приемом некоторых медикаментов.
• Энцефалит – воспалительное заболевание мозга, вызванное группой вирусов, переносчиками которого обычно являются насекомые. Похожее состояние – энцефалопатия – наблюдается при синдроме Рейе.
• Токсоплазмоз – паразитарное заболевание, способное поразить ребенка еще в утробе матери. В группу риска входят также грудные дети и люди с ослабленной иммунной системой.
• Субдуральный абсцесс (Субдуральная эмпиема) представляет собой гнойную инфекцию (осложнение другого заболевания, например, менингита или синусовых инфекций), которая, быстро развиваясь, становится причиной отека мозга и препятствует оттоку жидкости из его тканей.
• Опухоль. Разрастаясь, она сдавливает участок мозга, нарушая кровообращение и вызывая отек окружающей ткани.
• Перепад высот. По неподтвержденным данным, высота более полутора километров над уровнем моря способна стать причиной отека мозга, что наблюдается при острой форме горной болезни (так называемый высокогорный отек мозга).
Симптомы отека мозга
Симптомы отека мозга варьируются в зависимости от причины и тяжести состояния. Как правило, признаки заболевания развиваются внезапно:
• Головная боль
• Боль или онемение в области шеи
• Тошнота, рвота
• Головокружение
• Неравномерное дыхание
• Нарушения зрения
• Амнезия
• Нарушение равновесия и походки (атаксия)
• Затруднение речи
• Понижение уровня сознания (ступор)
• Судороги
• Потеря сознания
Диагностика отека мозга
Выбор методов диагностики зависит от симптомов и предварительного диагноза. Общие обследования и тесты, используемые для диагностики отека мозга:
• Обследование шейно-головного отдела
• Неврологическое обследование
• КТ головного мозга – с целью определения величины и локализации отека
• МРТ головного мозга – с целью определения величины и локализации отека
• Анализ крови для определения возможных причин отека
Лечение отека мозга
Иногда симптомы отека головного мозга (например, вследствие легкой формы горной болезни или небольшого сотрясения) проходят самостоятельно через несколько дней. Однако в более серьезных случаях требуется незамедлительная медицинская помощь.
Лечение с помощью комбинации хирургических и медикаментозных методов направлено на снабжение мозга кислородом. В результате отек уходит. Как правило, своевременная терапия способствует более раннему и полному выздоровлению и заключается в следующем:
• Оксигенотерапия – искусственное введение кислорода в дыхательные пути (через ингалятор или другие приспособления). В этом случае насыщенная кислородом кровь лучше питает поврежденный мозг.
• Внутривенное вливание. Внутривенное введение лекарственных препаратов позволяет поддерживать давление и кровоток в норме, а также помогает бороться с возможной инфекцией.
• Понижение температуры тела (гипотермия) является эффективным методом коррекции отека мозга. Однако в настоящее время он используется еще недостаточно широко.
Лекарственные препараты. В некоторых случаях при отеке мозга назначаются медикаменты. Их выбор определяется в зависимости от причины и симптомов, сопровождающих развитие отека.
Вентрикулостомия представляет собой дренаж цереброспинальной жидкости из желудочков головного мозга через катетер. Данная операция выполняется для уменьшения повышенного внутричерепного давления.
Целью хирургического вмешательства при отеке мозга могут быть:
• Удаление фрагмента кости черепа, чтобы уменьшить внутричерепное давление. Эта операция называется декомпрессивной краниэктомией.
• Устранение причины отека, например, восстановление поврежденного кровеносного сосуда или удаление новообразования.
Осложнения отека головного мозга
Как правило, отек мозга имеет отдаленные последствия. Проблемы, с которыми вы можете столкнуться в будущем, зависят от тяжести и локализации повреждения. Возможно, это будут:
• Нарушения режима сна
• Рассеянность
• Нарушения двигательной активности
• Головные боли
• Депрессия
• Нарушения коммуникативных способностей
Конечно, врачи постараются свести к минимуму все эти негативные последствия.
Профилактика отека головного мозга
Чтобы избежать такой серьезной проблемы, как отек мозга, необходимо не забывать о правилах безопасности в повседневной жизни. Вот несколько простых правил:
• Всегда надевайте защитный шлем, когда вы ездите на велосипеде или на роликах, занимаетесь контактными видами спорта – выполняете какие-либо действия, при которых можно получить травму головы.
• Не забывайте о ремнях безопасности в автомобиле.
• Контролируйте и поддерживайте в норме артериальное давление.
• Не курите.
• Поднимаясь в горы, давайте себе время на акклиматизацию к высоте.
Отёк мозга причины, симптомы, методы лечения и профилактики
Отёк мозга — патологическое состояние, при котором в церебральных тканях стремительно накапливается жидкость. Отёк головного мозга опасен для жизни и здоровья и требует незамедлительной врачебной помощи: если не оказать ее, пациент может погибнуть.
Отёк мозга может развиться после перенесённых черепно-мозговых травм, обширных инсультов, на фоне опухолей головного мозга, инфекционных заболеваний и гнойных процессов. Проблема дает о себе знать расстройствами сознания вплоть до комы, судорогами, а затем — мышечной атонией. Если вы заметили такие признаки у близкого, безотлагательно вызывайте скорую помощь.
Симптомы отёка мозга
Основной признак отёка мозга — расстройство сознания. Оно может проявляться в виде лёгкого сопора с сохранением рефлексов и отсутствием возможности двигаться или комы. В большинстве случаев пациент теряет сознание, у него происходят судороги, которые сменяются мышечной атонией.
Если отёк мозга развивается при хронической или медленно прогрессирующей церебральной патологии, на начальном периоде больной может оставаться в сознании. В таком случае он жалуется на:
Самые опасные проявления отёка мозга — парадоксальное дыхание с глубокими вдохами и поверхностными выдохами, нестабильность пульса, подъем температуры выше 40°C. Симптомы сопровождают сдавление ствола мозга и требуют незамедлительной помощи врача.
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 20 Декабря 2021 года
Содержание статьи
Причины
Разновидности
Отёк головного мозга может произойти у новорожденных и взрослых пациентов. Проблема возникает при инфекционных и неинфекционных поражениях и разделяется на разновидности по пораженной площади и особенностям патогенеза:
По локализации
По патогенезу
Диагностика
Чтобы диагностировать отёк головного мозга, врач собирает анамнез, оценивает неврологический статус, по возможности — проводит компьютерную или магнитно-резонансную томографию головного мозга, клинический и биохимический анализы крови.
В клинике ЦМРТ проводят первичную диагностику отёка головного мозга в условиях стационара максимально оперативно, параллельно с лечебными мероприятиями:
NSICU.RU neurosurgical intensive care unit
сайт отделения реанимации НИИ им Н.Н. Бурденко
Курсы повышения квалификации

Внутричерепная гипертензия

Асинхронии и графика ИВЛ

Водно-электролитные
нарушения
в нейрореанимации

Книга «Основы ИВЛ»

Рекомендации
по интенсивной терапии
у пациентов
с нейрохирургической патологией
Статьи → Нетипичное течение отека мозга, развившегося после удаления опухоли базальной локализации (наблюдение)
После удаления опухолей головного мозга может развиваться отек-набухание мозга иувеличиваться внутричерепное давление (ВЧД). Одной из вероятных и наименее изученныхпричин этого является нарушение венозного оттока. Тяжесть клинических проявлений иисходы венозной дисциркуляции значительно варьируют от головной боли и тошноты докоматозного состояния и летального исхода [14,17,22,26]. Вариабельность клиническойкартины определяется количеством сегментов венозной системы, в которых происходитнарушение оттока. Это было показано в эксперименте Fries G с соавторами [14], когдасвиньям последовательно производили окклюзию верхнего сагиттального синуса, мостиковыхи корковых вен, оценивая при этом клиническое состояние животных, измеряя ВЧД исодержание воды в ткани мозга. Было установлено, что выраженный отек мозга,внутричерепная гипертензия (ВЧГ), разрушение гематоэнцефалического барьера, а затем иартериальная гипоперфузия, приводящая к инфаркту мозга, развивалась только приодновременной окклюзии синуса, мостиковых и корковых вен, когда прекращался иретроградный, и коллатеральный венозный кровоток [1,14]. В то же время установлено, чтонаиболее выраженный неврологический дефицит возникает при нарушении оттока крови поглубоким и парасагиттальным венам или при заинтересованности большого количества венсильвиевой группы [24].
Общепринятых протоколов коррекции ВЧГ, развившейся вследствие нарушения венозногооттока, на сегодня нет. Мы приводим клиническое наблюдение пациентки с менингиомойкрыла основной кости, у которой в раннем послеоперационном периоде остро развилосьнарушение венозного оттока и устойчивая ВЧГ.
Клиническое наблюдение.
Была выполнена операция – субтотальное удаление менингиомы медиальных отделов основаниясредней черепной ямки слева птериональным доступом. Кавернозный синус былинфильтрирован опухолью. Эта часть опухоли не удалялась. Интраоперационно быликоагулированы две враставшие в капсулу опухоли крупные вены сильвиевой группы.
Кровопотеря не превысила 700 мл и была адекватно восполнена.
Пробуждение из наркозного сна было в обычные сроки. Нарастания общемозговой и очаговойневрологической симптоматики по сравнению с дооперационным уровнем не отмечалось.
Пациентка экстубирована через 2 часа после операции. Гемодинамика была стабильной.
Гомеостатические показатели были в пределах нормы.
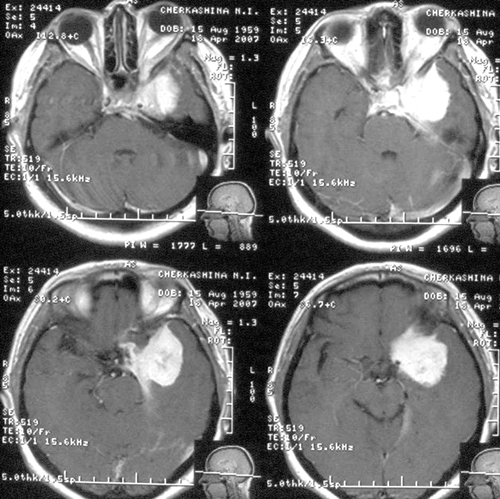
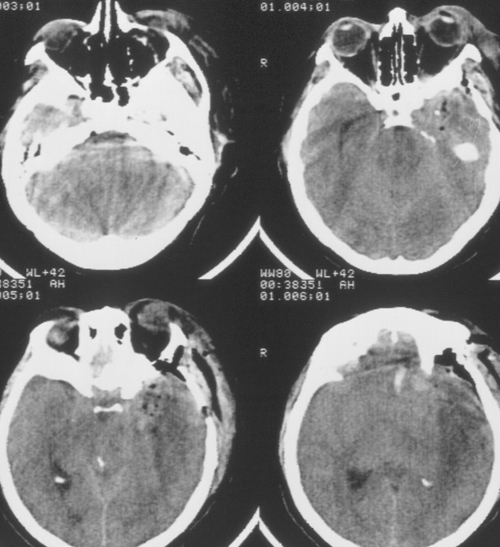
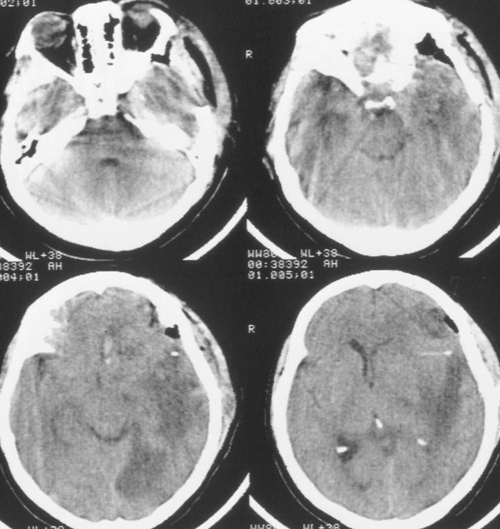
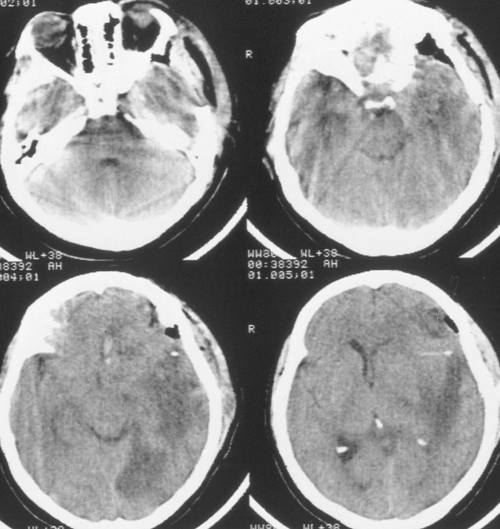
Состояние резко ухудшилось через 12 часов после операции. Развилось коматозноесостояние и правосторонний гемипарез (3 – 4 балла). В связи с дыхательнойнедостаточностью больная была интубирована, начата ИВЛ в режиме SIMV+PS. ПриКТ-исследовании головного мозга был выявлен преимущественно левополушарный отек,массивный очаг пониженной плотности, располагавшийся в лобно-теменно-височной областислева, отмечено смещение срединных структур слева направо на 9 мм. Базальные цистерныне визуализировались, желудочковая система была компремирована (Рис. 2). Притранскраниальной допплерографии линейная скорость кровотока была в пределах нормы. Установлен субдуральный/паренхиматозный датчик ВЧД (Codman, USA). Выявлена выраженнаяВЧГ (ВЧД 35 – 45 мм.рт.ст.).
Для коррекции ВЧГ использовались опции протокола лечения пациентов с черепно-мозговойтравмой, поскольку общепринятых протоколов коррекции ВЧГ при нарушении венозного оттоканет. Головной конец кровати был приподнят на 30º. Начата умеренная гипервентиляция,седация пропофолом (45 мкг/кг/мин), аналгезия фентанилом (0,02 мкг/кг/мин) имиорелаксация пипекуронием (0,5 мкг/кг/мин). Эти мероприятия были неэффективны – ВЧД оставалось на уровне 30 – 35 мм.рт.ст. через 20 минут после начала терапии. После этогобыла использована осмотерапия маннитолом (до 1,5 г/кг). ВЧД через 10 минут снизилось до20 – 25 мм.рт.ст., однако, через 30 мин вновь развилась выраженная ВЧГ (до 40мм.рт.ст.). Повторная инфузия маннитола оказалась неэффективной.
Было принято решение о проведении умеренной гипотермии. Индукция гипотермии началасьспустя час после ухудшения состояния. Использовалось наружное охлаждение и внутривенноевведение охлажденного физиологического раствора в дозе 20 мл/кг. Температура 33º С быладостигнута через два часа после индукции. ВЧД эффективно стабилизировалось на уровне 10– 12 мм.рт.ст. При гипотермии развились гипокалиемия (3,1 – 3,3 ммоль/л) игипомагниемия (0,39 – 0,41 ммоль/л), которые были эффективно корригированы применениемпрепаратов калия и магния. В качестве профилактики развития гипокоагуляции, учитываяранний послеоперационный период и эффекты гипотермии, проводилась плазмотрансфузия вдозе 15 мл/кг. При этом протромбиновый индекс был в пределах 75 – 85%, активированноечастично тромбопластиновое время – 28 – 33 секунды, фибриноген – 3,4 – 3,9 г/л.
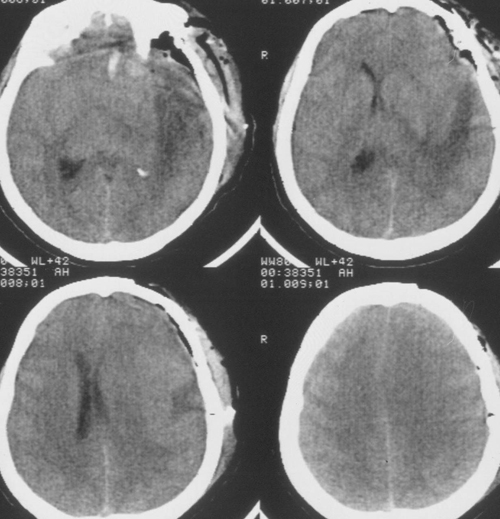
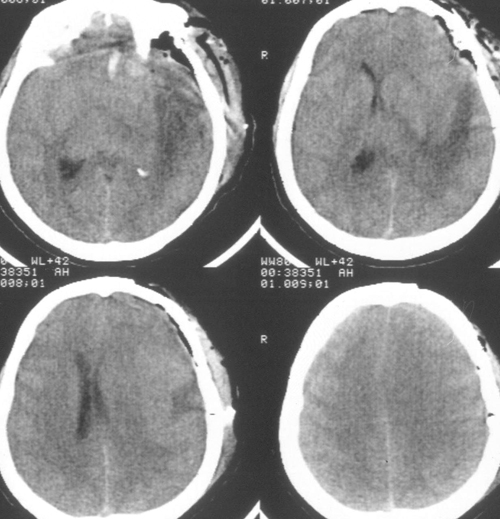
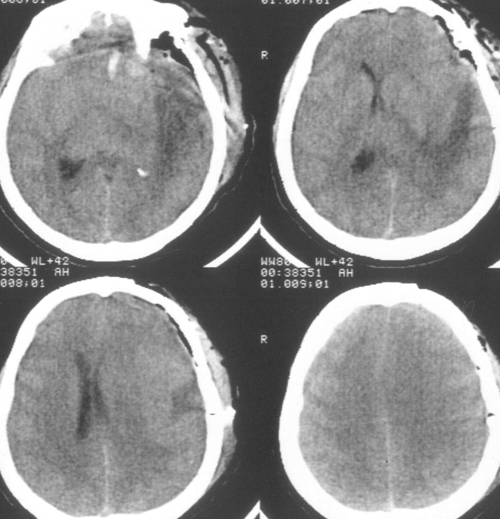
Температура тела 33ºС поддерживалась в течение 24 часов. Перед началом согревания быловыполнено контрольное КТ-исследование головного мозга, выявившее положительную динамикув виде появления базальных цистерн и уменьшения смещения срединных структур вправо до 5мм. Однако сохранялся отек мозга и очаг пониженной плотности в левом полушарии (Рис 3).
При достижении 35ºС (через 10 часов после начала согревания) появилась отчетливаятенденция к ВЧГ, поэтому темп согревания был снижен до ≈ 0,05 градуса в час. Внеседации больная выполняла простые инструкции, правосторонний гемипарез регрессировал.
Таким образом, уже на этом этапе были выявлены положительные эффекты гипотермии в видерегресса общемозговой и очаговой неврологической симптоматики.
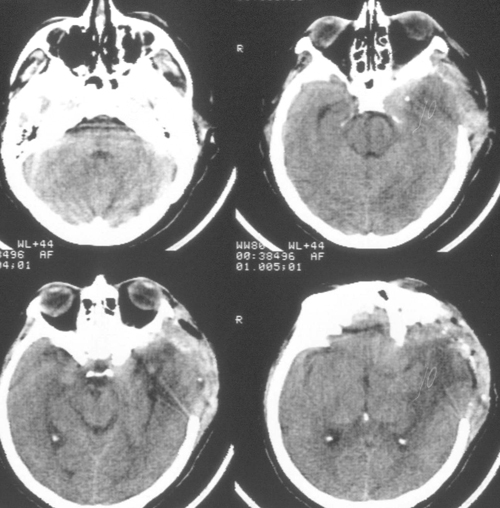
Седация продолжалась еще в течение 2 суток после выполнения наружной декомпрессии, амониторинг ВЧД – в течение 5 суток. В течение этого периода эпизодов внутричерепнойгипертензии не было. При КТ-исследовании была выявлена положительная динамика (Рисунок4). Больная была в сознании, но дезориентирована в месте, времени, личной ситуации.
Движения выявлялись во всех конечностях, без отчетливой ассиметрии. ИВЛ прекращеначерез 6 суток после декомпрессивной трепанации, а еще через 5 суток больная переведенаиз реанимации в нейрохирургическое отделение.
Спустя 1,5 месяца состояние пациентки было стабильным. Выявлялся корсаковский синдром.
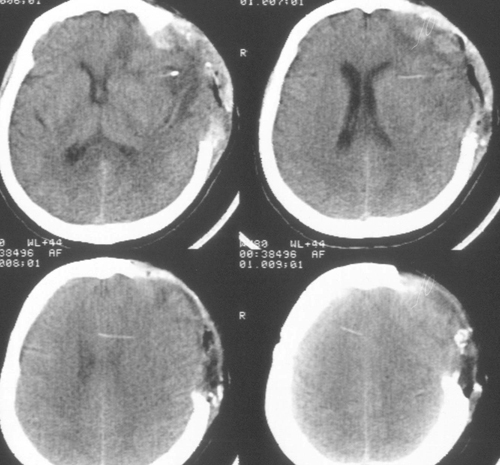
Речевых и двигательных нарушений не было. Было выполнено МРТ-исследование головногомозга с венографией, и в режиме диффузии (Рис 5), при котором выявлено отсутствиекровотока по поперечному и сигмовидному синуса слева. Кроме этого, диагностированобширный очаг церебромаляции лобно-височной области базальной локализации слева,который визуализировался и при КТ-исследовании в остром периоде, как очаг пониженнойплотности.
Через 2,5 месяца у больной развилась гидроцефалия, которая явилась показанием длявыполнения люмбоперитонеального шунтирования. Через 4 месяца больная выписана изИнститута в стабильном состоянии. Больная могла обслуживать себя самостоятельно.
Выраженность корсаковского синдрома уменьшилась. Через 6 месяцев после выпискипланируется повторная госпитализация пациентки для выполнения пластики костногодефекта. Дифференциальный диагноз при ухудшении состояния пациентки проводился междуартериальной ишемией и нарушением венозного оттока. Для нарушения венозного характерно:- отсутствие пробуждения из наркозного сна или ухудшение состояния через несколькочасов после операции [17];- при КТ-исследовании возможна визуализация очага пониженной плотности в первые суткипосле операции вследствие гидростатического отека [2];- интраоперационные данные о повреждении вен или синусов;- скорость кровотока при транскраниальной допплерографии остается нормальной илиснижается [4,29,30,33].- при МРТ-венографии выявляются измененные параметры [2]. Однако выполнение МРТ-исследования в остром периоде при наличии выраженной ВЧГ чревато развитием жизненноугрожающих осложнений.
Итак, дифференциальная диагностика позволила заподозрить у пациентки наличие нарушениявенозного оттока. Патогенез развившегося состояния можно представить следующим образом.
Интраоперационная окклюзия вен сильвиевой группы, включенных в опухоль, привела клокальной венозной дисциркуляции. Отсутствие кровотока по поперечному, сигмовидномусинусу (возможно, врожденное) и кавернозному синусу (инфильтрация опухолью)ограничивало компенсаторные возможности коллатерального перераспределения венозногооттока. Это привело к постепенному, в течение 10 – 12 часов после операции, наростаниюотека мозга, что, в свою очередь, вызвало дисциркуляцию в системе глубоких вен мозга.
Это явилось причиной острого ухудшения через 12 часов после операции с развитиемкоматозного состояния, вследствие выраженного отека мозга и его дислокации.
В настоящий момент отсутствует протокол коррекции ВЧГ при нарушении венозного оттока.
При неэффективности перечисленных опций для снижения ВЧД показано применениеагрессивных методов: барбитуровая кома, наружная декомпрессия или умеренная гипотермия.
Барбитураты не использовались, поскольку, из отчетов организации «Кохрановскоесотрудничество», специализирующейся на систематизации и анализе результатовисследований с использованием принципов доказательной медицины, следует, что: «нетдоказательств того, что терапия барбитуратами у пациентов с тяжелой черепно-мозговойтравмой улучшает исходы. Барбитураты вызывают артериальную гипотензию у каждогочетвертого пациента. Гипотензивный эффект барбитуратов будет нивелировать положительноевлияние снижения ВЧД на церебральное перфузионное давление…» [28].
Наружная декомпрессивная трепанация не была использована на этом этапе, поскольку, поданным Greenberg M.S, при нарушении венозного оттока вследствие венозных тромбозов онаприводит к снижению ВЧД, но не улучшает исходов заболевания [17]. При наружнойдекомпрессии изменяются интракраниальные соотношения, меняется ликвородинамика,повышается риск кровоизлияния в остатки опухоли или очаг ишемии при его наличии.
Известно, что при выраженном отеке мозга после декомпрессии может развиваться ущемлениеткани мозга в костном дефекте с развитием ишемии и вторичным нарушением венозногооттока на этом участке [11,27].
В приведенном наблюдении гипотермия во время ее проведения, во-первых, эффективностабилизировала ВЧД, во-вторых, позволила защитить мозг от ишемии. В отличие отартериальной ишемии, развивающейся, например, вследствие клипирования артерии, принарушении венозного оттока ишемия развивается позднее. Вначале появляется выраженныйгидростатический отек мозга. Именно этим манифестировало ухудшение состояния вприведенном наблюдении. Если коллатеральный или ретроградный венозный кровотокневозможен, то остро развивается несовместимый с жизнью отек мозга. При сохранностиколлатерального или ретроградного венозного кровотока, когда возможно егокомпенсаторное перераспределение, выраженность отека будет значительно варьировать[14]. При сохраняющемся нарушении оттока будут формироваться участки мозга, к которымне будет поступать адекватный объем артериальной крови. Вследствие этого разовьетсяишемия. Итак, при венозном инфаркте вначале развивается гидростатический отек, а затем– ишемия и ишемический отек. При артериальном инфаркте вначале развивается ишемия, азатем – отек. Поскольку в приведенном наблюдении при достижении нормотермии был регрессправостороннего гемипареза и восстановление сознания, а в дальнейшем не былодвигательных нарушений, то гипотермия, вероятно, имела церебропротективный эффект. Кроме этого, проведенная гипотермия обеспечила адекватные условия для выполнения впоследующем наружной декомпрессии.
Гипотермия является агрессивным методом коррекции ВЧГ. Наиболее часто описываемыми влитературе осложнениями являются гипокоагуляция [8,35], водно-электролитные нарушения[21], гемодинамические расстройства [12,34] и инфекционно-воспалительные осложнения[8,34]. Наиболее грозными проявлениями гипокоагуляции являются интракраниальныекровоизлияния. Это обусловило профилактическое использование свежезамороженной плазмы вприведенном наблюдении. Водно-электролитные нарушения при гипотермии проявляютсягипокалиемией и гипомагниемией [21]. Гемодинамические расстройства проявляются обычносинусовой брадикардией. Описаны более опасные нарушения ритма – асистолия и фибрилляцияжелудочков, однако, они развиваются или при температуре менее 28ºС или при длительностигипотермии более 48 часов [8,12,34]. Развившиеся в приведенном наблюдении гипокалиемия,гипомагниемия и гемодинамически незначимая брадикардия не угрожали витальным функциям ибыли корригированы незамедлительно при их развитии. Таким образом, умеренная гипотермияпоказала себя относительно безопасным методом контроля над ВЧД.
Период согревания является важным этапом в проведении гипотермии. В нашем наблюдениипри согревании появилась тенденция к повышению ВЧД. Это согласуется с данными рядаавторов. Так, Schwab S с соавторами показали, что согревание – это период высокогориска развития повторной и устойчивой ВЧГ, которая может приводить к летальному исходу[31,32]. Авторы доказали, что продолжительность согревания, превышающая 16 часов,достоверно уменьшает летальность. Поэтому скорость согревания в нашем наблюдениисоставила ≈ 0,05º в час. Не смотря на это, постепенно развилась устойчивая ВЧГ, чтостало показанием к выполнению наружной декомпрессивной трепанации с пластикой твердоймозговой оболочки. Выбранная тактика позволила не допустить усиления дислокации мозга исохранить структурность паренхимы мозга к моменту декомпрессии.
Данные литературы и наше наблюдение свидетельствуют о том, что гипотермия за счетсвоего церебропротективного эффекта, позволяет уменьшить зону уже сформировавшегосяишемического очага и не допустить дальнейшего ишемического повреждения. Однако в периодсогревания сохраняется риск развития повторной резистентной ВЧГ. В этих условияхнеобходимо выполнять наружную декомпрессию с пластикой твердой мозговой оболочки.
Гипотермия в этом случае будет создавать более благоприятные условия для выполненияоперации.
В заключение необходимо сказать, что у пациентов с опухолями базальной локализации враннем послеоперационном периоде возможно развитие отека мозга вследствие нарушениявенозного оттока. При этом стремительно развивается устойчивая ВЧГ. Дифференцироватьнарушение венозного оттока от других возможных причин развития отека мозга в остромпериоде достаточно сложно. Однако это состояние всегда необходимо рассматривать вкачестве возможной причины развития устойчивой ВЧГ. Умеренная гипотермия являетсяэффективным и безопасным методом коррекции отека мозга и ВЧГ при нарушении венозногооттока. Внутричерепная гипертензия, развившаяся на этапе согревания, являетсяпоказанием к выполнению наружной декомпрессии. И, конечно, необходимы дальнейшиеисследования в этом интересном и перспективном направлении.