Что такое плевральный шок
При возникновении шока, который проявляется в падении кровяного давления, учащении и ухудшении напряжения пульса, поверхностном дыхании, появлении сероватого цвета кожи лица и т. д., надо немедленно принять меры к его устранению, пока он не успел углубиться, после чего борьба с ним станет более трудной.
Для своевременного обнаружения проявлений шока у изголовья больного сидит врач, имеющий опыт в диагностике, профилактике и борьбе с шоком. Этот же врач, если потребуется, дает больному наркоз через герметическую маску или интратрахеально.
Критериями для суждения о состоянии больного являются цвет лица, наличие или отсутствие синюшности, состояние зрачков и голос больного. Из объективных показателей мы придаем решающее значение определению артериального давления, которое необходимо измерять через каждые 5 минут и сообразно с ними проводить весь комплекс противошоковых мероприятий.
Последние годы, наряду с измерением артериального давления во время и после операции, мы систематически измеряем больному венозное давление. Нами применяется метод прямой флеботонометрии с помощью флеботонометра, установленного на штативе и присоединенного во время операции к системе капельного переливания крови.
Регистрация венозного давления проводится каждые 5— 10 минут. Систематически эти данные сверяются с данными артериального давления, записью общего состояния больного, с этапом операции и глубиной наркоза.
Изменения динамики венозного давления во время операции на органах грудной клетки были изучены в нашей клинике А. Н. Мартынычевым у 100 больных, причем у большинства из них оно изучалось также и в послеоперационном периоде.
Наши наблюдения показали, что в течение всей операции венозное давление держится на высоких цифрах, значительно (нередко в 3—4 раза) превышающих исходные. На фоне такого высокого венозного давления в моменты наиболее травматичных этапов операции (разделении спаек, манипуляций на шокогенных зонах, париетальной плевре, корне легкого, у дуги аорты, а также в моменты возбуждения больного, при кашле, стонах, задержке дыхания и т. д.) наблюдались высокие подъемы кривой венозного давления (300—400 мм водяного столба и выше).
Во время операции пневмэктомии наиболее постоянно наблюдалось повышение венозного давления в моменты перевязки легочных сосудов и при наложении бронхофиксатора.
При плевро-пульмональном шоке кривые венозного и артериального давлений во всех случаях были довольно однотипными. Сначала наблюдался резкий и стойкий подъем венозного давления при неизменном артериальном давлении, а затем через некоторый промежуток времени (5—10—15 минут) наступало падение артериального давления и клинически отмечался шок.
У наиболее тяжело больных констатировано параллельное падение и артериального и венозного давления. Эти данные заставляют думать, что, повидимому, в отдельных случаях можно, ориентируясь на изменение венозного давления, раньше диагносцировать шок с целью более своевременной его профилактики и лечения.
Что такое плевральный шок
Гемоторакс является одним из наиболее частых последствий травм грудной клетки. Раннее выявление и лечение гемоторакса имеет первостепенное значение для прогноза заболевания. Около 60 % политравм связаны с травмой грудной клетки. По данным ВОЗ ежегодно в мире в результате травм и других несчастных случаев (внешних причин) погибают более 5 миллионов человек. Причем следует отметить, что более 70 % смертности от внешних причин приходится на трудоспособный возраст. Четвертая часть смертей связана с травмой грудной клетки [1].
Цель исследования: определение основных понятий и современных принципов диагностики и лечения гемоторакса для улучшения результатов ведения пациентов с этой патологией.
Этиология. Причины гемоторакса обычно подразделяются на травматические и нетравматические. Травматический гемоторакс является результатом тупой или проникающей травмы. Нетравматический гемоторакс может развиваться при различных заболеваниях или расстройствах, таких как неоплазия, легочная секвестрация, разрыв плеврального сращения в случае пневмоторакса, легочный инфаркт, туберкулез, легочная инфекция (например, геморрагическая лихорадка денге), легочные артериовенозные фистулы и абдоминальные аномалии [2].
Патофизиология. Интраплевральные или экстраплевральные травмы способны привести к гемотораксу. Физиологический ответ на гемоторакс может проявляться в раннем или позднем вариантах. Ранний ответ возможен в двух основных аспектах: гемодинамическом и дыхательном. Поздний ответ проявляется в двух формах: эмпиема и фиброторакс.
Степень тяжести патофизиологического ответа зависит от места повреждения, функционального резерва пациента и объема кровопотери [1].
Гемодинамический ответ является многофакторным ответом и зависит от тяжести гемоторакса в соответствии с его классификацией. Гемоторакс классифицируется в зависимости от количества кровопотери: минимальная, умеренная и массивная.
Минимальный гемоторакс определяется как кровопотеря без значительных гемодинамических изменений. Так, например, кровопотеря до 750 мл у пациента с весом 75 кг обычно протекает без какого-либо значительного гемодинамического ответа и классифицируется как минимальный гемоторакс. Гемодинамический ответ часто корректируется в зависимости от количества кровопотери, основного заболевания и места повреждения.
Если у пациента в плевральной полости уже имеется спаечный процесс, спайки могут ограничивать количество кровопотери, особенно из источников низкого давления, и способны спасти жизнь.
Кровопотеря более 30 % объема крови (1500–2000 мл) обычно связана с геморрагическим шоком (массивным гемотораксом) [3].
Респираторный ответ. На респираторную реакцию влияют многочисленные факторы. Дыхательная недостаточность, связанная с травмой, может возникнуть прямо или косвенно.
Косвенными причинами дыхательной недостаточности являются легочная инфекция, фиброторакс как позднее осложнение и травмы у пациентов с основным заболеванием.
Дыхательная недостаточность, связанная непосредственно с травмой, возникает в результате прямого повреждения легких, грудной стенки и сердца или системного ответа в форме ОРДС в результате диффузного альвеолярного повреждения с увеличением проницаемости капилляров [4].
Физиологическое разрешение гемоторакса. Дефибринация гемоторакса начинается через несколько часов после его образования. Некоторая степень дефибринации гемоторакса приводит к неполному свертыванию. После того как произошел лизис гемоторакса путем воздействия плевральных ферментов, увеличивается концентрация белка. Внутриплевральное гиперосмотическое давление создает положительный осмотический градиент и способствует образованию плеврального выпота.
Таким образом, относительно небольшое количество крови в плевральной полости может создавать эффект, аналогичный влиянию хронических субдуральных гематом, с течением времени втягивая жидкости и вызывая большой выпот с небольшим фактическим содержанием крови [3].
Поздняя физиологическая системная реакция. К поздним физиологическим реакциям гемоторакса относятся эмпиема и фиброторакс.
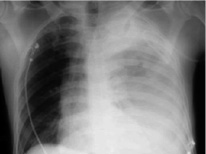
Первичное или вторичное инфицирование гемоторакса завершается эмпиемой. Бронхотрахеальные повреждения, травмы пищевода, диафрагмальные и субдиафрагмальные повреждения, скопление жидкости в субдиафрагмальной области и постхирургическое инфицирование способствуют развитию посттравматической эмпиемы (рис. 1) [5].
Рис. 1. Рентгенография грудной клетки; левосторонний гемоторакс после тупой травмы
Фиброторакс возникает в результате отложения фибрина на плевральных поверхностях. Недренируемая плевральная жидкость независимо от ее происхождения вызывает воспалительный ответ и приводит к воспалительному процессу на поверхности висцеральной и париетальной плевры. Стенки грудной клетки и диафрагма также поражаются аналогичным процессом, что в целом приводит и к поражению легочной ткани. Поражение легких ограничивает дыхательную функцию и, как правило, уменьшает объем легких [6].
Клинические проявления. При травмах грудной клетки клинические проявления зависят от механизма повреждения и перечня вовлеченных органов. Пациенты, перенесшие тупую травму грудной клетки, подвергаются значительному риску, который связан с характером травмы, осложнениями и смертностью [7]. В отличие от проникающей травмы грудной клетки биомеханическая сила, необходимая для получения значительного тупого повреждения грудной клетки, часто приводит к множественным травмам, включая травмы живота, головы и конечностей [8].
Тупые травмы грудной клетки. Тупые травмы грудной клетки могут вызывать гемоторакс, ушиб легкого, разрыв легочной артерии, травматическую легочную псевдокисту, легочную гематому, травматическую асфиксию и повреждения костного скелета. Множественные переломы ребер являются наиболее распространенными последствиями при тупых травмах грудной клетки и встречаются примерно в 36–50 % случаев (около 36 % с правой стороны и 51 % с левой стороны).
Небольшой гемоторакс может быть пропущен во время физического обследования и даже рентгенографии грудной клетки.
Повреждения грудной стенки подразделяются на простые и сложные.
Простые повреждения грудной стенки состоят из менее чем трех переломов ребер и поверхностных повреждений мягких тканей. Этот тип травмы обычно можно лечить консервативно.
Переломы трех или более ребер и флоттирующий перелом грудной клетки относятся к категории сложных повреждений грудной стенки и часто могут быть связаны со значительной степенью гемоторакса.
Гемоторакс может развиться через некоторое время после получения травмы. Возможным механизмом развития отсроченного гемоторакса является смещение сломанных ребер с разрывом паренхимы легких, повреждением диафрагмы или разрывом межреберных сосудов [1, 9].
Тупые внутригрудные травмы. Повреждения сосудов при тупых внутригрудных травмах обычно приводят к большим гемотораксам. Разрыв больших сосудов и травмы сердца могут привести к кровотечениям в плевральное пространство и последующей сосудистой ишемии. Реже при небольших сосудистых повреждениях могут возникать кровяные сгустки, которые способны остановить кровотечение.
В зависимости от характера и локализации повреждения меняется симптоматика, которая варьирует от менее тяжкой до тяжелой. Респираторные проявления, связанные с большим гемотораксом, а также тупость при перкуссии и отсутствие дыхательных шумов отмечаются как типичные признаки и симптомы при этой патологии [1, 4, 10].
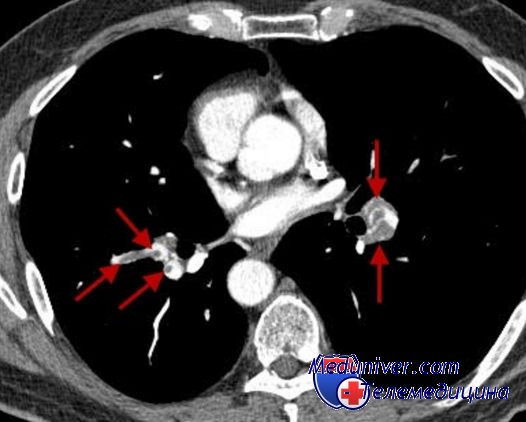
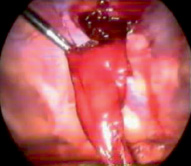
Проникающая травма. Наиболее распространенной причиной гемоторакса при проникающих ранениях является прямое повреждение сосудов грудной клетки. Также не следует упускать из виду и повреждения других внутригрудных структур, включая повреждения паренхимы сердца и легких. Травма паренхимы легких при проникающих ранениях грудной клетки очень распространена и обычно самоограничена, но эти повреждения обычно приводят к гемопневмотораксу (рис. 2) [11].
Рис. 2. Гемоторакс при проникающей травме. Рана, прикрытая сгустком, при удалении которого кровотечение возобновляется
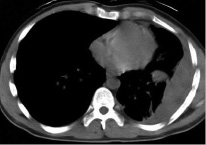
Клинические проявления при травматическом гемотораксе. В случае травмы грудной клетки следует провести тщательный и точный медицинский осмотр. Кровь в плевральной полости распространяется в положении лежа на спине и может быть легко пропущена во время физикального осмотра. Настоятельно рекомендуется также выполнять физикальное обследование пациента в вертикальном положении или в небольшом обратном положении Тренделенбурга, чтобы выявить меньшие гемотораксы. Менее 500 мл крови в костофреническом угле можно не заметить при физикальном обследовании (рис. 3).
Рис. 3. Левосторонний гемоторакс и ателектаз левой нижней доли
Гемоторакс также может возникнуть в результате внутрибрюшной травмы. Возможность повреждения органов брюшной полости, например селезенки, печени, желудка или сосудов, должна быть рассмотрена в каждом случае гемоторакса и особенно в случае встречающегося диафрагмального повреждения [12].
Лечебно-диагностическая система. Лечение гемоторакса подразделяется на периоды: в раннюю фазу (к примеру, при геморрагическом шоке, нарушениях дыхания или свернувшемся гемотораксе) и в позднюю фазу (при фибротораксе и эмпиеме плевры).
Шок. Этиология. Патогенез. Классификация
Острые кратковременные нарушения гемодинамики могут быть преходящим эпизодом при нарушении сосудистого тонуса, рефлекторно вызванного внезапной болью, испугом, видом крови, духотой или перегревом, а также при сердечной аритмии или ортостатической гипотензии на фоне анемии или гипотонии. Такой эпизод носит название коллапса и в большинстве случаев купируется самостоятельно без лечения. Из-за преходящего снижения кровоснабжения мозга может развиться обморок – кратковременная потеря сознания, которой часто предшествуют нейро-вегетативные симптомы: мышечная слабость, потливость, головокружение, тошнота, потемнение в глазах и шум в ушах. Характерны бледность, низкое АД, бради- или тахикардия. То же самое может развиться у здоровых людей при высокой температуре окружающей среды, поскольку тепловой стресс ведет к значительному расширению кожных сосудов и снижению диастолического АД. Более продолжительные расстройства гемодинамики всегда представляют опасность для организма.
Причины шока
Шок возникает при действии на организм сверхсильных раздражителей и может развиться при различных заболеваниях, повреждениях и патологических состояниях. В зависимости от причины различают геморрагический, травматический, ожоговый, кардиогенный, септический, анафилактический, гемотрансфузионный, нейрогенный и другие виды шока. Могут быть и смешанные формы шока, вызванные сочетанием нескольких причин. С учетом патогенеза происходящих в организме изменений и требующих определенных специфических лечебных мероприятий выделяют четыре основных вида шока
Гиповолемический шок возникает при значительном снижении ОЦК в результате массивного кровотечения или дегидратации и проявляется резким снижением венозного возврата крови к сердцу и выраженной периферической вазоконстрикцией.
Кардиогенный шок возникает при резком снижении сердечного выброса вследствие нарушения сократимости миокарда или острых морфологических изменениях клапанов сердца и межжелудочковой перегородки. Развивается при нормальном ОЦК и проявляется переполнением венозного русла и малого круга кровообращения.
Перераспределительный шок проявляется вазодилятацией, снижением общего периферического сопротивления, венозного возврата крови к сердцу и повышением проницаемости капиллярной стенки.
Экстракардиальный обструктивный шок возникает вследствие внезапного возникновения препятствия кровотоку. Сердечный выброс резко падает несмотря на номальные ОЦК, сократимость миокарда и тонус сосудов.
Патогенез шока
В основе шока лежат генерализованные нарушения перфузии, приводящие к гипоксии органов и тканей и расстройствам клеточного метаболизма (рис. 15. 2. ). Системные нарушения кровообращения являются следствием снижения сердечного выброса (СВ) и изменения сосудистого сопротивления.
Первичными физиологическими нарушениями, уменьшающими эффективную перфузию тканей служат гиповолемия, сердечная недостаточность, нарушение тонуса сосудов и обструкция крупных сосудов. При остром развитии этих состояний в организме развивается «медиаторная буря» с активацией нейро-гуморальных систем, выбросом в системную циркуляцию больших количеств гормонов и провоспалительных цитокинов, влияющих на сосудистый тонус, проницаемость сосудистой стенки и СВ. При этом резко нарушается перфузия органов и тканей. Острые расстройства гемодинамики тяжелой степени, независимо от причин, вызвавших их, приводят к однотипной патологической картине. Развиваются серьезные нарушения центральной гемодинамики, капиллярного кровообращения и критическое нарушение тканевой перфузии с тканевой гипоксией, повреждением клеток и органными дисфункциями.
Нарушения гемодинамики
В ответ на снижение АД усиливается активация адаптационных систем. Сначала происходит рефлекторная активация симпатической нервной системы, а затем усиливается и синтез катехоламинов в надпочечниках. Содержание норадреналина в плазме возрастает в 5-10 раз, а уровень адреналина повышается в 50-100 раз. Это усиливает сократительную функцию миокарда, учащает сердечную деятельность и вызывает селективное сужение периферического и висцерального венозного и артериального русла. Последующая активация ренин-ангиотензинового механизма приводит к еще более выраженной вазоконстрикции и выбросу альдостерона, задерживающего соль и воду. Выделение антидиуретического гормона уменьшает объем мочи и увеличивает ее концентрацию.
Сужение сосудов сердца и мозга происходит гораздо в меньшей степени по сравнению с другими зонами, и эти органы дольше других обеспечиваются кровью за счет резкого ограничения кровоснабжения других органов и тканей. Уровни метаболизма сердца и мозга высоки, а их запасы энергетических субстратов крайне низки, поэтому эти органы не переносят длительную ишемию. На обеспечение немедленных потребностей жизненно важных органов — мозга и сердца и направлена в первую очередь нейроэндокринная компенсации пациента при шоке. Достаточный кровоток в этих органах поддерживается дополнительными ауторегуляторными механизмами, до тех пор, пока артериальное давление превышает 70 мм рт. ст.
Централизация кровообращения – биологически целесообразная компенсаторная реакция. В начальный период она спасает жизнь больному. Важно помнить, что первоначальные шоковые реакции – это реакции адаптации организма, направленные на выживание в критических условиях, но переходя определенный предел, они начинают носить патологический характер, приводя к необратимым повреждениям тканей и органов. Централизация кровообращения, сохраняющаяся в течение нескольких часов, наряду с защитой мозга и сердца таит в себе смертельную опасность, хотя и более отдаленную. Эта опасность заключается в ухудшении микроциркуляции, гипоксии и нарушении метаболизма в органах и тканях.
Коррекция нарушений центральной гемодинамики при шоке включает в себя интенсивную инфузионную терапию, направленную на увеличение ОЦК, использование препаратов влияющих на тонус сосудов и сократительную способность миокарда. Лишь при кардиогенном шоке массивная инфузионная терапия противопоказана.
Нарушения микроциркуляции и перфузии тканей
Микроциркуляторное русло (артериолы, капилляры и венулы) является самым важным звеном системы кровообращения в патофизиологии шока. Именно на этом уровне происходит доставка к органам и тканям питательных веществ и кислорода, а также происходит удаление продуктов метаболизма.
Развивающийся спазм артериол и прекапиллярных сфинктеров при шоке приводит к значительному уменьшению количества функционирующих капилляров и замедлению скорости кровотока в перфузируемых капиллярах, ишемии и гипоксии тканей. Дальнейшее ухудшение перфузии тканей может быть связано с вторичной капиллярной патологией. Накопление ионов водорода, лактата и других продуктов анаэробного обмена веществ приводит к снижению тонуса артериол и прекапиллярных сфинктеров и еще большему снижению системного АД. При этом венулы остаются суженными. В данных условиях капилляры переполняются кровью, а альбумин и жидкая часть крови интенсивно покидают сосудистое русло через поры в стенках капилляров («синдром капиллярной утечки»). Сгущение крови в микроциркуляторном русле приводит к возрастанию вязкости крови, при этом увеличивается адгезия активированных лейкоцитов к эндотелиальным клеткам, эритроциты и другие форменные элементы крови слипаются между собой и образуют крупные агрегаты, своеобразные пробки, которые еще больше ухудшают микроциркуляцию вплоть до развития сладж-синдрома.
Сосуды, блокированные скоплением форменных элементов крови, выключаются из кровотока. Развивается так называемое “патологическое депонирование”, которое еще больше снижает ОЦК и ее кислородную емкость и уменьшает венозный возврат крови к сердцу и как следствие вызывает падение СВ и дальнейшее ухудшение перфузии тканей. Ацидоз, кроме того, снижает чувствительность сосудов к катехоламинам, препятствуя их сосудосуживающему действию и приводит к атонии венул. Таким образом, замыкается порочный круг. Изменение соотношения тонуса прекапиллярных сфинктеров и венул считается решающим фактором в развитии необратимой фазы шока.
Неизбежным следствием замедления капиллярного кровотока является развитие и гиперкоагуляционного синдрома. Это приводит к диссеминированному внутрисосудистому тромбообразованию, что не только усиливает расстройства капиллярного кровоообращения, но и вызывает развитие фокальных некрозов и полиорганной недостаточности.
Ишемическое поражение жизненно важных тканей последовательно приводит к вторичным повреждениям, которые поддерживают и усугубляют шоковое состояние. Возникающий порочный круг способен привести к фатальному исходу.
Нарушения метаболизма
В условиях пониженной перфузии капиллярного русла не обеспечивается адекватная доставка питательных веществ к тканям, что приводит к нарушению метаболизма, дисфункции клеточных мембран и повреждению клеток. Нарушаются углеводный, белковый, жировой обмен, резко угнетается утилизация нормальных источников энергии – глюкозы и жирных кислот. При этом возникает резко выраженный катаболизм мышечного белка.
Развивающееся при шоке повышение в плазме уровня адреналина, кортизола, глюкагона и подавление секреции инсулина воздействуют на обмен веществ в клетке изменениями в использовании субстратов и белковом синтезе. Эти эффекты включают увеличенный уровень метаболизма, усиление гликогенолиза и глюконеогенеза. Уменьшение утилизации глюкозы тканями почти всегда сопровождается гипергликемией. В свою очередь гипергликемия может приводить к снижению кислородного транспорта, нарушению водно-электролитного гомеостаза и гликозилированию белковых молекул со снижением их функциональной активности. Значимое дополнительное повреждающее воздействие стрессорной гипергликемии при шоке способствует углублению органной дисфункции и требует своевременной коррекции с поддержанием нормогликемии.
На фоне нарастающей гипоксии нарушаются процессы окисления в тканях, их метаболизм протекает по анаэробному пути. При этом в значительном количестве образуются кислые продукты обмена веществ, и развивается метаболический ацидоз. Критерием метаболической дисфункции служат уровень рН крови ниже 7, 3, дефицит оснований, превышающий 5, 0 мЭкв/л и повышение концентрации молочной кислоты в крови свыше 2 мЭкв/л.
Важная роль в патогенезе шока принадлежит нарушению обмена кальция, который интенсивно проникает в цитоплазму клеток. Повышенный внутриклеточный уровень кальция увеличивает воспалительный ответ, приводя к интенсивному синтезу мощных медиаторов системной воспалительной реакции (СВР). Воспалительные медиаторы играют значительную роль в клинических проявлениях и прогрессировании шока, а также и в развитии последующих осложнений. Повышенное образование и системное распространение этих медиаторов могут приводить к необратимым повреждениям клеток и высокой летальности. Использование блокаторов кальциевого канала повышает выживаемость пациентов с различными видами шока.
Действие провоспалительных цитокинов сопровождается высвобождением лизосомальных ферментов и свободных перекисных радикалов, которые вызывают дальнейшие повреждения — «синдром больной клетки». Гипергликемия и повышение концентрации растворимых продуктов гликолиза, липолиза и протеолиза приводят к развитию гиперосмолярности интерстициальной жидкости, что вызывает переход внутриклеточной жидкости в интерстициальное пространство, обезвоживание клеток и дальнейшее ухудшение их функционирования. Таким образом, дисфункция клеточной мембраны может представлять общий патофизиологический путь различных причин шока. И хотя точные механизмы дисфункции клеточной мембраны неясны, лучший способ устранения метаболических нарушений и предотвращения необратимости шока – быстрое восстановление ОЦК.
В развитии этих изменений ведущая роль принадлежит фактору некроза опухоли (ФНО), интерлекинам (ИЛ-1, ИЛ-6, ИЛ-8), фактору активации тромбоцитов (ФАТ), лейкотриенам (В4, С4, D4, E4), тромбоксану А2, простагландинам (Е2, Е12), простациклину, гамма-интерферону. Одновременное и разнонаправленное действие этиологических факторов и активированных медиаторов при шоке приводит к повреждению эндотелия, нарушению сосудистого тонуса, проницаемости сосудов и дисфункции органов.
Таким образом, в основе патогенеза шока лежат глубокие и прогрессирующие расстройства гемодинамики, транспорта кислорода, гуморальной регуляции и метаболизма. Взаимосвязь этих нарушений может привести к формированию порочного круга с полным истощением адаптационных возможностей организма. Предотвращение развития этого порочного круга и восстановление ауторегуляторных механизмов организма и является основной задачей интенсивной терапии больных с шоком.
Стадии шока
Шок представляет собой динамический процесс, начинающийся с момента действия фактора агрессии, который приводит к системному нарушению кровообращения, и при прогрессировании нарушений заканчивающийся необратимыми повреждениями органов и смертью больного. Эффективность компенсаторных механизмов, степень клинических проявлений и обратимость возникающих изменений позволяют выделить в развитии шока ряд последовательных стадий.
Стадия прешока
Шоку обычно предшествует умеренное снижение систолического АД, не превышающее 20 мм рт. ст. от нормы (или 40 мм рт. ст. при наличии у больного артериальной гипертензии), которое стимулирует барорецепторы каротидного синуса и дуги аорты и активирует компенсаторные механизмы системы кровообращения. Перфузия тканей существенно не страдает и клеточный метаболизм остается аэробным. Если при этом прекращается воздействие фактора агрессии, то компенсаторные механизмы могут восстановить гомеостаз без каких-либо лечебных мероприятий.
Ранняя (обратимая) стадия шока
Промежуточная (прогрессивная) стадия шока
Это жизнеугрожающая критическая ситуация с уровнем систолического АД ниже 80 мм рт. ст. и выраженными, но обратимыми нарушениями функций органов при немедленном интенсивном лечении. При этом требуется проведение искусственной вентиляции легких (ИВЛ) и использование адренергических лекарственных средств для коррекции нарушений гемодинамики и устранения гипоксии органов. Длительная глубокая гипотензия приводит к генерализованной клеточной гипоксии и критическому нарушению биохимических процессов, которые быстро становятся необратимыми. Именно от эффективности терапии в течение первого так называемого «золотого часа» зависит жизнь больного.
Рефрактерная (необратимая) стадия шока
Для этой стадии характерны выраженные расстройства центральной и периферической гемодинамики, гибель клеток и полиорганная недостаточность. Интенсивная терапия неэффективна, даже если устранены этиологические причины и временно повышалось АД. Прогрессирующая полиорганная дисфункция обычно ведет к необратимому повреждению органов и смерти.
Диагностические исследования и мониторинг при шоке
Диагностические исследования при шоке включают также клинический анализ крови, определение содержания электролитов, креатинина, показателей свертываемости крови, группы крови и резус-фактора, газов артериальной крови, электрокардиографию, эхокардиографию, рентгенографию грудной клетки. Только тщательно собранные и корректно интерпретированные данные помогают принимать правильные решения.
Центральное венозное давление
Низкое ЦВД является косвенным критерием абсолютной или косвенной гиповолемии, а его подъем выше 12 см вод. ст. указывает на сердечную недостаточность. Измерение ЦВД с оценкой его ответа на малую нагрузку жидкостью помогает выбрать режим инфузионной терапии и определить целесообразность инотропной поддержки. Первоначально больному в течение 10 минут вводят тест-дозу жидкости: 200 мл при исходном ЦВД ниже 8 см водн. ст. ; 100 мл – при ЦВД в пределах 8-10 см водн. ст. ; 50 мл – при ЦВД выше 10 см водн. ст. Реакцию оценивают, исходя из правила «5 и 2 см водн. ст. »: если ЦВД увеличилось более чем на 5 см, инфузию прекращают и решают вопрос о целесообразности инотропной поддержки, поскольку такое повышение свидетельствует о срыве механизма регуляции сократимости Франка-Старлинга и указывает на сердечную недостаточность. Если повышение ЦВД меньше 2 см вод. ст. – это указывает на гиповолемию и является показанием для дальнейшей интенсивной инфузионной терапии без необходимости инотропной терапии. Увеличение ЦВД в интервале 2 и 5 см водн. ст. требует дальнейшего проведения инфузионной терапии под контролем показателей гемодинамики.
Мониторинг гемодинамики в малом круге кровообращения
Инвазивный мониторинг кровообращения в малом круге производят с помощью катетера, установленного в легочной артерии. С этой целью обычно используют катетер с плавающим баллончиком на конце (Swan-Gans), который позволяет измерить ряд параметров:
Определение этих параметров значительно расширяют возможности мониторинга и оценки эффективности гемодинамической терапии. Получаемые при этом показатели позволяют:
Снижение насыщения кислородом смешанной венозной крови всегда является ранним показателем неадекватности сердечного выброса.
Диурез