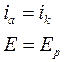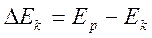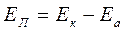Поляризация электродов и ее причины
|
В условиях, когда элемент не подключен к внешнему источнику напряжения (в.и.н.) и через электроды не протекает электрический ток, на границе электрод/раствор существует электрохимическое равновесие (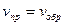
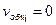
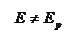
Отклонение электродного потенциала от равновесного значения при прохождении тока через электрод называется поляризацией.
Величина поляризации является мерой необратимости электродных процессов. Чем больше поляризация, тем более необратимый процесс.
Существует анодная и катодная поляризация.
Анодная поляризация определяется как разность между потенциалом электрода-анода, через который протекает ток, и равновесным потенциалом Ер, т. е.
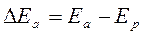
где Еа – потенциал заполяризованного электрода (анода). Анодная поляризация приводит к сдвигу потенциала электрода в сторону более положительных значений (+ΔЕа).
Катодная поляризация – это разность между равновесным потенциалом и потенциалом катода, через который протекает ток:
где Еk – потенциал заполяризованного катода. Величина катодной поляризации приводит к сдвигу потенциала электрода в сторону более отрицательных значений (-ΔЕа).
Функциональная зависимость между ∆Е и i называется поляризационной кривой. Различают соответственно катодную и анодную поляризационную кривую. Рассмотрим примеркатодной поляризационной кривой
Разность между потенциалами заполяризованных электродов дает э.д.с. поляризации:
Э.д.с. поляризации – это то избыточное напряжение, которое необходимо приложить к элементу сверх его э.д.с., чтобы начался процесс электролиза.
Таким образом, чем больше поляризация, тем больше напряжения нужно подать от в.и. на элемент для начала электролиза, что приводит к непродуктивному расходу электричества. Поэтому поляризация является негативным явлением, ее нужно либо минимизировать, либо устранять.
Для этого необходимо знать причину поляризации электродов.
Общей причиной поляризации электродов является замедленность протекания одной из стадий электродного процесса.
Если сдвиг электродного потенциала от равновесного значения при протекании тока обусловлен замедленностью собственно электрохимической реакцией (стадия 2), то такая поляризация называется электрохимической или просто перенапряжением. Изучается в области электрохимической кинетики (см. рис.). Если же поляризация обусловлена замедленностью стадии диффузии (стадия 1, 3), то она называется концентрационной и изучается в разделе диффузионной кинетики электродных процессов (см. рис.).
Таким образом, устранить или уменьшить поляризацию можно путем ускорения самой медленной стадии электрохимического процесса. Концентрационная поляризация устраняется путем усиления перемешивания раствора электролита, что значительно ускоряет диффузию. Электрохимическую поляризацию устранить крайне сложно, т. к. ускорить собственно электрохимическую реакцию можно, если изменить природу электрода, соответственно раствора электролита, плотность тока и т. д. То есть скорость электрохимической реакции зависит от множества факторов.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Поляризация электродов
Семестр. Лекция 8
Химические источники тока нашли еще более широкое применение, если бы удалось преодолеть их главный недостаток – нестабильность во времени значений потенциалов электродов. Состояние равновесия возможно только при отсутствии тока в цепи. В зависимости от величины тока эти потенциалы «съезжают» от своих исходных равновесных значений.
Смещение потенциала электрода от исходного равновесного или стационарного значения называется поляризацией электрода.Изменение во времени потенциала анода – анодная поляризация (Δεа). При этом потенциал анода смещается в положительную сторону от исходного значения. Потенциал катода вследствие катодной поляризации (Δεк)смещается в отрицательную сторону от своего начального значения. Потенциалы электродов сближают значения разность потенциалов (э.д.с.) снижается и в конечном счете стремится к нулю:
При Е =0 происходит прекращение работы гальванического элемента, это состояние полной поляризации.
Основных причин нестабильности значений потенциалов две. Первая связана с медленным протеканием процессов диффузии ионов в растворе электролита – это так называемая концентрационная поляризация. Вторая причина химическая, это замедление работы из-за кинетических проблем у самой электродной реакции окисления или восстановления. Такую поляризацию называют электрохимической или перенапряжением (η).
Выше на рис.6.4 изображен двойной электрический слой на цинковом электроде (аноде). Хорошо видно, что катионы цинка притягиваются к отрицательно заряженной поверхности цинка и «зависают» на ней, мешают следующим катионам выходить из металла в раствор и диффундировать по всему объему электролита. Катионы цинка на поверхности электрода гасят его отрицательный заряд, и тем самым потенциал смещается в положительную сторону. На катоде все наоборот. Катионы металла из объема раствора должны диффундировать к поверхности катода и восстанавливаться на ней. Эта диффузия не может протекать достаточно быстро, подвижность катионов металлов (см. рис.3.1) в растворе ограничена из-за большой гидратной «шубы», они не успевают подходить к поверхности катода в требуемом количестве, а потенциал смещается в отрицательную сторону.
Для снижения последствий концентрационной поляризации необходимо «заставить» ионы перемещаться быстрее, для этого раствор можно нагреть или перемешивать. Известно, что для восстановления работы сухого элемента требуется постучать по нему. Происходит смещение, частичное перемешивание электролита, поляризация устраняется, хотя и не надолго. Надежность работы батарейки определяется величиной тока. Чем меньше ток, тем поляризация меньше и элемент работает дольше (аккумулятор телефона в режиме ожидания). При увеличении силы тока электроды поляризуются очень сильно. Все основные усилия компаний-производителей химических источников тока направлены на решение проблемы снижения поляризуемости электродов, здесь все имеет значение – состояние поверхности электрода, его форма, состав электролита и т.д.
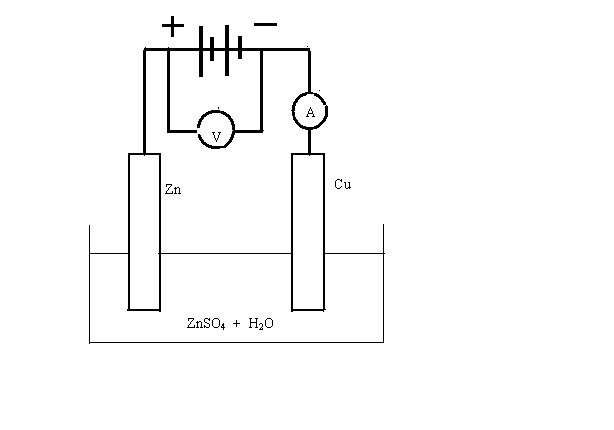
Представим себе теперь противоположный случай двухэлектродной системы, в которой под действием электрической энергии в растворе или расплаве электролита происходят окислительно-восстановительные реакции – процессы электролиза. Если воспользоваться сетью переменного тока, электроэнергия превращается только в тепло. Для электролиза необходим источник постоянного тока. Кроме того, нужна ванна с электролитом, называемая электролизером и два электрода. Важно то, из какого материала изготавливается анод. На аноде (при электролизе это положительно заряженный электрод) протекает процесс окисления. Большинство металлических материалов окисляются под действие электрического тока, материал катода особого значения не имеет. На этом электроде происходит реакция восстановления и необходимо лишь его способность проводить ток. Например, рассмотрим процесс электролиза раствора сернокислого цинка. В качестве анода используем металлический цинк, а в роли катода – медную пластину. Схема установки представлена на рис.8.1.
Рис.8.1 Электролиз раствора сульфата цинка
Под действие электрического тока на цинковом аноде начнется реакция его окисления, материал анода растворяется. Такие аноды так и называют растворимыми:
Катионы цинка, имеющиеся в растворе при диссоциации сульфата, диффундируют к поверхности отрицательно заряженного катода и восстанавливаются на нем:
(─)Zn 2+ +2e ↔ Zn ↓.
На поверхности меди образуется слой металлического цинка. Процесс называют гальваническим цинкованием, так на металл можно нанести слой или слои других металлов с целью защиты от коррозии или для улучшения внешнего вида изделия. Процесс используется также на предприятиях цветной металлургии. В результате металлургических операций полученные металлические медь, никель, кобальт загрязнены другими металлами, серой. Окончательная очистка проводится в цехах электролиза. Изделия погружаются в ванны и выполняют роль растворимого анода, на катоде осаждается только нужный чистый металл. Электролитической очисткой получают катодную медь, никель, кобальт.
Как и в гальваническом элементе, электроды при электролизе поляризуются. Потенциал анода во времени растет (а он заряжен положительно), потенциал катода снижается (этот электрод заряжен отрицательно). Минимальная разность потенциалов внешнего источника тока, при которой начинается процесс электролиза, называется потенциалом разложения электролита. Процесс начинается, но в результате поляризации разность потенциалов становится больше, и процесс останавливается, необходимо увеличивать разность потенциалов, но в конечном счете опять произойдет остановка. Результат – перерасход электроэнергии. Для снижения концентрационной поляризации электролит в ваннах нагревают практически до кипения (!). Соли тяжелых металлов механически в больших количествах попадают в атмосферу цеха электролиза. Это одно из самых вредных производств.

Электролиз проводят и в расплаве электролита, например при получении металлического алюминия. В этом случае ванна – это высокотемпературная печь для получения расплава. Допустим, в электролизер загружен расплав хлорида никеля, а в качестве анода использован графит, инертный по отношению к окислению электрическим током материал. Такой процесс называют электролизом с нерастворимым (инертным) анодом. На поверхности графита будет окисляться анион хлора, имеющийся в расплаве при диссоциации соли. Катион никеля будет восстанавливаться на катоде:
(+)2CI ─ ─ 2e ↔ CI2 ↑
(─)Ni 2+ + 2e ↔ Ni ↓.
Случай электролиза раствора сложнее в сравнении с расплавом, потому что электролизу может подвергаться и сама вода. Под действием электрического тока она разлагается на газообразные водород и кислород. Обсудим все возможные конкурирующие процессы при электролизе растворов электролитов.
1. Анодные процессы.
1.1 Анод растворимый. Материал анода М= Mg, AI, Zn, Fe, Mn, Cr, Sn и др.:
1.2 Анод инертный (графит, Pt, Ti, Nb).
(+)2CI ─ ─ 2e ↔ CI2 ↑
(+)2Br ─ ─ 2e ↔ Br2
(+)S 2─ ─ 2e ↔ S↓.
(+)2H2O ─ 4e ↔ O2↑ + 4H + при рН ≤ 7
(+)4OH ─ ─ 4e ↔ O2↑ + 2H2O при рН > 7.
2. Катодные процессы.
На этом электроде конкурируют два процесса восстановления:
(─)M n+ + ne ↔ M↓.
(─)2H + + 2e ↔ H2↑.
Чем больше электродный потенциал, тем легче происходит восстановление на катоде. Получается, что электролизом можно получить только металлы с положительными значениями стандартных электродных потенциалов, так как у водорода ε о Н2 = 0 (см. табл.6.1). на самом деле восстанавливаются катионы свинца, олова, никеля, железа, цинка, и только в случае очень активных металлов на катоде выделяется водород. Рассмотрим механизм реакции восстановления водорода на катоде:
Эта, казалось бы, простая реакция протекает совсем не просто, у нее пятистадийный механизм:
а) диффузия гидратированных ионов водорода к поверхности электрода из объема электролита;
б) стадия дегидратации Н3О + → Н + + Н2О;
в) стадия разряда H + + e → H;
г) стадия рекомбинации (образования молекул) H + H → H2;
д) стадия образования пузырьков газообразного водорода, покидающих его поверхность – H2↑. Только теперь можно считать процесс законченным.
Следствием такого сложного механизма является торможение процесса в целом, его невозможности протекать быстро и гладко без препятствий, иными словами речь идет о катодной электрохимической поляризации. В электрохимии создано две основных теории водородного перенапряжения. В теории замедленного разряда предполагается, что лимитирующей стадией процесса является стадия «в», а в теории замедленной рекомбинации – стадия «г». Вывод этих теорий по величине перенапряжения совпадает: ηH2 = 1,7В. От величины равновесного (стандартного) потенциала водорода нужно сместиться в отрицательную сторону (процесс катодный) на величину 1,7В (см. табл.6.1). Попадаем на алюминий. С учетом перенапряжения реакции восстановления водорода на катоде он оказывается на месте алюминия, совсем в другой области ряда напряжений. У всех металлов, расположенных в ряду ниже алюминия, потенциал оказывается больше, чем у водорода. Такие металлы и восстанавливаются на катоде:
(─)M n + + ne ↔ M↓. при условии ε о м > ε о AI
(─)2H + + 2e ↔ H2↑ при условии ε о м ≤ ε о AI и при рН ─ при pH ≥ 7.
Продемонстрируем общие закономерности на некоторых примерах.
Электролизу подвергается водный раствор йодистой меди CuI2. Анод инертный (по умолчанию).
Ион иода может окисляться, а ион меди легко восстанавливаться, так как ε о Cu > ε о AI.
(+)2I ─ ─ 2e ↔ I2↓.
(─)Cu 2 + + 2e ↔ Cu↓.
Пропускаем электрический ток через раствор фосфата калия K3PO4. Фосфат-ион не окисляется, а катион калия не восстанавливается. Имеет место электролиз воды. Сама вода практически не пропускает электрический ток, поэтому для ее электролиза делают добавки нейтрального по отношению к этому процессу электролита, который сам не подвергается электролизу:
Имеем раствор бромистоводородной кислоты HBr:
(+)2Br ─ ─ 2e ↔ Br2
(─)2H + + 2e ↔ H2↑.
Проводим электролиз раствора гидроксида натрия:
(+)4OH ─ ─ 4e ↔ O2↑ + 2H2O
Вместо раствора используем расплавленный гидроксид. Температура расплава выше 100 о С, вода улетает из электролизера в виде пара, на катоде образуется металлический натрий. Именно так и получают все активные щелочные, щелочноземельные металлы и алюминий:
(+)4OH ─ ─ 4e ↔ O2↑ + 2H2O↑
(─)Na + + e ↔ Na.
Для количественного расчета продуктов электролиза используют классический закон Фарадея: одинаковые количества электричества выделяют на электродах при электролизе эквивалентные массы различных веществ.
Один Фарадей электричества выделяет один эквивалент любого вещества. 1F = 96500 Кл (А•с) = 26,8 А•час. Примеры определения эквивалентной массы элементов приведены в лекции 5. Для цинка это (65/2) г/моль, алюминия (27/3) г/моль и т.д. Газы принято измерять в виде объема, а не массы. Для водорода эквивалентная масса 1г/моль, который при нормальных условиях занимает объем 11,2л. Для кислорода 8г/моль или 5,6л. Закон Фарадея можно записать в виде:
uде I – ток,А; t – время электролиза, с,ч; F – число Фарадея, m – масса продукта, г или V – его объем, л.
Электрохимическая поляризация. Перенапряжение



Когда электрод находится при потенциале, равном равновесному, на нем уста-навливается электрохимическое равновесие:
При смещении потенциала электрода в положительную или в отрицательную сторону на нем начинают протекать процессы окисления или восстановления. Отклонение потенциала электрода от его равновесного значения называется электрохимической поляризацией или просто поляризацией.

Рассмотрим простой пример поляризации. Пусть медный электрод находится в 0,1 M растворе CuSO4, не содержащем никаких примесей, в том числе рас-творенного кислорода. Пока цепь не замкнута, потенциал электрода при 25 0 C будет иметь равновесное значение, равное
Подключим электрод κ отрицательному полюсу источника тока — сделаем его катодом. Избыток электронов, который появится теперь на электроде, сдви-нет потенциал электрода в отрицательную сторону и одновременно нарушит равновесие. Электроны будут притягивать катионы меди из раствора — пойдет процесс восстановления:
Если подключить электрод не κ отрицательному, а κ положительному полюсу источника тока — сделать его анодом, то вследствие удаления части электронов потенциал электрода сместится в положительную сторону и равновесие также нарушится. Ho теперь на электроде будет протекать процесс окисления, так как в ходе этого процесса высвобождаются электроны:
Таким образом, поляризация электрода в отрицательную сторону связана с протеканием процесса восстановления, а поляризация в положительную сторо-ну — с протеканием процесса окисления. Процесс восстановления иначе назы-вают катодным процессом, а процесс окисления — анодным. B связи с этим поляризация в отрицательную сторону называется катодной поляризацией, а в положительную — анодной.
Другой способ поляризации электрода — это контакт его с электрохими-ческой системой, электродный потенциал которой имеет более положительное или более отрицательное значение, чем потенциал рассматриваемого электрода.
Рассмотрим работу медно-цинкового гальванического элемента. При разом-кнутой цепи как на медном, так и на цинковом электродах устанавливаются электрохимические равновесия. Ho электродные потенциалы, отвечающие этим равновесиям, различны. B случае 0,1 M растворов они равны:
При замыкании цепи оба электрода оказывают друг на друга поляризующее действие: потенциал медного электрода под влиянием контакта с цинком сдвига-ется в отрицательную сторону, а потенциал цинкового электрода под влиянием контакта с медью — в положительную. Иначе говоря, медный электрод поля-ризуется катодно, а цинковый — анодно. Одновременно на обоих электродах нарушаются электрохимические равновесия и начинают протекать электрохи-мические процессы: катодный процесс на медном электроде и анодный — на цинковом:
Протекание электродного процесса сопровождается изменением концентрации ионов электролита, участвующих в процессах электрохимического окисления или восстановления. Если ионы образуются в ходе электродного процесса, то их концентрация в приповерхностном слое электрода увеличивается, если они расходуются, то — уменыпается. Тогда, например, при восстановлении ионов металла Ме п+ и уменьшении их концентрации, произойдет сдвиг электродно-го потенциала катода в область меньших значений. Это следует из уравнения Нернста:
Аналогично, для анода произойдет сдвиг потенциала в область более высоких значений, так как прианодное пространство обогащается ионами. B результате напряжение гальванического элемента уменьшится и тем сильнее, чем больше величина тока. A при электролизе понадобится большая разность потенциалов, чем в условиях идеального перемешивания раствора. Такой вид поляризации электродов носит название концентрационной поляризации.

Если в электродном процессе получаются газы, то возможен другой вид по-ляризации — газовая. Газовая поляризация связана с тем, что образующиеся газы адсорбируются поверхностью электрода и, тем самым, препятствуют досту-пу новых ионов κ электроду. Разрядка ионов затрудняется. Ha катоде газовая поляризация обычно возникает при адсорбции выделяющегося водорода, а на аноде такая газовая «шуба» возникает при адсорбции получающегося кислоро-да. Для ослабления газовой поляризации электродов в электролит вводят спе-циальные вещества — деполяризаторы. B качестве деполяризаторов на катоде используют такие сильные окислители как К2Сr2О7, КМпО4, MnO2, окисляю-щие водород в момент появления, а на аноде — восстановители типа Na2SO3, NазРОз, переводящие кислород в восстановленную форму, хорошо растворяю-щуюся в растворе электролита.
При прохождении электрического тока и при взаимодействии с раствором электролита, материал поверхности электрода может образовывать различные химические соединения. Ha поверхностях металлических электродов образуют-ся соединения металла в различных степенях окисления с различной раство-римостью в растворе электролита. Если эти вещества — малорастворимы, то, находясь на поверхности электрода, они оказывают дополнительное сопротивле-ние протеканию электродного процесса. B пределыюм случае может возникнуть даже полная пассивация электрода. Такой вид поляризации, связанный с обра-зованием на поверхности электрода новых химических соединений, называется химической поляризацией.
Поляризация электрода — необходимое условие протекания электродного процесса. Рассмотрим катодное восстановление ионов водорода. Если катод из-готовлен из платины, то для выделения водорода с заданной скоростью необ-ходима определенная величина катодной поляризации. При замене платинового электрода на серебряный (при неизменных прочих условиях) для получения водорода с прежней скоростью понадобится большая поляризация. При заме-не катода на свинцовый поляризация потребуется еще болыиая. Следовательно, различные металлы обладают различной каталитической активностью по от-ношению κ процессу восстановления ионов водорода. Величина поляризации, необходимая для протекания данного электродного процесса с определенной скоростью, называется перенапряжением данного электродного процесса. Ta-ким образом, перенапряжение выделения водорода на различных металлах раз-лично.
B табл. 9.3 приведены для 1 н растворов величины катодной поляризации, которую необходимо осуществить на электроде для выделения на нем водорода со скоростью 0,1 мл в минуту с 1 см 2 рабочей поверхности электрода.
Таблица 9.3. Перенапряжение выделения водорода на различных метпаллах
| Металл электрода | Электролит | Перенапряже-ние выделения водорода, B | Металл электрода | Электролит | Перенапряже-ние выделения водорода, B |
| Железо Медь Серебро | HCl H2SO4 HCl | 0,5 0,6 0,7 | Цинк Ртуть Свинец | H2SO4 H2SO4 H2SO4 | 1,0 1,2 1,3 |
Выяснение связи между величиной поляризации и скоростью электродного процес-са является важнейшим методом изучения электрохимических процессов. При этом результаты измерений обычно представляют в виде поляризационных кривых — кри-вых зависимости плотности тока на электроде от величины поляризации. Вид по-ляризационной кривой того или иного электродного процесса отражает особенности его протекания. Методом поляризационных кривых изучают кинетику и механизм окислительно-восстановнтельных реакций, работу гальванических элементов, явления коррозии и пассивности металлов, различные случаи электролиза.