Ревматизм
Терминология
Ревматизм относится к числу тех заболеваний, о которых все знают или, как минимум, слышали. Однако бытующие представления о ревматизме варьируют весьма широко: от вынесенного из детства страха перед кедами («Нельзя постоянно в них ходить – простудишься и заболеешь ревматизмом!») и до более взрослого открытия: оказывается, ревматизмом болеют не ноги, а сердце. Внимательное изучение доступных источников порой только запутывает ситуацию. В самом деле, как понять такую болезнь, при которой страдает не отдельный орган и даже не функциональная система, а целый тип ткани в организме. Тем не менее, именно это и происходит при ревматизме.
Ревматизм — воспалительно-иммунное поражение соединительной ткани, которая в организме присутствует практически повсюду.
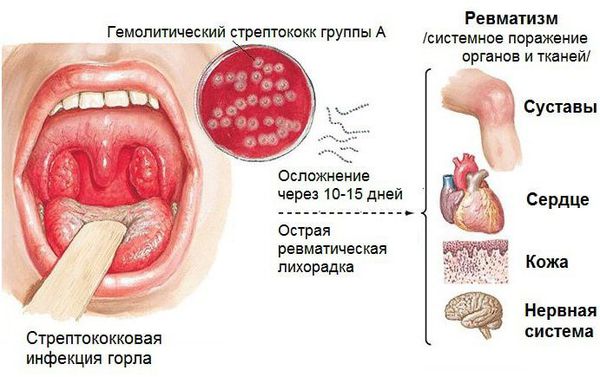
Страдают, как правило, соединительнотканные структуры сердца, суставов, сосудов, подкожных слоев. Значительно реже (1-6 процентов в общем объеме регистрируемого ревматизма) встречаются ревматические поражения центральной нервной системы, органов дыхания и зрения, желудочно-кишечного тракта.
Какой-либо эндемичности (региональной зависимости эпидемиологических показателей) ревматизм не обнаруживает: болеют везде. Однако есть четкая зависимость заболеваемости от возраста, – среди первичных пациентов преобладает категория 5-15 лет, – а также обратная корреляция с уровнем жизни населения. Учитывая, что большинство детей на земном шаре (до 80%) живут в т.н. развивающихся странах, не приходится удивляться широкому распространению ревматизма именно в «третьем мире».
В последние четверть века заболеваемость и летальность в России снизились более чем втрое. Однако, если речь идет о столь тяжелом заболевании, да еще и с преимущественно ранней манифестацией, никакие эпидемиологические данные нельзя считать «удовлетворительными», кроме нулевых. На сегодняшний же день статистика противоречива и носит, в основном, оценочный характер (причем это касается не только РФ): как правило, данные 1960‑90‑ых годов экстраполируются на нынешнюю ситуацию. Более-менее достоверной оценкой заболеваемости среди российских детей можно считать частоту на уровне 2-3 случая на 10 000 (и свыше 1,5% всех пороков сердца являются ревматическими); для сравнения, в странах третьего мира этот показатель варьирует от 60 до 220 на 10 000.
В заключение краткого общего обзора следует отметить, что сам термин «ревматизм» в настоящее время употребляется, главным образом, русскоязычной медициной. В официальном международном лексиконе это «Острая ревматическая лихорадка», «Ревматические болезни сердца», «Ревматоидный артрит» и т.п.; впрочем, шифром М79.0 (рубрика «Болезни костно-мышечной системы и соединительной ткани») в МКБ‑10 обозначается «Ревматизм неуточненный».
Причины
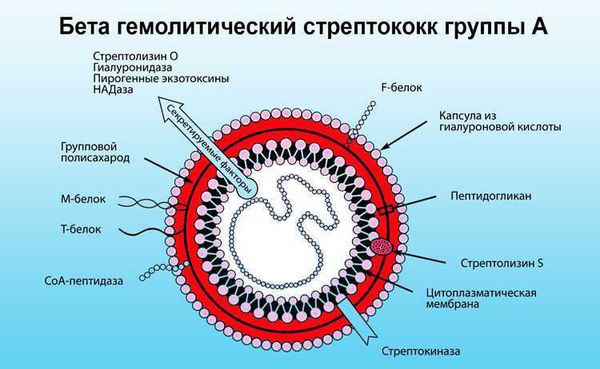
Среди причин и триггеров ревматических болезней чаще всего звучит гемолитический стрептококк А-группы, хотя этот патоген не является единственным из возможных. Острый или хронический очаг такой инфекции, – типичной локализацией которого является носоглотка (тонзиллиты, фарингиты, повторные ангины и т.д.), – может активизироваться под влиянием любого снижающего иммунитет фактора, так что с этой точки зрения ревматизм действительно можно считать одной из «болезней промоченных ног». Однако на этом сходство с так называемой простудой заканчивается. Начало собственно ревматического воспаления обусловлено особым аллергическим статусом (повышенной чувствительностью к токсинам инфекционного агента) и генетической предрасположенностью: иммунная система атакует не только патогенный микроорганизм, но и клетки соединительной ткани, обнаруживающее у некоторых людей определенное биохимическое сходство со стрептококком (или иным патогеном). Ревматизм нельзя считать наследственным заболеванием, но роль индивидуальной предрасположенности доказана. В целом, от 0,3 до 3% стрептококковых инфекций приводят к запуску ревматического процесса.
Следует понимать, что этиопатогенез ревматических воспалений, как и многих других полиэтиологических (многопричинных, многофакторных) заболеваний с вовлечением иммунных механизмов, в настоящее время остается недостаточно изученным и интенсивно исследуется специалистами разных профилей.
Симптоматика
По типу течения ревматические болезни стандартным образом делятся на острые и хронические. Клиника острого ревматизма недостаточно специфична; обычно она развивается стремительно и имитирует симптоматику ОРВИ (вкл. общее недомогание, лихорадку, суставно-мышечные боли и т.д.), что нередко затрудняет диагностику до появления критериальных признаков.
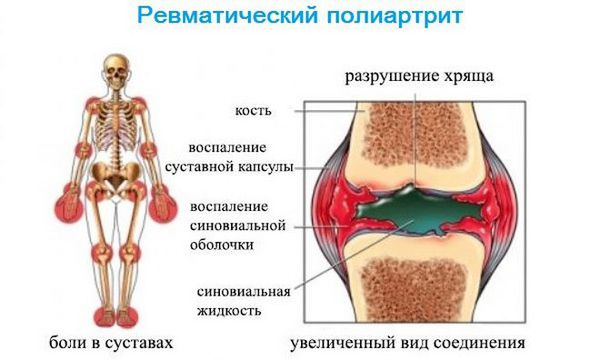
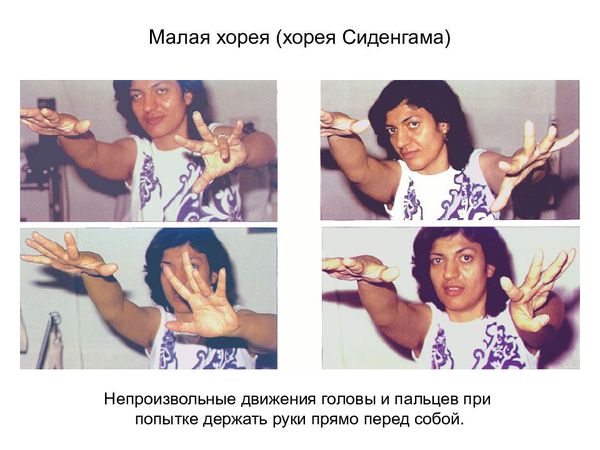
Хронический ревматизм является тяжелым, часто рецидивирующим (в т.ч. в зависимости от сезонных факторов) заболеванием, которое резко снижает качество жизни больного, по мере прогрессирования приводит к инвалидизации и при длительном злокачественном течении результирует летальным исходом. Клиническая картина определяется тем, какая именно система организма поражена в наибольшей степени. Наиболее распространенными формами ревматизма являются сердечная форма (симптоматика кардита, формирование пороков сердца и, как следствие, сердечной недостаточности), суставная форма (ревматоидный артрит: поражение суставных сумок и хрящевой ткани, отечность, болезненность, та или иная степень несостоятельности суставов), а также смешанная форма, при которой хроническое поражение суставов сочетается с нарастающей сердечно-сосудистой патологией. Кожная форма (аннулярная сыпь, ревматические узелки), а также неврологическая, легочная, желудочно-кишечная и офтальмологическая формы встречаются существенно реже, однако последствия могут быть не менее тяжелыми (гиперкинетические расстройства, плевриты, поражения сетчатки с частичной или полной слепотой).
Диагностика
Учитывая полиэтиологический характер и многообразие возможных клинических проявлений, диагностика ревматических заболеваний достаточно сложна; она требует тщательного многоэтапного обследования, которое начинается подробным изучением анамнеза. Клиническая картина должна отвечать ряду критериев – в частности, широко применяются критерии А.А.Киселя, критерии Джонса и др. Результаты лабораторных исследований (антитела, иммунные факторы, индикаторы воспаления) в диагностике ревматизма могут оказаться не столь информативными, как результаты клинического анализа. Из инструментальных методов первоочередными назначениями чаще всего становятся ЭКГ, ЭхоКГ, рентгенография, УЗИ, артроскопия и т.д.
Ревматические болезни необходимо дифференцировать с воспалительными процессами иной природы.
Лечение
В зависимости от особенностей конкретного случая, подбирается индивидуальная схема антибактериального лечения, назначаются гормонсодержащие и/или нестероидные противовоспалительные средства. Эрадикация патогена, купирование воспалительной симптоматики, нормализация сердечной деятельности, восстановление иммунного статуса, нормального сосудистого тонуса, суставных функций – все эти меры требуют постоянного контроля врача и в остром периоде должны осуществляться в стационарных условиях. В дальнейшем необходим мониторинг состояния (контрольное обследование не менее двух раз в год) и соблюдение ряда профилактических мер. Эффективным является курортно-санаторное лечение, физиотерапевтические процедуры по назначению врача. Прием антибиотиков при отсутствии противопоказаний назначают на длительный срок.
Одной из важнейших задач является предупреждение развития органических пороков сердца. Лечение должно начинаться как можно раньше, базироваться на результатах доказательной диагностики, носить комплексный характер и осуществляться в строгом соответствии с разработанной врачом стратегией, – включая последующее диспансерное наблюдение, решение медико-социальных вопросов, нормализацию и адаптацию образа жизни и т.д. Только при соблюдении данных условий можно говорить о благоприятном прогнозе или, по крайней мере, об уверенном терапевтическом контроле.
Что такое ревматизм (острая ревматическая лихорадка)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Семизаровой И. В., ревматолога со стажем в 33 года.
Определение болезни. Причины заболевания
Термин «ревматизм» в настоящее время употребляется в основном русскоязычной медициной. Согласно официальной международной терминологии, название заболевания — » острая ревматическая лихорадка». В обывательском понимании под термином «ревматизм» неверно подразумеваются исключительно заболевания опорно-двигательного аппарата.
Факторы риска развития ОРЛ
Этиология
Симптомы ревматизма
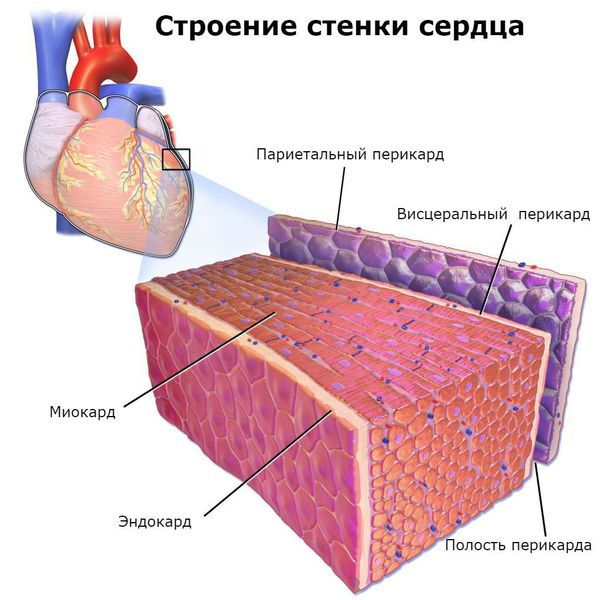
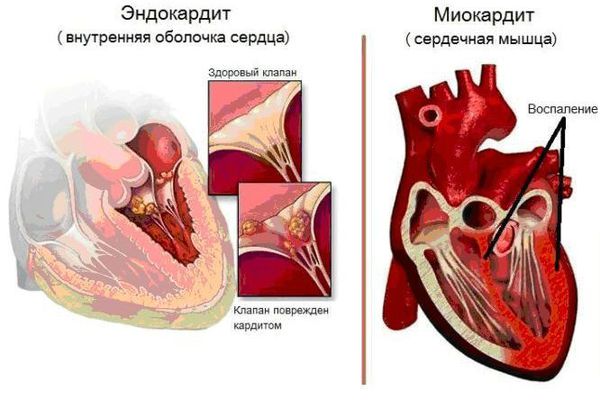
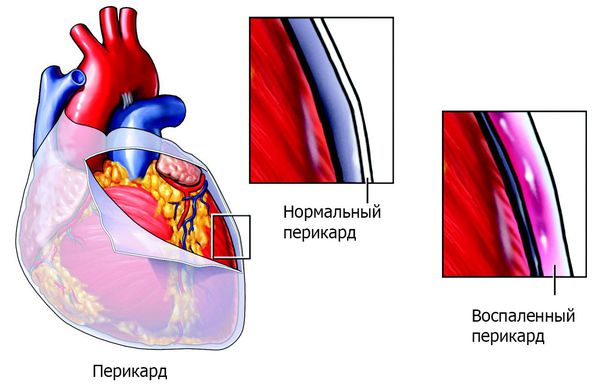
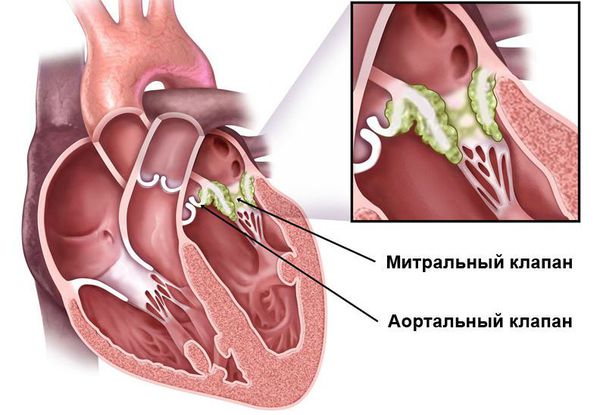
Основным, а в большинстве случаев и единственным проявлением ревматизма является поражение сердца, вызванное воспалением — ревмокардит (кардит). При ревмокардите происходит одновременное поражение миокарда и эндокарда. Это главный синдром, определяющий тяжесть и исход заболевания.
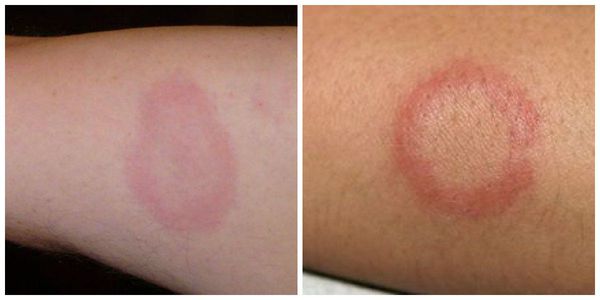
Кольцевидная эритема — редкое, но специфическое клиническое проявление ОРЛ. Она появляется в период наибольшей активности процесса примерно у 7-17 % детей. Кольцевидная эритема представляет собой незудящую сыпь бледно-розовой окраски. Она не возвышается над уровнем кожи, появляется на ногах, животе, шее, внутренней поверхности рук. Элементы сыпи имеют вид тонкого ободка, который исчезает при надавливании. Диаметр элементов — от нескольких миллиметров до ширины детской ладони.
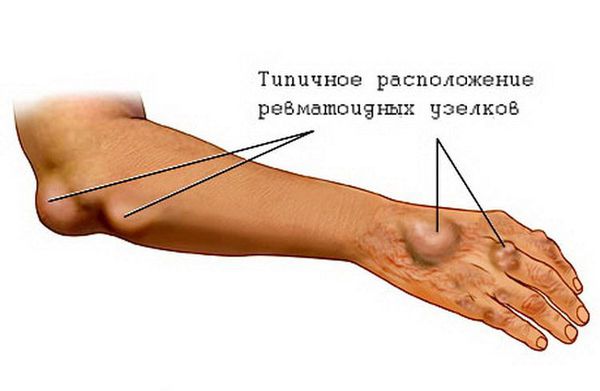
Подкожные ревматические узелки также являются редким признаком ОРЛ. Это округлые, плотные, безболезненные образования, варьирующие по размерам от 2 мм до 1-2 см. Они образуются в местах костных выступов (вдоль остистых отростков позвонков, краёв лопаток) или по ходу сухожилий (обычно в области голеностопных суставов). Иногда представляют собой скопления, состоящие из нескольких узелков. Часто сочетаются с тяжёлым кардитом.
Патогенез ревматизма
В ответ на проникновение стрептококковой инфекции организм начинает вырабатывать противострептококковые антитела. В то же время образуются иммунные комплексы, циркулирующие в крови и оседающие в микроциркуляторном русле. Стрептококк синтезирует токсины и ферменты. К токсинам относятся:
Ферменты — это гиалуронидаза, стрептокиназа и дезоксирибонуклеаза, они участвуют в развитии воспаления.
Установлено, что исход ревматизма определяется частотой формирования порока сердца, а частота формирования пороков сердца, в свою очередь, зависит от тяжести перенесённого ревмокардита. Известно также, что процент пороков сердца после первичного ревмокардита снизился в 2,5 раза. Следовательно, исход ревматизма стал более благоприятным.
Классификация и стадии развития ревматизма
Классификация и стадии развития заболевания
Код ревматизма по МКБ10 — 100-102.
По классификации Н.Д. Стражеско и В.Х. Василенко есть несколько стадий нарушения кровообращения:
По классификации Нью-Йоркской ассоциации кардиологов есть несколько функциональных классов (ФК):
Осложнения ревматизма
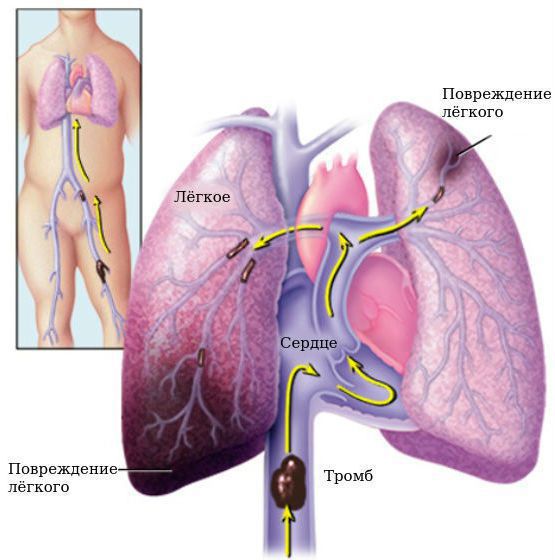
Осложнения при ОРЛ: тромбозы глубоких вен, тромбоэмболия лёгочных артерий, застойная сердечная недостаточность, инфекционный эндокардит, нарушение ритма и проводимости.
Тромбоэмболия лёгочной артерии — угрожающее жизни состояние, при котором из вен нижних конечностей или из левого предсердия отрывается тромб и закупоривает всю лёгочную артерию (при этом наступает смерть) или мелкие её ветви (в этом случае прогноз более благоприятный).
Сердечная недостаточность — это симптомокомплекс, характеризующийся одышкой, сердцебиениями, отёками нижних конечностей, увеличением печени. В начальной стадии эти признаки не так сильно выражены и могут быть обратимы. В конечной стадии они необратимы и заканчиваются летальным исходом.
Инфекционный эндокардит — инфекционное полипозно-язвенное воспаление эндокарда (внутренней оболочки сердца). При этом заболевании страдает не только сердце, но и другие внутренние органы. На сердечных клапанах образуются скопления микроорганизмов (вегетации), они могут отрываться от сердца и с током крови попадать в другие органы, например в мозг, почки, кишечник. Там они вызывают закупорку сосудов (тромбозы) с соответствующей тяжёлой клиникой вплоть до летального исхода.
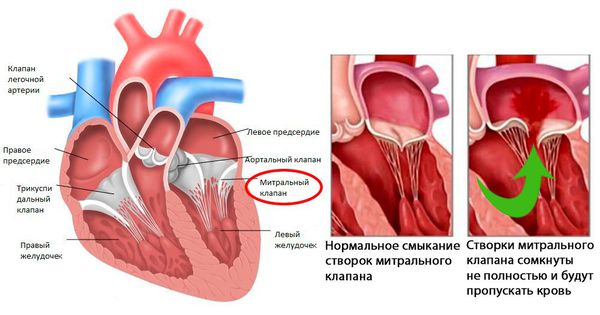
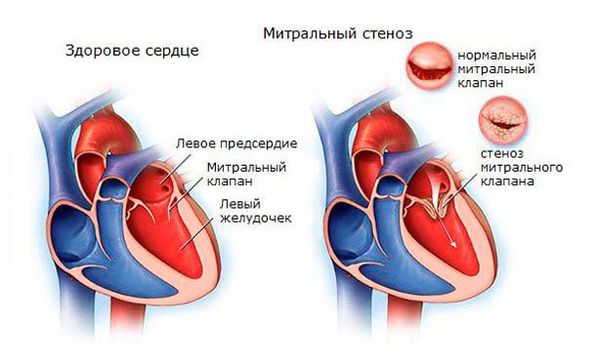
После перенесённой ОРЛ возможно формирование порока сердца. При возвратном (вторичном) ревмокардите число случаев последующего формирования порока сердца возрастает, особенно в подростковом возрасте. Ревматический процесс вызывает укорочение створок клапана (недостаточность) или сужение клапанного отверстия (стеноз). В результате возникают нарушения сердечного кровообращения и камеры сердца увеличиваются в размерах. Затем возникает и прогрессирует сердечная недостаточность.
Диагностика ревматизма
Для диагностики ОРЛ используют критерии Киселя — Джонса. Они были пересмотрены Американской кардиологической ассоциацией в 1992 году, а в 2003 году преобразованы Ассоциацией ревматологов России. Это очень важный шаг, так как он способствовал раннему распознаванию и правильной трактовке клинических явлений. Критерии Киселя — Джонса разделили на две группы: большие и малые.
К большим относятся:
Данные, подтверждающие предшествовавшую БГСА-инфекцию (бета-гемолитическую стрептококковую А инфекцию)
Вероятность ОРЛ высока, если подтверждено два момента:
Лабораторная диагностика
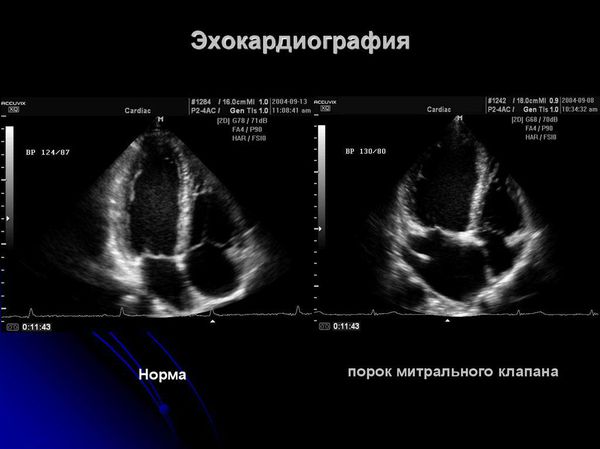
Инструментальные методы
Для оценки поражения сердца применяют:
Дифференциальный диагноз
Лечение ревматизма
При ОРЛ, особенно с выраженным кардитом, больные должны соблюдать постельный режим в течение 2-3 недель. В дальнейшем необходимо включать комплексы лечебной гимнастики.
НПВП (нестероидные противовоспалительные препараты) назначают в следующих случаях:
НПВП имеют выраженный противовоспалительный эффект и в течение 10-14 дней помогают снизить проявления лихорадки, артрита, приводят к положительной динамике кардита, улучшению лабораторных показателей. При длительном применении НПВП могут вызвать побочные реакции: изменение клеточных элементов крови, поражение слизистой желудочно-кишечного тракта и др. [1] [3] [5] С целью контроля периодически проводят исследования кала на скрытую кровь, по показаниям выполняют фиброгастроскопию, определяют лейкоциты и тромбоциты в периферической крови.
Симптоматическая терапия заключается в коррекции сердечной недостаточности, которая может развиться у больных с ревматическими пороками сердца или активным воспалением тканей, образующих клапаны сердца. Симптоматическое лечение подразумевает использование по показаниям сердечных гликозидов, диуретиков, и-АПФ и бета-блокаторов. Для лечения хореи назначают противовоспалительные препараты, при выраженных гиперкинезах дополнительно применяют нейротропные средства: фенобарбитал 0,015-0,03 г 3-4 раза в сутки или «Финлепсин» 0,4 г\ сут.
Прогноз. Профилактика
При своевременном и правильном лечении прогноз благоприятный. Если формируется порок сердца, то в дальнейшем необходима хирургическая коррекция (протезирование, пластика).
Профилактика
В соответствии с рекомендациями Комитета экспертов Всемирной организации здравоохранения (ВОЗ) различают первичную профилактику ревматической лихорадки (профилактику первичной заболеваемости) и вторичную (профилактику рецидивов болезни).
Первичная профилактика — это комплекс общественных и индивидуальных мер, которые направлены на предупреждение заболеваемости ангинами, фарингитами. Комплекс включает закаливание, повышение жизненного уровня, улучшение жилищных условий, обязательные прогулки на свежем воздухе.
Очень важно раннее лечение ангин и других острых заболеваний верхних дыхательных путей, вызванных стрептококком. Любое лечение ангины должно продолжаться не менее 10 дней. В этом случае возможно полное излечение стрептококковой инфекции.
Вторичную профилактику начинают ещё в стационаре, сразу после окончания 10-дневной терапии пенициллинами или макролидами. Важно иметь в виду — чем меньше возраст пациента при первой атаке, тем выше риск рецидива. Длительность вторичной профилактики определяется индивидуально.
Одновременно с осуществлением вторичной профилактики больным ОРЛ в случае присоединения острых респираторных инфекций, ангин, фарингита рекомендуется проведение текущей профилактики. Последняя предусматривает назначение 10-дневного курса лечения пенициллином.
Ревматологический комплекс
Ревматологические заболевания у людей чаще всего ассоциируются с заболеваниями суставов, хотя могут поражаться различные органы и системы. Как можно заподозрить ревматологическое заболевание и какие анализы необходимо сдать?
Ревматологические заболевания представляют большую группу заболеваний, поражающих соединительную ткань организма. Ещё их называют аутоиммунными или системными заболеваниями. Аутоиммунные – потому что иммунная система теряет способность распознавать «своё-чужое» и вырабатывает антитела против собственных клеток и тканей. Системные – так как соединительная ткань содержится во всех органах и сосудах, поэтому затрагиваются все системы организма в той или иной степени. Причина ревматологических заболеваний до конца неясна. Но последствия серьёзные, и раннее распознавание важно для своевременного лечения и предотвращения осложнений.
Как можно заподозрить ревматологическое заболевание?
Вышеперечисленные признаки могут возникать при ряде других заболеваний, хотя зачастую они являются единственными «тревожными сигналами» для начала обследования.
На самом деле, зачастую происходят изменения со стороны сердца, легких, почек, нервной системы и других внутренних органов, но они не имеют ярких проявлений. Иногда обращают внимание признаки поражения кожи – в виде различных высыпаний. Покраснения кожи лица в форме «бабочки» возникают при системной красной волчанке; утолщение кожи пальцев при склеродермии.
Как ставится диагноз?
Для того, чтобы установить ревматологическое заболевание, врач оценивает 2 критерия:
Только на основании совместной оценки клинического и лабораторного критериев возможно установить диагноз ревматологического заболевания и различить, какое именно заболевание из целой группы имеет место. Ни один критерий не используется изолированно!
Для Вашего удобства основные лабораторные тесты объединены в комплекс «Ревматологический, расширенный».
Что входит в состав комплекса?
Что нужно сдать и как подготовиться к исследованию?
Для исследования на ревматологический комплекс сдаётся венозная кровь утром натощак или через 3 часа после необильного приёма пищи. Накануне рекомендуется отказаться от алкоголя.
Ревматологическое заболевание хорошо лечится на ранних стадиях. Обращайте внимание на своё здоровье, будьте внимательны к себе и обследуйтесь своевременно!
Диагностика и лечение поражений нервной системы при ревматических заболеваниях
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими с
Ревматические болезни относятся к группе заболеваний, которые характеризуются развитием аутоиммунных процессов против антигенов почти всех органов и тканей организма, что сочетается с образованием аутоантител с органонеспецифическими свойствами.
Аутоиммунные процессы осуществляют информационный обмен между нейроэндокринной и иммунной системами, при этом главную роль играют аутоантитела к гормонам, медиаторам и их рецепторам. Продемонстрирован синтез нейропептидов в иммунокомпетентных клетках, а в клетках нейроэндокринной системы доказана возможность синтеза лимфокинов и монокинов.
Получены данные о нейрогенной регуляции функций иммунитета и их нарушений, в то же время иммунокомпетентные клетки и их медиаторы могут влиять на функцию центральной нервной системы (ЦНС) по принципу нейроиммуномодуляции. Показано, что свойством нейросекреции обладает вся центральная и периферическая нервная система. Влияние иммунной и нервной систем друг на друга реализуется через рецепторные структуры клеток, взаимодействие которых создает связи «рецептор-рецептор» и таким образом организует молекулярный механизм совместной работы обеих систем.
Функционирование клеток и сигнальная информация обеспечиваются медиаторами и нейротрансмиттерами в обеих системах, между нервной и иммунной системой происходит взаимообмен информацией с помощью цитокинов, стероидов и нейропептидов [1, 2].
Таким образом, доказана общность и взаимосвязь нервной и иммунной систем, сходство между их структурами и функциями и развитие нового направления современной иммунологии — нейроиммунологии [3, 4]. Широкий диапазон неврологических синдромов при аутоиммунных системных заболеваниях позволяет рассматривать их как модельные системы для изучения патогенетической роли иммунных механизмов поражения центральной и периферической нервной системы [5].
Потенциальными мишенями для аутоиммунной агрессии могут быть различные антигены нервной ткани, включая миелин, в том числе ассоциированный с гликопротеином, и его основной белок, ганглиозиды, белок ядер нейрональных клеток и другие [6]. Так, мишеневидные антигены при нейролюпусе представлены антигенами нейрональной ткани, рибосомальным Р-белком, рДНК, малым ядерным рибонуклеопротеидом, а также анионными фосфолипидами при антифосфолипидном синдроме, что обуславливает широкий спектр неврологической симптоматики при данной патологии [7, 8].
По данным различных авторов, частота поражений нервной системы при ревматических заболеваниях (РЗ) колеблется от 40% до 70% и выше, если учитывать психические синдромы и головную боль. Неврологические синдромы включены в классификационные критерии системных васкулитов, опубликованные Американской коллегией ревматологии в 1990 году, в диагностические критерии и критерии активности системной красной волчанки (СКВ), а также в ряд других диагностических критериев, в частности узелкового полиартериита у детей. Неврологические нарушения при РЗ требуют проведения дифференциальной диагностики и назначения адекватного лечения совместно ревматологом и неврологом.
При СКВ в диагностические критерии неврологических поражений включены судороги или психозы. Поражение ЦНС обусловлено в основном сосудистой патологией, к которой относят васкулопатию, тромбозы, истинные васкулиты, инфаркты и геморрагии [7]. В цереброспинальной жидкости обнаруживаются антинейрональные антитела, определяется повышение уровня белка, увеличение клеточного состава. Описаны разные виды судорожных припадков: большие, малые, по типу височной эпилепсии, а также гиперкинезы. При ЦНС-люпусе имеет место головная боль типа мигрени, устойчивая к анальгетикам, но отвечающая на лечение глюкокортикостероидами. Параличи черепных нервов обычно сопровождаются офтальмоплегией, мозжечковыми и пирамидными симптомами и нистагмом. Имеют место зрительные нарушения, преходящие нарушения мозгового кровообращения. Острый поперечный миелит встречается редко и имеет неблагоприятный прогноз. Психические синдромы разнообразны и характеризуются аффективными, органическими мозговыми или шизофреноподобными проявлениями [9, 10].
В рамках СКВ был описан и антифосфолипидный синдром. Этот синдром включает: рецидивирующие артериальные или венозные тромбозы, привычное невынашивание беременности и тромбоцитопению и дополнительные признаки: сетчатое ливедо, неврологические проявления: хорею, эпилепсию, мигренеподобную головную боль, нарушения мозгового кровообращения и деменцию вследствие множественных инфарктов, хронические язвы голеней, Кумбс-положительную гемолитическую анемию, клапанные поражения сердца и серологические маркеры — антифосфолипидные антитела, к которым относятся антикардиолипиновые антитела IgG и IgM и волчаночный антикоагулянт [11].
При системной склеродермии (ССД) неврологический синдром представлен в основном полиневритическими проявлениями, связанными с сосудистыми изменениями и фиброзными процессами в соединительной ткани. Для узелкового полиартериита характерны множественные мононевриты, для гранулематоза Вегенера — асимметричная полинейропатия, для неспецифического аортоартериита — дисциркуляторная энцефалопатия и нарушения мозгового кровообращения.
Собственные данные включали обследование 229 больных различными формами РЗ, среди которых 110 больных страдали системными заболеваниями соединительной ткани: 88 больных СКВ, 22 — ССД и 119 больных — системными васкулитами: облитерирующий тромбангиит (ОТ) — 21, узелковый полиартериит (УП) — 27, неспецифический аортоартериит — (НАА) — 32, геморрагический васкулит (ГВ) — 15 и гранулематоз Вегенера (ГрВ) — 2, другие формы — 22. Проведено детальное неврологическое исследование, ультразвуковая транскраниальная допплерография сосудов мозга, реоэнцефалография, компьютерная (КТ) и магнитно-резонансная томография (МРТ) головного мозга, электроэнцефалография, исследование иммунного статуса.
У большинства больных заболевания дебютировали кожным (50,6%), суставно-мышечным (35,4%) и сосудистым (27,1%) синдромом. Органные поражения в дебюте регистрировались с частотой 7%, синдром артериальной гипертензии — у 5,2%, лихорадка — у 7,0%, гематологические нарушения — 7,9%. Неврологические расстройства в дебюте заболевания отмечены у 12,2% и проявлялись моно- и полиневропатией и синдромом энцефаломиелополирадикулоневрита (ЭМПРН). Поражение периферической нервной системы в дебюте заболевания было особенно характерно для УП и наблюдалось у 30% больных. Основными синдромами дебюта со стороны ЦНС был цефалгический (10,5%) и вестибулярный (6,3%), чаще они наблюдались при НАА. Вовлечение ЦНС имело место у 96 (41,9%) больных, являясь наиболее выраженным при СКВ, НАА, УП.
Цереброваскулярная патология была доминирующей в клинической картине болезни у 34,7% больных, а иногда разнообразные симптомы поражения ЦНС развивались задолго до появления полисиндромной картины заболевания. Основные клинические проявления цереброваскулярной патологии включали: цефалгический (82%), астенический (76%), вестибулярно-атактический (80%), пирамидный (74%) синдромы, синдром вегетативно-сосудистой недостаточности (69%), диссомнический (79%) и базально-оболочечный (37%), гипопоталамической дисфункции (34,7%).
Описанная неврологическая симптоматика часто сочеталась с симптомами сосудистой недостаточности головного мозга, которые объединялись синдромом дисциркуляторной энцефалопатии 1 (11%), 2 (26,4%) или 3 (8%) степени. У 7,8% больных имели место преходящие нарушения мозгового кровообращения.
Гипоталамическая дисфункция у больных РЗ проявлялась полиморфными нейроэндокринными расстройствами, нарушением терморегуляции, преимущественно по типу пароксизмальной центральной гипертермии, инсомнией, патологией психоэмоциональной сферы.
Установлено достоверное преобладание у больных пирамидной недостаточности слева (41%). Преобладание пирамидной недостаточности справа регистрировалось реже (23,7%). Дистонические феномены в форме вестибулярно-мозжечковой установки кисти и диссоциированная мышечная гипотония в ногах также были более выражены слева. Полученные данные свидетельствуют о преобладающем поражении пирамидной и сенсорной систем, а также неспецифических структур правого полушария, которое тесно связано с гипоталамической областью и обеспечивает адаптацию организма к воздействующим факторам внешней среды. Обнаруженная функциональная асимметрия свидетельствует о срыве адаптационных механизмов нервной системы и указывает на роль дисфункции правополушарно-гипоталамической системы.
При использовании методов МРТ и/или КТ было выявлено изменение желудочковой системы в виде ее расширения или деформации и/или расширения субарахноидального пространства, а также очаговые поражения различных структур головного мозга, атрофия вещества мозга и краниовертебральные аномалии. Признаки наружной, внутренней или сочетанной гидроцефалии отмечались при всех нозологических формах. Очаговые изменения вещества мозга включали гиперденситивные зоны, гиподенситивные зоны с отеком или без него, единичные или множественные.
При исследовании сосудистой системы и мозгового кровообращения достоверно наблюдалось повышение тонуса сосудов, гипертонический и дисциркуляторный тип кровообращения по данным реоэнцефалографии (РЭГ) и увеличение линейной скорости кровотока по средней мозговой артерии. Больные с вовлечением ЦНС отличались по электроэнцефалографии: им были свойственны диффузные патологические изменения, наличие дезорганизации альфа-ритма, дизритмий и пароксизмальной активности.
Корреляционный анализ цереброваскулярной патологии и результатов инструментальных исследований сосудов головного мозга показал, что при всех нозологических формах у пациентов имело место нарушение венозной гемоциркуляции. В последующем происходило сужение церебральных артерий, ликвородинамические нарушения с формированием внутричерепной гипертензии, нарушением системы микроциркуляции в головном мозге. Очаговые поражения головного мозга отличались локализацией процесса в зависимости от нозологической формы. В табл. представлены основные неврологические проявления РЗ.
У 39% больных СКВ молодого возраста с поражением ЦНС имели место нарушения мозгового кровообращения, причем у половины из них инсульт развился в начале заболевания. Одновременно с инсультом в дебюте СКВ у больных чаще выявлялась «сосудистая бабочка» и/или вазоспастический синдром, повышение артериального давления, чаще диастолического. У этих больных отмечались умеренные или высокие титры кардиолипинов IgG, антител к нативной ДНК и ревматоидного фактора (РФ) IgM, что могло свидетельствовать о наличии текущего церебрального васкулита. Эти данные подтверждались выявлением гипертонуса резистивных интракраниальных сосудов и патологией микроциркуляторного русла в виде увеличения количества функционирующих капилляров, их выраженной извитостью с замедлением кровотока в артериолах. Изменения в свертывающей системе характеризовались синдромом гиперкоагуляции. Выявлены основные факторы риска развития инсульта у больных РЗ: артериальная гипертензия, поражения сердца, гиперкоагуляция, иммунное воспаление сосудистой стенки, асимметрия мозгового кровотока.
Среди больных РЗ цереброваскулиты (ЦВ) имели место у 28,3% больных. Диагноз ЦВ ставился при обнаружении очаговой неврологической симптоматики, изменений на глазном дне, снижения зрения, наличии признаков нарушения мозгового кровообращения, а также по результатам КТ и ядерно-магнитно-резонансной томографии (ЯМРТ), при которых выявлялись наружная и внутренняя гидроцефалия, очаговые изменения в коре и субкортикальном веществе. При этом с течением времени число очагов любой локализации в головном мозге нарастало. При магнитно-резонансном ангиографическом (МРА) исследовании отмечались множественные сегментарные неровности сосудистой стенки, циркулярные или эксцентричные стенозы и дилятация мелких и средних интракраниальных артерий с формированием аневризм, нарушения кровотока. Выявленное снижение интенсивности МРА-сигнала на фоне повышения активности ревматического процесса свидетельствовало о наличии ЦВ.
Иммунологическими маркерами ЦВ считали антитела к нативной ДНК, IgG-антитела к кардиолипину (аКЛ) и IgM аКЛ, антинейтрофильные цитоплазматические антитела (АНЦА), в меньшей степени — РФ и волчаночный антикоагулянт (ВА). Имели место клинико-иммунологические корреляции с неврологическими проявлениями.
Изолированный (первичный) ЦВ характеризовался обнаружением симптомов вовлечения ЦНС и такими признаками, как головная боль, судороги, менингеальный синдром, острая прогрессирующая энцефалопатия без признаков экстракраниального или системного васкулита, психические синдромы, деменция, прогрессирующее снижение интеллекта, инсульты, нарушения зрения, нистагм. Чаще перивентрикулярные очаги выявлялись в первый год заболевания.
Ряд больных обращались на консультацию к окулисту в связи с ухудшением зрения, вплоть до амавроза, наличием увеита, ишемического неврита. Ангиопатия сетчатки имела место у 41% этих больных, флебопатия — у 14%, ретиноваскулит — у 6%, ангиоспазм — у 13%, ангиосклероз — у 18%.
Полиневритический синдром встречался у подавляющего большинства больных (96,7%) в виде сенсорной, чувствительно-двигательной полиневропатии или в сочетании с поражениями ЦНС, с синдромом ЭПН и ЭМПРН. При ССД, ОТ и ГВ преобладали формы в виде чувствительной или чувствительно-двигательной полиневропатии, а при СКВ и НАА — формы с сочетанным поражением периферической НС (ПНС) и ЦНС — синдромы ЭПН и ЭМПРН. При ОТ и НАА отмечалась отчетливая диссоциация степени выраженности полиневропатии по оси тела, причем при ОТ симптоматика была более отчетливой в ногах, при НАА — в руках. В целом асимметричная полиневропатия имела место у 19,2% больных, достигая максимума при УП (59,3%).
Патология НС при РЗ нередко определяет прогноз, клиническую картину заболевания и качество жизни больных, а также требует обязательного сочетанного применения базисной противовоспалительной терапии, ангио- и нейропротекторов. К группе нейропротекторов относят Актовегин, Инстенон. Используются препараты, улучшающие мозговое кровообращение, — Винпоцетин, Кавинтон, метаболические средства с антигипоксантным действием — Ноотропил, Пирацетам, Церебролизин, по показаниям седативные и противосудорожные средства, антидепрессанты.
При РЗ терапия включает глюкокортикостероиды, иммуносупрессанты, иммуноглобулин, плазмаферез, иммуномодуляторы, дезагреганты, нестероидные противовоспалительные препараты и симптоматические средства.
Лечение состоит из нескольких этапов: быстрое подавление иммунного ответа в дебюте заболевания и при его обострениях (индукция ремиссии); длительная поддерживающая терапия иммуносупрессантами, в дозах, достаточных для достижения клинической и лабораторной ремиссии заболевания; определение степени повреждения органов или систем организма и их коррекция, проведение последующих реабилитационных мероприятий.
Первый этап включает эффективное подавление иммунного воспаления на ранних стадиях болезни и предполагает использование глюкокортикостероидов, иммуносупрессантов цитостатического действия типа Циклофосфана и антиметаболитного действия типа Метотрексата, цитокинсупрессивного препарата Циклоспорина А, внутривенного иммуноглобулина, назначение повторных курсов пульс-терапии метилпреднизолоном и Циклофосфаном, в сочетании с экстракорпоральными методами лечения.
При острых церебральных нарушениях при высокой активности СКВ используется схема пульс-терапии с введением Метипреда 1 г внутривенно 1 раз в день в течение 3 дней и с добавлением 800 мг Циклофосфана во 2-й день. При хроническом течении СКВ суточная доза преднизолона составляла 15–20 мг с последующим постепенным снижением, Циклофосфан применяется внутримышечно в дозе 400 мг в неделю до 1600–2000 мг на курс, затем по 200 мг в неделю в течение года и более. Апробируются препараты мофетила микофенолат и лефлуномид.
При патологии органа зрения назначают нестероидные противовоспалительные препараты в виде инъекций диклофенака, а затем пероральные препараты этой группы, дезагреганты, при наличии признаков воспалительной активности добавляют умеренные дозы глюкокортикостероидов, а при резком снижении зрения и выраженных признаках активности используют пульс-терапию.
Проводится определение наиболее эффективных и менее токсичных схем применения иммуносупрессивных препаратов, путей их введения, и включение в комплексное лечение больных препаратов, улучшающих микроциркуляцию и/или влияющих на реологические свойства крови (Гепарин, Фраксипарин, Трентал, Ралофект, Тиклид).
В ряде случаев назначают препараты типа Реаферона, а при наличии инфицированных язв, некрозов кожи или конечностей применяют антибиотики. Ввиду многообразия нозологических форм на выбор лекарственных средств в дебюте заболевания оказывает влияние распространенность патологического процесса и наличие интеркуррентной инфекции. Показано назначение ангиопротекторов и посиндромная терапия.
Учитывая высокий удельный вес неврологической патологии, больные РЗ должны проходить комплексное клинико-инструментальное неврологическое исследование уже на ранней стадии патологического процесса. Постановка диагноза РЗ и комплексная терапия глюкокортикостероидами и иммуносупрессантами способствуют коррекции нарушений ЦНС и ПНС.