Что такое вич-инфекция? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракина О. Ю., инфекциониста со стажем в 7 лет.
Определение болезни. Причины заболевания
ВИЧ-инфекция — это хроническое инфекционное заболевание, которое провоцирует вирус иммунодефицита человека, поражающий клетки иммунной системы (СD4). При отсутствии лечения закономерно приводит к синдрому приобретённого иммунодефицита (СПИДа). [6]
Вирус иммунодефицита человека принадлежит семейству ретровирусов (Retroviridae), роду Lentivirus. Впервые информация о болезни появилась в 1970 годах. Сам вирус был выделен в 1983 году одновременно во Франции вирусологом Франсуазой Барре-Синусси и в США учёным Робертом Гало, однако название, одобренное Всемирной организацией здравоохранения, получил только через пять лет — в 1987 году. Тогда же впервые был зарегистрирован случай ВИЧ-инфекции в СССР. [1] [2]
В настоящее время выделяют два типа вируса — ВИЧ-1 и ВИЧ-2, которые отличаются по своим структурным характеристикам. На территории России, США, Европы и Центральной Африки распространён вирус первого типа (ВИЧ-1), на территории Индии и Западной Африки эпидемиологическое значение имеет второй тип вируса (ВИЧ-2).
В естественных условиях ВИЧ в высушенном состоянии сохраняет активность на протяжении нескольких часов, в биологических жидкостях — несколько дней, в замороженной сыворотке крови — несколько лет. При нагревании до 70-80°C вирус гибнет через 10 минут, при обработке 70% раствором этилового спирта инактивируется через одну минуту. Также чувствителен к 0,5% раствору гипохлорита натрия, 6% раствору перекиси водорода, 5% раствору лизола, эфира или ацетона. [2]
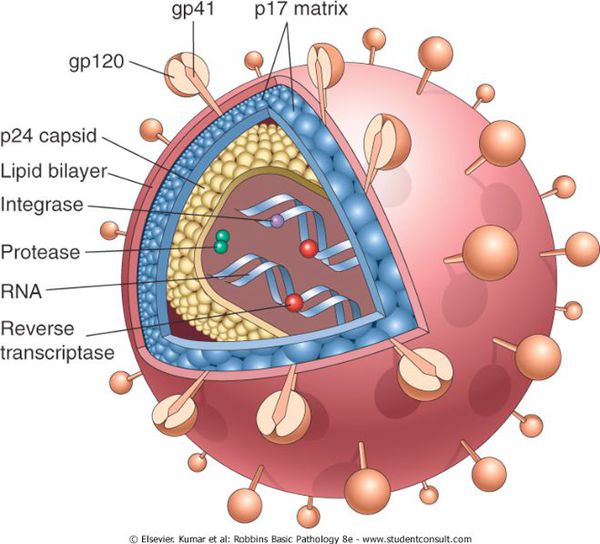
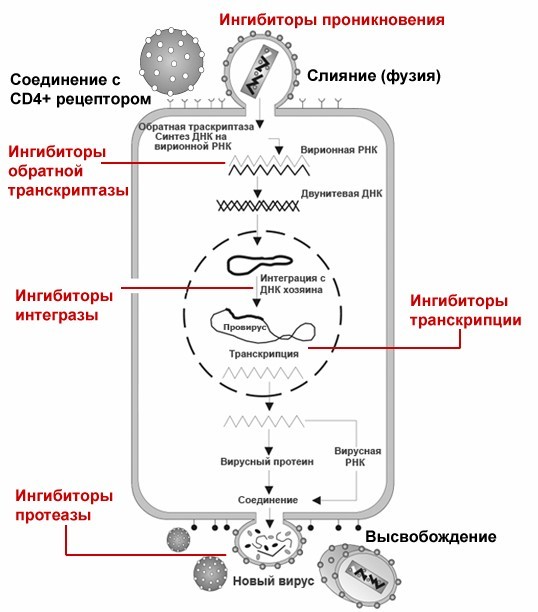
Форма вируса округлая, в центре расположено ядро, содержащее две нити рибонуклеиновой кислоты (РНК) и ферменты, необходимые для размножения — обратную транскриптазу (ревертазу), интегразу, протеазу, РНКазу. Ядро окружено внутренней белковой и наружной липидной оболочкой. Внутренняя оболочка ВИЧ-1 состоит из протеинов p17, p24 и p55. Наружная оболочка «пронизана» гликопротеином gp160, который состоит из фрагментов gp41 и gp120 (так называемых оболочечных белков). Gp41 и gp120 на поверхности вириона образуют отростки, с помощью которых ВИЧ присоединяется к рецепторам клеток-мишеней человека (клеткам организма, которые имеют рецептор — белок CD4). [1] [3]
Как передаётся ВИЧ
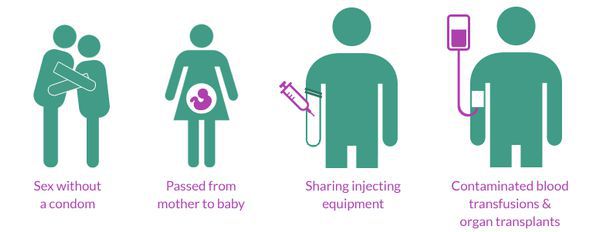
Пути передачи инфекции:
Важно отметить, что при поцелуях, общении, объятиях, рукопожатиях, использовании общей посуды и других предметов быта ВИЧ-инфекция не передаётся.
ВИЧ в России
По данным на 30 июня 2021 года, в России выявлено 1 528 356 человек с подтверждённым диагнозом «ВИЧ-инфекция», в том числе: 1 122 879 пациентов, живущих с ВИЧ, и 405 477 умерших.
ВИЧ-инфекция активно распространяется среди населения. Так, в первом полугодии 2021 года 67,3 % людей заразились при гетеросексуальных контактах, 28,9 % — при употреблении наркотиков и 2,9 % — при гомосексуальных контактах. [7]
Вероятность заразиться ВИЧ
При незащищённом вагинальном контакте женщины заражаются ВИЧ примерно в 8 случаях из 10 000, а мужчины — в 4 случаях. При незащищённом анальном сексе риск заразиться ВИЧ выше: пассивному партнёру вирус передаётся в 138 случаях из 10 000, активному — в 11 случаях. [10]
ВИЧ и беременность
Симптомы вич-инфекции
Инкубационный период ВИЧ длится от четырёх недель до трёх месяцев (в единичных случаях — до года).
Первые признаки ВИЧ
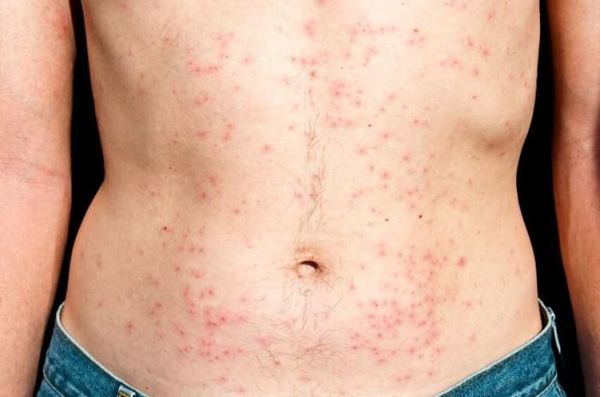
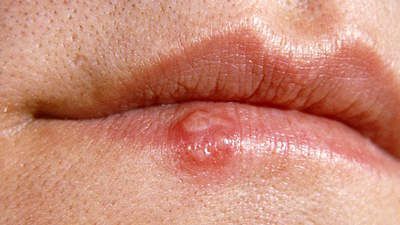
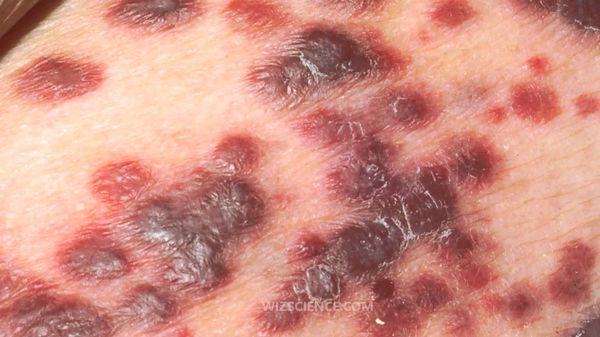
ВИЧ-инфекция не имеет специфических симптомов. Все клинические проявления могут относиться как к другим инфекционным и неинфекционным заболеваниям, так и к проявлениям вторичных заболеваний, которые развиваются на фоне иммунодефицита. Однако можно выделить лишь основные симптомы острой ВИЧ-инфекции, которые проявляются в первые три недели – три месяца от момента инфицирования:
Вышеперечисленные симптомы ВИЧ могут наблюдаться примерно у 30% заболевших. Ещё у 30-40% острая ВИЧ-инфекция может протекать в более тяжёлой форме (с развитием герпетической инфекции, пневмонии, менингита, энцефалита) и примерно у 30% не наблюдается.
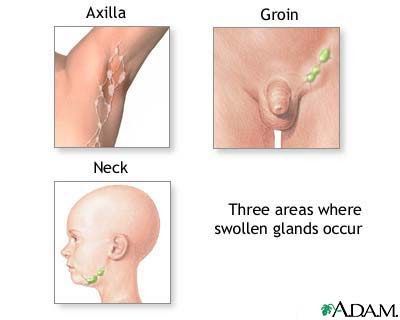
Продолжительность клинических проявлений в случае их возникновения варьируется от нескольких дней до нескольких месяцев. Обычно симптомы ВИЧ длятся около 2-3 недель, после чего все проявления исчезают. Исключение может составлять увеличение лимфоузлов, которое часто сохраняется на протяжении всего заболевания.
Не стоит искать у себя какие-либо симптомы ВИЧ. Единственная возможность узнать о наличии или отсутствии ВИЧ-инфекции — пройти лабораторное исследование крови на антитела к ВИЧ минимум через три месяца после «рискованной» ситуации или на РНК ВИЧ минимум через два месяца.
Патогенез вич-инфекции
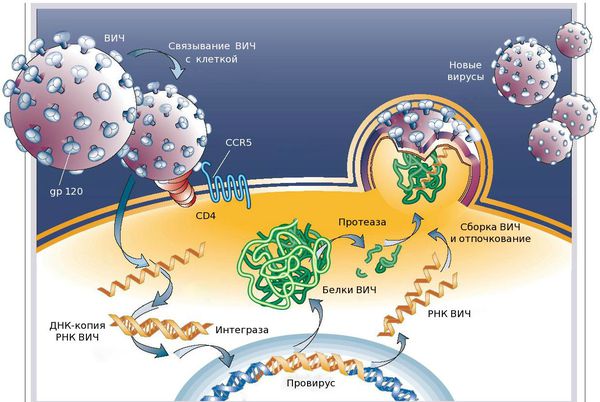
Проникнув в организм человека любым из вышеперечисленных способов, вирус с помощью специфического гликопротеида gp120 фиксируется на мембране клеток-мишеней, в которых есть белок CD4. Данный рецептор есть у Т-лимфоцитов (Т4, хелперы), он играет главную роль в иммунном ответе. Также белок CD4 есть у у моноцитов, макрофагов, эндотелиальных и других клеток.
После фиксации на мембране вирус проникает в клетку, там его РНК благодаря ферменту ревертазы синтезирует (создаёт) ДНК, которая встраивается в генетический аппарат здоровой клетки. Там она может существовать в виде провируса в течение всей жизни, при этом оставаясь неактивной. Когда провирус активируется, в заражённой клетке происходит активное накопление новых вирусных частиц, что приводит к разрушению текущей клетки и поражению новых. [3]
Свободный белок gp120 также способен соединяться с рецептором СD4, который присутствует у неинфицированных Т4 лимфоцитов. Вместе они распознаются иммунной системой как чужеродные и разрушаются клетками-киллерами. Ещё одной причиной гибели СD4 клеток являются биологически активные вещества, которые секретируют инфицированные ВИЧ макрофаги. Кроме того, у инфицированных Т-хелперов появляется способность формирования массивных скоплений, в связи с чем их количество резко уменьшается.
Клетки иммунной системы необходимы организму человека для его защиты от бактерий, вирусов, простейших, опухолевых клеток и других чужеродных агентов. Заражённые ВИЧ Т4 клетки не способны осуществлять свою основную функцию, в связи с чем разрушается иммунная система и нарушается нормальная реакция на чужеродные агенты. ВИЧ-инфицированный человек становится беззащитным перед микроорганизмами, даже включая те, которые не представляют опасности для незаражённого человека (оппортунистические инфекции), повышается риск развития онкологических заболеваний.
Также в патологический процесс зачастую вовлекается нервная система. Это становится причиной функциональных, а затем и трофических поражений нейронов и нарушения мозговой деятельности.
Классификация и стадии развития вич-инфекции
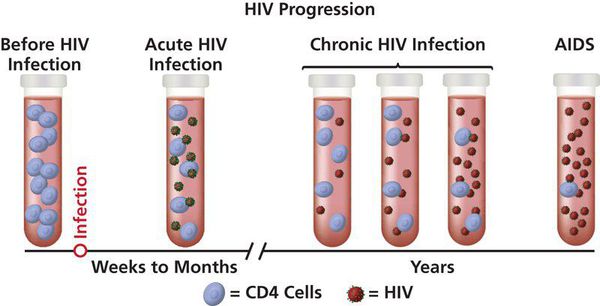
Выделяют пять стадий инфицирования:
1) Стадия инкубации — фаза от момента заражения до выработки антител и/или появления реакции, представленных признаками «острой ВИЧ-инфекции». Продолжительность — от четырёх недель до трёх месяцев (в единичных случаях — до года).
В среднем длительность стадии инкубации составляет от 3 до 6 месяцев. В тот период вирус в организме человека активно размножается, но никак себя не проявляет ни клинически, ни при лабораторном исследовании на антитела к ВИЧ. Однако человек в этой стадии уже заразен.
2) Стадия первичных проявлений — этап, который начинается, соответственно, через 3-6, максимум 12 месяцев от момента заражения. В этот период продолжается активное размножение вируса, и появляется первичный ответ в виде выработки антител или клинических проявлений. Поэтому вторую стадию ВИЧ-инфекции можно выявить при сдаче крови на антитела к ВИЧ.
Стадия первичных проявлений может быть бессимптомной (чаще всего), а также проявляться в виде ряда неспецифических признаков ВИЧ:
Принято считать, что человек находится в стадии острой ВИЧ-инфекции на протяжении 12 месяцев от появления антител к ВИЧ.
3) Субклиническая, или латентная, стадия ВИЧ — период замедленного размножения вируса, по сравнению с предыдущими стадиями. Антитела к ВИЧ в крови продолжают выявляться. Единственный признак ВИЧ — увеличение лимфатических узлов, которое возникает не всегда. Продолжительность стадии без специфического лечения — от 6 до 7 лет (в отдельных случаях может варьироваться от 2 до 20 лет).
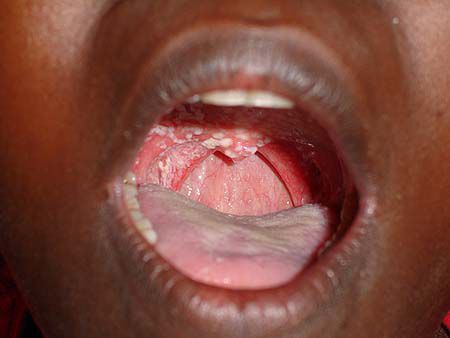
4) Стадия вторичных заболеваний — фаза, в которой продолжается репликация ВИЧ. Она сопровождается активной гибелью CD4-лимфоцитов и, следовательно, истощением иммунной системы. Всё это становится причиной развития вторичных (в том числе оппортунистических) инфекционных и/или онкологических заболеваний:
Продолжительность данной стадии зависит от заболевания, своевременного принятия мер и индивидуальных свойств иммунной системы.
5) Стадия СПИДа (терминальная стадия) — финальный этап течения ВИЧ-инфекции. Происходит развитие тяжёлых вторичных инфекций, угрожающих жизни, их генерализация (распространение по всему организму), развитие онкологических заболеваний и поражение центральной нервной системы, которое может сопровождаться неврологическими симптомами: растерянностью и забывчивостью, неспособностью сконцентрироваться, изменением поведения, головными болями, расстройствами настроения, нарушением координации и трудностями при ходьбе. [9]
При отсутствии своевременно назначенного специфического лечения стадия СПИДа наступает в среднем через 10-12 лет от момента инфицирования. [4]
Осложнения вич-инфекции
Осложнения ВИЧ-инфекции — это вторичные инфекции, развивающиеся на фоне иммунодефицита. К таким заболеваниям относятся:
Также могут возникнуть другие бактериальные и вирусные инфекции и онкологические заболевания. [4]
Диагностика вич-инфекции
Для диагностики ВИЧ-инфекции применяется специальный иммуноферментный анализ (ИФА). Он позволяет определить наличие антител к ВИЧ в организме человека. Соответственно, тест на ВИЧ будет достоверным только после завершения периода инкубации, т.е. после того, как организм выработает достаточное количество антител (не ранее четвёртой недели после заражения). У большинства людей тест будет достоверным через три месяца, однако для исключения ВИЧ-инфекции на 100% необходимо сдать анализ через 6 и 12 месяцев.
В случае положительного анализа на ВИЧ тот же образец крови исследуется в лаборатории ещё раз: если результат вновь положительный, то необходим тест другого типа — иммунный блоттинг. Положительный результат иммунного блоттинга (после положительного результата ИФА) достоверен на 99,9%, что является максимально точным для любого медицинского теста. Если же иммуноблот отрицательный, то делается вывод, что первый тест был ложноположительным, и ВИЧ у человека нет.
Результат иммуноблота может интерпретироваться как положительный, отрицательный или неопределенный (т.е. наличие в иммуноблоте как минимум одного белка к вирусу). Неопределённый результат может наблюдаться, если анализ сдан в период инкубации: заражение произошло не так давно, поэтому в крови пока находится немного антител к ВИЧ, но спустя некоторое время иммуноблот станет положительным. Также неопределённый результат может возникнуть при отсутствии ВИЧ-инфекции и наличии некоторых хронических заболеваний. В таком случае иммуноблот станет отрицательным, либо будет выявлена причина неопределённого результата.
Как считаю многие, анализ на ВИЧ-инфекцию сдаётся не при любом заборе крови. Однако данное исследование является добровольным для всех, кроме:
Люди, не относящиеся ни к одной из перечисленных категорий граждан, не сдают анализ на ВИЧ во время ежегодных профилактических медицинских осмотров, поэтому наличие медицинской книжки также не гарантирует отсутствие ВИЧ-инфекции.
Лечение вич-инфекции
В случае, если ВИЧ-инфекция обнаружена, человек встаёт на учёт в Центре по борьбе со СПИДом, где в дальнейшем наблюдается у врача-инфекциониста.
Лекарственного средства, которое могло бы полностью избавить от ВИЧ, в настоящее время нет. Однако, существуют препараты, значительно продлевающие жизнь и способные предупредить развитие СПИДа. Препараты для лечения показаны всем ВИЧ-инфицированным. Они предоставляются бесплатно после дообследования, назначаемого врачом-инфекционистом.
Препараты для лечения ВИЧ называются антиретровирусными (АРВ). Благодаря АРВ подавляется размножение вируса, в результате чего восстанавливается или не нарушается функция иммунной системы. ВИЧ-инфицированные пациенты, регулярно принимающие данные препараты, не способны передавать вирус даже при незащищённых половых контактах.
Особенность лечения ВИЧ-инфекции заключается в:
Для лечения используются хорошо изученные современные препараты, не оказывающие опасного токсического влияния на другие органы и системы, при условии соблюдения рекомендаций врача и своевременного обследования.
Прогноз. Профилактика
При раннем выявлении и своевременном начале специфического лечения продолжительность жизни ВИЧ-инфицированных людей может не уступать средней продолжительности жизни населения. Поэтому чрезвычайно важно как можно раньше начать наблюдение и лечение у специалиста.
Профилактика ВИЧ
К сожалению, вакцины от данной инфекции пока не существует.
Методами профилактики являются:
При положительном результате исследования на антитела к ВИЧ необходимо:
Хотелось бы отдельно отметить, что люди, живущие с ВИЧ, ничем не отличаются от других людей, кроме наличия в их организме вируса.
В последнее время среди ВИЧ-положительных пациентов гомосексуальной ориентации участились случаи развития анального рака под влиянием вируса ВПЧ. Для его профилактики институт СПИДа штата Нью-Йорк рекомендует пациентам проходить скрининг на анальную дисплазию. Он включает:
На развитие анального рака будет указывать боль и зуд в области ануса, кровянистые выделения, недержание кала, шишки и язвочки в перианальной зоне. Чтобы устранить осложнение, следует обратиться к колопроктологу.
Клетка памяти. Что мы знаем о резервуарах ВИЧ?
Уничтожение вируса иммунодефицита человека в так называемых резервуарах — проблема, решив которую, человечество наконец добьется полной победы над этой инфекцией. Что мы о них знаем, какие методы и подходы к работе с ними рассматривают ученые? И долго ли ждать прорыва? Об этом доклад доктора биологических наук, заведующей отделом общей вирусологии НИИ вирусологии им. Д.И. Ивановского МЗ РФ, прозвучавший на конференции PROHIV-2019. Публикуем его сокращенный пересказ.
Все мы хорошо знаем, что АРВТ достигла больших успехов, она весьма эффективна. Благодаря чему? Благодаря тому, что в клетке, в которой размножается вирус, есть специальные мишени для АРВТ-препаратов. Что это за мишени? Это ферменты вируса, отвечающие за проникновение в клетку, обратную транскрипцию, интеграцию и, наконец, созревание вирусных частиц.
Цель АРВТ — это стабильное снижение вирусной нагрузки. Каждый, кто лечит ВИЧ-инфекцию, хорошо знает, что сначала вирусная нагрузка снижается очень быстро. Практически за несколько недель она теоретически может упасть до неопределяемого уровня. Почему он достигается так быстро? Потому что на первом этапе применения АРВТ основной мишенью для лекарств являются СД4 лимфоциты, которые находятся, как мы понимаем, в кровотоке и легко доступны для препаратов.
Сейчас мы можем констатировать, что кроме уже названного этапа есть еще и второй этап снижения нагрузки. Этот этап связан с вирусом, попавшим в клетки-макрофаги. Лекарства сюда проникают намного хуже, намного медленнее. Тем не менее продолжение терапии позволяет несколько снизить вирусную нагрузку и в них.
Но что происходит с вирусной нагрузкой после того, как она стала неопределяемой? Чтобы ответить на этот вопрос, существуют так называемые ультрачувствительные методы. После того как вирусная нагрузка наконец выходит на плато, мы видим лишь единичные копии РНК вируса, но снизить ее еще больше уже не представляется возможным.
В момент так называемой «низкой виремии» возникает вопрос: откуда берется нагрузка? Варианта два: либо вирус где-то продолжает размножаться и его не достигает лекарство, либо существуют некие резервуары, в котором вирус хранится и время от времени выплескивается в организм.
На заре такого рода исследований первой мыслью, которая пришла в голову ученым, было увеличить интенсивность терапии, чтобы достичь полного уничтожения вирусных частиц в организме. Для этого были испробованы несколько вариантов, которые были связаны с повышением дозировок, с увеличением количества препаратов в схеме, с применением новых препаратов. Но ни один из перечисленных инструментов не привел к желаемым результатам. Это, очевидно, указывало на то, что размножение вируса не является главным источником остаточной виремии. Так, к настоящему времени сформировалось представление о так называемых резервуарах ВИЧ.
Спящие хелперы
Резервуары — это такие типы клеток либо зоны организма, в которых персистируют, как говорят, репликативно-компетентные вирусы. Что это означает? «Персистируют» — означает живут долго. «Репликативно-компетентный» означает способный к размножению, более того, могущий давать жизнеспособное вирусное потомство, то есть такие вирусы, которые могут заражать новые клетки.
по теме
Лечение
Как устроены ВИЧ и АРВТ? Объясняем на пальцах
Резервуары бывают двух видов: анатомические и клеточные. Анатомические резервуары — это такие зоны организма, куда не проникает либо плохо проникает лекарство. Таких зон в организме немало. Прежде всего, это центральная нервная система, лимфоузлы, это ЖКТ и костный мозг.
Главный клеточный резервуар — так называемые латентно-инфицированные клетки. Дело в том, что почти все клетки-мишени вируса, в первую очередь хелперные клетки, в определенный момент своей жизни, чтобы выполнить свою функцию, приходят в состояние активации, а после того, как они ее выполнили, дают себе команду апоптоза и погибают.
Но небольшая их часть переходит в так называемое «покоящееся состояние». Эти клетки составляют пул клеток иммунной памяти. Они практически прекращают свою жизнедеятельность. В них не происходит ни транскрипции, ни трансляции, а метаболизм поддерживается на очень низком уровне.
Если такая клетка в момент перехода из состояния активации в состояние памяти окажется инфицирована вирусом, то получается, что «провирус» в ней уже сформирован. Он находится в составе ее хромосомы, но до поры до времени не приводит к образованию новых вирусных частиц.
Клетки памяти сохраняют способность к делению. И делятся простым митозом. Часть из них погибает, но другие могут реактивироваться. Состояние их реактивации достигается разными способами. Иногда это химическое воздействие, иногда физическое, иногда какая-то дополнительная инфекция, которая оказывается в организме.
Как только латентно инфицированная клетка оказывается реактивирована, она начинает производить новые вирусные частицы. Что и дает ту самую остаточную виремию, о которой мы говорили выше.
Что делать с этим? Существуют две стратегии излечения. Одна из них называется стерилизующей терапией, или радикацией. Другая — функциональное излечение. Радикация — это полное уничтожение всех резервуаров в организме таким образом, чтобы в нем не осталось ни одной молекулы РНК и ни одной молекулы ДНК вируса.
Функциональное излечение предполагает, что вирус в организме остается в очень небольшом количестве, но при этом излечивающее воздействие приводит к тому, что последующая терапия такому пациенту больше не требуется.
Два пути
Первый случай радикации, о котором мы все уже слышали, — это, конечно, так называемый Берлинский пациент.
Для того, чтобы вирусу присоединиться к клетке, ему нужны два рецептора: один СД4, а другой CCR5. Полноценный CCR5 рецептор кодирует ген CCR5 дикого типа. Но бывает, что в составе этого гена встречается делеция, то есть потеря части хромосомы. Она называется дельта32. В этом случае у человека формируется неполноценный рецептор, а вирус не может присоединиться к клетке-мишени.
Люди с такой мутацией встречаются, и если эта мутация у них в гомозиготе, то они полностью защищены от инфицирования ВИЧ — за редкими исключениями.
Берлинскому пациенту, который был гетерозиготен по дельта32, в результате острого миелогенного лейкоза пришлось сделать полное облучение организма и химиотерапию. АРВТ временно пришлось отменить. После переливания стволовых клеток дельта32 двенадцать лет назад в его организме не удалось встретить ни РНК, ни ДНК вируса.
Так человечество столкнулась с первым случаем полного излечения от ВИЧ-инфекции.
Уже в этом году, летом, мы услышали еще о двух таких пациентах. У них ситуация была попроще. Лимфома Ходжкина. Лечение было менее тяжелым, им не делали полного облучения, да и химиотерапия была не такая тяжелая. Однократно каждому из них перелили стволовые клетки. В итоге: Лондонский пациент находится в ремиссии уже более двух лет, а Дюссельдорфский — приближается к году.
Считается, что это тоже случаи полного излечения. Но для всех пациентов такая терапия не подойдет. Несмотря на то, что инициатива продолжается и существует целая программа, которая собирает коллекцию стволовых клеток дельта32. На данный момент собрана коллекция потенциальных доноров: около 40 тысяч человек. Безусловно, не всем удастся подобрать донора.
Модификация этого подхода — генная терапия, которая предполагает, что можно взять клетки у человека, уже инфицированного ВИЧ, и вырезать ген CCR5, получив клетки, аналогичные стволовым клеткам дельта32.
В целом, теоретически, это вполне возможно сделать. Такие технологии недавно были использованы на мышах. Более того, в этом году подобную геннотерапевтическую манипуляцию, хоть эксперимент и был воспринят научным сообществом неоднозначно, провели на человеческих эмбрионах. Это знаменитые китайские близнецы.
Впрочем, тут же, появилось несколько публикаций о том, что отсутствие гена CCR5 не совсем безразлично для организма, и люди, у которых такой рецептор отсутствует, подвержены многим другим рискам.
по теме
Лечение
«Пятьдесят лет с ВИЧ». Насколько человечество близко к исцелению?
Альтернатива и тому, и другому — стратегия, которая называется «kick-and-kill». Она предполагает, что можно разбудить спящие клетки-резервуары и уничтожить вместе с вирусом.
Здесь речь идет о реактивации латентных клеток, чтобы сделать их доступными для АРВТ. На первый взгляд, идея очень хорошая, но на пути этой стратегии уже встретилось немало трудностей. Хотя в некоторых экспериментах объем резервуаров все-таки удавалось снизить, вирусная нагрузка остаточной виремии у пациентов сохранилась. То есть уничтожить вирус в организме врачам так и не удалось.
Основная проблема связана с тем, что резервуары неоднородны. Все клетки в организме, которые имеют на своей поверхности соответствующие рецепторы, могут быть инфицированы. Но они все разные. И разработать препарат, который одинаково работал бы со всеми ними, ученым еще не удалось.
Лабиринт из тупиков
Еще одна альтернатива — стратегия «block-and-lock». Если в ядре клетки уже присутствует провирусная ДНК, то для того, чтобы началась продукция вирусных частиц, на первом этапе должна произойти транскрипция. Должны образоваться вирусные РНК. Но если этот этап блокировать, инфицированная клетка, даже оказавшись активирована, не произведет новых вирусов.
Как этого добиться? На эту тему сейчас проходят исследования. Некоторые из них касаются ограничения процесса инициации транскрипций, в котором принимает участие белок, носящий название Tat. Это самый главный вирусный трансактиватор транскрипций. А также клеточные белки, которые связаны с этим же этапом.
Некоторые связаны с идеей блокирования окружения провирусной ДНК и изменением структуры хроматина. Новые препараты, работающие по этой технологии, так называемые ингибиторы фактора LEDGF/p75, скоро будут апробированы в клинике.
Итак, проблема полного излечения ВИЧ волнует сейчас очень многих ученых, но мы находимся в начале этого сложного лабиринта, который рано или поздно приведет нас к искомой цели.
В каком состоянии находится проблема на данный момент в целом? В этом лабиринте, как вы понимаете, много тупиков. И некоторые из этих тупиков уже пройдены, а это тоже очень важно. Важно понимать, куда ходить не стоит, потому что по мере того, как ошибочные решения будут исключаться, мы, наверное, найдем правильный ответ и придем к искомой цели.
Лично мне кажется, что сейчас настает очень интересный момент. Накопление новых данных идет с огромной скоростью. Во всем мире еженедельно публикуется множество исследований и многие выглядят очень и очень перспективно. А стало быть, в ближайшие несколько лет нам можно ожидать прорыва.