Что такое синдром Шёгрена? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бабинцевой Марины Юрьевны, эндокринолога со стажем в 27 лет.
Определение болезни. Причины заболевания
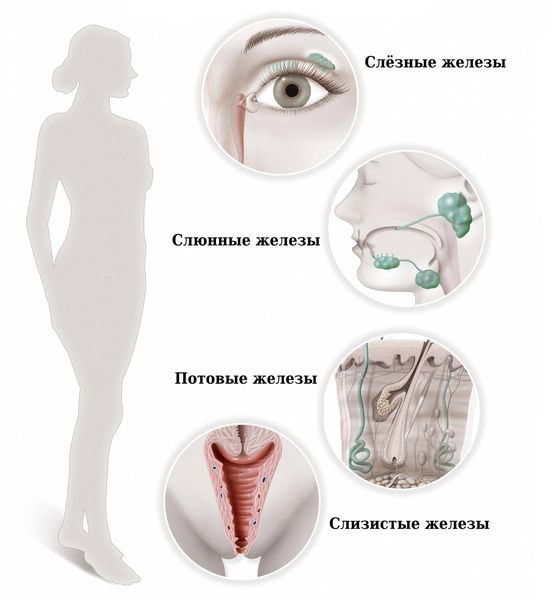
Синдром Шёгрена (Sjogren’s syndrome) — это аутоиммунное системное заболевание соединительной ткани, при котором поражаются железы внешней секреции: преимущественно слёзные и слюнные, а также потовые, сальные, слизистые и др. Характерными признаками болезни являются сухость глаз, полости рта и кожи.
Синонимы: болезнь Шёгрена, синдром Съегрена, «сухой» синдром, ксеродерматоз, синдром Предтеченского — Гужеро — Шёгрена.
Синдром Шёгрена бывает первичным и вторичным:
Распространённость
Причины развития синдрома Шёгрена
Наличие похожей патологии слюнных желёз у родственников (братьев и сестёр, родителей или детей) указывает на генетическую предрасположенность к развитию болезни Шёгрена.
Факторы риска развития синдрома Шёгрена
Симптомы синдрома Шёгрена
Проявления синдрома Шёгрена разнообразны. Среди них можно выделить две группы симптомов:
Симптомы, связанные с поражением желёз
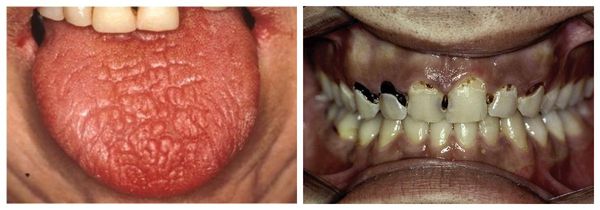
Нарушение работы слюнных желёз проявляется сухостью во рту (ксеростомией). Это второй постоянный симптомом «сухого» синдрома. Ещё до начала клинически выраженной картины болезни Шёгрена можно заметить сухость губ, «заеды» в уголках рта и стоматит. Со временем уменьшается количество слюны и появляется сухость во рту. Сначала она беспокоит только при волнении и физической нагрузке, затем постоянно. Больному приходится запивать сухую пищу и увлажнять рот во время разговора.
Поражение подслизистых желёз трахеи и бронхов вызывает у пациентов сухой лающий кашель.
Поражение потовых и сальных желёз — причина сухости кожи при болезни Шёгрена. Нарушение работы потовых желёз наружных половых органов вызывает жжение, зуд, иногда интенсивные жгучие боли.
Поражение желудочно-кишечного тракта часто становится причиной боли в животе различной локализации, тошноты, отрыжки воздухом с тухлым запахом и др. [1] [2]
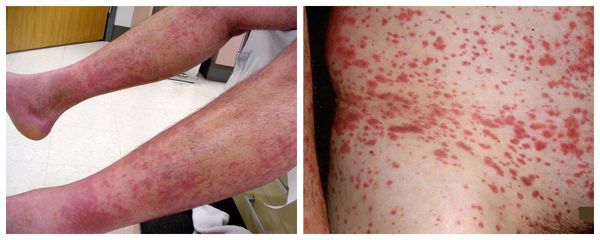
Внежелезистые системные проявления
Патогенез синдрома Шёгрена
Механизм развития синдрома Шегрена неясен. Считается, что под воздействием стресса или каких-либо факторов окружающей среды у генетически предрасположенных людей нарушается работа иммунной системы, что и приводит к развитию болезни.
Например, в слюнных железах под воздействием провоцирующих факторов повышается проницаемость клеточных мембран. Из-за этого секрет, который образуется в клетках желёз, не поступает в проток, он переполняет клетку и проникает через её оболочку в интерстициальную (соединительную) ткань. Белок, содержащийся в секрете, попадая в интерстициальную ткань, воспринимается организмом как чужеродный и вызывает образование антител против ткани железы.
Классификация и стадии развития синдрома Шёгрена
Классификация болезни Шёгрена по течению:
1. Подострый вариант. Он начинается с повышения температуры до 38–40 ˚C и симптомов одностороннего или двустороннего паротита (воспаления околоушных слюнных желёз). Пациент при этом чувствует дискомфорт, распирание или боль в проекции околоушных слюнных желёз. Эта область припухает, а при выраженном воспалительном отёке железы значительно увеличиваются в размерах.
Форма лица становится грушевидной. Кожа над поражённой слюнной железой туго натянута, лоснится, кожные складки не образуются или образуются с трудом. Также характерно выраженное поражение суставов: чаще воспаляются мелкие суставы кистей, но иногда процесс затрагивает и крупные суставы (коленные, плечевые, локтевые). Воспаление сопровождается сильной болью в суставах.
В анализах крови наблюдается увеличенная скорость оседания эритроцитов (СОЭ), повышенный уровень определённых иммуноглобулинов (антител), снижение количества лейкоцитов и высокие титры ревматоидного фактора. Подострый вариант болезни чаще развивается у молодых пациентов.
Нарушения параметров крови выражены умеренно, системные проявления, такие как регионарная лимфоаденопатия (увеличение лимфатических узлов), поражение почек и другие, отмечаются крайне редко. Этот вариант течения синдрома Шёгрена чаще встречается у пациентов старше 50 лет.
По стадиям развития:
По степени активности:
Осложнения синдрома Шёгрена
Инфекционные осложнения. Из-за сухости полости рта, носоглотки, слизистых оболочек глаз и изменения состава слюны и слёзной жидкости присоединяются бактериальные, герпесные или грибковые кератоконъюнктивиты, синуситы, трахеобронхиты и пневмонии.
Злокачественные проявления:
Поражение центральной и периферической нервной системы часто бывает опасно жизнеугрожающими осложнениями. Они возникают у 2–4 % больных. К таким осложнениям относятся острое нарушение мозгового кровообращения (инсульт), поражение ЦНС по типу рассеянного склероза, поперечный миелит, тяжёлый цереброваскулит и др. [10]
Диагностика синдрома Шёгрена
Пациент с начальными признаками болезни Шёгрена может оказаться на приёме у стоматолога, офтальмолога, оториноларинголога, терапевта и ревматолога. Диагностика основана на выявлении у больных одновременного поражения глаз и слюнных желёз, а также лабораторных признаков аутоиммунного заболевания.
Сбор жалоб и осмотр
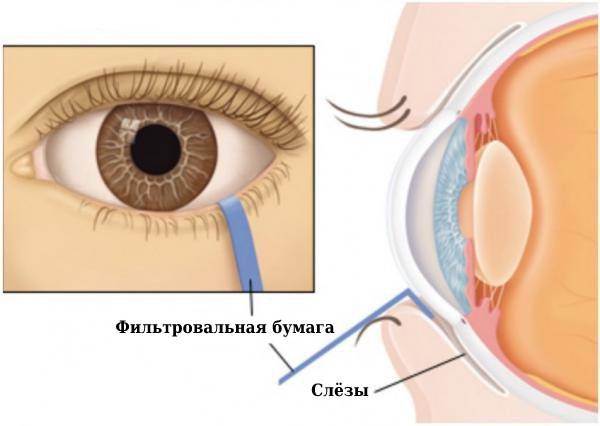
К типичным офтальмологическим симптомам болезни относят постоянную сухость глаз на протяжении трёх месяцев и более, ощущение песка в глазах, необходимость использовать искусственные слёзы три раза в день и чаще.
При осмотре врач отмечает сухость склеры и конъюнктивы, расширение сосудов конъюнктивы, белые или желтоватые выделения крошковатого вида или густой вязкой консистенции. Из-за уменьшения слёз развивается сухой конъюнктивит или блефароконъюнктивит с дистрофией и изъязвлением слизистой оболочки глаз.
Состояние слюнных желёз сначала определяют с помощью сиалометрии, когда врач собирает слюну пациента в пробирку, затем оценивает её количество. Также слюнные железы исследуют с помощью инструментальных методов диагностики.
Инструментальная диагностика
Сиалография. Это рентгенконтрастное исследование слюнных желёз. При синдроме Шёгрена сиалография показывает характерные признаки: изменение строения долек и повреждение протоков железы. Также определяется выход контрастного вещества в ткань желёз за пределы протоков. Поэтому контуры протоков нечёткие, вокруг них определяется «облачко» контрастной массы, проникшей в окружающие ткани.
УЗИ и МРТ. Эти методы позволяют оценить структуру желёз и внутрижелезистых лимфоузлов, контролировать динамику лечения и отличить болезнь от опухоли слюнных желёз.
Лабораторная диагностика
В ходе лабораторной диагностики выполняют:
Дифференциальная диагностика
Лечение синдрома Шёгрена
Лечение проводится в зависимости от наличия железистых и внежелезистых проявлений и иммуновоспалительной активности заболевания.
В первую очередь всем пациентам с синдромом Шёгрена рекомендуется немедикаментозное лечение:
Лечение железистых проявлений
При поражении слюнных желёз используют заменители слюны. Их изготавливают на основе муцина и метилцеллюлозы, они смазывают и увлажняют полость рта, облегчая состояние пациента.
Часто удаётся стимулировать остаточную функцию слюнных и слёзных желёз, для этого используются агонисты М1 и М3 мускариновых рецепторов: Пилокарпин или Цевимелин.
Лечение внежелезистых проявлений
Основой лекарственной терапии болезни Шегрена являются две группы препаратов:
Они назначаются при системных проявлениях заболевания и высокой активности процесса, подтверждённой лабораторными показателями.
Пациентам с васкулитом назначается Циклофосфан в комбинации с Преднизолоном. Дозы подбираются в зависимости от тяжести внежелезистых симптомов. Доза Преднизолона при тяжёлых угрожающих жизни системных проявлениях увеличивается.
У пациентов с такими симптомами может использоваться также пульс-терапия Преднизолоном или комбинированная пульс-терапия Преднизолоном и Циклофосфаном. При этом в начале лечения применяются значительные дозы препаратов, затем они снижаются и пациент длительно получает умеренные или низкие дозы. Пульс-терапия позволяет уменьшить ежедневную дозу пероральных глюкокортикоидов и цитостатиков и избежать осложнений, возникающих из-за их длительного применения. Длительный приём глюкокортикоидов может привести к стероидному диабету, язве желудка или двенадцатиперстной кишки, повышению артериального давления и др. Цитостатики уменьшают количество нейтрофилов и тромбоцитов, токсично влияют на сердце, печень и почки. Кроме того, применение препаратов обеих этих групп снижает иммунитет и повышает риск присоединения инфекции.
Экстракорпоральная терапия — это метод интенсивной терапии болезни Шёгрена. К ней относится гемосорбция, криоаферез, плазмоферез, двойная фильтрация плазмы, которая проводится одновременно с пульс-терапией. Эти методы основаны на очистке крови и плазмы от циркулирующих иммунных комплексов и агрессивных аутоантилел вне тела пациента на специальном оборудовании.
Абсолютные показания для экстракорпоральной терапии:
Прогноз. Профилактика
Кроме нарастающего поражения слюнных и слёзных желёз со временем прогрессируют и внежелезистые проявления. Причиной летального исхода может быть генерализованный васкулит, опухоли (чаще всего желудочно-кишечного тракта) и аутоиммунные пацитопении (одновременное снижение лейкоцитов, эритроцитов и тромбоцитов), реже интерстициальный нефрит с почечной недостаточностью, острый инфаркт миокарда и острое нарушение мозгового кровообращения.
Факторы риска неблагоприятного исхода при болезни Шёгрена: анемия, лейкопения или тромбоцитопения, генерализованная лимфаденопатия, спленомегалия (увеличение селезёнки), значительное увеличение околоушных слюнных желёз, полиневропатия, криоглобулинемическая пурпура. Эти факторы могут возникать одновременно, или один фактор может предшествовать другому.
Профилактика синдрома Шёгрена
Первичная профилактика направлена на предотвращение болезни. Так как этиология болезни Шёгрена неизвестна, методов первичной профилактики не существует.
Вторичная профилактика проводится, чтобы предотвратить прогрессирование болезни и развитие осложнений. Для этого необходимо своевременное и адекватное лечение. Чтобы начать лечение как можно раньше, пациенту нужно обратиться к врачу при первых признаках болезни: сухости глаз и полости рта, рецидивирующей или постоянной припухлости в области слюнных желёз. Насторожить должен также прогрессирующий множественный пришеечный кариес.
Урогенитальный синдром: гинекологические симптомы часто появляются первыми
Дайджест Академии акушерства и гинекологии №1/2016
С проявлениями урогенитального синдрома, в частности, гиперактивностью мочевого пузыря (ГМп) сталкивается большинство женщин, дост игнув возраста менопаузы. О том, как на эту проблему, находящуюся на стыке нескольких медицинских специальностей, смотрят гинекологи, мы побеседовали с ведущим гинекологом-эндокринологом, руководителем поликлинического отделения ГБУЗ МО МОНИИАГ, врачом высшей квалификационной категории по специальности «акушерство и гинекология», доктором медицинских наук, профессором Верой Ефимовной Балан.
– Вера Ефимовна, с какими трудностями для гинеколога сопряжено лечение урогенитального синдрома?
Первое, что стоит отметить, – у этого симптомокомплекса или синдрома очень сложный патогенез. сегодня изучают множество молекулярно-генетических аспектов, но для практической медицины результаты этих исследований мало что меняют и набор препаратов, которыми мы лечим, очень ограничен. вся терапия, к сожалению, симптоматическая, патогенетической терапии гМп пока нет, и наша основная задача сделать так, чтобы пациент как можно лучше переносил лечение. Мы не можем вылечить гиперактивный мочевой пузырь, понятно, что это лечение практически пожизненное. надо найти какую-то середину, чтобы осложнений было меньше, ремиссии были дольше и так далее.
– А насколько эта проблема исследована и как давно является предметом пристального изучения?
Урогенитальная атрофия, думаю, существует с тех пор, как продолжительность жизни женщины стала превышать возраст наступления менопаузы. так было не всегда, природа поступала следующим образом: перестала женщина рожать, где-то близко к менопаузе и природа убирала эту женщину из популяции. А когда увеличилась продолжительность жизни, появились симптомы, которые мы сегодня называем менопаузальными, в том числе-урогенитальная атрофия. пристальный интерес к этой проблеме появился только в конце 70-х – начале 80-х годов. обусловлено это тем, что недержание мочи связали со старением и эстрогенным дефицитом. кроме того, именно в начале 80-х годов появился эстриол, то есть тот гормональный препарат, который перевернул представления гинекологов об урогенитальной атрофии. хотя всерьёз гинекологи начали заниматься этим вопросом только в самом конце 80-х – начале 90-х годов. терминология с годами изменялась: чаще всего говорили о сенильном кольпите, хотя воспаления, как правило, в этой ситуации нет. говорили и говорят «атрофический кольпит», «сенильный» и «атрофический» уретрит, «тригонит», «уретральный синдром». на сегодня наиболее ёмкие термины – «урогенитальная атрофия» и «урогенитальные расстройства». в МкБ10 есть только одна позиция, которая отражает ситуацию: N95.2, «постменопаузальный атрофический вагинит».
– А в чём причина таких терминологических расхождений?
Сегодня терминология меняется, и, гинекологи об этом знают. я бы не сказала, что она изменилась кардинально, это только попытка смены терминологии нашими и международными ассоциациями. эксперты сочли, что в термине «вульвовагинальная атрофия», которым очень часто пользуются на западе, абсолютно не рассмотрены мочевые расстройства (у нас они рассматриваются очень давно), и предложили перейти к термину «генитоуринарный синдром». наши термины: «урогенитальная атрофия» и «урогенитальный синдром» – существуют в России приблизительно с 1998 года. почему терминология меняется? термин «атрофия» подразумевает окончательную потерю функциональности. кроме того, в сМи с трудом приживается слово «влагалище». и «вульвовагинальная атрофия», как я уже сказала, не охватывает мочевые нарушения: ургентные или императивные позывы, дизурию, рецидивирующие инфекции. гинекологические симптомы появляются первыми, но я всегда говорю о том, что они просто ощущаются быстрее: женщина в первую очередь обращает внимание именно на гинекологические симптомы.
– Как бы ни называлось это расстройство, давайте разберёмся, чем оно, в первую очередь, опасно.
Давайте начнём с того, что же такое урогенитальные расстройства. это комплекс вагинальных и мочевых симптомов, развитие которых является осложнением атрофических процессов в эстроген-зависимых тканях и структурах нижней трети мочеполового тракта. при этом атрофические изменения в урогенитальном тракте – один из основных «маркеров» эстрогенного дефицита. согласно нашим собственным данным, почти у 20% пациенток они появляются одновременно с яркими проявлениями климактерического синдрома. женщина быстрее обращает внимание на приливы и потливость, они ей очень мешают, и это заметно окружающим. А вот урогенитальная атрофия развивается исподтишка, не сразу начинает мешать, и обращают внимание на этот симптом, в основном, через 5 лет или больше, когда он проходит уже не в лёгкой, а в тяжёлой форме и очень сильно снижает качество жизни.
– Как высока распространённость проблемы в целом по популяции и есть ли какие-то группы пациентов, требующие особого отношения?
Частота возникновения урогенитального синдрома колеблется от 13% в перименопаузе до 60% в постменопаузе длительностью более 5 лет. наибольшие частота и выраженность наблюдаются у курящих женщин и у пациенток, получающих лечение по поводу рака молочной железы. это особая группа пациенток, здесь мы связаны по рукам и ногам. даже локальные эстрогены нам не всегда разрешают назначать онкологи, но этот момент сейчас пересматривается в международном сообществе, и считается, что у локальных препаратов не должно быть тех же противопоказаний, что у системных. таким образом, онкологические заболевания, включая рак молочной железы, никак не должны относиться к противопоказаниям, потому что локальные эстрогены системным действием не обладают.
– С какими проявлениями синдрома чаще всего сталкиваются гинекологи?
Для начала, это вагинальные симптомы, в числе которых сухость и зуд во влагалище, диспареуния (болезненные ощущения во время полового акта), рецидивирующие вагинальные выделения (но не инфекционного рода), опущение стенок влагалища, кровоточивость вагинальной слизистой (это связано с тем, что при эстрогеновом дефиците начинает, в первую очередь, страдать кровоток) и сексуальные нарушения. другая сторона медали – это симптомы цистоуретральной атрофии или мочевые симптомы. здесь нежелательно применять, например, понятие «атрофический цистит», здесь нет воспаления, это симптомы, связанные с атрофией уротелия, который делается крайне чувствительным к попаданию даже небольшого количества мочи в мочевой пузырь. здесь важны следующие симптомы: частые дневные и ночные мочеиспускания, дизурия, рецидивирующие инфекции мочеполового тракта, цисталгия, неотложные позывы к мочеиспусканию, ургентное, стрессовое и смешанное недержание мочи. если эти симптомы появляются вместе с последней менструацией, то есть вступлением женщины в менопаузу или через несколько лет после, то мы относим их к мочевым проявлениям урогенитальной атрофии, а если у женщин более молодого возраста (чаще всего после родов), мы не говорим об этом, но известно, что тяжесть симптомов значительно усугубляется в постменопаузе, если ранее пациентка не задумывалась о лечении.
– Две эти группы симптомов чаще проявляются по отдельности или вместе?
У трети пациенток в постменопаузе могут быть изолированные проявления генитоуринарного синдрома, однако по последним данным у 65–100% женщин симптомы вагинальной и цистоуретральной атрофии сочетаются. изолированные симптомы мы можем, конечно, лечить без системной менопаузальной гормонотерапии, но к сожалению, две трети больных и более сочетают урогенитальную атрофию и менопаузальный синдром с остеопорозом и высоким риском сердечнососудистых заболеваний. тогда нам приходится думать о системной терапии или сочетании её с локальными препаратами.
– Расскажите, пожалуйста, немного о диагностике расстройства.
Для начала необходимо задать пациентке простые вопросы: сколько раз в день она мочится? если пациентка отвечает «10–12», у нас в голове срабатывает соответствуюий сигнал. следующий вопрос: сколько раз вы встаёте ночью? следом за ним: если вам хочется в туалет, вы можете доделать то, чем были заняты: к примеру, суп доварить или допечатать какой-то текст? если женщина говорит «нет, я вынуждена всё бросить и бежать в туалет», – значит, у этой пациентки наверняка есть гМп, и мы должны дальше обследовать её. хорошо помогают дневники мочеиспускания, однако часто наши пациентки не любят много записывать. тогда приходится задавать дополнительные вопросы, чтобы получить чёткую количественную оценку этого симптомокомплекса.
– Мы уже выяснили, что сама проблема существует достаточно долго и, возможно, эволюционно обусловлена. А как давно появились лекарства, способные облегчить её проявления?
Сходность вагинального эпителия и уротелия, а также способность уротелия синтезировать гликоген была описана ещё в 1947 году. в следующем, 1948 году описана чувствительность уротелия к эстрогену, а в 1957 году показана реакция уротелия на введение эстрогенов у женщин в постменопаузе. то есть, вероятно, ещё ранее было необходимо соединить взгляды урологов и гинекологов на проблему. в те времена, к сожалению, не было препаратов, которые можно было бы очень долго использовать для лечения любых проблем в урогенитальном тракте, связанных с атрофическими изменениями. патогенез связан с дефицитом эстрогенов, первой развивается ишемия во всех структурах урогенитального тракта, только через несколько лет снижается пролиферация уротелия и вагинального эпителия,. страдают коллагеновые структуры урогенитального тракта и мышечные структуры уретрального тракта, развиваются симптомы вагинальной и цистоуретральной атрофии, стрессовое, ургентное и смешанное недержание мочи. профессор питер смит в 1990 году за открытие рецепторов в урогенитальном тракте у женщин получил нобелевскую премию, он показал количественно, сколько же рецепторов находится в различных структурах урогенитального тракта. если мы сравнивать с маткой, где их100%, то во влагалище локализуется 60%, а в уретре и мочевом пузыре 40%. в мышцах тазового дна и коллагеновых структурах – только 25%, поэтому для мышц необходимы не только лекарственные препараты и менопаузальная гормонотерапия, но и обязательная тренировка мышц тазового дна, поведенческая терапия.
Стоит также упомянуть о локализации рецепторов к половым гормонам в урогенитальном тракте. если во влагалище есть и а, и в рецепторы эстрогена, в промежности и нижней трети влагалища доминируют андрогеновые рецепторы, в мочевом пузыре и уретре – в рецепторы эстрогена, поэтому этим структуры могут чуть позже отвечать на воздействие эстрогенов, чем, например, стенки влагалища. для того, чтобы полностью восстановить структуры урогенитального тракта, гормонотерапия должна использоваться на первом этапе не менее трех месяцев. сегодня изучены и найдены новые формы эстрогеновых рецепторов в вагинальных биоптатах и, соответственно, рассматриваются другие препараты, кроме эстрогенозаместительной гормонотерапии, это тоже очень интересно. Много говорят о селективных эстроген-рецепторных модуляторах.
– К примеру, первый курс пройден, пациентка три месяца исправно лечилась. что произошло за это время?
Через три месяца под влиянием эстрогенов восстанавливается кровоток, и это, наверное, основной результат терапии. возобновляются процессы пролиферации в уротелии и вагинальном эпителии, а также восстанавливается популяция лактобацилл, уровень PH нормализуется сократительная активность миофибрилл влагалищной стенки, детрузора и уретры, улучшается иннервация урогентиального тракта. кроме того, повышается синтез а, и в-адренорецепторов, а также мускариновых рецепторов, восстанавливается чувствительность к норадреналину и ацетилхолину. также улучшается эластичность коллагена за счёт деструкции старого и синтеза нового. вдобавок, отмечается существенное влияние на локальный иммунитет, который защищает женщину от восходящей инфекции и абсолютно эстроген-зависим.
– В чём на сегодня преимущество назначения локальных эстрогенов?
По результатам предпринятого масштабного исследования, препараты гормонотерапии системного воздействия в 20–45% случаев не оказывают системного воздействия на симптомы урогенитальной атрофии. немедикаментозная терапия, в свою очередь, по эффективности приближается к плацебо, а вот локальные формы эстрогенов оказывают минимальное системное воздействие и приводят к регрессу атрофических изменений в урогенитальном тракте.
– Можно ли выделить наиболее эффективные из них?
Мета-анализ 15 рандомизированных исследований с участием 3 тыс. женщин показывает, что эстриол остаётся самым эффективным и безопасным средством, поскольку у него практически нет системной абсорбции, и это очень важно для наших пациенток, перенесших рак молочной железы. примером препарата, содержащего эстриол, может являться «овестин» или его аналого « овипола» в форме свечей или крема.
– А проводились ли сравнительные исследования эффективности комбинированной и моно-терапии ГМп?
Наши последние, 2016 года, данные свидетельствуют о том, что как сочетанная терапия, так и монотерапия М-холинолитиками эффективны в отношении симптомов гМп. через 3 месяца лечения частота поллакиурии снижается в 8 раз, ноктурии – в 4,5 раза, ургентности – в 4,4 раза, а ургентного недержания мочи – в 3 раза. при этом важным преимуществом сочетанной терапии является более выраженное снижение основного симптома гМп – ургентности (в 1,7 раз) и уменьшение частоты рецидивов в 2,5 раза. то есть женщина имеет возможность без терапии М-холинолитиками, а только с локальными эстрогенами продержаться до следующего курса в два с половиной раза дольше, чем при монотерапии.
– Можно ли выделить факторы риска относительно этого расстройства и каким-то образом воздействовать на них?
По определению профессора евгения леонидовича вишневского, гиперактивный мочевой пузырь – хроническое рецидивирующее заболевание, в основе которого лежат процессы ишемии и сосудистый стресс. соответственно, основными факторами риска тут являются воспалительные заболевания (к примеру, рецидивирующий цистит), беременность, неврологические заболевания и, собственно, климактерический период. если мы возьмём популяционные данные, то мы увидим, что в 20% случаев нарушения мочеиспускания приходятся на женщин репродуктивного возраста, хотя мы и привыкли связывать эту проблему со старением. нами проведено о крупное исследование относительно нарушений мочеиспускания у беременных женщин. выяснилось, что во время беременности нарушений мочеиспускания нет только у 20% пациенток. чаще всего симптомы связывают с ростом матки, нарушениями гормональных взаимоотношений, – причин может быть много. изучив структуру нарушений, мы увидели, что доминирует гиперактивный мочевой пузырь. до недавнего времени это считалось практически нормой. дальше мы посмотрели, что происходит после родов. сравнив картину во время беременности и через 4 месяца после родоразрешения, мы увидели, что беременность – это действительно очень высокий фактор риска нарушения мочеиспусканий. у большинства женщин они действительно проходят, но у 15,7% остаются. в большинстве случаев это симптомы гМп. таким образом, нарушения, возникшие при беременности, могут сохраняться на всю оставшуюся жизнь. далее они могут проходить на какое-то время или обостряться, а вот после менопаузы уже развиваются стойкие формы нарушений мочеиспускания.
– С какими сложностями, помимо самих симптомов, могут сталкиваться пациентки?
К сожалению, далеко не все препараты, используемые при лечении гМп и урогенитального синдрома, дотируются государственно. если на западе женщина, как правило, оплачивает только гигиенические средства, и то частично, то у нас затраты на лекарства могут составлять половину средней пенсии. при выборе лечения нужно учитывать, что препараты не всегда хорошо переносятся, дорого стоят, и надо найти врача, который правильно подберёт терапию, сможет подобрать Мхолинолитик индивидуально. одни препараты позволяют манипулировать дозировкой, другие – нет, но всегда выбирается минимально эффективная доза, чтобы женщина как можно дольше могла получать терапию. к примеру, очень важным стало появление на нашем рынке «уротола» дженерика толтеродина. «уротол» один из самых доступных препаратов для наших женщин. несмотря на большое количество побочных действий у всех препаратов этого ряда, есть только одно абсолютное противопоказание – глаукома.
– Каким образом действует такое лекарство?
В механизме действия важно только одно: пока мы даём препарат, он блокирует действие ацетилхолина на мускариновые рецепторы и предотвращает сокращение детрузора. если прекратить прием, все симптомы возвращаются. пока не создан препарат, способный вылечить гиперактивный мочевой пузырь « уротол» значительно снижает количество мочеиспускания и эпизодов ургентного недержания мочи. другой очень важный момент: согласно рекомендациям Международной Ассоциации по менопаузе, симптомы вагинальной атрофии легко купируются эстрогенами, и препараты антимускаринового действия в комбинации с локальными эстрогенами являются терапией первой линии у женщин с гМп в климактерии. но при этом ни системная, ни локальная гормональная терапия не являются профилактикой стрессового недержания мочи.
– С вашей точки зрения, лечение этого расстройства является задачей, в первую очередь, гинеколога или уролога?
Гиперактивный мочевой пузырь – это проблема абсолютно междисциплинарная, смысла нет её делить между гинекологами и урологами. к кому женщина пришла, у того она и будет лечиться. кроме того, важна роль неврологов, травматологов и врачей общей практики. основной момент лечения – назначение мхолинолитиков и менопаузальной гормонотерапии. какой она будет, зависит от женщины, но здесь должна обязательно присутствовать локальная терапия эстрогенами. на сегодня это даже не оспаривается.
Беседовала В.А. Шадеркина