Что такое строение атома в химии 8 класс
Ключевые слова конспекта: строение атома, элементарные частицы, протоны и электроны в атомах, атомный номер, массовой число, число нейтронов, нуклид, изотопы, ионы, катионы, заряд иона.
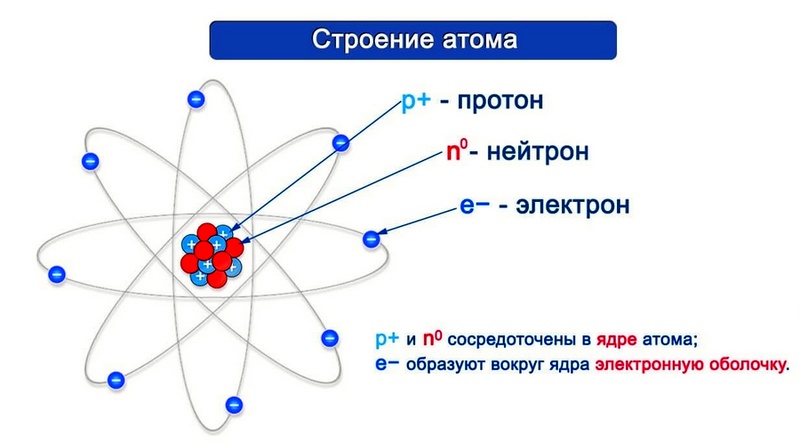
Согласно модели Резерфорда каждый атом состоит из находящегося в его центре ядра и электронной оболочки. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре. Электроны движутся вокруг ядра. Число электронов атома равно положительному заряду ядра.
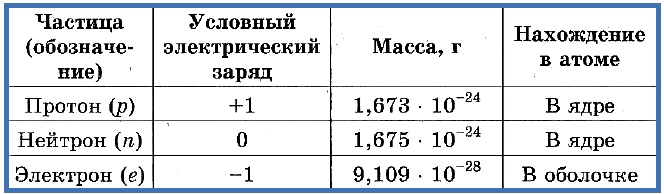
Элементарные частицы — это протоны, электроны и нейтроны, из них состоят все атомы.
Таблица 1. «Элементарные частицы атома»
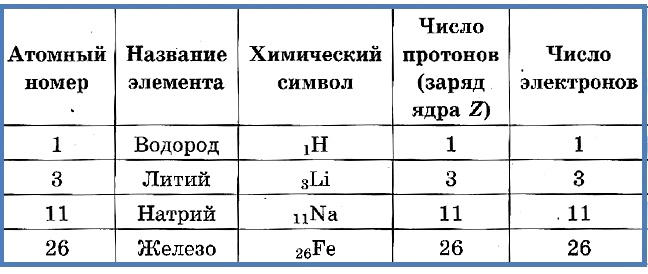
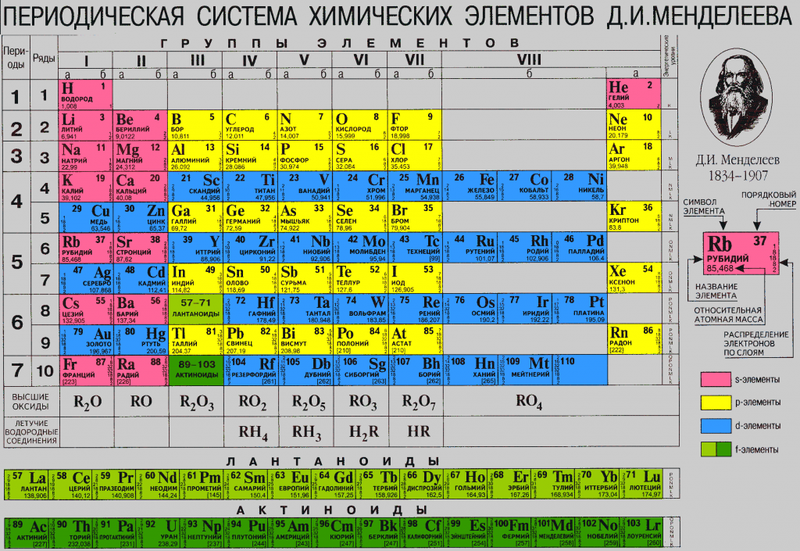
Число протонов разное у атомов различных видов, оно определяет заряд ядра атома и равно атомному номеру элемента в таблице Менделеева. Поскольку атом — электро-нейтральная частица, число электронов в нем равно числу протонов.
Таблица 2. «Протоны и электроны в атомах»
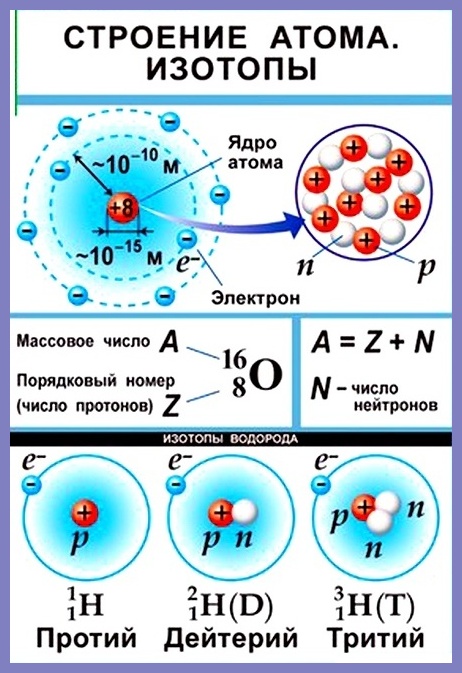
Атомный номер указывают слева внизу от символа элемента, например: 1Н, 26Fe. Обозначение атомного номера — прописная латинская буква Z.
Массовое число атома А — это сумма чисел его протонов и нейтронов в ядре. Массовое число указывают слева вверху от символа элемента или добавляют к названию элемента через дефис, например: 23 Na или натрий-23.
Массовое число кислорода, А( 16 О) = 16 = (8р + 8n).
Число нейтронов N в ядре атома определяют по формуле: N = A — Z. Например, для атома натрия с массовым числом 23, 23 Na: А = 23, Z = 11, N = А – Z = 23 — 11 = 12.
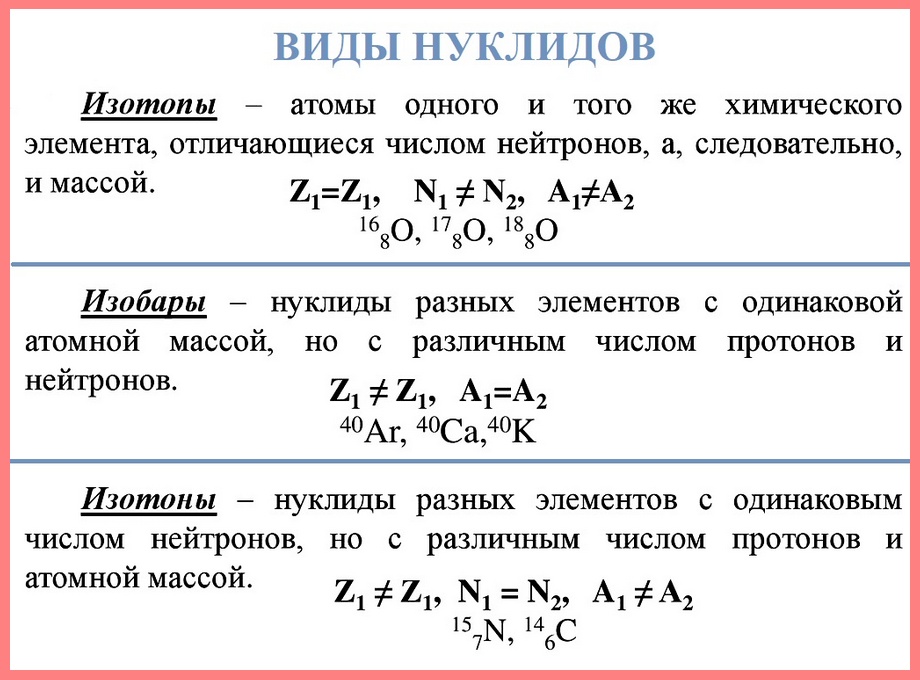
Нуклид — это вид атомов с определенным числом протонов и нейтронов в ядре. Например, в природе встречается три вида нуклидов кислорода: 16 О, 17 О и 18 О.
Изотопы — это атомы одного вида с одинаковым числом протонов, но разным числом нейтронов. Так, атомы 16 О, 17 О и 18 О — это изотопы. Природные изотопы урана — 234 U, 235 U и 238 U.
Таблица 3. «Обозначение и название ионов»
Конспект урока по химии «Строение атома».
Строение атома. 8-й класс
Класс: 8
Презентация к уроку
Цель урока: создать условия для формирования таких понятий, как атом, орбиталь, изотопы, протон, нейтрон, электрон. Продолжать формировать умение работать с Периодической системой, рассмотреть физический смысл порядкового номера элемента. Познакомить с историей открытия строения атома.
Тип урока: урок усвоения новых знаний.
Ход урока
2. Изучение нового материала.
Ребята, сегодня тема нашего урока: «Строение атома».
ПЛАН УРОКА
2. Практическая часть.
Впервые понятие «атом» ввел Демокрит, но он не вкладывал в него столь глубокий смысл.
В основе философии Демокрита лежит учение об атомах и пустоте как двух принципах, порождающих многообразие космоса. Атом есть мельчайшее «неделимое» тело, не подверженное никаким изменениям. Неделимость атома аналогична неделимости «бытия».
Гораздо позже в 1904 году Томсон представил свою новую модель атома. Она представляла собой также равномерно заряженную положительным электричеством сферу, внутри которой вращались отрицательно заряженные корпускулы, число и расположение которых зависело от природы атома. После открытия радиоактивности, эта модель не соответствовала действительности.
Резерфорд исследовал особенности прохождения альфа-частиц через тонкие металлические пластинки.
Планетарная модель Резерфорда
Положительный заряд сконцентрирован в ядре атома, а отрицательно заряженные электроны находятся вокруг него
А сейчас ребята, обсудим некоторые термины, запишите их в словарик.
Запись а.е.м. – означает атомную единицу массы
В ядре сосредоточена большая часть массы атома
Посмотрите на таблицу.
| частица | место нахождения | масса | заряд |
| Протон P+ | ядро | 1 а.е.м | +1 |
| Нейтрон n0 | ядро | 1а.е.м. | 0 |
| Электрон e- | орбиталь | 0 | -1 |
Порядковый номер элемента:
Практическая часть
Заполни таблицу
А сейчас ребята выполним небольшой тест
Тестовые задания
Поменяйтесь заданиями с соседом по парте, проверим ответы:
МОЛОДЦЫ! ЭТО ВАМ УДАЛОСЬ.
Установите соответствие, соединив стрелками (слайд 17)
Вы справились. Желаю дальнейших успехов в изучении химии!
Домашние задание: параграф 6, 7, упр. 3 стр.24
Химия
Именная карта банка для детей
с крутым дизайном, +200 бонусов
Закажи свою собственную карту банка и получи бонусы
План урока:
Строение атома
Сегодня мы будем путешествовать в микромир – мир атома. Даже если превратить нас в песчинку, то по сравнению с размером ядра атомов химических элементов, мы будем гигантами.
Атом нельзя увидеть, невозможно потрогать, он на столько мал, что существует только в нашем воображении. До XIX века учёные оперировали только одной характеристикой атома – это его масса. Наука не оперировала понятиями, что ядро атома содержит более мелкие частицы. Почему элементы отличаются массой. Атом долгое время считали «неделимым». Но отличия в массе подвигли искать причину в строении.
Как описать строение, то чего невозможно увидеть, а можно только представить. Ведь современные электронные микроскопы появились только в XX веке.
Атом – как мельчайшая частица, известна ещё с древних времён. Древнегреческий философ Демокрит считал, что свойства веществ определяются определённым типом атома. Даже тонкая материя, душа, по его мнению, состоит из атомов. Так тела бывают в разных агрегатных состояниях, поэтому атомы металлов будут с зубцами, жидкости будут обладать гладкими, это будет причиной их текучести.
Долгое время атом считали неделимым. Заглянув в словарь синонимов, можно увидеть пару синонимов для слова атом, неделимый, мельчайшая частица. Теория о неделимости существовала до XIX века, пока экспериментально не подтвердили, что ядро атома состоит из более мелких частиц. Но как они располагаются в атоме, как конфеты драже в кармашке, или по версии Томсона, который сравнивал электроны с изюминками, хаотично разбросанных в кексе. Учёный с Японии Хантаро Нагаока сравнил атом с загадочной планетой Сатурн, которая известна своим кольцом. Саму планету он сравнил с массивным ядром, а роль кольца отдал электронам.
В конце XIX века, начале XX происходит стремительное развитие науки, открываются новые частицы α и β. Позже было установлено, что это ядро атома элемента Не и электроны.
В ходе данных исследований было доказано, что атом представляет совокупность заряженных и нейтральных частичек.
Анализируя размеры, важно запомнить, что радиус ядра атома, будет всегда значительно меньше радиуса всего атома. Этот факт объясняется тем, что частицы составляющие ядро более компактно упакованы, чем электроны.
Ядро атома
Орешки фундука явно вы видели. В середине ореха находится большое ядро, занимающее почти всю массу ореха, оставляя малое пространство между скорлупой.
Ядро атома элемента имеет в составе протоны и нейтроны, которые принято называть нуклонами.
Данные частицы не относятся к элементарным, научно доказано, что они состоят с кварков (в словарь). Нейтроны в ядре атома не несут никакого заряда, они нейтральны. Протоны в ядре атома определяют его заряд.
Сумма протонов и нейтронов составляет массовое число ядра атома (нуклонное).
Вы наверняка замечали, что значение Ar в ПСХЭ имеет вид не целого числа, с чем это связано? Причина кроется в том, что химические элементы существуют в виде изотопов.
Чтобы понять суть этого понятия, давайте вспомним, чем особенный каждый элемент? Заряд ядра атома постоянен, другими словами, неизменимое количество протонов. Значит, это будет разновидность элементов, которые будут отличаться нуклонным числом, и как следствие, количеством нейтронов.
Именно по причине существования изотопов, Ar не имеет целого числового значения. Например, количество изотопов хлора – 2.
Масса изотопов и их процентное содержание составляют относительную массу элемента.
Возможно, вы ранее замечали, что в ПСХЭ есть пара элементов, которые нарушают порядок размещения по увеличению относительной атомной массы. Это пары K – Ar, Co – Ni, Te – I.
Некоторые изотопы отличаются особенной способностью самовольно превращаться в другие элементы – это явление носит название радиоактивность, а сами элементы – радиоактивные. Таким образом, они делятся на стабильные и радиоактивные изотопы.
Изотопы элементов после Висмута в ПСХЭ, начиная с 84, будут относиться к радиоактивным элементам.
Электроны в атоме
Давайте рассмотрим, какое место занимают электроны в атоме. Если ядро составляет 99,86 % от массы, а, как известно, что количество протонов и электронов равно. То на долю электронов приходится всего 0,14% от массы.
На данный момент, электрон считают элементарной частицей.
Модель Резерфорда (планетарная) на очень примитивном уровне даёт представление,как располагаются электроны и протоны в атоме, поскольку атом имеет достаточно сложное строение.
Электрон настолько мал и находится в постоянном движении с достаточно большой скоростью, что зафиксировать его в определённом месте и времени сложно. Именно по этой причине говорят, что электрон в атоме находится не в заданной точке, а может там предположительно находиться, потому что его зафиксировать в определённый момент времени невозможно.
Ядро атома Водорода имеет 1 протон, вокруг которого вращается один электрон. Но как быть, если количество электронов в атоме будет два и более, каким образом они будут размещаться.
Поскольку они двигаются с достаточной большой скоростью, то чтобы указать распределение электронов в атоме используют 4 числа – орбитальные характеристики.
Прежде чем, мы перейдём к орбитальным характеристикам, давайте представим многоэтажный дом, в который необходимо разместить жителей, в нашем случае – это электроны.
Первая орбитальная характеристика
Другими словами, представляем, что наш многоэтажный дом содержит 7 этажей. Цифры 1, 2, 3, 4, 5, 6, 7 обозначают номер этажа или энергетические уровни электрона в атоме.
Вторая орбитальная характеристика
Возвращаемся к нашему, многоэтажному дому, орбитальное число показывает типы орбиталей или в сравнении с домом квартиры s, p, d и f.
Третья орбитальная характеристика
Представить квартиру, в виде ячейки или квадрата, так вот магнитное квантовое число указывает число орбиталей.
Смотрим, на первом этаже размещается только s-квартиры, которые будут однокомнатными. На втором этаже уже имеется две квартиры s и р, т.е. однокомнатная и трёхкомнатная. На третьем этаже s, p, d. Четвёртый, пятый и шестой этажи размещают 4 квартиры s, p, d и f.
Четвёртая орбитальная характеристика
Это означает, что в одной ячейке (квадрате), может поселиться не больше двух электронов.
Вот на таком достаточно примитивном уровне, мы рассмотрели состояние электронов в атоме. Но как они там располагаются? Каждый электрон занимает своё определённое место, согласно энергии.
Рассмотрим распределение электронов по энергетическим уровням в атоме. Наверняка вы заметили, что наш дом семиэтажный. Как думаете, по какой причине? ПСХЭ содержит 7 периодов (7 этажей). Если элемент находится во втором периоде, значит, его электроны будут занимать 1 и 2 этаж и никаким образом не могут попасть на 5 или 6 этажи. В данном примере 2 этаж будут называть внешним, научным языком – внешним энергетическим уровнем (он крайний).
Главные правила образования оболочки электронов в атоме
Давайте дадим волю фантазии, допустим, к нашему семиэтажному дому подошёл Бор, не лес как вы могли подумать, а элемент. Смотрим в шпаргалку, как вы уже догадались, это будет периодическая таблица, и ищем там его расположение. Бор занимает ячейку под номером 5. Эта ячейка находится во втором периоде, третьей группе. Значит, число электронов в атоме 5, они размещаются на I и II этажах. Первый уровень будут занимать 2 электрона. Значит на второй этаж (внешний уровень) переходят оставшиеся 3. Два будут занимать s-подуровень, один будет размещаться на р-подуровне. Строение оболочки атома В (бор).
Составим электронную и графическую схему элемента на примере Si и V с помощью алгоритма.
Обратите внимание, чтобы составить электронную формулу элемента, достаточно знать его расположение в ПСХЭ. Итак, начинаем по порядку.
Существует основное состояние электрона в атоме и возбуждённое, которое возникает, если к атому применить некоторую определённую энергию. Электроны во внешнем электронном слое атома имеют способность перемещаться, занимая место на свободной орбитали, образуя при этом возбуждённое состояние.
Обратите внимание, число неспаренных электронов отвечает валентности элементов: Li (I), Be (II), B (III), C (II и IV).
Периодичность свойств элементов. Электроотрицательность
С развитием учения о строении атома, периодический закон занимает ещё больше значимое место в естествознании. Уже неоднократно говорилось, что ПСХЭ является уникальной подсказкой. Достаточно знать расположение и строение электронных оболочек атомов элементов, и возникает возможность судить о том, какими характеристиками он будет обладать. В настоящее время периодический закон имеет формулировку, данную Менделеевым, с небольшим уточнением.
За то, какими свойствами будет наделён элемент, отвечают электроны, которые размещены на внешнем энергетическом уровне. Их ещё называют валентные электроны атома, именно они отвечают за периодическое изменение свойств элементов.
С увеличением массы атома в пределах периода, количество электронов также возрастает, пока не заполнятся все вакантные ячейки уровня.
В ходе химической реакции происходит «движение» электронов. Т.е. одни элементы будут отдавать их, а вторые принимать.
Рассмотрим на примере, образования вещества NaCl.
Обобщая данный пример, сделаем вывод, элементы, которые содержат малое количество электронов на внешнем уровне (1 – 3) будут только отдавать электроны – и они будут относиться к металлам. Неметаллы характеризуются способностью принимать электроны.
Из определения сделаем вывод, что наибольшую электроотрицательность имеет Фтор (F), нет ни одного элемента, кому бы он смог отдать свой электрон, а будет только забирать. Минимальную ЭО будет иметь Франций (Fr).
Ещё одна важная причина изменения свойств элементов, которая изменяется периодически, это радиус атома. Если ЭО характеризует неметаллы, то по радиусу судят о металлических свойствах. Металлы легко отдают электроны, чем дальше они находятся от ядра, тем легче «отрываются». Радиус атома с увеличением заряда ядра в периоде уменьшается, так как ядро начинает сильнее притягивать электроны.
Строение атома

Всего получено оценок: 3037.
Всего получено оценок: 3037.
Атом – наименьшая частица вещества. Его изучение началось еще в Древней Греции, когда к строению атома было приковано внимание не только ученых, но и философов. Каково же электронное строение атома, и какие основные сведения известны об этой частице?
Строение атома
Уже древнегреческие ученые догадывались о существовании мельчайших химически частиц, из которых состоит любой предмет и организм. И если в XVII-XVIII вв. химики были уверены, что атом неделимая элементарная частица, то на рубеже XIX-XX вв., опытным путем удалось доказать, что атом не является неделимым.
Атом, будучи микроскопической частицей вещества, состоит из ядра и электронов. Ядро в 10000 раз меньше атома, однако практически вся его масса сосредоточена именно в ядре. Главной характеристикой атомного ядра, является то, что он имеет положительный заряд и состоит из протонов и нейтронов. Протоны заряжены положительно, а нейтроны не имеют заряда (они нейтральны).
Атом любого элемента можно обозначить электронной формулой и электронно графической формулой:
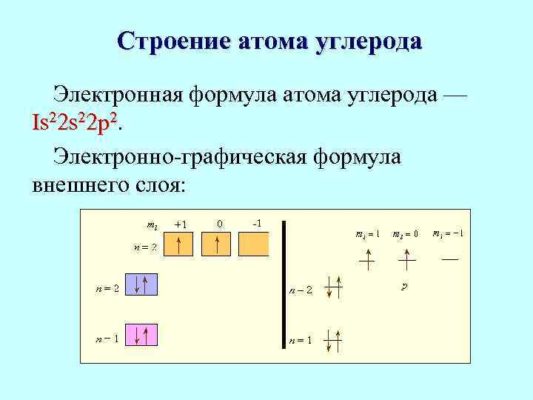
Единственным химическим элементом из периодической системы, в ядре которого не содержатся нейтроны, является легкий водород (протий).
Электрон является отрицательно заряженной частицей. Электронная оболочка состоит из движущихся вокруг ядра электронов. Электроны имеют свойства притягиваться к ядру, а между друг друг на них оказывает влияние кулоновское взаимодействие. Чтобы преодолеть притяжения ядра, электроны должны получать энергию от внешнего источника. Чем дальше электрон находится от ядра, тем меньше энергии для этого необходимо.
Модели атомов
На протяжении долго времени ученые стремились познать природу атома. На раннем этапе большой вклад внес древнегреческий философ Демокрит. Хотя сейчас его теория и кажется нам банальной и слишком простой, в тот период, когда представления об элементарных частицах только начинало зарождаться, его теория о кусочках материи воспринималась совершенно серьезно. Демокрит считал, что свойства любого вещества зависят от формы, массы и других характеристик атомов. Так, например, у огня, полагал он, острые атомы – поэтому огонь обжигает; у воды атомы гладкие, поэтому она способна течь; у твердых предметов, по его представлению, атомы были шереховатые.
Демокрит считал, что из атомов состоит абсолютно все, даже душа человека.
В 1904 году Дж. Дж. Томсон предложил свою модель атома. Основные положения теории сводились к тому, что атом представлялся положительно заряженным телом, внутри которого находились электроны с отрицательным зарядом. Позже эта теория была опровергнута Э. Резерфордом.

Также в 1904 году японским физиком Х. Нагаока была предложена ранняя планетарная модель атома по аналогии с планетой Сатурн. Электроны по этой теории объединены в кольца и вращаются вокруг положительно заряженного ядра. Эта теория оказалась ошибочной.
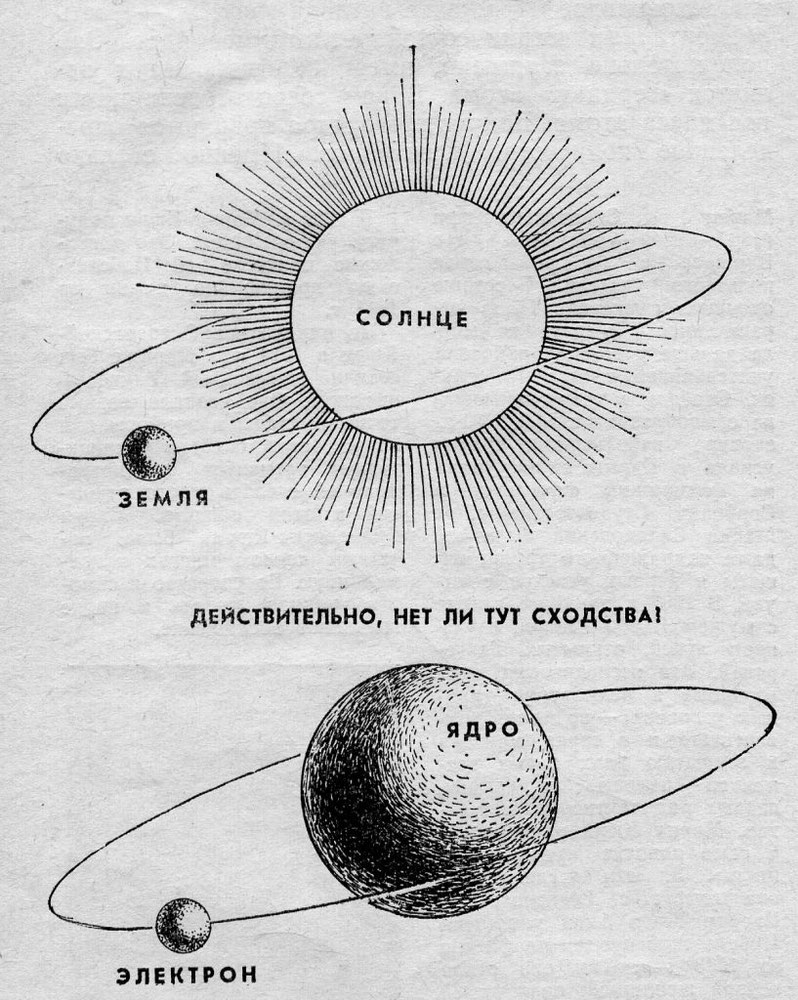
В 1911 году Э. Резерфорд, проделав ряд опытов, сделал выводы, что атом по своему строению похож на планетную систему. Ведь электроны, словно планеты, движутся по орбитам вокруг тяжелого положительно заряженного ядра. Однако это описание противоречило классической электродинамике. Тогда датский физик Нильс Бор в 1913 году ввел постулаты, суть которых заключалась в том, что электрон, находясь в некоторых специальных состояниях, не излучает энергию. Таким образом, постулаты бора показали, что для атомов классическая механика неприменима. Планетарная модель, описанная Резерфордом и дополненная Бором, получила название – планетарная модель Бора-Резерфорда.

Дальнейшее изучение атома привело к созданию такого раздела, как квантовая механика, с помощью которого объяснялись многие научные факты. Современные представления об атоме развились из планетарной модели Бора-Резерфорда.
Что мы узнали?
В данной статье по химии (8 класс) рассказывается кратко и понятно о строении атома. На протяжении многих веков ученые разных стран изучали мельчайшие частицы вещества. Появлялись разные теории, модели и разные формулы строения атома. Современные представления об атоме основываются на модели Бора-Резерфорда, по которой атом состоит из ядра и электронного облака, в котором электроны движутся вокруг ядра.
Основы строения атома. Просто о сложном
Все в мире состоит из атомов. Но откуда они взялись, и из чего состоят сами? Сегодня отвечаем на эти простые и фундаментальные вопросы. Ведь многие люди, живущие на планете, говорят, что не понимают строения атомов, из которых сами и состоят.
Естественно, уважаемый читатель понимает, что в данной статье мы стараемся изложить все на максимально простом и интересном уровне, поэтому не «грузим» научными терминами. Тем, кто хочет изучить вопрос на более профессиональном уровне, советуем читать специализированную литературу. Тем не менее, сведения данной статьи могут сослужить хорошую службу в учебе и просто сделать Вас более эрудированными.
Атом – это частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, которая является носителем его свойств. Иными словами, это мельчайшая частица того или иного вещества, которая может вступать в химические реакции.
История открытия и строение
Понятия атома было известно еще в Древней Греции. Атомизм – физическая теория, которая гласит, что все материальные предметы состоят из неделимых частиц. Наряду с Древней Грецией, идеи атомизма параллельно развивался еще и в Древней Индии.
Не известно, рассказали тогдашним философам об атомах инопланетяне, или они додумались сами, но экспериментально подтвердить данную теорию химики смогли много позже – только в семнадцатом веке, когда Европа выплыла из пучины инквизиции и средневековья.
Долгое время господствующим представлением о строении атома было представление о нем как о неделимой частице. То, что атом все-таки можно разделить, выяснилось только в начале двадцатого века. Резерфорд, благодаря своему знаменитому опыту с отклонением альфа-частиц, узнал, что атом состоит из ядра, вокруг которого вращаются электроны. Была принята планетарная модель атома, в соответствии с которой электроны вращаются вокруг ядра, как планеты нашей Солнечной системы вокруг звезды.
Ядро атома имеет положительный электрический заряд, а электроны, вращающиеся по орбите – отрицательный. Таким образом, атом электрически нейтрален.
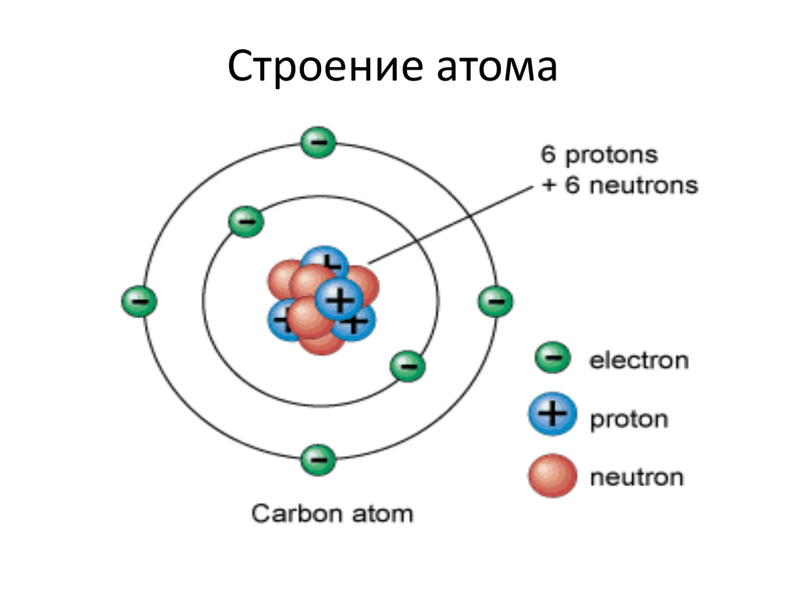
Ниже приведем элементарную схему строения атома углерода.
Схема строения атома
Свойства атомов
Масса
Массу атомов принято измерять в атомных единицах массы – а.е.м. Атомная единица массы представляет собой массу 1/12 части свободно покоящегося атома углерода, находящегося в основном состоянии.
В химии для измерения массы атомов используется понятие «моль». 1 моль – это такое количество вещества, в котором содержится число атомов, равное числу Авогадро.
Размер
При этом, масштабы вещей таковы, что, по сути, атом на 99% состоит из пустоты. Ядро и электроны занимают крайне малую часть его объема. Для наглядности, рассмотрим такой пример. Если представить атом в виде олимпийского стадиона в Пекине (а можно и не в Пекине, просто представьте себе большой стадион), то ядро этого атома будет представлять собой вишенку, находящуюся в центре поля. Орбиты электронов при этом находились бы где-то на уровне верхних трибун, а вишня весила бы 30 миллионов тонн. Впечатляет, не так ли?
Если предсавить атом в виде стадиона, ядро будет размером с вишню в центре поля
Откуда взялись атомы?
В самом начале формирования Вселенной никаких атомов не было и подавно, существовали лишь элементарные частицы, под воздействием огромных температур взаимодействующие между собой. Как сказал бы поэт, это был настоящий апофеоз частиц. В первые три минуты существования Вселенной, из-за понижения температуры и совпадения еще целой кучи факторов, запустился процесс первичного нуклеосинтеза, когда из элементарных частиц появились первые элементы: водород, гелий, литий и дейтерий (тяжелый водород). Именно из этих элементов образовались первые звезды, в недрах которых проходили термоядерные реакции, в результате которых водород и гелий «сгорали», образуя более тяжелые элементы. Если звезда была достаточно большой, то свою жизнь она заканчивала так называемым взрывом «сверхновой», в результате которого атомы выбрасывались в окружающее пространство. Так и получилась вся таблица Менделеева.
Так что, можно сказать, что все атомы, из которых мы состоим, когда-то были частью древних звезд.
Почему ядро атома не распадается?
В физике существует четыре типа фундаментальных взаимодействий между частицами и телами, которые они составляют. Это сильное, слабое, электромагнитное и гравитационное взаимодействия.
Именно благодаря сильному взаимодействию, которое проявляется в масштабах атомных ядер и отвечает за притяжение между нуклонами, атом и является таким «крепким орешком».
Не так давно люди поняли, что при расщеплении ядер атомов высвобождается огромная энергия. Деление тяжелых атомных ядер является источником энергии в ядерных реакторах и ядерном оружии.
Итак, друзья, познакомив Вас со структурой и основами строения атома, нам остается только напомнить о том, что наши авторы готовы в любой момент прийти Вам на помощь. Не важно, нужно Вам выполнить диплом по ядерной физике, или самую маленькую контрольную – ситуации бывают разные, но выход есть из любого положения. Подумайте о масштабах Вселенной, закажите работу в Zaochnik и помните – нет поводов для беспокойства.