Силы Ван-дер-Ваальса
Ван-дер-ваальсовы силы — силы межмолекулярного (и межатомного) взаимодействия с энергией 10 — 20 кДж/моль. Этим термином первоначально обозначались все такие силы, в современной науке он обычно применяется к силам, возникающим при поляризации молекул и образовании диполей. Открыты Я. Д. ван дер Ваальсом в 1869 году.
Ван-дер-Ваальсовы силы межатомного взаимодействия инертных газов обусловливают возможность существования агрегатных состояний инертных газов (газ, жидкость и твёрдые тела).
К ван-дер-ваальсовым силам относятся взаимодействия между диполями (постоянными и индуцированными). Название связано с тем фактом, что эти силы являются причиной поправки на внутреннее давление в уравнении состояния реального газа Ван-дер-Ваальса. Эти взаимодействия в основном определяют силы, ответственные за формирование пространственной структуры биологических макромолекул.
Содержание
Классификация ван-дер-ваальсовых сил
Ван-дер-ваальсовое взаимодействие состоит из трех типов слабых взаимодействий:
До сих пор многие авторы исходят из предположения, что ван-дер-ваальсовые силы определяют межслоевое взаимодействие в слоистых кристаллах, что противоречит экспериментальным данным: масштабу анизотропии температуры Дебая и, соответственно, масштабу анизотропии решёточного отражения. Исходя из данного ошибочного [4] предположения построены многие двумерные модели, «описывающие» свойства, в частности графита и нитрида бора.
Проявления в природе
См. также
Примечания
Литература
 |
 Химическая связь Химическая связь | |||||||
|---|---|---|---|---|---|---|---|
| Внутримолекулярное взаимодействие |
| ||||||
| Межмолекулярное взаимодействие |
| ||||||
Полезное
Смотреть что такое «Силы Ван-дер-Ваальса» в других словарях:
силы Ван-дер-Ваальса — van der Valso jėgos statusas T sritis Standartizacija ir metrologija apibrėžtis Elektrinės kilmės molekulių sąveikos jėgos. atitikmenys: angl. van der Waals forces vok. Van der Waalssche Kräfte, f rus. ван дер ваальсовые силы, f; силы Ван дер… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
силы Ван-дер-Ваальса — van der Valso jėgos statusas T sritis chemija apibrėžtis Elektrinės kilmės molekulių sąveikos jėgos. atitikmenys: angl. van der Waals forces rus. Ван дер Ваальсовые силы; силы Ван дер Ваальса … Chemijos terminų aiškinamasis žodynas
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — ВАН ДЕР ВААЛЬСА УРАВНЕНИЕ, уравнение состояния (см. УРАВНЕНИЕ СОСТОЯНИЯ), описывающее свойства реального газа (см. РЕАЛЬНЫЙ ГАЗ). Предложено Й. Д. Ван дер Ваальсом (см. ВАН ДЕР ВААЛЬС Йоханнес Дидерик) в 1873 г. Широко используется для… … Энциклопедический словарь
ВАН-ДЕР-ВААЛЬСА ЗАНОН — (Van der Wa als), уравнение состояния реальных газов (см. Аггрегатное состояние), не подчиняющихся закону Бойля и Гей Люссака (pv= = КТ), справедливого для газов идеальных. Если обозначить объем газа через v, давление через р, абсолютную темп,… … Большая медицинская энциклопедия
Ван дер Ваальса формула — В. формула, одинаково прилагаемая и к газообразному и к жидкому состоянию какого либо вещества, выражает зависимость между объемом, температурой и давлением, под которым находится рассматриваемое вещество, при посредстве лишь двух постоянных для… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Ван-дер-Ваальса силы — силы межмолекулярного взаимодействия, возникающие из за аппроксимации молекул дипольными моментами, и далее соответствующие взаимодействию между ними, такими, что на малых расстояниях они оказываются отталкивающими, а на больших расстояниях… … Начала современного естествознания
Уравнение Ван-дер-Ваальса — Уравнение состояния Стат … Википедия
Ван-дер-Ваальс — Ван дер Ваальс, Ян Дидерик Ян Дидерик Ван дер Ваальс Johannes Diderik van der Waals Дата рождения … Википедия
Ван-дер-Ваальс, Ян Дидерик — Ян Дидерик Ван дер Ваальс нидерл. Johannes Diderik van der Waals … Википедия
Ван-Дер-Ваальс — Ян Дидерик Ван дер Ваальс Johannes Diderik van der Waals выдающийся учёный физик, лауреат Нобелевской премии по физике Дата рождения: 23 ноябр … Википедия
Нобелевские лауреаты: Йоханнес Ван дер Ваальс
Сегодняшний герой рубрики «Как получить Нобелевку» начал свой путь с самых низов. Его с полным правом можно назвать «селф мейд меном»: не имея права официально учиться в университете, он самостоятельно получил образование, будучи школьным учителем, написал докторскую, удостоенную внимания самого Максвелла, и, в конце концов, именно он окончательно подтвердил существование молекул. Итак, встречайте: Йоханнес Ван дер Ваальс.
Йоханнес Дидерик Ван дер Ваальс
Родился: 23 ноября 1837 года, Лейден, Нидерланды.
Умер: 8 марта 1923 года, Амстердам, Нидерланды.
Нобелевская премия по физике 1910 года. Формулировка Нобелевского комитета: «За работу, посвященную уравнению состояния газов и жидкостей (for his work on the equation of state for gases and liquids)».
Йоханнес Ван дер Ваальс был сыном плотника в Лейдене, старшим из десяти детей Якобуса Ван дер Ваальса и Элизабет Ван дер Берг. Он родился 27 ноября 1837 года и стал одним из самых возрастных лауреатов Нобелевской премии первого десятилетия. Увы, законы в XIX веке были не самые добрые, и человек из низших классов и в «просвещенной» Европе, по крайней мере, в Нидерландах, не имел никакого права учиться в университете. Поэтому, окончив среднюю школу, юный Ван дер Ваальс пошел… учителем в младшую школу. Пять лет, с 1856 по 1861 годы, он посещал специальные курсы для того, чтобы иметь право преподавать в средней школе.
В 1862 году он начал посещать лекции по астрономии, математике и физике, став вольнослушателем Лейденского университета. Тем не менее, он не мог считаться обычным студентом, поскольку не получил образования в классических языках, латыни и греческом, который преподавали в классических нидерландских гимназиях. Но после того, как он прошел все эти курсы, он получил право преподавать в любой школе и даже руководить ей. Получив возможность выбора, Ван дер Ваальс в 1866 году поехал работать директором школы в Гаагу. Почему Гаага? От нее было недалеко до Лейдена, в университете которого Ван дер Ваальс надеялся все-таки учиться.
Ван-дер-Ваальса уравнение
Полезное
Смотреть что такое «Ван-дер-Ваальса уравнение» в других словарях:
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — ВАН ДЕР ВААЛЬСА УРАВНЕНИЕ, уравнение состояния (см. УРАВНЕНИЕ СОСТОЯНИЯ), описывающее свойства реального газа (см. РЕАЛЬНЫЙ ГАЗ). Предложено Й. Д. Ван дер Ваальсом (см. ВАН ДЕР ВААЛЬС Йоханнес Дидерик) в 1873 г. Широко используется для… … Энциклопедический словарь
Ван-дер-Ваальса уравнение — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнение Ван дер Ваальса Уравнение Дитеричи Разделы термодинамики Начала термодинамики Уравнени … Википедия
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — одно из первых уравнений состояния реального газа. Предложено в 1873 голл. физиком Я. Д. Ван дер Ваальсом (J. D. van der Waals). Для моля газа, имеющего объём V при темп ре Т и давлении р, имеет вид: (p+a/V2)(V b)=RT, где R универсальная газовая… … Физическая энциклопедия
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — предложенное Й. Д. Ван дер Ваальсом (1873), уравнение состояния реального газа, учитывающее конечность объема молекул и наличие межмолекулярных сил притяжения; для одного моля имеет вид: (p+a/V2)(V b) V = RT,где: p давление, V мольный объем, T… … Большой Энциклопедический словарь
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — ур ние состояния реального газа. Для пмолей газа, имеющего объем Vпри т ре Ти давлении р. имеет вид: где R газовая постоянная, аи b постоянные Ван дер Ваальса, характерные для данного в ва. Член 2/V2 учитывает притяжение молекул газа (уменьшение… … Химическая энциклопедия
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ — [по имени голл. физика Я. Д. Ван дер Ваальса (J. D. vanderWaals; 1837 1923)] ур ние состояния реального газа? где р давление, V объём, Т термодинамич. темп pa, т масса газа, М его молярная масса, R газовая постоянная, а и b константы, зависящие… … Большой энциклопедический политехнический словарь
Ван дер Ваальса уравнение — предложенное Й. Д. Ван дер Ваальсом (1873) уравнение состояния реального газа, учитывающее конечность объёма молекул и наличие межмолекулярных сил притяжения; для одного моля газа имеет вид: (р + a/V2)(V – b) = RT, где р давление, V объём… … Энциклопедический словарь
ВАН ДЕР ВААЛЬСА УРАВНЕНИЕ — предложенное И. Д. Ван дер Ваальсом (1873) ур ние состояния реального газа, учитывающее конечность объёма молекул и наличие межмол. сил притяжения; для и молей газа имеет вид: (р + n2а/V2)( V nb) = nRT, где р давление, V объём, Т абс. темп ра, R… … Естествознание. Энциклопедический словарь
Уравнение Ван-дер-Ваальса — Уравнение состояния Стат … Википедия
Уравнение состояния газа Ван-дер-Ваальса — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнение Ван дер Ваальса Уравнение Дитеричи Разделы термодинамики Начала термодинамики Уравнени … Википедия
Ван дер Ваальс
Ван дер Ваальс
| Ян Дидерик Ван-дер-Ваальс | |
| Johannes Diderik van der Waals | |
 | |
| выдающийся учёный-физик, лауреат Нобелевской премии по физике | |
|---|---|
| Дата рождения: | |




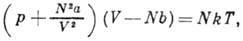
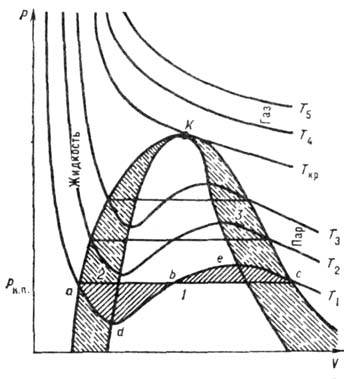
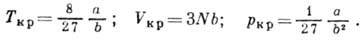
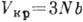 , хорошо согласуются с полученными др. методами.
, хорошо согласуются с полученными др. методами. 


