Врожденные пороки сердца (ВПС) у детей
Врожденные пороки сердца (ВПС) у детей – патологии, частота которых среди новорожденных в странах Европы и СНГ составляет от 0,8 до 1%.
Что провоцирует / Причины Врожденных пороков сердца (ВПС) у детей:
ВПС у ребенка – наследственное заболевание. Тяжесть зависит от того, насколько выражена генетическая склонность, и насколько повлияли на плод неблагоприятные факторы среды.
Неблагоприятные факторы среды:
Врожденные пороки сердца у детей могут быть частью синдрома с множественным поражением органов и систем, который вызван аномалиями хромосом или мутацией каких-либо генов. Такая форма требует обследования ребенка и его родных людей в генетическом центре.
Структура врожденных пороков сердца у новорожденных детей
| ВПС | Частота % |
| Дефект межжелудочковой перегородки | 25-30 |
| Открытый аортальный проток | 12 |
| Дефект межпредсердной перегородки | 10 |
| Стеноз клапана легочной артерии | 10 |
| Тетрада Фалло | 5-10 |
| Стеноз аортального клапана | 5 |
| Коарктация аорты | 5 |
| Общий артериальный ствол | 5 |
| Транспозиция магистральных сосудов | 5 |
Факторы риска рождения ребенка с врожденными пороками сердца:
Патогенез (что происходит?) во время Врожденных пороков сердца (ВПС) у детей:
Формирования сердца плода происходит к концу I триместра беременности. При помощи такого метода как УЗИ уже на 16-18-й неделе можно выявить большую часть вырожденных пороков сердца. Диагноз ставится окончательно во II или III триметре. При ВПС у детей может быть цианоз, если увеличено количество восстановленного гемоглобина эритроцитов до 50 г/л. На это влияют такие факторы как:
Цианоз влияет на изменения периферической крови: полицитемию и гипергемоглобинемию. Хроническая кислородная недостаточность вызывает изменение ногтевых фаланг – пальцы напоминают барабанные палочки.
Существует 3 фазы течения врожденных пороков сердца:
Первая фаза – происходят реакции адаптации и компенсации на нарушения динамики кровообращения. Если гемодинамика нарушена значительно, появляется нестойкая гиперфункция миокарда, аварийный вариант по В. В. Ларину и Ф. 3. Меерсону, поэтому легко развивается декомпенсация.
Вторая фаза – относительной компенсации. Физическое развитие ребенка улучшается, как и его моторная активность.
Третья фаза – терминальная. Она наступает при исчерпывании компенсаторных возможностей и развитии дистрофических и дегенеративных изменений в сердечной мышце и паренхиматозных органах. Различные заболевания и осложнения приближают развитие этой фазы болезни, которая обязательно оканчивается летальным исходом.
Ф. 3. Меерсон и его коллеги выделяют 3 стадии компенсаторной гиперфункции сердца:
1. Аварийная
Увеличивается интенсивность функционирования структур миокарда. Появляются признаки острой сердечной недостаточности. Появляется изменение обмена.
2. Вторая стадия
Фиксируют нормальную интенсивность функционирования структур миокарда. Прогрессируют нарушения обмена, структуры и регуляции сердца.
3. Стадия прогрессирующего кардиосклероза и постепенного истощения
Снижается интенсивность синтеза нуклеиновых кислот и белков в гипертрофированном миокарде.
В периоде относительной компенсации постепенно развивается синдром капилляротро-фической недостаточности системы гемомикроциркуляции, приводящий к несоответствию транскапиллярного кровотока сердечному выбросу. Как следствие этого появляются метаболические расстройства в тканях, а также дистрофические, атрофические и склеротические изменения во внутренних органах.
Симптомы Врожденных пороков сердца (ВПС) у детей:
Классификация
Различают больше 100 видов врожденных пороков сердца у детей. Существует также большое количество классификаций, в том числе МКБ-10. Часть исследователей делят ВПС на синие и белые. При синих у ребенка наблюдается синий оттенок кожи, а при белых кожа бледная. Пороки синего типа включают транспозицию магистральных сосудов, тетраду Фалло, атрезию легочной артерии и т.д. Пороки белого типа: дефект межжелудочковой перегородки, дефект межпредсердной перегородки и пр.
Рекомендуется как можно раньше выявлять пороки сердца, чтобы своевременно оказать помощь ребенку. Распознать ВПС у младенцев можно по таким признакам:
При врожденных пороках сердца у детей наблюдаются изменения на электрокардиограмме, при эхокардиографическом исследовании, при рентгенографическом обследовании. На протяжении первых 10 лет жизни малыш с ВПС может выглядеть здоровым, даже кожа будет нормального оттенка. Но дальше ребенок начинает отставать в физическом развитии, у него появляется одышка при физических нагрузках, кожа синеет или бледнеет. Тогда рекомендуется срочно обратиться к врачу.
Диагностика Врожденных пороков сердца (ВПС) у детей:
Врачи обращают внимание на проявленные симптомы, которые были описаны выше, и такие факторы:
При диагностике используют рентген и ЭХО-кардиографию, ФКГ, ЭКГ, клинический анализ крови. Среди специальных методов исследования при подозрении на ВПС у детей – ангиография и зондирование сердца.
Если ребенок без подозрения на ВПС попадает к кардиологу, у него могут выявить сердечные шумы. У старших детей выявляют мягкий систолический шум в шестом межреберье, который становится более интенсивным после физической нагрузки, при лихорадке и изменении положения тела. Может быть также машинообразный шум во втором межреберье слева от грудины – при открытом артериальном протоке. Пансистолический шум с эпицентром в четвертом-пятом межреберьях слева от грудины выявляют при ДМЖП и митральной регургитации у ребенка. Если есть диастолически шумы, необходимо дополнительное кардиологическое обследование.
Эхокардиография – метод кардиологического обследования, который дает детальную информацию о характере сердечных аномалий и внутрисердечной гемодинамике. раньше вместо этого метода применялась катетеризация сердца. Этот метод не применяется изолировано, его нужно сравнивать с результатами ФКГ, ЭКГ и пр.
Врач при диагностике после определения основных гемодинамических нарушений должен уточнить анатомический вариант порока сердца. Далее уточняют фазу течения порока, ищут вероятные осложнения, которые могли возникнуть.
Лечение Врожденных пороков сердца (ВПС) у детей:
ВПС лечат хирургическими методами и терапевтическими. Последние часто являются вспомогательными. Плод обследуют еще до рождения, тогда же решается вопрос о применении хирургических методов лечения врожденных пороков сердца у детей. Роды в таких случаях рекомендуется проводить в родильных отделениях при кардиохирургических больницах.
Терапевтическое лечение применяют, если операцию можно перенести на более поздние сроки. Что касается так называемых бледных пороков, лечение зависит от того, насколько оказывает влияние на состояние ребенка порок с течением месяцев и лет. Есть большие шансы, что понадобится терапевтическое лечение.
Профилактика Врожденных пороков сердца (ВПС) у детей:
Вопрос о продолжении рода должен приниматься обдуманно и взвешенно. Если есть информация, что в вашей семье или в роду мужа кто-то страдал пороками сердца, учитывайте вероятность того, что ребенок родится с врожденным пороком сердца (ВПС). Беременная должна донести эту информацию до врача, который ее наблюдает, чтобы он был более внимательным, искал у плода признаки ВПС. Во время беременности обязательно нужно проходить УЗИ.
К каким докторам следует обращаться если у Вас Врожденные пороки сердца (ВПС) у детей:
В 2/3 случаев пороки клинически не проявляются сразу после рождения, т.е. сначала бывают совершенно бессимптомными. Но в 1/3 случаев состояние ребенка тотчас после рождения может быть очень тяжелым. Он синюшен, у него одышка, он постоянно беспокойно плачет, не может брать грудь. С каждым днем ему становится все хуже и хуже. Он требует незамедлительной, экстренной помощи, т.к. находится в «критическом состоянии». Не верьте тем, кто скажет, что ему нельзя ничем помочь. Отчаяние — плохой помощник, а незнание — самый страшный враг. Незамедлительно нужно получить специализированную помощь. А такая помощь сегодня – есть, и она должна быть оказана в первые часы и дни жизни ребенка, иначе он погибнет.
Такое критическое состояние у новорожденного может быть вызвано не только ВПС. Но ВПС — наиболее частая причина. Поэтому ее надо или подтвердить или отвергнуть в первую очередь.
И вот тут вы можете столкнуться, как и многие родители, с первой психологической проблемой: вы не хотите верить, что у ребенка «что-то с сердцем». А врачи говорят вам, что надо срочно что-то сделать. Или — наоборот: вы настаиваете на том, что у него «что-то есть», а медики говорят: «Не волнуйтесь, он в порядке»… Кому верить — себе или врачам? Первое, что вы должны сделать в такой ситуации, — немедленно показать ребенка специалисту-кардиологу, а если такого нет рядом — поехать в ближайший специализированный центр, где есть нужная аппаратура.
Специальность «детская кардиология» появилась в нашей огромной стране относительно недавно, и поэтому профессионально подготовленные врачи, как правило, работают в больших, специализированных центрах. Таких центров в России уже очень много, и при подозрении вашем или вашего врача на врожденный порок сердца — надо обязательно обследовать ребенка там. Пусть подозрения не подтвердятся и у ребенка порока сердца нет. Но лучше сделать обследование, и сделать вовремя, чем упустить сроки, которые во многих случаях решают его и вашу судьбу.
И, если вы или ваш педиатр что-то подозревает, никогда не верьте тем, кто будет говорить: «Не надо ничего делать», «Он нормальный», «Может, еще «перерастет»?» или «Все — от Бога»… Может быть, многое действительно не в наших руках, но современные возможности медицины сегодня поразительны, и к знаниям и помощи профессионалов необходимо прибегнуть.
Но вот вы попали туда, где занимаются детской кардиологией. Нужно поставить точный диагноз, чтобы определить, что и как делать дальше и нужно ли вообще что-то делать.
Несколько слов о наследственности
Слияние яйцеклетки и сперматозоида означает начало новой жизни, и эта жизнь несет в себе всю генетическую информацию обоих родителей. Говорят: «Она похожа на папу…», «Он похож на моего дедушку по маме». А что это значит? Каждый из нас несет в себе огромную информацию не только о наших родителях и дедушках-бабушках, но и о пра-пра-прародителях. Эта информация в виде молекул белка заключена в сперматозоиде и яйцеклетке. При их соединении оба «банка данных» сливаются, и будущий ребенок несет их в себе. Структурной единицей информации является ген, или молекула белка. Слово «ген» означает «род», и факт наследования различных признаков был хорошо известен в древности, но наука о генах — генетика — возникла относительно недавно.
Каждая зародившаяся клетка несет в себе тысячи генов и каждый из этих генов заведует каким-либо процессом развития, например, образованием мозга, костей, или — сердца и какой-либо его части. Это называют «генетическим кодом» и ребенок обладает суммой кодов обоих родителей. Коды несут в себе и передают «признаки», т.е. «выражают» себя во вполне осязаемых и видимых чертах вашего ребенка. Но — не только видимых, но и скрытых: строение костей и внутренних органов, их функция в жизни и даже характер, поведение и привычки. Эти признаки могут быть очевидны и проявиться в первом поколении, т.е. у вашего сына или дочки. Но они могут проявиться и у внука, и даже — у правнука. И мы не понимаем, почему вдруг у родителей-блондинов может родиться ребенок-шатен. Или — голубоглазый, тогда как у папы и мамы глаза карие. В таких случаях говорят, что проявление определенного гена стало «доминантным». Это не означает, что другого гена – матери или отца — у ребенка в «коде» нет. Он есть, но не проявляет себя в этом поколении. Ученые называют этот ген рецессивным, т.е. скрытым.
К сожалению, обычно люди не могут проследить точно свою родословную дальше 3-4 колена. Мы говорим: «Бабушка по отцу умерла рано. От сердца». Или читаем в литературе даже прошлого века: «У них было пять детей, но двое умерли во младенчестве». От чего? Что с ними было? Да, были тогда и непобежденные еще инфекции, и антисанитария, но были и врожденные пороки, о которых просто не знали. Хотя люди очень давно заметили, что в закрытых сообществах, где браки разрешались лишь между хорошо известными друг другу, а подчас и родственными семьями, количество врожденных пороков, отклонений, гораздо выше. Не случайно браки между близкими родственниками, даже двоюродными, издавна были запрещены религией.
Сегодня геном человека прочитан, но до практического применения большинства знаний генетики еще очень далеко. И пока ни ученые, ни тем более вы или ваш партнер не можете точно знать, за что несут ответственность ваши гены в виде рецессивных признаков, когда и в чем они могут проявиться. Так что никого и никогда не надо винить в том, что у ребенка — врожденный порок сердца. Освободитесь от этого чувства. Забудьте о возможных причинах. Важнее разобраться в последствиях неверного развития и известных сегодня путях исправления этой неожиданной ошибки природы.
В семье, в которой уже есть ребенок с пороком сердца, при планировании следующей беременности крайне важно пройти всестороннее комплексное обследование с использованием современных инструментальных и лабораторных диагностических методик, медико-генетическую экспертизу. По отношению ко всему населению вероятность рождения ребенка с пороком сердца составляет примерно 1 на 100 здоровых детей. Вероятность рождения такого ребенка немного выше у тех, сестры или братья которых имеют ВПС.
Вероятность возникновения порока сердца у ребенка, если его брат/сестра страдают ВПС следующая:
ВПС, выявленный у брата/сестры
Вероятный риск возникновения ВПС у следующего ребенка в семье, %
Тактика педиатра при критических врожденных пороках сердца у новорожденных детей
В структуре младенческой смертности аномалии развития занимают третье место, и половину случаев летальности определяют врожденные пороки сердца (ВПС).

Масштаб проблемы подчеркивает высокая частота ВПС: в разных странах этот показатель варьирует от 0,6% до 2,4% в год у детей, родившихся живыми, с учетом внутриутробной гибели плода и ранних выкидышей общая частота ВПС составляет 7,3% [1, 3].
Пренатальная диагностика. С целью снижения младенческой смертности используется пренатальный ультразвуковой скрининг, позволяющий выявить большинство ВПС до 24-й недели гестации. При подозрении на порок проводится прицельное УЗИ плода на аппарате экспертного класса. Основная задача — предотвратить рождение детей с неоперабельными пороками — синдромом гипоплазии левого сердца (СГЛС), гипертрофической кардиомиопатией с признаками органического поражения миокарда, множественными пороками развития плода. Пренатальный консилиум должен предложить прерывание беременности только при условии точной диагностики некурабельного порока [2, 4].
Учитывая высокую летальность новорожденных детей и младенцев от ВПС, для данной возрастной группы пациентов создана классификация, основанная на определении ведущего клинического синдрома, эффективности терапевтической тактики и определяющая сроки хирургического вмешательства [3, 4].
Синдромальная классификация ВПС у новорожденных и детей первого года жизни (Шарыкин А. С., 2005)
Данные состояния могут сочетаться, усугубляя тяжесть состояния детей, 50% этих детей требуют хирургического или терапевтического вмешательства на первом году жизни.
Гемодинамика. Критические пороки характеризуются дуктус-зависимым легочным или системным кровообращением, их объединяет внезапное резкое ухудшение внешне благополучного при рождении ребенка, связанное с уменьшением кровотока через артериальный проток. Дуктус-зависимое легочное кровообращение при ТМС, атрезии (или критическом стенозе легочной артерии) с интактной МЖП обеспечивает кровоток через проток в малый круг кровообращения, и при его ограничении или прекращении развивается тяжелая артериальная гипоксемия, острая гипоксия органов и тканей.
Клиника ВПС с легочным дуктус-зависимым кровообращением
Анатомия одного из самых частых критических пороков — транспозиции магистральных сосудов — заключается в неправильном отхождении аорты — из правого и легочной артерии — из левого желудочка, что способствует разобщению кругов кровообращения: в системе малого круга циркулирует артериальная кровь, в системе большого круга — венозная.
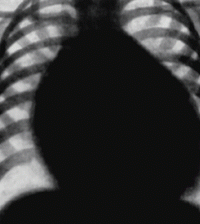
Естественное течение порока очень тяжелое. Ребенок рождается в срок с нормальной массой тела, но в первые часы после рождения появляется диффузный цианоз кожи, особенно выраженный на периферии — цианоз лица, кистей, стоп. Состояние крайней степени тяжести обусловлено тяжелой артериальной гипоксемией. Одышка, тахикардия появляются через 1–2 часа после пережатия пуповины. Отмечается прогрессирующее ухудшение состояния. Ребенок вялый, заторможенный, легко охлаждается.
При закрытии фетальных коммуникаций острая гипоксия приводит к развитию полиорганной недостаточности и гибели новорожденного в течение нескольких часов. При выживании ребенка в течение нескольких недель нарастает сердечная недостаточность. Быстро развивается тяжелая гипотрофия. Необходимо отметить, что в случае адекватной тактики наблюдения и лечения, а также своевременной — до месяца — хирургической коррекции порока у ребенка (так как только в этот период возможна радикальная коррекция методом артериального переключения магистральных сосудов) полностью восстанавливается физиологическая гемодинамика, темпы роста и развития, физическая и в последующем социальная адаптация. Если коррекция порока проводится позже — исходы менее благоприятны.
Диагностические критерии ТМС включают:
Схема обследования новорожденного ребенка с подозрением на ВПС:
Кроме того, наблюдение ребенка предполагает мониторинг газов крови (рО2, рСО2), сатурации кислорода (SatO2) с помощью пульсоксиметрии и метаболических показателей — рН, ВЕ. Газообмен в легких не нарушен, если РаО2 находится в пределах 60–80 мм рт. ст., SаО2 — 96–98%. Артериальная гипоксемия развивается при РаО2 менее 60 мм рт. ст. и уровне насыщения гемоглобина 85–75%.
Задачи педиатра (неонатолога):
Транспортировка в кардиохирургический центр оптимальна в течение первых недель, первого месяца жизни. Предварительно необходимо сообщить в кардиохирургический стационар о больном с врожденным пороком сердца с дуктус-зависимым кровообращением. Период наблюдения до момента перевода и транспортировка в центр проводится на фоне инфузии препарата простагландина Е (Алпростан, Вазапростан).
Клиника ВПС с системным дуктус-зависимым кровообращением (группа пороков включает СГЛС, выраженную коарктацию аорты, перерыв дуги аорты). Наиболее позитивным примером пороков данной группы является выраженная предуктальная коарктация, занимающая от 1% до 10% среди критических ВПС. При данном пороке резко ограничен или полностью отсутствует кровоток из проксимальной ее части (ниже места отхождения артериального протока) к дистальной. Нарушение гемодинамики, соответственно, заключается в том, что в нисходящую аорту (в большой круг) небольшой объем крови поступает только из легочной артерии через артериальный проток. При закрывающемся артериальном протоке остро развивается гипоперфузия органов и тканей и полиорганная недостаточность. Клиника: доношенный новорожденный с резким ухудшением в первые несколько дней жизни — адинамия, холодные конечности, симптом гипоперфузии периферических тканей («белого пятна»), пульс малого наполнения, высокое АД на руках и низкое или не определяется на ногах, одышка, тахикардия, олигоурия с нарастающей азотемией, гепатомегалия с ростом трансаминаз, некротизирующий энтероколит.
Рассмотрим диагностику и оптимальную терапевтическую тактику в отношении пациента с выраженной коарктацией аорты на конкретном клиническом примере.
Из анамнеза: состояние ухудшилось внезапно на 14-е сутки жизни, когда ребенок стал вялым, появилась выраженная одышка, госпитализирован машиной «скорой помощи». Мальчик от второй, нормально протекавшей беременности, срочных родов с массой 3220 г, оценкой по шкале Апгар 5 (9) баллов. Выписан из родильного дома в удовлетворительном состоянии, находился на естественном вскармливании. Периодически отмечались эпизоды беспокойства, метеоризм.
При поступлении ребенок интубирован, проводится ИВЛ с низким содержанием кислорода во вдыхаемой смеси. Обследование в стационаре выявило кардиомегалию (кардиоторакальный индекс — 80%), обеднение легочного рисунка, по данным электрокардиографии — сочетанную перегрузку обоих желудочков. Эхокардиография установила гипоплазию аорты ниже места отхождения левой подключичной артерии (и выше локализации артериального протока), в типичном для артериального протока месте — точечный кровоток (закрывающийся артериальный проток). Через 6 часов состояние ребенка ухудшилось: развилась олигурия, отмечен рост креатинина до 213 ммоль/л, трансаминаз в 4–5 раз от уровня лабораторной нормы. Гуморальная активность не установлена.
Обоснование диагноза и тактики: учитывая клинику выраженной дыхательной и в последующем — полиорганной недостаточности в сочетании с кардиомегалией, системной артериальной гипертензией, почечной и печеночной недостаточностью, по клиническим данным следовало заподозрить коарктацию аорты. Внезапное ухудшение состояния ребенка в отсутствие признаков инфекции позволяет думать о дуктус-зависимом системном кровообращении, с учетом данных визуализации сердца и сосудов имеет место диагноз: «ВПС, предуктальная коарктация аорты, артериальная гипертензия 2 ст., вторичная, полиорганная недостаточность».
С момента подтверждения диагноза по данным ЭхоКГ необходимо начать терапию Вазапростаном 0,02 (с увеличением дозы до 0,05 мкг/кг/мин) с целью восстановления кровотока через артериальный проток. При данном пороке шунт направлен из легочной артерии в нисходящую аорту, и только эта небольшая порция крови обеспечивает весь большой круг кровообращения.
Расчет дозы и методика введения. Вес ребенка при поступлении — 3220 г. В 1 ампуле содержится 20 мкг Вазапростана. В данном случае введение препарата начали с дозы 0,02 мкг/кг/мин, то есть потребовалось 0,02 ´ 3,2 = 0,064 мкг/кг/мин. За час доза препарата составила 0,064 ´ 60 = 3,8 мкг/час. Для введения препарата 1 ампулу (20 мкг Вазапростана) развели в 20 мл физиологического р-ра (в 1 мл — 1 мкг). При отсутствии эффекта в течение двух часов доза была увеличена до 0,04–0,05 мкг/кг/мин: соответственно скорость введения препарата увеличилась до 7,6–9,5 мл/час. В данном случае был очень показателен контроль терапии — через 6 часов инфузии отмечено улучшение состояния, усиление дующего систолического шума во втором межреберье слева, увеличение размеров потока через артериальный проток по данным ЭхоКГ. Переведен на поддерживающую дозу Вазапростана — 0,01 и затем 0,005 мкг/кг/мин, которая сохранялась в течение всего периода наблюдения в педиатрическом стационаре и в ходе транспортировки при переводе в кардиохирургический стационар. В данном клиническом случае полностью отойти от ИВЛ было невозможно (учитывая тяжесть дыхательной недостаточности), на 5-й день госпитализации (19-е сутки жизни) ребенок на фоне терапии переведен в клинику им. Мешалкина, где была успешно проведена коррекция порока — формирование аортолегочного шунта.
В случаях развития сердечной недостаточности у новорожденных при пороках, сопровождающихся массивным сбросом крови в малый круг кровообращения, применяется тот же принцип мониторинга основных показателей и симптоматическая терапия:
При появлении симптомов перегрузки малого круга (аускультативно — усиление, расщепление 2-го тона на легочной артерии, на ЭхоКГ — увеличение давления в легочной артерии более 30 мм рт. ст. после шести суток жизни), а также признаков нарушения диастолической функции сердца рекомендуется применять препараты из группы ингибиторов ангиотензин-превращающего фермента (иАПФ). Используется Капотен (каптоприл) в дозе 0,5–1 мг/кг при условии контроля системного АД. Терапевтическое действие иАПФ связано со снижением периферического сопротивления сосудов и частичным депонированием крови, в результате чего уменьшается объем крови, возвращаемой в правые отделы сердца. Соответственно уменьшается объем шунта и нагрузка на левые камеры и сосуды малого круга. Кроме того, известно, что иАПФ являются ингибитором апоптоза, стимулированного гипоксией, что объясняет ангио- и кардиопротективный эффект препаратов.
Таким образом, тактика педиатра, включающая раннюю диагностику критических ВПС и терапию, управляющую внутрисердечной, центральной и периферической гемодинамикой, а также по возможности ранняя координация действий с кардиохирургическим центром способны существенно улучшить прогноз больных и уменьшить показатели младенческой смертности.
Литература
Е. Ю. Емельянчик*, доктор медицинских наук, профессор
Д. Б. Дробот*, доктор медицинских наук, профессор
Е. П. Кириллова*, кандидат медицинских наук, доцент
В. А. Сакович*, доктор медицинских наук, профессор
Е. В. Басалова**
А. Ю. Черемисина*
*ГОУ ВПО Красноярский ГМУ им. профессора В. Ф. Войно-Ясенецкого,
**Краевая клиническая детская больница, Красноярск




