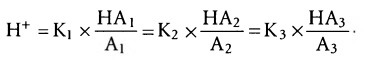Что такое буферность клетки
а) Внутриклеточные буферные системы и роль белков. Белки вследствие высокого содержания во внутриклеточной жидкости являются наиболее важными компонентами внутриклеточных буферных систем.
Несмотря на то, что рН в клетках немного ниже, чем снаружи, его величина внутри клеток изменяется в соответствии с колебаниями во внеклеточной жидкости. Протоны и бикарбонаты медленно и в небольшом количестве диффундируют через клеточную мембрану, поэтому для восстановления равновесия обычно требуется несколько часов. Исключение составляют лишь эритроциты, в которых равновесие восстанавливается очень быстро.
СО2, тем не менее, способен к быстрой диффузии через мембрану. Диффузия компонентов бикарбонатной буферной системы изменяет рН внутри клеток в соответствии с колебаниями во внеклеточной жидкости. По этой причине внутриклеточные буферные системы препятствуют изменению рН во внеклеточной жидкости, хотя для достижения максимального результата может потребоваться несколько часов.
В эритроцитах главным является гемоглобиновый буфер (Нb), действующий следующим образом:
В дополнение к высокой концентрации белков в клетках другим фактором, увеличивающим буферную емкость, является значение рК белков, близкое к 7,4.
б) Изогидрическое правило: в растворе, содержащем несколько буферных систем, поддерживается одна и та же концентрация ионов водорода. Ранее мы исследовали индивидуальные свойства каждой из буферных систем в отдельности, без учета их взаимодействий с другими. Тем не менее, все они работают слаженно, поскольку уровень содержания ионов Н+ во всех жидких средах одинаков. Но каждый раз, когда возникает изменение концентрации протонов во внеклеточной жидкости, этому препятствуют все буферные системы. Это явление называют изогидрическим правилом, которое выражается следующим уравнением:
где K1, К2, К3 — константы диссоциации трех соответствующих кислот, HA1, HA2, HA3 и A1, A2, A3 — концентрация свободных анионов, которые составляют основания трех буферных систем.
Согласно этому правилу любое условие, изменяющее равновесие в одной из буферных систем, также смещает его и во всех остальных, поскольку буферные системы взаимодействуют между собой, перераспределяя ионы Н+.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Физиология и нарушения кислотно-основного состояния (методические материалы к практическим и семинарским занятиям)
Информация
Справочное пособие содержит информацию о физиологии кислотно- основного состояния (КОС). Представлена информация о методах лабораторной диагностики нарушений КОС. Перечислены варианты нарушений и методы коррекции. Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
Физиология кислотно-основного состояния
В норме сильных кислот образуется 50 – 100 ммоль/сутки. При избыточном образовании они вызывают тяжелые нарушения. Это происходит при анаэробном окислении глюкозы.
В норме окисление глюкозы происходит аэробно: С6Н12О2 + 6О2 = 6Н2О + 6СО2 + 38 АТФ
Рис. 1. Доставка 02 к тканям и первые стадии элиминации CO2
Рис. 2. В легких бикарбонат снова превращается в С02 и выводится
Транспорт кислорода из легких к тканям и из тканей к легким обусловлен изменениями, которые воздействуют на сродство кислорода к гемоглобину. На уровне тканей из-за снижения рН это сродство уменьшается (эффект Бора) и вследствие этого улучшается отдача кислорода. В крови легочных капилляров сродство гемоглобина к кислороду увеличивается из-за снижения рС02 и возрастания рН по сравнению с аналогичными показателями венозной крови, что приводит к повышению насыщения артериальной крови кислородом.
Первичные изменения КЩС и компенсаторные реакции
Биология. 10 класс
Конспект урока
Урок 2. «Неорганические соединения клетки. Углеводы и липиды. Регулярные и нерегулярные биополимеры»
3. Перечень вопросов, рассматриваемых в теме;
Урок позволит выявить особенности химического состава организмов, роль неорганических (воды, солей) и органических (углеводов, липидов) веществ в жизни клетки и организма.
Обучающиеся узнают, какие химические элементы входят в состав живых организмов, рассмотрят самое важное минеральное вещество на Земле, структуру молекулы воды и её биологическую роль, выяснят физические и химические свойства воды, благодаря которым возможно существование жизни на Земле.
Также обучающиеся увидят особенности строения органических веществ, узнают, на какие классы делятся углеводы и липиды, их значение для жизнедеятельности клетки и организма в целом.
4. Глоссарий по теме (перечень терминов и понятий, введенных на данном уроке);
Биологически значимые элементы, органогены, неорганические вещества, вода, водородная связь, гидрофильные вещества, гидрофобные вещества; органические вещества, регулярные и нерегулярные биополимеры; углеводы, липиды
Биологически значимые элементы – химические элементы, необходимые живым организмам для обеспечения нормальной жизнедеятельности.
Органогены — химические элементы, входящие в состав всех органических соединений, составляют около 98% массы клетки (углерод, водород, кислород, азот).
Неорганические вещества (неорганические соединения) клетки — простые вещества и соединения, не являющиеся органическими, не имеют характерного для органических веществ углеродного скелета.
Органические вещества – это сложные соединения, основой строения которых являются атомы углерода, составляют отличительный признак живого. Органические соединения многообразны, но четыре группы из них имеют всеобщее биологическое значение: белки, нуклеиновые кислоты, углеводы и липиды.
Водородная связь – вид взаимодействия между молекулами вещества. Молекулы воды удерживаются за счет водородных связей, которые возникли между частично положительным атомом водорода одной молекулы и частично отрицательным атомом кислорода другой молекулы. Водородные связи заметно слабее по сравнению с ковалентными. Однако они намного крепче, чем стандартное молекулярное притяжение частиц, свойственное твёрдым и жидким телам.
Гидрофильные вещества – хорошо растворимые в воде вещества, молекулы которых полярны и легко соединяются с молекулами воды. К ним относятся ионные соединения (содержат заряженные частицы): соли, кислоты, основания и полярные соединения (в молекулах присутствуют заряженные группы): сахара, простые спирты, аминокислоты.
Гидрофобные вещества– нерастворимые в воде вещества, энергия притяжения молекул которых к молекулам воды меньше энергии водородных связей молекул воды. К числу гидрофобных веществ относятся жиры, полисахариды, нуклеиновые кислоты, большинство белков.
Буферность – способность клетки поддерживать слабощелочную реакцию своего содержимого на постоянном уровне.
Полимер (от греч. «поли» — много) — многозвеньевая цепь, в которой звеном является какое-либо относительно простое вещество — мономер.
Регулярные полимеры – полимеры, в молекуле которых группа мономеров периодически повторяется (полисахариды).
Нерегулярные полимеры – полимеры, в которых нет определенной закономерности в последовательности мономеров (белки, нуклеиновые кислоты, некоторые полисахариды).
Углеводы – органические соединения, состоящие из атомов углерода, кислорода и водорода. В большинстве углеводов водород и кислород находятся, как правило, в тех же соотношениях, что и в воде (отсюда их название — углеводы).
Полисахариды – высокомолекулярные углеводы, молекулы которых представляют собой длинные линейные или разветвлённые цепочки моносахаридных остатков, соединённых гликозидной связью. При гидролизе образуют моносахариды или олигосахариды.
Липиды — обширная группа органических соединений, включающая жиры и жироподобные вещества. Молекулы простых липидов состоят из спирта и жирных кислот, сложных — из спирта, высокомолекулярных жирных кислот и других компонентов
5. Основная и дополнительная литература по теме урока (точные библиографические данные с указанием страниц);
6. Открытые электронные ресурсы по теме урока (при наличии);
1.Российский общеобразовательный Портал www.school.edu.ru
2 Единая коллекция цифровых образовательных ресурсов www.school-collection.edu.ru
3.Каталог образовательных ресурсов по биологии http://www.mec.tgl.ru/index.php?module=subjects&func=viewpage&pageid=133
7. Теоретический материал для самостоятельного изучения;
В состав живой клетки входят те же химические элементы, которые входят в состав неживой природы. Из 104 элементов периодической системы Д. И. Менделеева в клетках обнаружено 60.
Их делят на три группы:
Молекулярный состав клетки сложный и разнородный. Отдельные соединения — вода и минеральные соли — встречаются также в неживой природе; другие — органические соединения: углеводы, жиры, белки, нуклеиновые кислоты и др.— характерны только для живых организмов.
Вода составляет около 80 % массы клетки; в молодых быстрорастущих клетках — до 95 %, в старых — 60 %.
Роль воды в клетке велика.
Она является основной средой и растворителем, участвует в большинстве химических реакций, перемещении веществ, терморегуляции, образовании клеточных структур, определяет объем и упругость клетки. Большинство веществ поступает в организм и выводится из него в водном растворе. Биологическая роль воды определяется специфичностью строения: полярностью ее молекул и способностью образовывать водородные связи, за счет которых возникают комплексы из нескольких молекул воды. Если энергия притяжения между молекулами воды меньше, чем между молекулами воды и вещества, оно растворяется в воде. Такие вещества называют гидрофильными (от греч. «гидро» — вода, «филее» — люблю). Это многие минеральные соли, белки, углеводы и др. Если энергия притяжения между молекулами воды больше, чем энергия притяжения между молекулами воды и вещества, такие вещества нерастворимы (или слаборастворимы), их называют гидрофобными (от греч. «фобос» — страх) — жиры, липиды и др.
Органические вещества в комплексе образуют около 20—30% состава клетки.
Углеводы — органические соединения, состоящие из углерода, водорода и кислорода. Их делят на простые — моносахариды (от греч. «монос» — один) и сложные — полисахариды (от греч. «поли» — много).
Моносахариды (их общая формула СnН2nОn) — бесцветные вещества с приятным сладким вкусом, хорошо растворимы в воде. Они различаются по количеству атомов углерода. Из моносахаридов наиболее распространены гексозы (с 6 атомами С): глюкоза, фруктоза (содержащиеся в фруктах, меде, крови) и галактоза (содержащаяся в молоке). Из пентоз (с 5 атомами С) наиболее распространены рибоза и дезоксирибоза, входящие в состав нуклеиновых кислот и АТФ.
Полисахариды относятся к полимерам — соединениям, у которых многократно повторяется один и тот же мономер. Мономерами полисахаридов являются моносахариды. Полисахариды растворимы в воде, многие обладают сладким вкусом. Из них наиболее просты дисахариды, состоящие из двух моносахаридов. Например, сахароза состоит из глюкозы и фруктозы; молочный сахар — из глюкозы и галактозы. С увеличением числа мономеров растворимость полисахаридов падает. Из высокомолекулярных полисахаридов наиболее распространены у животных гликоген, у растений — крахмал и клетчатка (целлюлоза). Последняя состоит из 150—200 молекул глюкозы.
Углеводы — основной источник энергии для всех форм клеточной активности (движение, биосинтез, секреция и т. д.). Расщепляясь до простейших продуктов СO2 и Н2O, 1 г углевода освобождает 17,6 кДж энергии. Углеводы выполняют строительную функцию у растений (их оболочки состоят из целлюлозы) и роль запасных веществ (у растений — крахмал, у животных — гликоген).
Липиды — это нерастворимые в воде жироподобные вещества и жиры, состоящие из глицерина и высокомолекулярных жирных кислот. Животные жиры содержатся в молоке, мясе, подкожной клетчатке. При комнатной температуре это твердые вещества. У растений жиры находятся в семенах, плодах и других органах. При комнатной температуре это жидкости. С жирами по химической структуре сходны жироподобные вещества. Их много в желтке яиц, клетках мозга и других тканях.
Роль липидов определяется их структурной функцией. Из них состоят клеточные мембраны, которые вследствие своей гидрофобности препятствуют смешению содержимого клетки с окружающей средой. Липиды выполняют энергетическую функцию. Расщепляясь до СO2 и Н2O, 1 г жира выделяет 38,9 кДж энергии. Они плохо проводят тепло, накапливаясь в подкожной клетчатке (и других органах и тканях), выполняют защитную функцию и роль запасных веществ.
8. примеры и разбор решения заданий тренировочного модуля (не менее 2 заданий).
Найдите и выделите цветом по вертикали и горизонтали названия химических элементов:
Тип вариантов ответов: Текстовые,Графические, Комбинированные.
Правильный вариант/варианты (или правильные комбинации вариантов):
Подсказка:при необходимости обратитесь к дополнительным материалам
Заполните пропуски в тексте, выбрав вариант ответа из выпадающего списка.
Выпадающий список 1.
Выпадающий список 2.
Тип вариантов ответов: Текстовые, Графические, Комбинированные.
Правильный вариант/варианты (или правильные комбинации вариантов):выделены жирным шрифтом
Выпадающий список 1.
Выпадающий список 2.
Подсказка:В большинстве клеток организма рН составляет 7,0 – 7,4.
Что такое буферность клетки
Одним из условий наиболее полной оценки состояния почвенного плодородия является определение совокупности показателей, характеризующих его со всех сторон имеющегося в почве вещества: твердого, жидкого, воздушного и живого. С другой стороны, существует ряд интегральных характеристик, позволяющих в комплексе оценить почву не только как средство питания сельскохозяйственных растений, но и как самостоятельный объект биогеоценоза, взаимодействующий с окружающей средой. В частности, к таким показателям относится содержание гумуса в почве, степень ее кислотности и щелочности, емкость обмена, буферная способность и другие. К последней относят свойство почвы оказывать сопротивление к изменению собственного состояния под влиянием какого-либо фактора окружающей среды [6].
Современные научные изыскания нетрадиционных кремнийсодержащих источников питания культурных растений описывают их положительное влияние на агрохимическую и микробиологическую характеристику почвы и, в том числе, позитивное влияние на обменную кислотность [1, 2, 5]. Известно, что диатомиты представляют собой преобразованные остатки диатомовых водорослей, обладающие емкостью поглощения и содержащие большое количество амфотерного элемента кремния (более 82 % SiO2). В связи с этим предполагается, что диатомиты могут проявлять буферные свойства и способны повлиять на буферность почвы.
Цель исследования. Изучение кислотно-основных свойств диатомита Инзенского месторождения Ульяновской области и светло-серой лесной легкосуглинистой почвы, обработанной диатомитовым порошком.
Материалы и методы исследования
В опыте № 1 образец Инзенского диатомита был проанализирован на определение кислотности его суспензий потенциометрическим методом. Определение рН водной и солевой (1 n раствор KCl) вытяжек порошка диатомита, предварительно размолотого и просеянного через сито с диаметром ячеек в 0,5 мм, проводилось с помощью ионометра PortLab-102, откалиброванного по трем буферным растворам – 4,01, 6,86 и 9,18 ед. рН. Результаты измерений представлены в таблице.
В опыте № 2 изучалась кислотно-основная буферность светло-серой лесной легкосуглинистой почвы и порошка диатомита. Буферность определялась потенциометрическим методом по Аррениусу [7] с определением площадей буферности в кислотном и щелочном интервалах [3], результаты которого представлены на рис. 1.
В опыте № 3 изучалось действие диатомита на буферные свойства светло-серой лесной легкосуглинистой почвы. для этого почва предварительно компостировалась с тонкоразмолотым порошком диатомита в течение 4-х месяцев в полиэтиленовых пакетах при t ≈ +25 ºС с еженедельным увлажнением до 60 % от ПВ и перемешиванием. Доза диатомита составила 1,5 г/кг почвы. В дальнейшем проводилось определение кислотно-основной буферности по Аррениусу, результаты которого представлены на рис. 2.
Результаты исследования и их обсуждение
Установлено, что водная вытяжка диатомита (табл. 1), независимо от его соотношения с водой, обладала слабощелочной реакцией. Такое явление можно объяснить наличием в составе диатомитовой породы около 50 мг-экв. ионов Ca2+ и Mg2+, способных к обменным реакциям, а также амфотерными свойствами кремния, входящего в состав диатомита в большом количестве. В частности, элемент кремний, проявляющий двойственные кислотно-основные свойства, в структуре исследуемого вещества образует, в том числе, и соединения основной природы типа Si(OH)4, которые, диссоциируя в растворе, подщелачивают его ионами ОН– [6].
При взаимодействии солевого раствора гидролитически нейтральной соли (1 n раствора KCl) с диатомитом в различных объемных соотношениях отмечалось снижение показателя рН относительно его определения в водной вытяжке диатомита. Предполагается, что диатомит обладает определенной емкостью поглощения, из которой, по-видимому, раствор хлористого калия вытесняет кислотные катионы. Например, такие катионы как Al3+ и Fe3+, содержание веществ которых в диатомовой агроруде превышает соответственно 5 % и 2 %, способны образовывать в растворе соединения кислотного характера, которые и подкисляют среду. В итоге выделяющиеся из диатомита катионы способствуют незначительному увеличению кислотности суспензии и, как следствие, снижению ее рН.
Повышение показателя рНводн. при увеличении соотношения экстрагирующего вещества и диатомита, очевидно, свидетельствует о повышении растворимости щелочных соединений, входящих в состав агроруды при разбавлении ее порошка. Увеличение же показателя кислотности (рНсол.) диатомита при разбавлении его солевым раствором, в свою очередь, может говорить о повышении степени вытеснения всех катионов из диатомита в раствор, большинство которых, очевидно, имеет щелочную природу.
На рис. 1 (опыт № 2) видно, что исследуемая почва обладает определенной буферной силой, причем ее площадь в кислотном интервале (рН 1-7) немного больше площади щелочного интервала (рН 7-14), что обусловлено присутствием большего количества кислотных ионов (H+, Al3+, Fe3+) в ППК почвы относительно щелочных (Ca2+, Mg2+). Поэтому в расчете полной дозы извести, необходимой для снижения кислотности светло-серой лесной легкосуглинистой почвы, берется увеличенная доля значения гидролитической кислотности почвы – 1,2 от НГ [4]. Кроме того, установлено, что диатомит Инзенского месторождения также обладает буферными свойствами. Причем, площадь буферной силы в щелочном интервале визуально несколько больше площади кислотного. Это явление также подтверждает слабощелочные свойства исследуемого вещества.
Определение актуальной и обменной кислотности диатомита
Буферность
Смотреть что такое «Буферность» в других словарях:
буферность — В химии океана — процесс, благодаря которому углеродный цикл в морской воде поддерживает отношение ионов Н+ к ионам ОН близким к единице, или нейтральный водородный показатель рН. [http://www.oceanographers.ru/index.php?option=com glossary… … Справочник технического переводчика
Буферность — * буфернасць * buffering устойчивость системы к изменениям, вызываемым внешними факторами … Генетика. Энциклопедический словарь
буферность — buferingumas statusas T sritis augalininkystė apibrėžtis Atsparumas išorinių veiksnių sukeliamiems pakitimams. atitikmenys: angl. buffering rus. буферность … Žemės ūkio augalų selekcijos ir sėklininkystės terminų žodynas
буферность — б уферность, и … Русский орфографический словарь
Буферность почвы — (от англ. buff смягчать толчки), способность почвы сохранять реакцию среды (pH) при действии кислот и щелочей. Экологический энциклопедический словарь. Кишинев: Главная редакция Молдавской советской энциклопедии. И.И. Дедю. 1989. Буферность почвы … Экологический словарь
Буферность почвы — совокупность свойств почвы, определяющих ее барьерную функцию, обуславливающую уровни вторичного загрязнения химическими веществами контактирующих с почвой сред: растительности, поверхностных и подземных вод, атмосферного воздуха. Основными… … Официальная терминология
буферность почвы — Способность почвы противостоять изменению реакции почвенного раствора в кислую или щелочную сторону. [ГОСТ 20432 83] буферность почвы Способность почвы противостоять изменению ее свойств при воздействии различных факторов [ГОСТ 27593 88] Тематики … Справочник технического переводчика
БУФЕРНОСТЬ БИОСФЕРЫ — способность биосферы противостоять (нейтрализовать) антропогенным загрязнениям и др. вредным воздействиям. Экологический энциклопедический словарь. Кишинев: Главная редакция Молдавской советской энциклопедии. И.И. Дедю. 1989 … Экологический словарь
БУФЕРНОСТЬ ПОПУЛЯЦИИ — способность популяции предотвращать потери, возникающие в случае, когда среда становится неблагоприятной. Термин предложил Р. Уиттекер (1970). Экологический энциклопедический словарь. Кишинев: Главная редакция Молдавской советской энциклопедии. И … Экологический словарь