Что такое дипольность воды в биологии
Неорганические вещества клетки. Вода, соли, их роль в жизнедеятельности клетки.
Большинство химических соединений, которые входят в состав клетки, встречаются только в живой природе. Почти все молекулы за небольшим исключением, встречающиеся в клетке, относятся к соединениям углерода и рассматриваются в курсе органической химии. Однако вода встречается и в живой, и в неживой природе. В среднем почти 70% от массы живых организмов составляет вода. Но содержание воды в клетке может колебаться в зависимости, например, от ее конкретного вида или возраста. Помимо воды в клетках в значительных количествах встречаются некоторые соли, которые важны для осуществления функций живых организмов.
Вода (H2O) представляет собой вещество, которое в физическом и химическом отношении существенно отличается от других растворителей. Жизнь возникла в первичном океане, и в процессе дальнейшего развития природа использовала уникальные свойства воды.
У воды в отличии от других жидкостей необычайно высокие температуры кипения и плавления и высокая удельная теплоемкость. Также отличительными особенностями воды являются большая удельная теплота испарения, плавления и высокое поверхностное натяжение. Вода имеет все эти свойства благодаря тому, что ее молекулы более прочно связаны друг с другом в отличии от молекул других растворителей.
Эти уникальные свойства воды оказывают большое влияние на жизнедеятельность клеток. Например, высокая теплоемкость воды, т.е. способность поглощать тепло при незначительном изменении своей собственной температуры, предохраняет клетки от резких изменений температуры. Высокую теплоту испарения воды живые организмы используют для предохранения от перегрева. Вспомним, что испарение жидкости животными и растениями — это защитная реакция на повышение температуры. Благодаря высокой теплопроводности воды обеспечивается равномерное распределение теплоты по всему организму, а благодаря тому, что вода плохо сжимается, клетки обладают упругостью и могут поддерживать свою форму.
Свои уникальные физические и химические свойства вода получила благодаря особенностям структуры своей молекулы, а точнее, благодаря тому, как именно в молекуле воды располагаются электроны в атомах кислорода и водорода. Два электрона, располагающиеся на внешней электронной орбите атома кислорода в молекуле воды, объединяются с двумя электронами, принадлежащими атомам водорода (у атома водорода на внешней орбите только один электрон). Благодаря этому в молекуле воды образуются две ковалентные связи (между атомом кислорода и двумя атомами водорода). Электроотрицательность * атома кислорода выше, чем у атомов водорода, благодаря чему, электроны притягиваются к нему сильнее. В результате этого на атоме кислорода появляется частично отрицательный заряд, а на атомах водорода — частично положительный. Между более отрицательно заряженными атомами кислорода одних молекул воды и более положительно заряженными атомами водорода других молекул воды образуются так называемые водородные связи, и молекулы воды оказываются связанными между собой.
* Электроотрицательность — это способность атома в молекуле смещать к себе общие электронные пары. Относится к фунадментальным свойствам атома и выражается в количественных характеристиках.
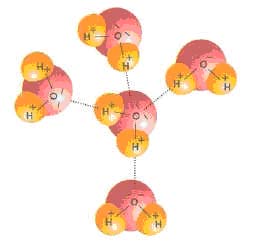
5 молекул воды с водородными связями между ними
На рисунке изображены молекулы воды. Ковалентные связи связывают атомы кислорода и водорода внутри каждой молекулы (сплошные линии), а водородные связи образуются между соседними молекулами (пунктирные линии).
Водородные связи примерно в 20 раз более слабые, чем ковалентные. Поэтому они легко образуются и разрываются. Даже при температуре кипения (100°С) взамодействие между молекулами воды остается достаточно сильным. Именно водородные связи обеспечивают структурированность воды и объясняют такие ее свойства, как высокие температуры кипения и плавления, а также высокую теплоемкость.
Другое важное свойство молекулы воды — ее дипольность. В молекуле воды, как отмечалось ранее, атомы кислорода имеют небольшой отрицательный заряд, а атомы водорода — положительный. Т.к. угол между связями H-O-H составляет 104.5°, получается, что отрицательный заряд в молекуле воды сосредотачивается на одной стороне, а положительный — на другой. Благодаря дипольности молекулы воды имеют способность к ориентации в электрическом поле. Это свойство объясняет, что вода является уникальным растворителем. Если в молекулах веществ присутствуют заряженные группы атомов, они, вступая в электростатическое взаимодействие с молекулами воды, растворяются в ней. Такие вещества с заряженными или полярными группами, растворяющиеся в воде, называются гидрофильными.
Растворение NaCl в воде.
Способность воды растворять кристалл NaCl зависит от электростатического притяжения между полярными молекулами воды и заряженными ионами натрия и хлора.
К гидрофильным соединениям, которые в большом количестве есть в клетках, относятся соли, некоторые низкомолекулярные органические соединения (органические кислоты, аминокислоты, простые сахара), а также полимеры: некоторые полисахариды, белки, нуклеиновые кислоты. Однако существует ряд веществ, почти не имеющих заряженных атомов, и, поэтому, не растворяющихся в воде. Такие вещества называются гидрофобными. К ним, например, относятся липиды (жиры). Гидрофобные вещества не взаимодействуют с водой, но могут взаимодействовать друг с другом. Поэтому они хорошо растворяются в некоторых органических растворителях, как, например, хлороформ. Липиды, относящиеся к гидрофобным соединениям, формируют двумерные структуры (биологические мембраны), практически непроницаемые для воды.
По сравнению с другими растворителями вода может растворить больше химических веществ, благодаря своей полярности. Жизнедеятельность клетки невозможна без многочисленных химических реакций, которые осуществляются в ее водной среде, где растворены различные химические вещества. Также вода растворяет и продукты реакций. Затем в растворенном виде они выводятся из клеток и многоклеточных организмов. За счет перемещения воды в организмах животных и растений осуществляется обмен различными веществами между тканями. Еще одним важным свойством воды является то, что, как химическое соединение, вода вступает во многие химические реакции, которые протекают в клетке. Такие реакции называют реакциями гидролиза. В свою очередь, молекулы воды сами образуются в результате многих реакций в клетках живых организмов.
Т.к. масса атома водорода мала, а атом кислорода в молекуле воды удерживает его единственный электрон, протон (ядро атома водорода, лишенное электрона) способен отрываться от молекулы воды. В результате этого из молекулы воды образуются гидроксильный ион (ОН — ) и протон (Н + ).
H2O H + + OH —
Данный процесс называют диссоциацией воды. Гидроксильные ионы и протоны, которые образуются при диссоциации воды, являются, в свою очередь, участниками многих важных реакций в живых организмах.
Необходимо отметить, что анионы слабых кислот вступают в химические реакции, происходящие в клетке. Например, для синтеза АТФ, одного из важных соединений для клетки, необходимы анионы фосфорной кислоты. О синтезе АТФ я расскажу более подробно позднее. Неорганические вещества в живых организмах содержатся не только в растворенном, но и в твердом состоянии. В качестве примера можно привести кости, где преобладает фосфат кальция и в меньшем количестве фосфат магния. В раковинах моллюсков преобладает карбонат кальция.
Что такое дипольность воды в биологии
Из-за блокировщика рекламы некоторые функции на сайте могут работать некорректно! Пожалуйста, отключите блокировщик рекламы на этом сайте.
Свойства воды и ее роль в клетке:
На первом месте среди веществ клетки стоит вода. Она составляет около 80% массы клетки. Вода важна для живых организмов вдвойне, ибо она необходима не только как компонент клеток, но для многих и как среда обитания.
2. Многие химические процессы протекают только в водном растворе.
4. Вода обладает высокой теплоемкостью и теплопроводностью.
5. Вода обладает уникальным свойством: при охлаждении ее от +4 до 0 градусов, она расширяется. Поэтому лед оказывается легче жидкой воды и остается на ее поверхности. Это очень важно для организмов, обитающих в водной среде.
6. Вода может быть хорошим смазочным материалом.
Биологическая роль воды определяется малыми размерами ее молекул, их полярностью и способностью соединяться друг с другом водородными связями.
Биологические функции воды:
транспортная. Вода обеспечивает передвижение веществ в клетке и организме, поглощение веществ и выведение продуктов метаболизма. В природе вода переносит продукты жизнедеятельности в почвы и к водоемам.
метаболическая. Вода является средой для всех биохимических реакций, донором электронов при фотосинтезе; она необходима для гидролиза макромолекул до их мономеров.
вода участвует в образовании смазывающих жидкостей и слизей, секретов и соков в организме.
За очень немногими исключениями (кость и эмаль зуба), вода является преобладающим компонентом клетки. Вода необходима для метаболизма (обмена) клетки, так как физиологические процессы происходят исключительно в водной среде. Молекулы воды участвуют во многих ферментативных реакциях клетки. Например, расщепление белков, углеводов и других веществ происходит в результате катализируемого ферментами взаимодействия их с водой. Такие реакции называются реакциями гидролиза.
Вода служит источником ионов водорода при фотосинтезе. Вода в клетке находится в двух формах: свободной и связанной. Свободная вода составляет 95% всей воды в клетке и используется главным образом как растворитель и как дисперсионная среда коллоидной системы протоплазмы. Связанная вода, на долю которой приходится всего 4% всей воды клетки, непрочно соединена с белками водородными связями.
Из-за асимметричного распределения зарядов молекула воды действует как диполь и потому может быть связана как положительно, так и отрицательно заряженными группами белка. Дипольным свойством молекулы воды объясняется способность ее ориентироваться в электрическом поле, присоединяться к различным молекулам и участкам молекул, несущим заряд. В результате этого образуются гидраты
Благодаря своей высокой теплоемкости вода поглощает тепло и тем самым предотвращает резкие колебания температуры в клетке. Содержание воды в организме зависит от его возраста и метаболической активности. Оно наиболее высоко в эмбрионе (90% ) и с возрастом постепенно уменьшается. Содержание воды в различных тканях варьируется в зависимости от их метаболической активности. Например, в сером веществе мозга воды до 80%, а в костях до 20%. Вода — основное средство перемещения веществ в организме (ток крови, лимфы, восходящие и нисходящие токи растворов по сосудам у растений) и в клетке. Вода служит «смазочным» материалом, необходимым везде, где есть трущиеся поверхности (например, в суставах). Вода имеет максимальную плотность при 4°С. Поэтому лед, обладающий меньшей плотностью, легче воды и плавает на ее поверхности, что защищает водоем от промерзания. Это свойство воды спасает жизнь многим водным организмам.
Изучение движения молекулы воды в электрическом и магнитном полях
ИЗУЧЕНИЕ ДВИЖЕНИЯ
МОЛЕКУЛЫ ВОДЫ В ЭЛЕКТРИЧЕСКОМ И МАГНИТНОМ ПОЛЯХ
Оглавление
Характеристики воды 3
Электрические свойства молекул и дипольный момент 4
Движение молекулы воды в электрическом поле 5
Магнитный дипольный момент 7
Движение молекулы воды в магнитном поле 8
Список литературных источников 9
Введение
Вода – одно из самых распространенных веществ на нашей планете, она имеет огромное значение в эволюции как живой, так и неживой природы. Спектр применения воды необычайно широк: быт, промышленность, сельское хозяйство – этот список можно продолжать сколь угодно долго. Именно поэтому изучением воды, ее физических и химических свойств, до сих пор занимаются ученые всего мира. Вода, казалось бы, самое обыкновенное вещество, но имеет столько неразгаданных тайн и неизученных свойств.
Тема данной исследовательской работы – «Изучение движения молекулы воды в электрическом и магнитном полях». Чтобы больше понять о веществе, нужно рассмотреть его мельчайшую частицу – атом либо молекулу. В этой работе будут рассмотрены некие свойства молекулы воды.
Изучение движения молекулы представляет практический интерес. Как влияет на молекулу однородное, неоднородное электрическое поле? Каким образом молекула движется в магнитном поле?
Характеристики воды
Вода (оксид водорода) – бинарное неорганическое соединение, химическая формула – 
При нормальных условиях вода – прозрачная жидкость, не имеющая ни цвета (в малом объеме), ни запаха, ни вкуса. В твёрдом состоянии называется льдом (кристаллы льда могут образовывать снег или иней), а в газообразном – водяным паром. При атмосферном давлении вода замерзает (превращается в лёд) при температуре в 0°C и кипит (превращается в водяной пар) при температуре 100°C.
Плотность воды – 0,9982 г/куб. см., ее динамическая вязкость (ст. усл.) – 0,00101 Па•с (при 20°C), ее кинематическая вязкость (ст. усл.) – 0,01012 кв. см/с (при 20°C), температура плавления – 0°C, температура кипения – 99,974°C, молярная теплоёмкость (ст. усл.) – 75,37 Дж/(моль•К), теплопроводность (ст. усл.) – 0,56 Вт/(м•K).
При давлении в 611,73 Па температура кипения и плавления совпадает и становится равной 0,01°C. Такое давление и температура называются тройной точкой воды. [3]
При более низком давлении вода не может находиться в жидком состоянии, и лёд превращается непосредственно в пар. Температура возгонки льда падает со снижением давления.
При температуре 374°C (647 K) и давлении 22,064 МПа вода проходит критическую точку. В этой точке плотность и другие свойства жидкой и газообразной воды совпадают. [4]
При более высоком давлении нет разницы между жидкой водой и водяным паром, следовательно, нет и кипения или испарения.
При таянии льда, его плотность увеличивается (с 0,9 до 1 г/куб. см). Почти у всех остальных веществ при плавлении плотность уменьшается. При нагревании от 0°C до 4°C (точнее 3,98°C), вода сжимается. Благодаря этому могут жить рыбы в замерзающих водоёмах: когда температура падает ниже 4°C, более холодная вода, как менее плотная остаётся на поверхности и замерзает, а под льдом сохраняется положительная температура. Высокая температура и удельная теплота плавления (0°C и 333,55 кДж/кг), температура кипения (100°C) и удельная теплота парообразования (2250 КДж/кг), по сравнению с соединениями водорода с похожим молекулярным весом. Высокая теплоёмкость жидкой воды. Высокая вязкость. Высокое поверхностное натяжение.
Это свойство воды используется живыми существами. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде. Вода необходима для жизни всех без исключения одноклеточных и многоклеточных живых существ на Земле.
Вода имеет показатель преломления n=1,33 в оптическом диапазоне. [4] Однако она сильно поглощает инфракрасное излучение, и поэтому водяной пар является основным естественным парниковым газом. Он отвечает более чем за 60% парникового эффекта. [4] Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, на чём основан принцип действия микроволновой печи. [4]
Электрические свойства молекул и дипольный момент
Электрические свойства молекул – важные характеристики строения молекул. Изучение таких свойств устанавливает закономерности связи свойств со строение молекул. Знание электрических свойств поможет при описании явлений, происходящих при помещении молекулы в электрическое поле, в чем и состоит цель данной работы.
Молекулы всех веществ делятся на полярные (дипольные) и неполярные. В дипольных молекулах центры отрицательных и положительных зарядов не совпадают, к таким молекулам относится молекула воды.
Атомы в молекуле воды расположены под углом, вершина которого – атом кислорода, он является центром распределения отрицательного заряда, а между атомами водорода – центр распределения положительного заряда. Заряды создают молекулярные силовые поля. [2] Количественная характеристика полярности определяется электрическим моментом диполя, который равен произведению величины положительного заряда на расстояние между зарядами и направлен от отрицательного заряда к положительному:

где q – величина положительного заряда, I – вектор с началом в отрицательном заряде и концом в положительном.
Для системы из N частиц электрический дипольный момент равен

где 



Для воды дипольный момент равен: 

Движение молекулы воды в электрическом поле
Итак, будет ли электрическое поле действовать на помещенную в него молекулу воды? Каково это действие? Каким будет движение молекулы, поступательным или вращательным? Какова будет скорость молекулы, ее перемещение, ускорение?
Прежде всего, необходимо рассмотреть движение заряженных частиц в электрическом поле. На заряженную частицу в электростатическом поле действует кулоновская сила, которую можно найти по следующей формуле:

Кулоновская сила сообщает ускорение:

где m – масса заряженной частицы [1].
Но вода – диэлектрик, то есть молекула воды нейтральна. Действует ли на нее электрическое поле?
Так как молекула воды – диполь, то действие электрического поля направлено на ее разноименные полюса. На положительные полюса действует сила, направленная по линиям напряженности поля, а на отрицательный полюс – сила, направленная против линий напряженности. Электрическое поле окажет на молекулу воды ориентирующее действие вдоль направления поля. Этому препятствует хаотическое тепловое движение молекул, стремящееся произвольно «разбросать» диполи. В итоге совместного действия поля и теплового движения возникает преимущественная ориентация дипольных электрических моментов вдоль поля, возрастающая с увеличением напряженности электрического поля и с уменьшением температуры [2].
В однородном внешнем электрическом поле с напряженностью Е на заряды диполя будут действовать силы F1 = F2 = qE. Разложим их на составляющие 








Рис.1.3. Диполь в однородном электрическом поле





Вращающий момент (момент сил), действующий на молекулу во внешнем поле в скалярной и векторной формах:

Вектор момента направлен перпендикулярно плоскости рисунка, то есть при помещении диполя в электрическое поле 


Молекула приобретает угловое ускорение 




Момент инерции молекулы воды может быть выполнен по формуле классической механики:

где K – общее число химических элементов, образующих исследуемую молекулу; 



Момент инерции служит мерой инертности тела при вращении, а следовательно, играет ту же роль, что и масса при поступательном движении.
В однородном электрическом поле молекула воды будет поворачиваться вокруг своего центра масс вдоль силовых линий поля, но вращательного движения происходить не будет, движение молекулы будет колебательным.
В неоднородном электрическом поле на положительный и отрицательный заряды молекулы будут действовать неодинаковые силы, их значения будут различны по модулю.
Рис. 1.4. Диполь в неоднородном электрическом поле








В неоднородном электрическом поле молекула воды не просто будет поворачиваться, но еще и начнет притягиваться к области усиления поля, то есть туда, где гуще силовые линии. Таким образом, движение молекулы относительно электрического поля можно считать поступательным.
Магнитный дипольный момент
Исследование взаимодействий полюсов постоянных магнитов привело к представлению о существовании магнитных зарядов, аналогичных электрическим зарядам. Пара таких магнитных зарядов, равных по модулю и противоположных по знаку, рассматривались как магнитный диполь. Позднее было установлено, что магнитных зарядов не существует, что магнитные поля создаются движущимися электрическими зарядами, то есть электрическими токами. Однако понятие о магнитном дипольном моменте сохранили, поскольку на больших расстояниях от замкнутых проводников, по которым протекают токи, магнитные поля оказываются такими же, как если бы их порождали магнитные диполи.
Магнитный момент (магнитный дипольный момент) – основная величина, характеризующая магнитные свойства вещества. Магнитным моментом обладают элементарные частицы, атомные ядра, электронные оболочки атомов и молекул. Магнитный момент элементарных частиц (электронов, протонов, нейтронов и других), как показывает квантовая механика, обусловлен существованием у них механического момента – спина. [8] Спин имеет квантовую природу и не связан с перемещением частицы как единого целого.

где h – постоянная Планка, равная 
Экспериментально установлено, что в этих единицах (в соответствии с правилами квантовой механики) наблюдаемые проекции всех спинов на заданное направление принимают либо целое, либо полуцелое значение (либо 1, 2, 3… либо 


Магнитный дипольный момент атома или ядра аналогичен характеристике стрелки компаса. Он представляет собой вращающий момент, действующий на атом или ядро в магнитном поле. Дипольный момент – векторная величина. Магнитный момент атома высчитывается:

где q – заряд электрона, h – постоянная Планка, c – скорость света, 




Намагничивание магнетиков (любого класса) характеризуется намагниченностью, которая определяется как векторная сумма магнитных моментов атомов магнетика в единице объема:


Где J – намагниченность, 

Физическая величина, коэффициент, характеризующий связь между магнитной индукцией 




Магнитная восприимчивость — физическая величина, характеризующая связь между магнитным моментом (намагниченностью) вещества и магнитным полем в этом веществе.

где J – намагниченность веществ под действием магнитного поля, 

Движение молекулы воды в магнитном поле
Будет ли действовать магнитное поле на молекулу воды? Вода – диамагнетик, то есть вещество, результирующий магнитный момент атомов которого равен нулю. Атомы воды не имеют собственных магнитных полей. Но, электроны атома, помещенного во внешнее магнитное поле, приобретают дополнительное вращение, обусловленное полем. В магнитном поле диамагнитный атом приобретает магнитный момент, следовательно, он создает собственное магнитное поле.
При наличии внешнего магнитного поля все атомы диамагнетика (воды) приобретают магнитные моменты одного направления, противоположного внешнему полю. Поля магнитных диполей-атомов усиливают друг друга, и магнетик приобретает собственное магнитное поле направления, противоположного внешнему магнитному полю. Внутри магнетика магнитное поле ослабляется. Однако намагничивание диамагнетика имеет место лишь в присутствии внешнего поля. При снятии поля диамагнитный эффект немедленно исчезает.
Что происходит при помещении молекулы воды в магнитное поле? Когда диполь воды помещается в магнитное поле, на него действует сила Лоренца, заставляющая молекулу совершать колебательные движения.
Сила Лоренца – сила действия электромагнитного поля согласно классической (неквантовой) электродинамике на точечную заряженную частицу. Выражается:

Где q – заряженная частица,