Гепарин (Heparin)
Владелец регистрационного удостоверения:
Произведено:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Гепарин
Раствор для в/в и п/к введения прозрачный, от бесцветного до светло желтоватого или желтовато-коричневатого цвета.
| 1 мл | |
| гепарин натрия | 5000 МЕ |
Фармакологическое действие
Антикоагулянт прямого действия, относится к группе среднемолекулярных гепаринов. В плазме крови активирует антитромбин III, ускоряя его противосвертывающее действие. Нарушает переход протромбина в тромбин, угнетает активность тромбина и активированного фактора X, в некоторой степени уменьшает агрегацию тромбоцитов.
Для нефракционированного стандартного гепарина соотношение антиагрегантной активности (антифактора Xa) и антикоагулянтной активности (АЧТВ) составляет 1:1.
Увеличивает почечный кровоток; повышает сопротивление сосудов мозга, уменьшает активность мозговой гиалуронидазы, активирует липопротеинлипазу и обладает гиполипидемическим действием. Снижает активность сурфактанта в легких, подавляет чрезмерный синтез альдостерона в коре надпочечников, связывает адреналин, модулирует реакцию яичников на гормональные стимулы, усиливает активность паратгормона. В результате взаимодействия с ферментами может увеличивать активность тирозингидроксилазы мозга, пепсиногена, ДНК-полимеразы и снижать активность миозиновой АТФазы, пируваткиназы, РНК-полимеразы, пепсина.
Имеются данные о наличии у гепарина иммунодепрессивной активности.
Фармакокинетика
После п/к введения C max активного вещества в плазме наблюдается через 3-4 ч. Гепарин плохо проникает через плаценту вследствие большого молекулярного веса. Не выделяется с грудным молоком.
T 1/2 из плазмы составляет 30-60 мин.
Показания активных веществ препарата Гепарин
Профилактика и терапия: тромбоз глубоких вен, тромбоэмболия легочной артерии (в т.ч. при заболеваниях периферических вен), тромбоз коронарных артерий, тромбофлебиты, нестабильная стенокардия, острый инфаркт миокарда, мерцательная аритмия (в т.ч. сопровождающаяся эмболией), ДВС-синдром, профилактика и терапия микротромбообразования и нарушения микроциркуляции, тромбоз почечных вен, гемолитико-уремический синдром, митральный порок сердца (профилактика тромбообразования), бактериальный эндокардит, гломерулонефрит, волчаночный нефрит.
Профилактика свертывания крови во время операций с использованием экстракорпоральных методов кровообращения, при проведении гемодиализа, гемосорбции, перитонеального диализа, цитафереза, форсированного диуреза, при промывании венозных катетеров.
Приготовление образцов несвертывающейся крови для лабораторных целей и переливания крови.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| D59.3 | Гемолитико-уремический синдром |
| D65 | Диссеминированное внутрисосудистое свертывание [синдром дефибринации] |
| I20.0 | Нестабильная стенокардия |
| I21 | Острый инфаркт миокарда |
| I26 | Легочная эмболия |
| I33.9 | Острый эндокардит неуточненный |
| I34.0 | Митральная (клапанная) недостаточность |
| I48 | Фибрилляция и трепетание предсердий |
| I74 | Эмболия и тромбоз артерий |
| I80 | Флебит и тромбофлебит |
| I82 | Эмболия и тромбоз других вен |
| N00 | Острый нефритический синдром (острый гломерулонефрит) |
| N03 | Хронический нефритический синдром |
| N08.5 | Гломерулярные поражения при системных болезнях соединительной ткани |
| Z51.4 | Подготовительные процедуры для последующего лечения или обследования, не классифицированные в других рубриках |
Режим дозирования
Побочное действие
Со стороны свертывающей системы крови: возможны кровотечения ЖКТ и мочевых путей, кровотечение в месте введения, в областях, подвергающихся давлению, из операционных ран, а также кровоизлияния в других органах, гематурия, тромбоцитопения.
Со стороны пищеварительной системы: тошнота, снижение аппетита, рвота, диарея, повышение активности печеночных трансаминаз.
Аллергические реакции: гиперемия кожи, лекарственная лихорадка, крапивница, ринит, кожный зуд и ощущение жара в подошвах, бронхоспазм, коллапс, анафилактический шок.
Со стороны свертывающей системы крови: тромбоцитопения (может быть тяжелой вплоть до летального исхода) с последующим развитием некроза кожи, артериального тромбоза, сопровождающегося развитием гангрены, инфаркта миокарда, инсульта.
Местные реакции: раздражение, боль, гиперемия, гематома и изъязвления в месте введения.
Прочие: преходящая алопеция, гипоальдостеронизм.
Противопоказания к применению
Применение при беременности и кормлении грудью
Применение при беременности возможно только по строгим показаниям, под тщательным медицинским контролем.
Противопоказание: угрожающий выкидыш, роды (в т.ч. недавние).
Возможно применение в период грудного вскармливания по показаниям.
Применение при нарушениях функции печени
Применение при нарушениях функции почек
Применение у детей
Применение у пожилых пациентов
Особые указания
C осторожностью применять у пациентов, страдающих поливалентной аллергией (в т.ч. при бронхиальной астме), при артериальной гипертензии, стоматологических манипуляциях, сахарном диабете, эндокардите, перикардите, при наличии внутриматочного контрацептива, при активном туберкулезе, лучевой терапии, печеночной недостаточности, хронической почечной недостаточности, у пациентов пожилого возраста (старше 60 лет, особенно женщины).
Не рекомендуется в/м введение гепарина из-за возможности развития гематомы, а также в/м введение других препаратов на фоне лечения гепарином.
С осторожностью применяют наружно при кровотечениях и состояниях повышенной кровоточивости, тромбоцитопении.
Во время лечения гепарином необходим контроль показателей свертывания крови.
Для разведения гепарина используют только физиологический раствор.
При развитии тяжелой тромбоцитопении (снижение количества тромбоцитов в 2 раза от первоначального числа или ниже 100 000/мкл) необходимо срочно прекратить применение гепарина.
Риск кровотечения может быть сведен до минимума при тщательной оценке противопоказаний, регулярном лабораторном контроле свертывания крови и адекватном дозировании.
Лекарственное взаимодействие
Противосвертывающее действие гепарина усиливается при одновременном применении антикоагулянтов, антиагрегантов и НПВС.
Алкалоиды спорыньи, тироксин, тетрациклин, антигистаминные средства, а также никотин уменьшают действие гепарина.
ПРИМЕНЕНИЕ ГЕПАРИНОВ В КЛИНИЧЕСКОЙ ПРАКТИКЕ
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Статья посвящена вопросам профилактики и лечения тромбозов и нарушений микроциркуляции. Описываются гепарины – антикоагулянты приямого действия, получившие наибольшее распространение в мировой клинической практике.
The paper deals with the prevention and treatment of thromboses and microcirculatory disorders, outlines heparins, direct-acting anticoagulants, which are widely used clinical practice all over the world.
Проф. В.А. Макаров, Т.Б. Кондратьева Гематологический центр ВГНЦ, Московская медицинская академия им. И.М. Сеченова
Prof. V.A. Makarov, T.B. Kondratyeva All-Russian Heparinology Research Center, I.M. Sechenov Moscow Medical Academy
П роблемы профилактики и лечения тромбозов, а также нарушений микроциркуляции имеют важное значение для клинической практики. В России и странах СНГ отмечается неуклонный рост числа больных с заболеваниями, сопровождающимися тромбозами и эмболиями. К подобным заболеваниям относятся инфаркт миокарда, тромбозы сосудов конечностей, мозга, легких, глаз и др. Часто тромбоз возникает после оперативных вмешательств, особенно на фоне использования аппаратов искусственного кровообращения. Показано, что причиной тромбоза может быть не только повреждение сосудистой стенки, но и патологические изменения ферментов свертывания крови и естественных антикоагулянтов. Активация свертывающей системы крови (т.е. ферментов, активирующих фибринообразование) характерна и для ДВС-синдрома. Последний является наиболее распространенной формой патологии гемостаза. Он часто встречается при многих заболеваниях и патологических состояниях, в частности при инфекционных болезнях, шоке, травматичных хирургических вмешательствах, терминальных состояниях, акушерской патологии, злокачественных опухолях, деструктивных процессах в органах и тканях, иммунной и иммунокомплексной патологии, острых аллергических реакциях, после обильных кровотечений, массивных гемотрансфузий, при передозировке лекарственных средств с прокоагулянтной активностью и др. [1].
В связи с этим в указанных клинических ситуациях возникает необходимость использования веществ, препятствующих фибринообразованию, т. е. антикоагулянтов. Наибольшее распространение в клинической практике всего мира получили гепарины, относящиеся к группе антикоагулянтов прямого действия (т. е. взаимодействующих непосредственно с факторами свертывания крови).
Гепарины – это различающиеся по молекулярной массе гликозаминогликаны, состоящие из сульфатированных остатков Д-глюкозамина и Д-глюкуроновой кислоты. Эти полимеры образуются в организме человека и животных и содержатся в основном в тучных клетках. Впервые они были обнаружены в 1916 г. J. McLean. В 1918 г. W. Howel и E. Holt выделили этот антикоагулянт из печени собаки (отсюда название – «гепарин»). Клиническое применение гепарина стало возможным после 1930 г., когда были получены его натриевые соли.
Механизм антикоагулянтного действия гепаринов зависит от молекулярной массы. В нефракционированных препаратах (препаратах первого поколения) под названием «гепарин» преобладают высокомолекулярные фракции гликозаминогликана. Действие этих препаратов связано с тем, что они образуют комплекс с антитромбином III, ведущий к возрастанию способности последнего ингибировать тромбин, фактор Хагемана, факторы IX, X, XI и др.
Низкомолекулярные фракции гепарина (менее 6 кД), содержащиеся в таких препаратах, как надропарин, даль- тепарин, эноксипарин, ревипарин и др., обладают иным механизмом антикоагулянтного действия. Последний связан в основном с ингибированием активности фактора Ха. В меньшей степени эти препараты влияют на активность фактора IIа (тромбина) и других факторов свертывания крови. Следует отметить, что для профилактики тромбообразования торможение активности фактора Ха более выгодно, чем воздействие на нижележащие фазы фибринообразования (см. рисунок), так как требует меньшего количества препарата.
Гепарины долгое время выделяли из печени и легких крупного рогатого скота, затем из кишечника свиней, что оказалось выгоднее. Низкомолекулярные гепарины производят путем деполимеризации высоко- и среднемолекулярных полимеров.
В настоящее время основными показаниями для проведения гепаринотерапии определены венозные тромбозы, тромбоэмболия легочной артерии, ДВС-синдром, нестабильная стенокардия, острый инфаркт, ишемический инсульт. С профилактической целью препараты гепарина используют при хирургических вмешательствах, при недостаточности кровообращения, для профилактики свертывания крови при использовании экстракорпорального кровообращения. Таким образом, препараты гепарина применяются у значительного контингента больных.
Несмотря на то что гепаринотерапия проводится уже в течение 6 десятков лет и препараты гепарина доминируют и сегодня над другими антикоагулянтами прямого действия, лечение гепаринами сопряжено с риском возникновения ряда осложнений. В первую очередь – это возникновение кровотечений. Кровотечения при гепаринотерапии связаны не только с избыточной ингибицией фибринообразования, но и с тем, что на фоне данной терапии развивается тромбоцитопения. При этом возможны два варианта тромбоцитопении. При первом варианте кратковременная, быстрокупирующаяся после отмены гепарина тромбоцитопения связана с его способностью активировать агрегационную функцию тромбоцитов, потенцировать действие других стимуляторов агрегации и ослаблять анатиагрегационный эффект простациклина. При втором иммунном варианте наряду с повышенной внутрисосудистой агрегацией и потреблением тромбоцитов в микротромбы выявляются специфические аутоантитела к определенным тромбоцитарным рецепторам.
К числу других осложнений гепаринотерапии относятся аллергические реакции, остеопороз, приапизм, а также снижение уровня антитромбина III.
В последние годы проведено большое количество сравнительных исследований по оценке эффективности, безопасности и удобства клинического использования нефракционированных и низкомолекулярных препаратов гепарина. Установлено, что гепарины низкой молекулярной массы обладают большей биодоступностью (более чем в 3 раза) при подкожном введении, чем нефракционированные препараты. Период полувыведения в 2 – 4 раза больше у низкомолекулярных гепаринов, что способствует удлинению срока действия препарата. В связи с этим препараты низкомолекулярных гепаринов можно вводить 1 – 2 раза в сутки. Различия в фармакокинетике объясняются меньшей склонностью низкомолекулярных гепаринов связываться с белками плазмы, такими как богатый гистидином гликопротеин, тромбоцитарный фактор 4, витронектин, фибронектин, фактор Виллебранда и др. Таким образом, препараты нефракционированного гепарина удаляются в две фазы: фазу быстрого насыщения, т. е. связывания с белком, и фазу почечного клиренса. Гепарины же низкой молекулярной массы почти полностью удаляются почками.
Препараты нефракционированного гепарина вводят внутривенно, в виде капельных инфузий, подкожно, внутримышечно. Низкомолекулярные гепарины вводят подкожно, внутримышечно, а некоторые препараты и перорально.
К преимуществам гепаринов с низкой молекулярной массой относится меньшая вероятность развития тромбоцитопении. Возможно, в значительной степени с этим связан тот факт, что при использовании этих препаратов наблюдается меньший процент геморрагических осложнений. На основе этих закономерностей лечение низкомолекулярными гепаринами не нуждается в таком тщательном лабораторном контроле, как лечение нефракционированными препаратами.
Часто в качестве лабораторного контроля эффективности препарата определяют время свертывания и рекальцификации цельной крови, частичное тромбопластиновое время в различных модификациях, активированное время свертывания. Однако эти методики не отличаются высокой восприимчивостью. Они мало чувствительны к низким концентрациям гепарина в крови. Несколько более восприимчив тест активированного частичного тромбопластинового времени (АЧТВ), а также тромбинового (а лучше тромбинкальциевого) времени. При использовании теста АЧТВ показано, что при гепаринотерапии (нефракциониравонным гепарином) для достижения терапевтического эффекта необходимо удлинение времени в 1,5 – 2,5 раза. Более специфичными являются методы, основанные на измерении активности тромбина при его ингибировании плазмой больного, леченного гепарином (т. е. определяется анти-IIа-антитромбиновая активность гепарина). Чувствительность метода возрастает при такой постановке, когда в плазму вносится тромбин повышенной активности и активность регистрируется с помощью хромогенного субстрата (например, S-2288).
При контроле лечения препаратами низкомолекулярных гепаринов особое значение имеет определение анти-Ха-активности плазмы. В качестве индикатора реакции целесообразно использовать хромогенные субстраты. В связи с этим интересно сравнить соотношение антитромбиновой и анти-Ха-активностей у различных препаратов гепарина. У нефракционированного гепарина она примерно равна 1. У нефракционированных гепаринов это соотношение составляет: для дальтепарина – 2.2, логипарина – 1.5, надропарина – 3.5, эноксопарина – 3.9 [2]. Вопросы дозирования препаратов гепарина и контроля лечения при различных заболеваниях изложены во многих публикациях, справочниках и руководствах [3 – 6].
В последние годы был проведен ряд исследований с анализом больших групп больных по сравнительной оценке клинической эффективности препаратов нефракционированного и низкомолекулярного гепарина. По данным J. Hirst [7], при лечении венозного тромбоза нефракционированными гепаринами и оральными антикоагулянтами повторные венозные тромбоэмболии отмечены в 0,8% случаев, при лечении нефракционированным препаратом и оральными антикоагулянтами – в 3,2%. Смертность в первом случае составила 3,2%, в том числе вследствие тромбоэмболии легочной артерии – 0,1%, а во втором случае – 5,9%, в том числе вследствие тромбоэмболии легочной артерии – 0,2%. Выраженная кровоточивость составила при лечении низкомолекулярными гепаринами 3%, а нефракционированными – 6,7%, малая кровоточивость в первом случае составила 11%, во втором – 9,9%. Улучшение показателей венограмм в первом случае составило 65,3%, во втором – 52%. По данным F.J.J. Turpie [8], смертность при лечении венозных тромбозов нефракционированным гепарином составила 7,1%, а при лечении низкомолекулярным гепарином – 3,9%. При нестабильной стенокардии нефракционированный гепарин и низкомолекулярный гепарин обладают близкими по силе эффектами в плане предотвращения смерти, развития инфаркта миокарда, реваскуляризации и др. [9].
В литературе встречаются данные о том, что низкомолекулярные гепарины более безопасны в плане геморрагических осложнений, чем нефракционированные гепарины при нарушениях мозгового кровообращения [10].
Суммируя изложенное, можно заключить, что в настоящее время большинство исследователей считают низкомолекулярные гепарины по силе действия не уступающими нефракционированному гепарину. Однако, как было указано ранее, они имеют ряд преимуществ. Это объясняет тот факт, что после 13 лет клинического применения низкомолекулярные препараты постепенно вытесняют нефракционированный гепарин во многих областях медицины.
Появление низкомолекулярных гепаринов в клинике совпало по времени с внедрением и других новых антикоагулянтов прямого действия. Речь идет прежде всего о гирудине, его производных, а также синтетических и пептидных ингибиторах тромбина. Указанные препараты не нуждаются в эндогенных кофакторах, в частности антитромбине III. Однако следует учесть, что в случае возникновения опасности геморрагий, отравление этими препаратами труднее купировать, так как они пока не имеют специфических антагонистов. Между тем эффект гепаринов снимается специфическими антагонистами – протамина сульфатом, полибреном и др.
Исходя из тех преимуществ, которыми обладают гепарины, поиск новых антикоагулянтов прямого действия активно ведется среди сульфатированных полимеров. В частности, полисульфаты пентозана, дерматана и др. также применяются за рубежом в клинической практике. Однако они уступают гепаринам по удельной активности и безопасности применения.
В лаборатории патологии и фармакологии гемостаза Гематологического научного центра РАМН [11] разрабатывается новый антикоагулянт хиторин, представляющий собой смесь гепарина и полисульфата хитозана определенной молекулярной массы и степени сульфатирования. Подобный состав обусловлен тем, что авторам впервые удалось показать способность полисульфата хитозана потенцировать антикоагулянтный эффект гепарина. Хиторин, обладая близкой к гепарину удельной активностью, меньше влияет на концентрацию тромбоцитов в крови и обладает меньшей геморрагической активностью. Завершающиеся доклинические испытания свидетельствуют о низкой токсичности хиторина.
Таким образом, за 60 лет применения в клинике препараты гепарина показали высокую эффективность в профилактике и лечении тромбозов и ДВС-синдрома. За последние 13 лет удалось выявить преимущества низкомолекулярных препаратов гепарина перед нефракционированными препаратами. Гепарины служат основой для разработки новых антикоагулянтов прямого действия.
1. Баркаган З.С. Геморрагические заболевания и синдромы. М., Мед., 1988.
2. Annotation: low molecular weight heparin (S). Brit J Haematol 1995;90:1.
3. Баркаган З.С. В кн.: Руководство по гематологии, по ред. А.И. Воробьева, М., Мед., т.2, 1985, с.160.
4. Бокарев И.Н., Щепотин Б.М., Ена Я.Н. Внутрисосудистое свертывание крови. Киев, Здоров`я, 1989.
5. Исследование системы крови в клинической практике. Под ред. Г.И. Козинца и В.А. Макарова, М. Триада-Х, 1997.
6. Машковский М.Д. Лекарственные средства. т.1, Харьков, Торсинг, 1997, с.462.
7. Hirsh J, et al. Low molecular weight heparin in the treatment of patients with acute venous thromboembolism. Thrombos Haemostas 1995;74(1):360.
8. Turpie AJJ. New therapeutic opportunities for heparins: what does low molecular weight heparin offer? Thrombosis and Thrombolysis 1996;3:145.
9. Fragmin During Instability in Coronary Artery Disease (FRJSC) Study Group. Low molecular weight heparin during instability in coronary artery disease. The Lancet 1996;347:561.
10. Kay R, Wong KS, Yu YL, et al. Low molecular weight heparin in ischemic stroke. Fiss study. N Engl Med 1995;333(4):1588.
11. Дрозд Н.Н., Макаров В.А., Башков Г.В. и др. Влияние совместного введения гепарина и сернокислого эфира хитозана на функцию гемостаза. Эксп. и клин. фармакол, 1996, 59, 1, 30.
Причины геморрагических осложнений у пациентов стационара, получающих лечебные дозы антикоагулянтов
Широкое применение антикоагулянтов (АК) нередко сопровождается нежелательными явлениями, среди которых чаще всего встречаются геморрагические осложнения.
Оценить частоту и структуру кровотечений, связанных с использованием АК в многопрофильном стационаре, и разработать план мероприятий, направленных на снижение риска развития данных осложнений.
Материалы и методы
Ретроспективно проанализированы электронные истории болезни пациентов, госпитализированных в многопрофильный стационар с 01.01.2015 по 15.03.2018 и перенесших геморрагические осложнения (в том числе при поступлении в стационар) на фоне приема «лечебных»» доз АК, назначенных по следующим показаниям: фибрилляция предсердий, тромбоз глубоких вен, тромбоэмболия легочной артерии, механический протез сердечного клапана. Оценивали частоту, локализацию, тяжесть и предотвратимость кровотечений, а также их основные и дополнительные причины по методу Root Cause Analysis (RCA, анализ основных причин).
На протяжении 38 месяцев АК в «лечебных» дозах получали 2093 пациента. У 43 (2,1%) из них были зарегистрированы геморрагические осложнения. Частота назначения варфарина, низкомолекулярных гепаринов (НМГ) и прямых оральных антикоагулянтов (ПОАК) составила 28%, 32% и 46%, соответственно. Частота кровотечений при лечении разными АК достоверно не различалась и составила 2,8% при приеме варфарина, 1,6% – ПОАК и 2,2% – НМГ. Чаще всего встречались желудочно-кишечные кровотечения (33%) и гематурия (21%). Факторы пациента признаны основной причиной кровотечений в 83,7% случаев, факторы персонала – в 14,0%, организационные факторы – в 2,3%. С ошибками использования ЛС были связаны 16% кровотечений. Сопутствующие заболевания пациента были самой частой причиной кровотечений (63%). Потенциально предотвратимыми были 35% кровотечений.
По итогам RCA был составлен план устранения потенциально предотвратимых факторов кровотечений, связанных с пациентом, персоналом и организацией лечебно-диагностического процесса.
Широкое применение антикоагулянтов (АК) нередко приводит к нежелательным явлениям (НЯ), требующим обращения за медицинской помощью. Общее число обращений по поводу НЯ, развивающихся на фоне приема антикоагулянтных препаратов, в 2,4 раза превышает таковое при применении опиоидов [1]. По данным Института безопасной лекарственной практики (Institute for Safe Medication Practice), в 2016 году в США зарегистрировано 22 тыс сообщений о развитии НЯ при приеме АК, что составило примерно 10% от всех обращений за медицинской помощью пациентов, принимающих АК [2]. В США в 2013-2014 гг. антикоагулянты были самой частой причиной обращения за неотложной помощью по поводу НЯ; примерно в половине случаев (48,8%) пациенты нуждались в госпитализации [1]. Доля лекарственных нежелательных реакций среди всех осложнений, связанных с оказанием медицинской помощи в стационаре, составляет 39,6% [3]. Число НЯ в стационаре на 1000 выписанных пациентов, получавших нефракционированный гепарин (НФГ), составило 6,0, низкомолекулярные гепарины (НМГ) или прямые оральные АК (ПОАК) – 7,6, варфарин – 3,7 [3].
Основную долю НЯ, связанных с АК, составляют кровотечения (около 80%) различной локализации [1], которые возникают у 8-19% пациентов, длительно получающих препараты этой группы 6. У пациентов, принимавших АК для профилактики тромбоэмболических осложнений при фибрилляции предсердий, чаще развивались желудочно-кишечные кровотечения (8495 из 17218 случаев), а также внутримозговые кровоизлияния (1809 из 17218 случаев) [7].
Профилактика НЯ, связанных с приемом АК, в том числе кровотечений, способствует снижению расходов на медицинскую помощь. Например, внедрение программы «Saving Lives and Saving Money: Hospital-Acquired Conditions», разработанной Agency for Healthcare Research and Quality, привело к снижению частоты НЯ в стационарах США в 2010-2014 гг. и позволило съэкономить более 1 млрд долларов [3]. Затраты на лечение последствий НЯ, связанных с приемом АК, в США оцениваются в 40 640$ в расчете на одно событие (учитывая стоимость медикаментов и трудозатрат медперсонала) [8].
Эффективным инструментом анализа и управления риском возникновения НЯ является анализ основных причин (root cause analysis – RCA) [9]. Объединенная комиссия по аккредитации медицинских учреждений США (Joint Commission AHO) в 1997 году впервые использовала метод RCA для анализа ошибок локализации операционного поля (неверная сторона операции). Однако ряд исследователей указывают на низкую эффективность RCA при отсутствии активных действий по устранению выявленных причин события [10]. В настоящее время комплекс «анализ + действие» (RCA2) предполагает не только выявление причин НЯ, но и составление и реализацию плана мероприятий по их устранению [11].
Целью исследования была оценка частоты и структуры кровотечений, связанных с использованием АК в многопрофильном стационаре, с последующей разработкой плана мероприятий, направленных на снижение риска развития данных осложнений.
Материал и методы
В ретроспективное исследование включали пациентов, госпитализированных в Многопрофильный медицинский центр Банка России (Москва) с 01.01.2015 по 15.03.2018 и перенесших геморрагические осложнения на фоне применения «лечебных» доз АК, в том числе, при поступлении в стационар. Показания к применению АК в «лечебных» дозах включают в себя следующие: профилактика тромбоэмболий у пациентов с ФП и механическим клапаном сердца, лечение тромбоза глубоких вен, сопровождающегося или не сопровождающегося тромбоэмболией легочной артерии, лечение нестабильной стенокардии и инфаркта миокарда без зубца Q, лечение острого инфаркта миокарда с подъемом сегмента ST, профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
Критерии включения в исследование: развитие кровотечения на фоне применения «лечебных» доз АК; наличие в клиническом диагнозе заболевания (МКБ-10) следующих состояний: фибрилляция и трепетание предсердий (I48), протез сердечного клапана (Z95.2), флебит и тромбофлебит бедренной вены (I80.1), флебит и тромбофлебит других глубоких сосудов нижних конечностей (I80.2), флебит и тромбофлебит бедренной вены, других сосудов нижних конечностей в сочетании с легочной эмболией (I26).
Критерии невключения в исследование: анемия без документального подтверждения состоявшегося кровотечения; возникновение кровотечения на фоне применения «профилактических» доз АК; наличие в клиническом диагнозе заболевания (МКБ-10) следующих состояний: постфлебитический синдром (I87.0) (без указания даты тромбоза), флебит и тромбофлебит поверхностных сосудов нижних конечностей (I80.0), венозные тромбозы (I81-I82), легочная эмболия (I26) при отсутствии флебита и тромбофлебита бедренной вены, других сосудов нижних конечностей.
Тяжесть кровотечения оценивалась по классификациям GUSTO и TIMI [12].
Геморрагические осложнения были проанализированы с помощью методологии RCA по аналогии с формой выявления основной причины возникновения кровотечения при применении варфарина (Michigan Anticoagulation Quality Improvement Initiative) [13]. Итогом анализа RCA стало выявление основных причин возникновения кровотечений при применении «лечебных» доз АК (одна причина у каждого пациента). Основной причиной кровотечения эксперт называл фактор, который, предположительно, играл ключевую роль в развитии события (не зависит от прочих факторов, является «корневым» фактором при ответе на вопрос «почему возникло кровотечение?»). В описание результатов не вошли группы причин, не выявленных при анализе. Изза большого количества возможных факторов развития кровотечений определяли также дополнительные причины (несколько у одного пациента). У разных пациентов одни и те же причины развития кровотечений могли быть как основными, так и дополнительными. Такие группы причин, как «протоколы/процедуры организации», «управление информацией», «тех. и мат. обеспечение», относились к факторам организации, группа причин «коммуникация» не рассматривалась из-за ретроспективного анализа.
Среди основных/дополнительных причин развития кровотечений выявляли ошибки использования лекарственных средств (ЛС), для анализа которых использовали «Класси фи кацию ошибок, связанных с ЛС», разработанную Фон дом фармацевтической помощи Европы (Pharmaceutical Care Network Europe Foundation) [14].
Группы причин, в отношении которых можно применить профилактические меры, считались «потенциально предотвратимыми», остальные причины по умолчанию являлись «непредотвратимыми».
Статистическая обработка данных проведена непараметрическими методами с помощью прикладной программы «IBM SPSS Statistics v22». Для сравнения количественных показателей использовали U-тест Манна-Уитни, качественных – критерий X 2 Фишера. При ненормальном распределении применяли непараметрические методы описательной̆ статистики: медиана, интерквартильный размах (interquartile range – IQR). Различия считали достоверными при p
Результаты
Эпидемиология назначения «лечебных» доз АК. Из медицинской информационной системы ИНТЕРИН ретроспективно были отобраны случаи назначения пациентам «лечебных» доз» АК – 2093 (9%) из 23046 пациентов за 38,5 месяцев. Из 2093 электронных историй болезни с помощью поиска по ключевым словам «кровотечение», «-рагия», «геморраг-«, «гемма-» (в графе «клинический диагноз») были отобраны 64 случая кровотечений на фоне приема «лечебных» доз АК, из которых 43 соответствовали критериям включения и невключения в исследование. Показаниями к назначению АК в «лечебных» дозах (n=2093) были фибрилляция предсердий (71%), венозные тромбоэмболические осложнения (18%), острый коронарный синдром (8%), прочие тромбозы (2%) и механический протез клапана (1%).
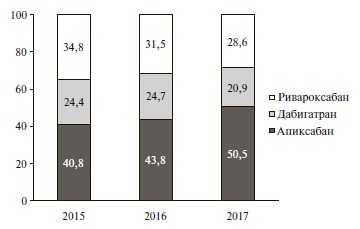
Структура назначений различных АК в 2015-2017 гг. представлена в табл. 1. Чаще всего назначали ПОАК, причем частота их назначения постепенно увеличи валась со временем (примерно на 9% в 2017 г. по сравнению с 2015 г.). Среди ПОАК наиболее распространенным препаратом был апиксабан (рис. 1).
| 2015 | 2016 | 2017 | Всего за 38 мес | |
|---|---|---|---|---|
| Примечание: разница между 2015 и 2016 гг. и между 2016 и 2017 гг. недостоверна | ||||
| Все АК, n (% от пролеченных за год) | 634 (8,8) | 629 (9,0) | 684 (9,3) | 2093(100) |
| АК, n (% от АК за год) | ||||
| Варфарин, | 153 (24,1) | 142 (22,6) | 137 (20,0) | 460 (21,9) |
| НМГ | 202 (31,9) | 195 (31,0) | 218 (31,9) | 670 (32,0) |
| ПОАК | 279 (44,0) | 292 (46,4) | 329 (48,1) | 963 (46,0) |
Характеристика пациентов и антикоагулянтной терапии. Общая характеристика включенных в исследование пациентов представлена в табл. 2. Самыми частыми сопутствующими заболеваниями были артериальная гипертония (95,0%) и сахарный диабет (39,5%). У 30 (90,5%) пациентов терапию АК назначали на неопределенно длительный срок. Девять (21,0%) пациентов ранее получали нестероидные противовоспалительные препараты регулярно в течение месяца и более, 10 (23,0%) – антиагреганты. Двадцать (46,5%) из 43 случаев кровотечений были выявлены при поступлении в стационар (в 19 случаях они послужили причиной госпитализации). У 30 пациентов текущая госпитализация была повторной: 17 (56,7%) из них госпитализировались в течение последних 6 месяцев, 8 (26,7%) – 6-12 месяцев назад и 5 (15,6%) – 1-5 лет назад. Хирур ги ческое вмешательство в течение последнего месяца было выполнено 23 (53,5%) пациентам; у 17 (74%) из них источник кровотечения находился в области послеоперационной раны.
| Показатели | Значения |
|---|---|
| Примечание: *метастазы, текущая химио- или лучевая терапия, отсутствие ремиссии в последние 6 мес | |
| Всего пациентов | 43 |
| Женщины, n (%) | 15 (35,0) |
| Возраст, медиана (IQR) | 73 (11,0) |
| Механический протез клапана, n (%) | 2 (4,5) |
| Фибрилляция предсердий, n (%) | 30 (70,0) |
| Тромбоз глубоких вен, n (%) | 11 (25,5) |
| Кровотечение в анамнезе, n (%) | 14 (32,5) |
| Индекс коморбидности Charlson, медиана (IQR) | 11,5 (6,0) |
| Сахарный диабет, n (%) | 17 (39,5) |
| Инсульт в анамнезе, n (%) | 10 (23,0) |
| Артериальная гипертония, n (%) | 41 (95,0) |
| Активная опухоль,* n (%) | 9 (21,0) |
Все пациенты на момент развития кровотечения получали АК в «лечебных» дозах: НМГ – 15 (34,9%), варфарин – 13 (30,2%) и ПОАК – 15 (34,9%), в том числе ривароксабан – 7, апиксабан – 5 и дабигатран – 3. Стандартные дозы АК принимали 18 (42,8%) пациентов, сниженные – 15 (34,9%) и повышенные – 10 (23,3%).
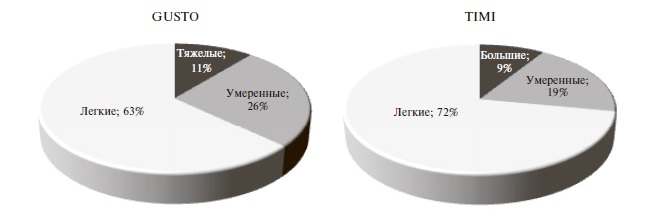
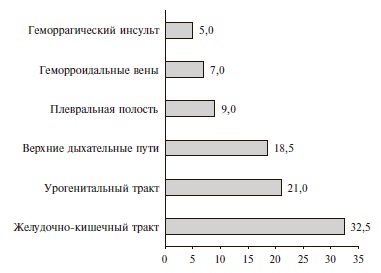
Частота и характеристика кровотечений. В целом частота кровотечений при применении «лечебных» доз АК составила 2,1%, или 18,5 случаев на 10 000 выписанных пациентов. Частота кровотечений на фоне приема варфарина, НМГ и ПОАК достоверно не отличалась: 2,8%, 2,2% и 1,6%, соответственно. Большинство кровотечений были легкими (63% – по классификации GUSTO и 72% – по классификации TIMI) (рис. 2). В 35 (81,5%) случаях после кровотечения терапия АК была приостановлена, а 14 (32,5%) пациентам потребовалось переливание крови. Структура кровотечений по локализации представлена на рис. 3.
Анализ основных и дополнительных причин развития кровотечений. Основные и дополнительные причины развития кровотечений распределяли на 3 категории – факторы пациента, персонала и факторы организации (системные факторы, связанные с организацией клинических процессов). Всего было выделено 169 причин, включая 43 основных и 126 дополнительных (рис. 4).
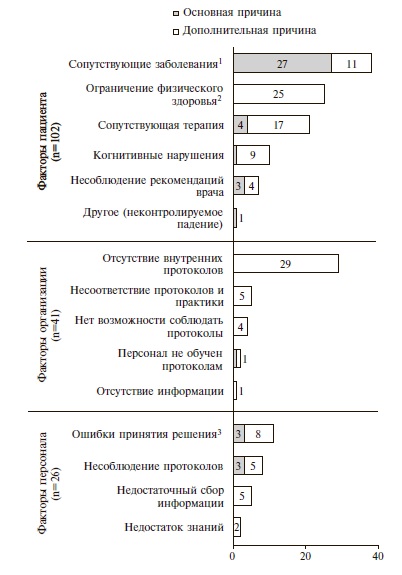
Факторы, связанные с пациентом, были признаны основной причиной кровотечений в 83,7% случаев (36 событий), факторы персонала – в 14,0% (6 событий) и факторы организации – в 2,3% (1 событие). Доля «потенциально предотвратимых» основных причин составила 35,0% (15 событий): факторы, связанные с пациентом, – 7, факторы персонала – 6, факторы организации – 1.
Среди дополнительных причин кровотечений при использовании «лечебных» доз АК факторы, связанные с пациентом, имелись в 52,5% случаев (66 событий), факторы организации – в 31,5% (40 событий), факторы персонала – в 16,0% (20 событий). Доля «потенциально предотвратимых» дополнительных причин составила 71,4% (90 событий): факторы, связанные с пациентом, – 30, факторы персонала – 20, факторы организации – 40. Среднее количество дополнительных причин возникновения кровотечений на одного пациента – 2,9.
Ошибки, связанные с использованием ЛС. Основной причиной 7 (16,3%) из 43 кровотечений были ошибки использования ЛС: отсутствие систематического пересмотра антикоагулянтной терапии при лабильном уровне МНО во время приема варфарина (2 случая), некорректный режим дозирования ривароксабана (повышение дозы) у пациентов с тромбозом глубоких вен (1), отсутствие коррекции дозы НМГ по массе тела пациента (1), превышение длительности лечения АК у пациента со спровоцированным тромбозом дистальных глубоких вен (1), неоправданное назначение антиагреганта на фоне терапии АК (1), неверная периоперационная тактика ведения пациента, принимающего варфарин (1).
Ошибки использования ЛС составили 20,6% от дополнительных причин, относящихся к факторам персонала и пациента (26 из 126): систематическое отсутствие пересмотра антикоагулянтной терапии при лабильном уровне МНО во время приема варфарина (4 случая), повышение/снижение дозы АК из-за отсутствия периодического пересмотра риска кровотечения пациента (7), несоблюдение пациентом рекомендаций врача (4), неоправданное назначение антиагрегантов при лечении АК (3), отсутствие пересмотра длительности терапии у пациентов с тромбозом глубоких вен в анамнезе, с существующим постфлебитическим синдромом (3), отсутствие расчета дозы НМГ в зависимости от массы тела пациента (3).
Профилактика кровотечений при лечении АК. По итогам анализа составлен план мероприятий по устранению потенциально предотвратимых причин кровотечений у пациентов, получающих «лечебные дозы» АК.
Обсуждение
Частота кровотечений у пациентов, принимающих «лечебные» дозы АК, в настоящем исследовании составила 18,5 на 10 000 выписанных пациентов. По данным Американского агентства по качеству и исследованиям в здравоохранении, частота кровотечений при приеме АК у пациентов в возрасте старше 65 лет в стационарах США в 2011 г. равнялась 16,4 на 10 000 выписанных пациентов [15]. Разница в частоте кровотечений может быть обусловлена высоким средним возрастом пациентов в нашем исследовании (73±11 лет), а также увеличением частоты назначения АК по сравнению с таковой в 2011 г. Таким образом, геморрагические осложнения были отмечены у 2% пациентов, которые в стационаре получали «лечебные» дозы АК. Для сравнения, кровотечения развиваются у 8-19% пациентов, длительно получающих терапию АК, в том числе амбулаторно [46]. Можно предполагать, что большая часть кровотечений при приеме АК возникает на амбулаторном этапе.
В нашем исследовании кровотечения развивались у пожилых пациентов с сопутствующими заболеваниями, которым АК назначали на неопределенно длительный срок (90,5%), преимущественно по поводу ФП (70%). Чаще всего у пациентов с ФП возникали желудочнокишечные кровотечения – в 37% случаев. В исследовании R. Hart и соавт. частота кровотечений этой локализации у пациентов с ФП составила 49% [7]. Высокая частота повторных госпитализаций (70%), кровотечений в анамнезе (32,5%), активных онкологических заболеваний (21%) свидетельствует о тяжести состояния пациентов, явившейся самой частой основной причиной возникновения кровотечений при приеме «лечебных доз» АК (63% всех основных причин). Факторы пациента были основной причиной 83,7%
кровотечений. Сходные данные приводят C. Graves и соавт. [16]. Доля тяжелых кровотечений составила 11,5% по классификации GUSTO и 9,5% по классификации TIMI. В аналогичном исследовании Gregory и соавт. доля тяжелых кровотечений по критериям GUSTO достигла 32% [8].
В нашем исследовании кровотечения развивались у 2,8% пациентов, получавших варфарин. В работе Daniels и соавт. частота кровотечений на фоне приема варфарина у пациентов терапевтического и хирургического профиля составила 1,5% и 13,5%, соответственно [17]. При лечении ПОАК мы зарегистрировали кровотечения у 1,6% пациентов. В Германии (German Claims Database) частота кровотечений у амбулаторных и стационарных пациентов с ФП, принимающих ПОАК, была выше (8%), что может свидетельствовать о более высоком риске кровотечений на амбулаторном этапе лечения [18]. Частота кровотечений у пациентов, которым назначали «лечебные» дозы НМГ, составила 2,2%. Следует отметить, что препараты этой группы получали около двух третей пациентов с внутрибольничными геморрагическими осложнениями (не при поступлении). Это может быть связано с назначением НМГ пациентам с высоким риском кровотечения или их применением в периоперационном периоде (около половины пациентов перенесли оперативное вмешательства в течение месяца до развития кровотечения). В 74% (17 из 23 пациентов) случаев источник кровотечения находился в области послеоперационной раны, что могло быть связано с несовершенством «хирургического» гемостаза (помимо высокого риска кровотечения пациента).
Низкая приверженность (несоблюдение рекомендаций врача, когнитивные нарушения) пациентов ассоциировалась с сокращением времени нахождения МНО в терапевтическом диапазоне при приеме варфарина. Тяжесть состояния пациентов в 27 случаях (63%) была ключевым фактором развития кровотечений, при этом 23 из 27 пациентов находились в периоперационном периоде.
У каждого пятого пациента среди основных и дополнительных причин кровотечений при применении «лечебных» доз АК были отмечены ошибки использования ЛС, в том числе связанные с выбором препарата (например, продолжение приема антагониста витамина К у пациентов, у которых МНО систематически находилось за пределами целевого диапазона), режима дозирования или длительности лечения АК, необоснованным назначением антиагрегантов на фоне приема АК. Отсутствие собственных внутренних протоколов терапии АК в ММЦ до конца 2017 г. могло быть причиной высокой частоты «факторов организации» (29%) среди дополнительных причин возникновения кровотечений.
Ограничения работы
Данное исследование проводилось ретроспективно путем анализа электронных историй болезни, поэтомуинформация о ряде факторов, способствующих возникновению кровотечений (например, ограничение передачи информации), отсутствовала. Ограничение выборки, в частности исключение из анализа «профилактических» доз» АК, могло повлиять на итоговую структуру результатов. Основные и дополнительные причины возникновения кровотечений определялись ретроспективно и носят вероятностный характер.
Заключение
Геморрагические осложнения развивались примерно у 2% стационарных пациентов, получавших «лечебные» дозы АК. Частота кровотечений была ниже всего при лечении ПОАК, хотя риск их развития достоверно не отличался при применении различных АК, в том числе НМГ и варфарина. Самыми частыми основными причинами развития кровотечений на фоне «лечебных доз» АК были факторы пациента (83,8%). Высокая доля «потенциально предотвратимых» событий (35,0%), а также большое количество «потенциально предотвратимых» дополнительных причин кровотечений (71,4%) у пациентов, получающих «лечебные» дозы АК, свидетельствует о необходимости разработки профилактических мер. Анализ структуры назначений АК и причин развития кровотечений по методу RCA позволяет составить целенаправленный план устранения «потенциально предотвратимых» нежелательных лекарственных реакций.





