Гидроксихлорохин
Химическое название
2-[[4-[(7-Хлор-4-хинолинил)амино]пентил]этиламино]этанол (в виде сульфата)
Химические свойства
Горький белый кристаллический порошок, молярная масса = 335,872 г/моль. Гидроксихлорохин (на латинском языке Hydroxychloroquine) — это производное 4-аминохинолина. Лекарство включено в список важных и жизненно необходимых лекарственных средств.
Основные различия хлорохина и Гидроксихлорохина в строении — это гидроксильная группа, которой замещен один из СН3. Такие изменения отразились на способности препарата противостоять некоторым заболеваниям и на количестве побочных реакций. При лечении также используют гидроксихлорохина фосфат и hydroxychloroquine sulfate.
Фармакологическое действие
Противомалярийное, противовоспалительное, противопротозойное, иммунодепрессивное.
Фармакодинамика и фармакокинетика
Препарат проявляет активность против всех видов плазмодиев (кроме P. falciparum), обладает гамонтоцидным и шизонтоцидным действием. Вещество способно уплотнять лизосомальные мембраны и предотвращать выход лизосомальных ферментов, нарушая процессы нормальной репликации ДНК, РНК и утилизацию гемоглобина эритроцитарными формами плазмодия.
Также оказывает выраженное противовоспалительное и иммунодепрессивное действие. Связывает свободные радикалы и снижает активность протеолитических ферментов — коллагеназы и протеазы, хемотаксис лимфоцитов и лейкоцитарных клеток. Это предотвращает распад тканей хрящей.
Известно, что Гидроксихлорохин достаточно активно подавляет бесполые эритроцитарные формы, гаметы Plasmodium malariae, Plasmodium vivaх. Однако, лекарственное средство не действует на Plasmodium falciparum, штаммы Plasmodium falciparum, на внеэритроцитарные формы Plasmodium ovale, Plasmodium vivax и Plasmodium malariae. Поэтому не назначается в профилактических целях для предупреждения заболеваний, ассоциированных с перечисленными выше организмами. Лекарство не применяется для предотвращения рецидивов этих заболеваний.
Как правило, средство используют в форме таблеток. После проникновения в пищеварительный тракт препараты хорошо и быстро устраиваются. Максимальная концентрация достигается через 60-120 минут. Объем распределения средства в организме — 5-10 л на кг.
Гидроксихлорохин обладает способностью накапливаться в тканях печени, в легких, печени и селезенке. Концентрация лекарства и органах и тканях достигается в 200-700 раз больше, чем плазменная. Вещество накапливается в ЦНС, лейкоцитах, эритроцитах и тканях, насыщенных меланином. Преодолевает плацентарный барьер, метаболизируется в печени, метаболиты неактивны. Выводится половина вещества за 120 часов, ликвидируется с помощью почек (четверть в неизмеренном виде), с калом (меньше 10%).
Показания к применению Гидроксихлорохина
Противопоказания
Осторожность рекомендуют соблюдать:
Побочные действия
Касаемо побочных реакций, препарат хорошо изучен и можно определить и предугадать проявление множества нежелательных реакций.
Лекарство Гидроксихлорохин может вызвать:
Гидроксихлорохин, инструкция по применению (Способ и дозировка)
Лекарство принимают внутрь, во время или после еды, запивая молоком.
Инструкция по применению при ревматоидном артрите
Лечение назначают длительное, так как эффекты начинают проявляться через несколько недель. А необходимый эффект — через несколько месяцев лечения. Если в течение полугода лечения не возникли положительные изменения в состоянии, то прием лекарства прерывают.
Взрослые пациенты могут принимать минимально эффективные дозировки препарата, не более 6,5 мг на кг веса в день. Допустимо принимать Гидроксихлорохин 200 мг, 400 мг в сутки.
Лечение системной красной волчанки
Начальная средняя дозировка составляет 0,4 г, 1 или 2 раза в сутки. Назначают на несколько месяцев или недель, контролируя состояние пациентов. Далее лечение проводят дозировками 0,2-0,4 г.
Гидроксихлорохин при малярии
Для профилактики острых приступов малярии (P. malariae и штаммами Plasmodium falciparum) — по 0,4 грамма один раз в неделю. Для детей дозировка составляет 6,5 мг на кг веса в день, но не более дозировки для взрослого.
Профилактику малярии начинают за 14 дней до поездки. В противном случае, применяют нагрузочную дозировку 0,8 г, и 12,9 мг на кг веса за 2 приема, через 6 часов. Лечение продолжают еще 2 месяца после выезда.
При острых приступах анемии используют 800 мг препарата, 400 мг через 6 или 8 часов, потом 400 мг в течение двух следующих дней (в общем — 2 грамма гидроксихлорохина сульфата).
Для радикального лечения малярии, вызванной Plasmodium malariae и Plasmodium vivax используют дополнительно производные 8-аминохинолона.
Передозировка
При острой передозировке наблюдается кардиотоксичность, понижение артериального давления, головные боли, повышенная возбудимость, головокружение, судороги, кома, проблемы со зрением, вплоть до остановки сердца и дыхания. При хронической интоксикации возникает гипертрофия миокарда.
Чрезвычайно опасна передозировка у маленьких детей, даже при приеме 1-2 грамм препарата велика вероятность летального исхода.
Пострадавшему промывают желудок, назначают Активированный уголь, проводится форсированный диурез, назначают аммония хлорид, чтобы подкислить мочу.
Взаимодействие
Гидроксихлорохин может увеличивать плазменную концентрацию Дигоксина и, чтобы не возникало гликозидной интоксикации, дозировки антиаритмического средства снижают.
Вещество усиливает действие инсулина и некоторых гипогликемических средств, может потребоваться уменьшение дозы этих препаратов.
Антациды снижают процессы всасывания Гидроксихлорохина, рекомендуется соблюдать между приемом этих препаратов интервал 4 часа.
Существует большой риск усиления действия аминогликозидов на нервно-мышечную передачу.
Циметидин плохо сочетается с антималярийными препаратами, увеличивает их плазменные концентрации и риск возникновения побочных реакций.
Пиридостигмин и Неостигмин усиливают действие антималярийного средства.
Лекарство не рекомендуется сочетать с интрадермальной человеческой диплоидно-клеточной вакциной против бешенства. Это приводит к снижению интенсивности образования антител при первичной иммунизации.
Условия продажи
Условия хранения
Таблетки хранят в месте, недоступном для детей при температуре до 25 градусов.
Особые указания
Токсическое воздействие лекарства на сетчатку глаза сильно зависит от дозы. Не рекомендуется превышать суточную дозу.
Перед тем, как начинать прием Гидроксихлорохина рекомендуют пройти обследование глаз — состояние глазного дна, остроту зрения, оценку цветового зрения и полей зрения. При лечении такие обследования нужно проходить не реже одного раза в пол года.
Обследование нужно проходить чаще пациентам из группы риска:
Если у пациента наблюдаются офтальмологические побочные реакции, то лекарство сразу же отменяют и наблюдают за состоянием пациента. Зрительные расстройства и заболевания сетчатки могут прогрессировать и после отмены лекарства.
Нужно соблюдать особую осторожность при лечении пациентов с почечной и печеночной недостаточностью. Рекомендуют скорректировать дозировку препарата. Суточная доза подбирается исходя из уровня плазменной концентрации Гидроксихлорохина.
При длительном лечении препаратом необходимо периодически сдавать полный анализ крови. Если у пациента возникли нарушения гематологических показателей, лекарство нужно отменить.
Все пациенты, которые длительно принимают лек. средство должны наблюдаться у невролога в отношении работы скелетных мышц, выраженности сухожильных рефлексов. Если наблюдается слабость мышц, лекарство отменяют.
Пациенты, которые проходят терапию данным лек. средством должны соблюдать осторожность при управлении автомобильным транспортом, при выполнении работы, которая требует высокой концентрации внимания и точности.
Лечение коронавируса Гидроксихлорохином
На сегодняшний день ученые и медики возлагают большие надежды на лечение коронавируса COVID-19 с помощью Гидроксихлорохина. Были проведены небольшие исследования и экспериментальное лечение пациентов во Франции, активно препарат применялся в Китае.
Достаточно известный инфекционист из Франции, глава Средиземноморского института инфекционных заболеваний Дидье Раульт провел небольшие клинические испытания препарата на 36 пациентах, зараженных коронавирусом COVID-19. Врач отметил, что на 6 день лечения вирусная нагрузка у больных значительно снизилась, а стойкий эффект достигался при сочетании Гидроксихлорохина и Азитромицина (антибиотик). Марсельский институт активно прописывает больным данную комбинацию лекарств и берет на себя всю ответственность за возможные негативные последствия.
Президент США Дональд Трамп, в свою очередь, «прорекламировал» Гидроксихлорохин против коронавируса в своем твиттере. Президент заявил, что препарат вскоре будут использовать во всем мире для лечения Covid-19. После этого заявления во многих аптеках США уже раскупили лекарство от малярии, а фарм. компании стали увеличивать объем производства препарата.
Однако, в конце апреля 2020 года были опубликованы результаты проведенного в США ретроспективного исследования (368 пациентов с COVID-19) в центрах оказания мед. помощи ветеранам Veteran Health Administration. Часть пациентов (97 человек) совместно со стандартным лечением дополнительно принимали Гидроксихлорохин, часть (113 человек) принимали Гидроксихлорохин + Азитромицин, оставшаяся часть пациентов не проходила лечение данными препаратами.
Анализируя количество летальных исходов, ученые пришли к выводу, что прием Гидроксихлорохина только ухудшает ситуацию. Больных, принимавших лекарство, умерло 27,8%. Принимавших лекарство вместе с Азитромицином умерло 22%. Больных, не принимавших для лечения Гидроксихлорохин, умерло 11,4%.
Ряд специалистов настаивают на том, что эффективность этого препарата против коронавируса не доказана, он обладает обширным списком побочных эффектов, а его передозировка может привести к плачевным последствиям. Известны уже случаи самолечения данным лек. средством, которые привели к летальному исходу. Медики настоятельно не рекомендуют заниматься самолечением!
При беременности и лактации
При лечении средством грудное вскармливание прекращают. Препарат не рекомендуется назначать при беременности.
Минздрав исключил гидроксихлорохин из клинических рекомендаций по лечению ковида
Клинические рекомендации — советы для врачей, а не строгие правила, отступать от которых запрещает закон. Однако все равно хорошо, что этот препарат исключили из рекомендаций. Теперь у врачей, которые его не назначают, точно не возникнет юридических проблем, а пациенты перестанут получать неэффективное лечение.
Будьте внимательны к источникам информации о здоровье — и сходите к врачу
Наши статьи написаны с любовью к доказательной медицине. Мы ссылаемся на авторитетные источники и ходим за комментариями к докторам с хорошей репутацией. Но помните: ответственность за ваше здоровье лежит на вас и на лечащем враче. Мы не выписываем рецептов, мы даем рекомендации. Полагаться на нашу точку зрения или нет — решать вам.
Что такое гидроксихлорохин
Во-первых, препарат используют для профилактики и лечения малярии. Эту болезнь вызывают одноклеточные паразиты — малярийные плазмодии. Лекарство накапливается в организме паразита и мешает ему переваривать главный эритроцитарный белок — гемоглобин. В итоге чувствительные к хлорохину паразиты погибают от голода, не успев размножиться, и человек выздоравливает.
Как победить выгорание
Как гидроксихлорохин оказался в российских клинических рекомендациях
На момент начала клинических испытаний уже было известно, что в лабораторных экспериментах, то есть в пробирке, хлорохин разрушает частицы вируса-предшественника возбудителя коронавирусной болезни SARS-CoV-2 и препятствует размножению некоторых вирусов в лабораторных культурах клеток.
Кроме того, ученые очень рассчитывали на противовоспалительный эффект лекарства. Они надеялись, что гидроксихлорохин сможет подавить цитокиновый шторм — бурную иммунную реакцию, которая развивается у некоторых людей с тяжелой коронавирусной болезнью.
Поскольку ранние данные давали надежду, что гидроксихлорохин поможет тяжелобольным пациентам, 28 марта 2020 года авторитетный американский надзорный орган — Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, или FDA, — разрешил врачам использовать этот препарат в стенах больниц.
Часто задаваемые вопросы о разрешении на экстренное использование хлорохинфосфата и гидроксихлорохинсульфата для некоторых госпитализированных пациентов с COVID-19 — бюллетень FDAPDF, 193 КБ
Опираясь на данные китайских и американских исследований и на отечественный опыт применения препарата, эксперты Минздрава пришли к выводу, что гидроксихлорохин в низких дозах допустимо назначать пациентам с легкой и среднетяжелой формой COVID-19 в первые 3—5 дней болезни.
В итоге препарат включили в первую версию временных методических рекомендаций по профилактике и лечению коронавирусной болезни. Гидроксихлорохин присутствовал в регулярно обновляемых клинических рекомендациях вплоть до десятой версии, которую приняли 8 февраля 2021 года.
Почему гидроксихлорохин исключили из клинических рекомендаций
Кроме того, у пациентов COVID-19 препарат часто провоцировал осложнения. Например, учащенное сердцебиение — тахикардию. Многие пациенты, которые пытались самостоятельно лечиться гидроксихлорохином, отравились, причем некоторые до смерти. В итоге 15 июня 2020 года FDA отозвало экстренное разрешение на использование гидроксихлорохина для лечения коронавирусной болезни. Все прежние рекомендации для этого препарата остались в силе.
От применения гидроксихлорохина при COVID-19 отказались во всем мире. Однако в российские клинические рекомендации гидроксихлорохин входил вплоть до 7 мая 2021 года, то есть до одиннадцатой версии клинических рекомендаций. Но теперь Минздрав официально подтвердил, что врачи имеют полное право не назначать пациентам с коронавирусной болезнью этот ненужный и небезопасный препарат.
Для многих людей это все еще актуально. По данным сайта стопкоронавирус.рф, 17 мая 2021 года в России 9328 новых случаев заражения COVID-19.
Журнал «Сырье и Упаковка»
Текущий номер
Ближайшие выставки
Партнеры
Гипохлориты и их применение в средствах бытовой химии
30.03.2020
| Д. А. Меркулов, к.х.н., зав. кафедрой фундаментальной и прикладной химии, ФГБОУ ВПО «Удмуртский государственный университет», г. Ижевск |
Введение
Гипохлоритами называют соли хлорноватистой кислоты HClO. Наиболее распространенными из них являются гипохлорит натрия, гипохлорит кальция и гипохлорит калия. Гипохлориты широко применяются для обеззараживания питьевой воды, отбеливания, дегазации и дезинфекции. Гипохлориты являются одними из самых важных химических соединений.
| Систематическое наименование | Традиционное название | Хим. формула | CAS № | М, г/моль |
|---|---|---|---|---|
| Гипохлорит натрия | Хлорноватистокислый натрий, лабарракова вода (гипохлорит натрия в смеси с хлоридом натрия и гидроксидом натрия) | NaClO | 7681–52–9 | 74,44 |
| Гипохлорит калия | Хлорноватистокислый калий, жавелевая вода (гипохлорит калия в смеси с гидрокарбонатом калия и хлоридом калия) | KClO | 7778–66–7 | 90,55 |
| Гипохлорит кальция | Хлорноватистокислый кальций, хлорная известь (гипохлорит кальция в смеси с хлоридом кальция, оксихлоридом кальция и гидроксидом кальция) | Ca(ClO) 2 | 7778–54–3 | 142,98 |
История открытия
В 1774 г. шведский химик Карл Вильгельм Шееле получил хлор (Cl 2 ) в результате взаимодействия оксида марганца(IV) MnO 2 и соляной кислоты (HCl). Позже, в 1785 г. французский химик Клод Луи Бертолле обнаружил, что водный раствор газообразного хлора («хлорная вода»), содержащий хлорноватистую и хлороводородную кислоты, может отбелить белье, и сообщил о своих выводах Французской академии наук.
Cl 2 + H 2 O = HClO + HCl
Знания об отбеливающих свойствах хлора были незамедлительно использованы Джеймсом Уаттом на текстильной фабрике в Глазго. Несмотря на то, что отбеливание с использованием хлора был значительно эффективнее традиционных способов отбеливания солнечным светом, слабыми растворами кислот и щелочей, применение хлора ограничивалось его токсичностью и разрушающим действием на ткани. Для стабилизации раствора газообразного хлора в воде и безопасности его применения, в 1787 г. на Парижском предприятии Societe Javel хлор стали пропускать через водный раствор карбоната калия (поташа)
Cl 2 + K 2 СO 3 = 2KHCO 3 + KClO + KCl.
Глава предприятия Леонард Альбан назвал новый продукт «Eau de Javel» («жавелевая вода»), и вскоре белильная жидкость стала популярной во Франции и Англии.
В 1820 г. француз Антуан Лабаррак усовершенствовал способ получения отбеливателя, заменив поташ на более дешевый гидроксид натрия (каустическую соду). Полученный раствор гипохлорита и хлорида натрия получил название «Eau de Labarraque» («лабарракова вода»).
Cl 2 + 2NaOH = NaClO + NaCl + H 2 O.
Широкое применение гипохлоритов для обеззараживания питьевой воды и дезинфекции стало возможным гораздо позже, в начале XX века, благодаря развитию промышленного производства хлора электролизом поваренной соли.
Физические свойства
Гипохлориты встречаются нам преимущественно в виде водных растворов, хотя некоторые из них можно выделить в твердом виде. Так, известен безводный гипохлорит натрия, который представляет собой неустойчивое бесцветное кристаллическое вещество. Из кристаллогидратов наиболее устойчивой формой является NaClO×5H 2 O. Это соединение представляет собой белые или бледно-зеленые ромбические кристаллы, расплывающиеся на воздухе. При нагревании пентагидрата гипохлорита натрия до температуры 24,4°С, он плавится. Кристаллогидрат NaClO×2,5H 2 O плавится при температуре 57,5°С. Моногидрат крайне неустойчив и разлагается выше 60°С, при более высоких температурах разложение протекает со взрывом.
Таблица 2. Плотности и температуры замерзания водных растворов гипохлорита натрия.
В отличие от гипохлорита калия, известного только в растворах, гипохлорит кальция можно выделить в форме бесцветных кристаллов, устойчивых в сухой атмосфере без углекислого газа. Из водных растворов гипохлорит кальция можно выделить в виде кристаллогидратов Ca(ClO) 2 ×2H 2 O, Ca(ClO) 2 ×3H 2 O, Ca(ClO) 2 ×4H 2 O.
Кислотно-основное равновесие между хлорноватистой кислотой и гипохлорит-ионом описывается обратимой реакцией с константой равновесия Ka = 2,63×10 –8 при 20°С.
Используя константу равновесия Ka, можно рассчитать мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от рН (рис.1).
Данные свидетельствуют, что при подкислении растворов гипохлоритов увеличивается доля неустойчивой хлорноватистой кислоты. При рН 7,58 существуют преимущественно гипохлорит-ионы.
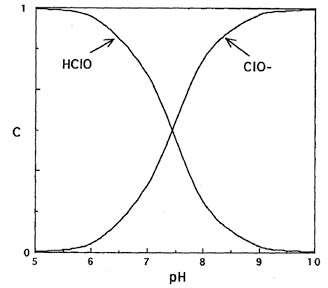
Рис. 1. Мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от кислотности среды.
Химические свойства
Гипохлориты являются неустойчивыми соединениями, легко разлагающимися с выделением кислорода. Разложение твердых гипохлоритов натрия и кальция можно представить уравнениями
2NaClO = 2NaCl + O 2 ↑ и 2Сa(ClO) 2 = СaCl 2 + O 2 ↑.
Процессы при комнатной температуре происходят медленно, а при нагревании могут протекать со взрывом. Параллельно реакциям, сопровождающимся образованием хлоридов и свободного кислорода, могут протекать реакции диспропорционирования
Разложение гипохлоритов в водных растворах зависит от кислотности раствора и его температуры. В сильнокислых средах при рН ≤ 3 хлорноватистая кислота при комнатной температуре разлагается до хлора и кислорода
4HClO = 2Cl 2 ↑ + O 2 ↑ + 2H 2 O.
Если при подкислении используется соляная кислота или в растворе присутствуют хлориды, образование кислорода не происходит
HClO + HCl = Cl 2 ↑ + H 2 O.
Хлорноватистая кислота очень слабая, поэтому она может быть вытеснена из раствора ее солей действием углекислого газа
ClO – + CO 2 + H 2 O = HCO 3 – + HClO.
В слабокислых и нейтральных средах при 3 2 ↑.
В нейтральных и щелочных растворах имеет место конкурирующая реакция образования хлоридов и хлоратов
При комнатной температуре реакция диспропорционирования протекает медленно, но при температурах выше 70°С эта реакция становится преобладающей.
В щелочных средах при рН > 7,5 в растворах преобладают гипохлорит-ионы, разлагающиеся следующим образом:
Около 95% от общего количества гипохлорит-ионов разлагается в результате последовательных реакций (1) и (2), причем реакция (1) является самой медленной (лимитирующей) и определяет общую скорость процесса. Реакция (3) не является основной, но отвечает за выделение кислорода, количество которого может быть значительным.
В присутствии некоторых ионов металлов, например, меди, никеля, кобальта наблюдается каталитическое разложение гипохлорит-ионов. Ионы железа обладают слабым каталитическим действием и являются сокатализаторами в сочетании с другими ионами металлов. В простейшем случае, при содержании ионов меди(II) в растворе в концентрации 1мг/кг порядки гомогенной реакции по гипохлориту и по меди(II) равны единице.
Гетерогенный катализ металлами и их нерастворимыми соединениями, является сложным и плохо воспроизводимым. Из нерастворимых катализаторов наибольшее мешающее влияние оказывает никель и его оксиды, которые попадают в растворы гипохлоритов при их контакте с легированными никелевыми сталями, используемыми для изготовления трубопроводов и резервуаров.
На константы скорости реакций (1)-(3) большое влияние оказывает ионная сила растворов. Высокие концентрации электролитов уменьшают константы скорости реакций и обеспечивают разумную стабильность при хранении растворов электролитов. Увеличение концентрации гипохлорит-ионов, напротив, уменьшает их стабильность в водных растворах. На рис. 2 показан феномен «кривой пересечения». Растворы гипохлорита натрия с концентрацией 9% и 5% при хранении разлагаются настолько, что через 50 недель показывают одинаковую концентрацию вещества, а через 100 недель первоначально более концентрированный раствор содержит гипохлорит-ионов меньше, чем разбавленный.
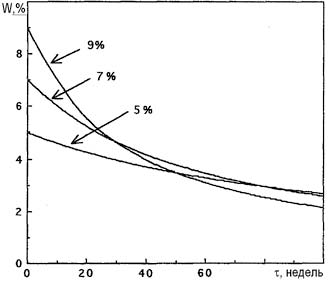
Рис. 2. Разложение гипохлорита натрия различных концентраций при 30°С.
Повышение температуры способствует ускорению процессов разложения гипохлоритов, поэтому целесообразно хранить растворы гипохлоритов в прохладном месте для обеспечения срока годности (рис. 3).

Рис. 3. Влияние температуры на разложение 5%-ного раствора NaClO.
Для стабилизации водных растворов гипохлоритов, а так же продуктов на их основе, каждый производитель применяет собственные методы, которые редко публикуются в виде статей. Однако известны некоторые запатентованные методы, которые, не претендуя на полноту, можно представить следующим списком:
Направление окислительно-восстановительных процессов с участием гипохлорит-ионов и хлорноватистой кислоты обусловлены значениями стандартных электродных потенциалов полуреакций в водной среде:
2HClO + 2H + + 2e – = Cl 2 ↑ + 2H 2 O, E° = 1,630 В,
HClO + H + + 2e – = Cl – + H 2 O, E° = 1,500 В.
в нейтральной и щелочной среде
Таким образом, гипохлорит-ионы и хлорноватистая кислота обладают выраженными окислительными свойствами, причем их окисляющая способность в кислой среде значительно выше, чем в нейтральной и щелочной средах.
Дезинфицирующее действие
Гипохлориты являются одними из лучших антибактериальных средств. Они убивают микроорганизмы очень быстро даже при очень низких концентрациях.
Наивысшее бактерицидное действие гипохлоритов проявляется в нейтральной среде, когда концентрации хлорноватистой кислоты и гипохлорит-ионов приблизительно равны (рис. 1). Образующиеся при разложении гипохлоритов активные частицы (атомарный кислород и хлор) обладают высоким биоцидным действием. Они уничтожают микроорганизмы, взаимодействуя с биополимерами в их структуре, способными к окислению. Аналогичным образом, например, действуют клетки человека нейтрофилы, гепатоциты и др., которые синтезируют хлорноватистую кислоту и сопутствующие высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциями.
Бактерицидная активность гипохлоритов настолько велика, что они способны привести к гибели дрожжеподобных грибов, вызывающих кандидоз, Candida albicans, в течение 30 секунд при действии 5,0 – 0,5%-го гипохлоритного раствора. Патогенный Enterococcus faecalis погибает через 30 секунд после обработки 5,25%-ым раствором и через 30 минут после обработки 0,5%-ым раствором. Грамотрицательные анаэробные бактерии, такие как Porphyromonas gingivalis, Porphyromonas endodontalis и Prevotella intermedia, погибают в течение 15 секунд после обработки 5,0 – 0,5%-м раствором гипохлорит-ионов.
Несмотря на высокую биоцидную активность гипохлоритов, некоторые потенциально опасные простейшие организмы, например, возбудители лямблиоза или криптоспоридиоза, к сожалению, устойчивы к его действию.
При помощи гипохлорит-ионов можно успешно обезвреживать различные токсины (табл. 3).
Таблица 3. Результаты инактивации токсинов при 30-минутной экспозиции различных концентраций гипохлорита натрия («+» – токсин инактивирован; «–» – токсин остался активен).
| Токсин | 2,5% NaClO + 0,25 н. NaOH | 2,5% NaClO | 1,0% NaClO | 0,1% NaClO |
|---|---|---|---|---|
| Т-2 токсин | + | – | – | – |
| Бреветоксин | + | + | – | – |
| Микроцистин | + | + | + | – |
| Тетродотоксин | + | + | + | – |
| Сакситоксин | + | + | + | + |
| Палитоксин | + | + | + | + |
| Рицин | + | + | + | + |
| Ботулотоксин | + | + | + | + |
Методы анализа
Качественными реакциями на гипохлорит-ион могут служить:
Наиболее распространенным методом количественного анализа гипохлорит-иона является титриметрический метод с использованием йодида калия. Для проведения испытания водный раствор или водную суспензию, содержащие гипохлорит-ион, смешивают с избытком раствора йодида калия в сернокислой среде. Выдерживают герметично закрытую смесь в течение 5 минут в темном месте. Выделившийся йод титруют стандартизированным раствором тиосульфата натрия. В качестве индикатора вблизи точки эквивалентности используют крахмальный раствор.
При количественном определении гипохлорит-иона косвенным йодометрическим методом результаты анализа пересчитывают на концентрацию «активного хлора» в ыделившегося при реакции
2H + + ClO – + Cl – = Cl 2 ↑ + H 2 O.
Альтернативным методом количественного определения гипохлорит-иона является потенциометрический анализ с использованием бром-ионселективного электрода. Концентрацию гипохлорит-иона находят методом добавок анализируемого раствора к стандартному раствору или методом уменьшения концентрации анализируемого раствора при его добавлении к стандартному раствору.
Способы получения наиболее важных товарных продуктов
Крупнотоннажными гипохлоритсодержащими продуктами являются гипохлорит натрия и гипохлорит кальция. Их глобальный объем производства превышает 1 млн тонн/год. При этом почти половина этого объема используется в быту, а другая половина в промышленности. Гипохлорит калия, являющийся исторически первым гипохлоритом, нашедшим промышленное применение, производится в ограниченном количестве.
Для промышленного производства гипохлорита натрия используются химический и электрохимический методы. При химическом методе производится хлорирование водных растворов гидроксида натрия. Суть химического превращения не изменилась со времен его открытия и применения Лабарраком
Cl 2 + 2NaOH = NaClO + NaCl + H 2 O.
Существуют две производственные схемы данного метода:
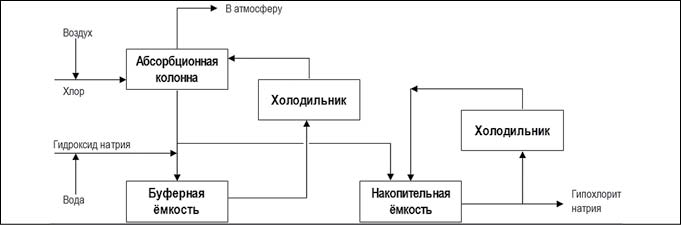
Рис. 4. Химический метод получения гипохлорита натрия основным процессом (рис. с сайта https://ru.wikipedia.org)
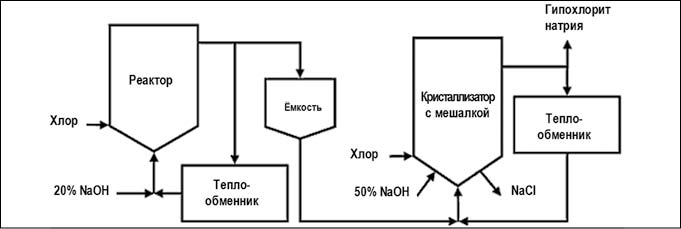
Рис. 5. Химический метод получения гипохлорита натрия концентрированным процессом (рис. с сайта https://ru.wikipedia.org)
При электрохимическом методе получения гипохлорита натрия водный раствор хлорида натрия подвергается электролизу в электролизере с открытыми электродными зонами (бездиафрагменный способ). Гидроксид натрия, образующийся на катоде, и хлор, выделяющийся на аноде, беспрепятственно смешиваются в ходе электрохимического процесса
NaCl + H 2 O = NaClO + H 2 ↑(суммарная реакция).
Гипохлорит кальция производится в виде хлорной извести, представляющей собой смесь целевого продукта с хлоридом кальция и гидроксидом кальция. В качества сырья для получения хлорной извести используется порошкообразный гидроксид кальция (пушенка), содержащий менее 1% свободной влаги и разбавленный влажным воздухом хлор. Небольшая влажность исходных веществ обеспечивает начало реакции гидролиза хлора, сопровождающейся нейтрализацией образующихся кислот известью. Затем реакция продолжается за счет воды, выделяющейся из гидроксида кальция при хлорировании
2Сa(OH) 2 + 2Cl 2 = Сa(ClO) 2 + СaCl 2 + 2H 2 O (суммарно).
Хлорирование пушенки осуществляется в аппаратах непрерывного действия – механических полочных камерах Бакмана.
Таблица 4. Производители гипохлорита натрия в России.
| Название предприятия | Сайт предприятия |
|---|---|
| «Каустик» ЗАО, г. Стерлитамак | www.kaus.ru/ |
| «Каустик» ОАО, г. Волгоград | www.kaustik.ru/ |
| «Новомосковский хлор» ООО, г. Новомосковск | www.hlor.biz/ |
| «Сода-хлорат» ООО, г. Березняки | www.soda.perm.ru/ |
Характеристика товарных гипохлоритов, обращение, хранение и транспортировка
В Российской Федерации гипохлориты производятся в соответствии с ГОСТ 11086–76 «Гипохлорит натрия. Технические условия» и ГОСТ 1692–85 «Известь хлорная. Технические условия». Гипохлорит натрия по назначению и показателям выпускается двух марок «А» и «Б» (табл. 5).
Таблица 5. Физико-химические показатели и назначение гипохлорита натрия по ГОСТ 11086–76