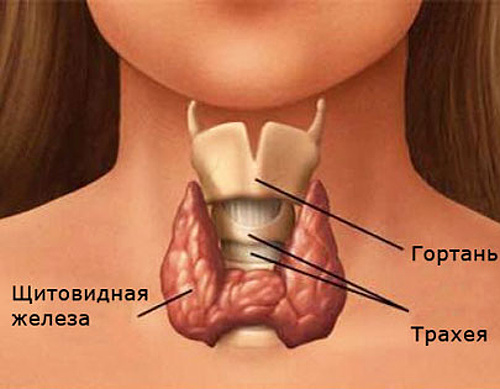
Что такое ЦДК при УЗИ щитовидной железы?
Современное УЗИ щитовидки в большом количестве случаев проводится с использованием ЦДК. Оно позволяет специалисту наиболее точно рассмотреть состояние органа у человека. Такой метод даёт возможность установить причину поражения, а также направление и скорость его распространения. Всё это помогает сделать современное медицинское обеспечение, которое исследует поток крови внутри тканей.
На сегодняшний день подобный способ диагностирования наиболее эффективен. Далее рассмотрим более тщательно, что такое ЦДК при УЗИ щитовидной железы.
Мнения специалистов и разные подходы
В современной медицине лучшим способом для выявления и предотвращения заболеваний на ранних стадиях считается УЗИ. Но число больных с каждым годом растёт, поэтому врачам приходится внедрять новые технологии. Это нужно для получения более точной картины заболевания. Намного расширить возможности привычного УЗИ помогло цветное допплеровское картирование, в сокращении ЦДК. Хотя, используя данную технологию в практике, некоторые специалисты оценивают её неоднозначно.
Выделяется три основных подхода:
Главная ценность метода не только в выявлении дефектов кровоснабжения щитовидной железы, но и возможность обнаруживать опухоли на начальных стадиях развития. ЦДК позволяет получить информацию из самой глубины происходящего. Благодаря этому, квалифицированный специалист может провести дифференциацию отклонений.
Он сможет распознать, где доброкачественная опухоль, а где злокачественная. Оборудование позволяет видеть структуру и строение ткани в нескольких масштабах.
Пациенту назначается УЗИ щитовидки с ЦДК, если у него наблюдаются следующие симптомы:
Информация, получаемая с помощью ЦДК
Такой метод в наше время можно отнести к самому используемому в мире. Ведь информация, полученная с помощью современной технологии, помогает понять степень пораженности эндокринной железы, а также всей системы в целом. Если применять ДК в цветном варианте, то врач может обследовать не только щитовидку, но и жидкость вокруг неё. Такой возможности нет ни у одного другого оборудования. Специалист проверит состояние сосудов пациента.
Цветное допплеровское картирование даёт возможность анализировать информацию в “прямом эфире”. На дисплее эндокринолог видит красный и синий цвет, которые передают данные о движении крови. Нужно отметить, что цвета – это не тип сосудов и артерий. Для этого врач пользуется специальным списком, в котором подробно описана проблема и тип болезни.
Основные данные, получаемые оборудованием:
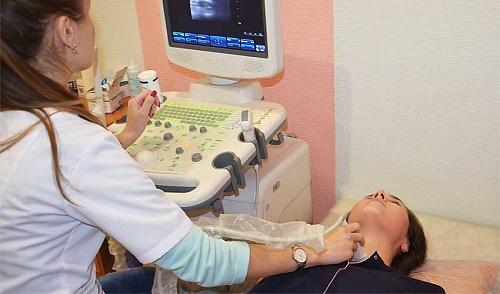
Назначение метода
Специалист назначает УЗИ с ЦДК при подозрении на определённые заболевания, такие как:
Очень часто такой метод обследования используется при постоянной отечности ног у человека. При отеках сильно заметны вены, появляются частые боли в конечностях, регулярные судороги.
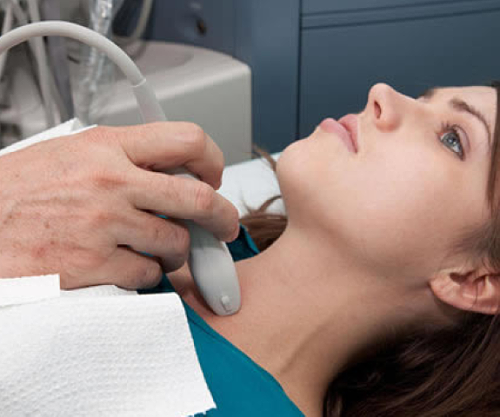
Описание процедуры, подготовка к ней
Перед процедурой пациент должен с ней ознакомится и морально подготовиться. Посещать врача в шоковом или стрессовом состоянии категорически запрещается. Такое состояние не позволит понять точной картины происходящего, потому что все органы будут сильно напряжены. Рекомендуется ограничить употребление мясных продуктов перед процедурой.
При посещении кабинета УЗИ с собой пациент берёт какое-либо полотенце или пеленку, на которую укладывается человек во время обследования. Полотенцем убираются излишки геля, которым смазывается место исследования. Такая процедура никак не влияет на организм.
Существует некоторые противопоказания, запрещающие проведение обследование щитовидной железы:
Учёными выделяется несколько достоинств УЗИ с цветным допплеровским картированием:
Самым главным плюсом ЦДК является безопасность процедуры для беременных. Такой метод не несёт никакого вреда для развивающегося плода. Он активно начинает внедряться в клиники и больницы всего мира.
Щитовидная железа — скрытая опасность: особенности расшифровки УЗИ щитовидной железы
Щитовидная железа — скрытая опасность. Особенность расшифровки УЗИ щитовидной железы
Мы давно знаем, что Россия является эндемичной областью заболеваний щитовидной железы. Трудно найти человека, чей знакомый или родственник не жаловался бы на проблемы с щитовидкой. Справедливости ради следует отметить, что культура профилактических исследований в России в последнее время возросла. Особенно длинные очереди стоят у дверей специалистов УЗИ. Однако просто пройти ультразвуковое исследование щитовидной железы недостаточно. Не менее важно правильное прочтение результата обследования.
Что показывает УЗИ щитовидки
Ультразвуковое исследование щитовидной железы позволяет получить точную информацию о ее состоянии. Прежде всего, внимание уделяется расположению, форме, контуру и, конечно же, размерам железы.
Что касается общего размера и объема, железа может быть нормальной, увеличенной (гиперпластической) или уменьшенной (гипопластической). Существуют также случаи асимметрии железы, отсутствия части доли (гемиагенез) и полного отсутствия железы (агенез-аплазия).
Нормы объема щитовидки варьируются в зависимости от возраста и пола. Верхний предел для женщин составляет 18 см3, для мужчин — 25 см3. Когда дети становятся старше, железы растут.
Какие заболевания щитовидной железы выявляются при ультразвуковом исследовании
Список заболеваний щитовидной железы довольно разнообразен. Большинство из них выявляются именно при ультразвуковом исследовании.
Также бывает, что ультразвук выявляет изменения, но железа функционирует нормально. Например, при некоторых типах узлового зоба лабораторные данные — гормоны щитовидной железы и их антитела — могут быть в пределах нормы. В этом случае важно проконсультироваться с врачом-эндокринологом, осмотреть узел и оценить его размеры, что делается при повторных ультразвуковых исследованиях.
В заключении есть фраза: «Структура щитовидной железы — диффузно неоднородная, зернистая». На какую патологию это указывает?
В сонографическом заключении можно увидеть данные об однородности или неоднородности железистой паренхимы, о качестве зерен. Эти данные предоставляют информацию о структуре паренхимы.
Нормальная паренхима щитовидной железы однородна, т. е. однородна, с равными экосистемами. А при указанных заболеваниях она иногда выражается в ее диффузной или локальной неоднородности и размере зерна (от мелких до крупных зерен).
Одна из ультразвуковых характеристик — эхогенность железистой паренхимы. Эхогенность нормальной паренхимы несколько выше, чем у окружающих тканей. В заключение пациенты сталкиваются в основном с информацией о вторичной эхогенности. При избытке соединительной ткани, фиброзных процессах, усилении кальцификации, эхогенности железы увеличивается, а при воспалительных заболеваниях она в основном уменьшается. Хотя этот признак также относительный.
Что значит узловой зоб? Можно ли только на основании экологических данных выяснить, является ли узел доброкачественным или злокачественным?
Узловой зоб представляет собой очаговое очаговое поражение щитовидной железы — различных размеров, форм, структур и экоструктур, единичных или нескольких. Основной задачей ультразвука является обнаружение подозрительных узлов.
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/04/Многоузловой-зоб.jpg?fit=450%2C142&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/04/Многоузловой-зоб.jpg?fit=900%2C283&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/04/%D0%9C%D0%BD%D0%BE%D0%B3%D0%BE%D1%83%D0%B7%D0%BB%D0%BE%D0%B2%D0%BE%D0%B9-%D0%B7%D0%BE%D0%B1.jpg?resize=900%2C283&ssl=1″ alt=»Многоузловой зоб» width=»900″ height=»283″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/04/Многоузловой-зоб.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/04/Многоузловой-зоб.jpg?resize=450%2C142&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/04/Многоузловой-зоб.jpg?resize=768%2C241&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Многоузловой зоб
Узелок щитовидной железы может быть как доброкачественным, так и злокачественным. Большинство узелков являются доброкачественными (коллоидные узелки, кисты, аденомы, так называемые псевдокисты), но в 1-15 случаях РАС также обнаруживаются злокачественные образования — папиллярный рак, фолликулярный, медуллярный или анапластический.
Размеры опухоли являются переменными. Мы часто сталкиваемся с небольшими (до 1 см) злокачественными узлами, которые нельзя тестировать вручную (не пальпируемые узелки). Наиболее распространенным из злокачественных процессов является папиллярный рак (50-80%).
К сожалению, определить характер узловой формации только на основании экологических данных невозможно. Можно только предположить злокачественность процесса. Подозрение связано со следующими экологическими признаками:
Специфичность одних только этих признаков не высока, но в случае одновременного обнаружения двух или более симптомов необходимо провести пункционную биопсию узла с цитологическим исследованием полученного материала.
Одна из важных особенностей опухоли — является васкуляризация или кровоснабжение узла. Большинство злокачественных узелков резко васкуляризованы, хотя есть и аваскулярные (бескровные) опухоли. Кроме того, усиленная васкуляризация обнаруживается в активно функционирующих (токсических) узлах, которые часто оказываются коллоидными, а не злокачественными. Таким образом, экологических данных недостаточно для подтверждения окончательного диагноза, но выявление потенциально опасных узлов — прерогатива врача-сонографиста.
Цветовое допплеровское картирование в диагностике опухолей матки
Диагностическое значение цветового допплеровского картирования (ЦДК) трудно переоценить. Сущность этого метода состоит в возможности визуализации всех движущихся жидкостей организма в режиме реального времени и проведении анализа их движения. Исследование кровотока в сосудах новообразований, которые имеют свои характерные особенности, позволяет считать этот метод важным в дифференциальной диагностике доброкачественных и злокачественных опухолей матки [5].
ЦДК позволяет оценить три параметра кровотока одновременно: направление, скорость и характер (однородность и турбулентность). В силу высокой разрешающей способности применяемой в настоящее время аппаратуры возможна визуализация и идентификация мельчайших сосудов вплоть до системы микроциркуляторного русла, невидимых при сканировании в В-режиме [3,4].
Система васкуляризации опухоли, как правило, представлена множеством мелких, очень тонких, аномальных по форме и расположению сосудов, хаотично разбросанных в пределах опухолевых тканей. Кровоток в этих сосудах характеризуется крайне низким сосудистым сопротивлением, высокой скоростью и разнообразным направлением. Изображение кровотока при этом отличается выраженной яркостью цветового сигнала, а в «окраске» опухолевых тканей могут преобладать как основные цвета, так и «мозаичная» форма картирования. Эти особенности кровотока обусловлены наличием большого количества артериовенозных анастомозов среди новообразованных сосудов, которые обеспечивают высокую кинетическую энергию кро-вотока и объясняют широкую вариабельность его направления [5].
Метод ЦДК обладает высокой чувствительностью, специфичностью и точностью в ранней диагностике опухолевых заболеваний внутренних половых органов и их диф-ференцировке по степени злокачественности. Оцененный с помощью ЦДК уровень васкуляризации позволяет прогнозировать быстроту роста выявленного образования [4, 5].
Миома матки. Исследования, выполненные A. Kuljak и I. Zalud [18], показали, что из 291 наблюдения доброкачественных онколей матки в 157 (54%) случаях отмечались признаки васкуляризации опухоли, о чем свидетельствует обнаружение цветовых сигналов в ткани новообразования. Из 17 случаев злокачественных опухолей матки интенсивная васкуляризация выявлена в 16 (94%) наблюдениях, что подтверждено последующими морфологическими исследованиями.
Анализ кривых скоростей кровотока при миоме матки позволил установить следующие особенности. У всех пациенток отмечалось снижение резистентности в обеих маточных артериях. Диастолический кровоток всегда обнаруживался в основных артериях, кровоснабжающих миоматозные узлы. Cреднее значение индекса резистентности на уровне кровотока миометрия составило 0,54. Степень васкуляризации больше зависела от размеров опухоли, нежели от ее локализации. Численные значения индекса резистентности в маточных артериях в среднем составили 0,74+/-0,09 при васкуляризированных узлах и 0,80+/-0,10 при аваскуляризированной миоме матки (контроль 0,84+/-0,09) [5, 18-20].
Установлено, что рост миоматозных узлов напрямую зависит от увеличения кровотока в сосудистой системе матки. Кровоснабжение миоматозных узлов осуществляется из сосудов, представляющих собой ответвления терминальных отделов маточной артерии. Миоматозные узлы растут за счет пролиферации гладких мышечных клеток и фиброзной соединительной ткани, образуя псевдокансулу. Поэтому при ЦДК чаще видны сосуды, располагающиеся на периферии миоматозного узла. Расширенные сосуды, просматриваемые в наружной трети миоматозного узла, чаще всего представлены расширенными венами и артериями. Плотность расположения сосудов зависит от гистологического строения узла и от его локализации. Большее количество артерий отмечается но периферии узла, так как они являются продолжением аркуатных сосудов матки. В центральной части сосуды визуализируются в очень небольшом количестве. В этих случаях при морфологическом исследовании отмечаются некротические, дегенеративные и воспалительные изменения миоматозного узла [5, 16, 18-20].
Частота визуализации сосудов внутриопухолевого кровотока, но данным различных авторов, характеризуется большим разбросом (54-100%). Это обусловлено использованием различных доступов (трансвагинальное и трансабдоминальное сканирование). Установлено, что степень васкуляризации миоматозных узлов зависит не только от их размеров, но и от локализации [5,13,16,18-20].
По данным F. Aleem и М. Predanic [12], наиболее васкуляризованы субсерозные миоматозные узлы. При изучении показателей кровотока в этих узлах отмечены наиболее низкие численные значения индекса резистентности (ИР 0,43), что, по-видимому, зависит от крупного сечения артерии, проходящей через ножку субсерозного миоматозного узла. Интерстициальные и субмукозные миоматозные узлы характеризуются более высокой сосудистой резистентностью (ИР 0,59 и 50 соответственно).
Отмечается также снижение показателей сосудистой резистентности в маточных артериях и артериях неизмененного миометрия.
По данным S.E. Huang [17], внутриопухолевые значения пульсационного индекса пропорциональны размерам матки. Однако они не выявили зависимости показателей пульсационного индекса от клеточной пролиферации и ангиогенеза.
Принимая во внимание значительный разброс численных значений индекса резистентности в разных зонах миоматозного узла, авторы рекомендуют проводить регистрацию кривых скоростей внутриопухолевого кровотока как минимум в 3 участках узла. Измерения проводятся в подозрительных зонах узла (участки сниженной эхогенности, кистозные полости), которые, как правило, располагаются в центре узла опухоли [5, 16, 18, 19].
Карцинома эндометрия. Рак эндометрия является довольно частой патологией и занимает второе место среди всех злокачественных заболеваний женских половых органов. Статистические данные последних лет свидетельствуют о существенном увеличении заболеваемости раком эндометрия. В нашей стране она ежегодно увеличивается приблизительно на 6% [2].
Многочисленные исследования свидетельствуют о том, что основное внимание при диагностике рака эндометрия отводится определению толщины М-эха [10]. В менопаузе этот показатель, превышающий 5 мм, рассматривается как ведущий эхографический признак данной патологии, что требует комплексного обследования для уточнения диагноза (раздельное диагностическое выскабливание).
С точки зрения В.Н. Демидова [1, 2], наиболее характерными признаками рака эндометрия являются следующие:
— неоднородность внутренней структуры образования;
— неровность контуров;
— более высокая эхогенность но сравнению с мышцей матки;
— большие размеры образования, составляющие половину толщины матки или более;
— повышенная звукопроводимость;
— наличие жидкостных включений неправильной формы и различной величины;
— заметное увеличение размеров образований при динамическом наблюдении;
— отсутствие четкого изображения контуров матки вследствие перехода опухолевого процесса на смежные органы.
В настоящее время известно, что в большинстве случаев рак эндометрия возникает на фоне предраковых заболеваний. Г.М. Савельева и В.Н. Серов [7] наблюдали переход доброкачественных неопластических процессов в рак у 79% больных. К предраковым заболеваниям относят атипическую гиперплазию, аденоматозные полипы, железисто-кистозную гиперплазию в менопаузе (особенно рецидивирующую) или развивающуюся на фоне нейроэндокринных нарушений. Другие виды патологии эндометрия переходят в рак крайне редко.
Однако применение ЦДК с анализом кривых скоростей кровотока является более точным методом диагностики карциномы эндометрия, так как в подавляющем болыиинстве случаев заболевания отмечаются патологические кривые скорости кровотока, характерные для сосудов со сниженной резистентностью.
Однако более оправдано оценивать кривые скоростей кровотока в специфических сосудах (внутри- и периопухолевых). Пульсациоиный индекс является менее чувствительным критерием, чем индекс резистентности сосудов [20].
С. Ракиц и соавт. [6] провели проспективный анализ 64 случаев патологии эндометрия с использованием классической серой шкалы в сочетании с цветовым допплеровским картированием для диагностики рака эндометрия. Патологический кровоток, неоваскуляризация характеризовались присутствием «горячих точек» в эндометрии. «Горячие точки» заметно отличались от окружающих кровеносных сосудов. «Горячие точки» представляют собой последовательность вновь образованных хаотичных шунтов и альтернативных изменений в кровотоке. Индексы резистентности и пульсации измерялись в отдельных кровеносных сосудах, что позволило доказать отсутствие мышечной оболочки в стенке артериальных сосудов в бассейне неоваскуляризации. В случае патологии диастолический кровоток был ускорен, но индексы оставались низкими. Границы объемов для ИР 0,4 и ИП 1 в исследовании не отличались от общепринятых.
Л.Е. Терегулова [9], обследуя 218 пациенток с гистологически подтвержденным раком эндометрия, пришла к выводу, что ультразвуковое исследование позволяет определить степень развития рака эндометрия, глубину инвазии и распространенность процесса, так как с ростом аденокарциномы эндометрия вначале становятся доступными для регистрации венозные, а затем артериальные сосуды с характерным для злокачественных опухолей низким индексом резистентности: ИР
Ультразвуковая диагностика рака щитовидной железы
Опубликовано в журнале:
Визуализация в клинике »» N17, Декабрь 2000 DIAGNOSIS OF THYRIOD CANCER
E.Ю. Трофимова, H.Н. Волченко, З.Д. Гладунова, Н.Е. Шаматава
Trofirnova Ye.Yu., Volchenko N.N., Gladunova Z.D., Shamatava N.Ye.
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
Herzen Moscow Cancer Research Institute, Moscow
В обзоре приводятся данные о распространенности рака щитовидной железы. Рассматриваются алгоритмы скрининга, описываются различные инструментальные методы диагностики рака. Главное внимание уделено освещению значения, возможностей, ограничений ультразвукового исследования (УЗИ) как основного метода в силу его доступности, высокой информативности, чувствительности и специфичности в выявлении не только опухоли в самой щитовидной железе, но и пораженных регионарных лимфоузлов. Анализируются также сведения о значимости и диагностической роли изучения кровотока в опухолевых узлах с помощью ультразвукового допплеровского картирования. Существенный акцент делается на использовании тонкоигольной аспирационной пункции (ТАП) с цитологическим и гистологическим исследованием пунктатов, ее диагностических возможностях и преимуществе процедуры пунктирования под ультразвуковым контролем (ТАП-УЗИ). Авторы описывают также возникающие ошибки и их причины и возможные осложнения ТАП.
Ключевые слова: щитовидная железа, ультразвуковая диагностика, онкология, опухоли щитовидной железы, пункция щитовидной железы, тонкоигольная аспирационная пункция.
Key words: thyroid gland, ultrasound diagnosis, oncology, tumors of thyroid gland, thyroid puncture, fine-needle aspiration puncture.
Злокачественные опухоли щитовидной железы составили в 1998 году 1,47% в общей структуре онкологической заболеваемости. Эпидемиологи и клиницисты наблюдают увеличение заболеваемости раком щитовидной железы и последние годы [27].
После аварии на Чернобыльской АЭС рак щитовидной железы становится социальной проблемой. При обследовании популяции в зонах, пострадавших от радиации, среди заболеваний на первое место выходят злокачественные новообразования. Отмечено, что рост заболеваний щитовидной железы, а также ее ракового поражения, тем выше, чем больше радиоактивное загрязнение [15, 16, 28].
Для клинициста, по мнению Hopkins C.R. и Reading С.С. [47], диагностическая линия включает осмотр, лабораторные анализы, УЗИ и тонкоигольную аспирационную пункцию под контролем УЗИ (ТАП-УЗИ).
Клиническая диагностика опухолей щитовидной железы основана на изучении отдельных симптомов и их совокупности, проявляющихся в процессе развития новообразования, и включает сбор анамнеза, осмотр и пальпацию. Из-за отсутствия четких патогномоничных признаков клиническая диагностика может представлять значительные трудности при распознавании отдельных образований [13, 19].
Трудности возникают при выявлении собственно узла, уточнении морфологической формы опухоли, оценке распространенности опухолевого процесса при раке щитовидной железы. Быстрый рост опухоли и наличие плотного бугристого узлового образования с ограничением подвижности позволяют заподозрить злокачественную опухоль [7, 19]. Одной из самых важных и сложных проблем является диагностика ранних форм рака щитовидной железы [5, 19].
Расширение возможностей визуализации щитовидной железы улучшило наше понимание ее заболеваний. Для исследования щитовидной железы используют радионуклидную диагностику (РНД), магнитно-резонансную томографию (МРТ), компьютерную томографию (КТ) [7, 48].
Некоторое время тому назад считали, что выявление «горячего» узла при проведении РНД исключает наличие рака. Но в дальнейшем было установлено, что это не совсем так. «Холодные» узлы могли оказаться и доброкачественными, и злокачественными [41]. По данным Simonin R. et аl. [63], 11,5% «горячих» узлов у взрослых оказались злокачественными. Brendel A.J. [33] отметил низкую эффективность РНД в выявлении медуллярного рака щитовидной железы.
КТ и МРТ не получили широкого распространения в диагностике рака щитовидной железы из-за высокой стоимости и технической сложности исследования [7].
В настоящее время УЗИ заняло ведущее место как самостоятельный метод первичной диагностики заболеваний щитовидной железы. Методика осмотра самой щитовидной железы разработана и описана достаточно хорошо [4, 11].
При описании узла оценивают границы, форму, контур (четкий, нечеткий, размытый, фестончатый, не определяется), структуру (однородная или неоднородная, гипо-, гипер-, изоэхогенная), учитывают наличие ободка и дорсального усиления эхосигнала [4, 11, 18, 22].
Особую онкологическую настороженность вызывают гипоэхогенные узлы с гетерогенной структурой, неровными и нечеткими котурами [16, 17, 22].
По мнению М.М. Абдулхалимовой с соавт. [1], П.С. Ветшева с соавт. [4] и Messina G. et аl. [57], ультразвуковая картина злокачественной опухоли может быть различной: структура узла может быть гипоэхогенной солидной, изоэхогенной солидной, гиперэхогенной солидной, смешанной и кистозной. Messina G. et аl. [57] считают, что гипоэхогенная солидная структура узла не патогномонична, но подозрительна в отношении рака, особенно при изолированном узле у мужчин и при продолжающемся росте опухоли на фоне проведения подавляющей терапии. Раковый узел в 60-70% случаев имеет гипоэхогенную структуру. Гиперэхогенная структура выявляется лишь в 2-4% узлов; 15-25% опухолей оказываются изоэхогенными; редка и смешанная структура опухоли (5-10%) [57]. По данным Meko J.B. и Norton J.A. [56], наиболее вероятно злокачественное поражение выявляют в узлах размерами более 3 см с кистозно-солидной структурой или солидно-кистозных. В случае рака внешние границы опухоли четко не определяются, встречаются анэхогенные участки, представляющие собой полости распада, и микрокальцинаты [1, 4, 18, 22]. По мнению Okour К.I. [59], злокачественный узел обычно бывает гипоэхогенным (53,7%), имеет неровный контур (58%) и слабо очерчен (62%), по структуре является солидным (88,4%) и содержит жидкостные включения.
По данным Kumar А. et аl. [52], А.П. Припачкиной [17] и М.М. Абдулхалимовой с соавт. [1], в ультразвуковой картине нет специфических патогномоничных для рака щитовидной железы признаков, но метод УЗИ позволяет выявить непальпируемые узлы злокачественной опухоли в щитовидной железе у 20,6% больных.
Чувствительность УЗИ в выявлении рака щитовидной железы различна; она зависит от размера опухоли, характера изменений ткани щитовидной железы, опыта исследователя. О сложности диагностики рака на фоне аденом, многоузлового зоба и аутоимунного тиреоидита пишут многие исследователи [17, 30, 57]. Наличие многоузлового зоба снижает чувствительность предоперационного УЗИ в диагностике узловых образований с 90% до 64% [44].
В нашей стране сохраняется рост числа пациентов с диагнозом, подтвержденным при морфологическом исследовании [26, 27]. Результативность пункционной биопсии щитовидной железы, по данным разных авторов, может достигать 78,2-95%) [34, 35, 38].
По мнению Gimondo P. et al. [43], ТАП-УЗИ позволяет уточнить необходимый в каждом конкретном случае тип хирургического вмешательства. Использование этого метода уменьшило число тиреоидэктомий с 19,2% до 8,5%, поскольку диагноз был уточнен до операции. По данным Takashima S. et al. [65], ТАП-УЗИ позволило уточнить стадию у 90% больных, отобрать пациентов, которым действительно показана операция, и избежать ненужного оперативного вмешательства у ряда больных.
Применение тонкоигольной пункционной биопсии под визуальным контролем позволило пунктировать и непальпируемые образования размерами от 3-4 мм. Метод прост, практически не имеет противопоказаний и может быть выполнен в амбулаторных условиях [24, 35, 59].
Цитологическое исследование пунктата является наиболее быстрым морфологическим методом дооперационной диагностики. Его чувствительность в диагностике онкологических заболеваний высока. Ответ может быть получен в зависимости от используемых красителей и методики окраски уже через 5-60 мин [23].
Главным условием успешной цитологической диагностики при патологии щитовидной железы является правильно выполненная пункция, когда в цитологических препаратах имеется достаточное количество клеток, что позволяет делать уверенное цитологическое заключение. Однако в препаратах, полученных без визуального контроля, клеточный материал отсутствует чаще, чем при ТАП-УЗИ (табл. 1).
Таблица 1. Частота отсутствия клеточного материала в пунктатах при выполнении ТАП-УЗИ и ТАП без визуального контроля (%)
Результативность цитологического заключени при пункции щитовидной железы, по данным разных авторов, колеблется в пределах 58,2-70% [19].
При ТАП щитовидной железы чувствительность цитологического исследования полученного материала составляет 94-95% при специфичности 90% и точности 94% [30, 62, 69] (табл. 2).
Таблица 2. Чувствительность тонкоигольной аспирационной пункции под контролем УЗИ (%)
| Авторы, год | Чувствительность | Специфичность | Точность |
| Brom Ferral R. et al., 1993 | 95 | 100 | — |
| Carmeci С. et al., 1998 | 100 | 100 | — |
| Cochand Priollet B. et al., 1997 | 95 | 87,7 | 89 |
| Horvath F. et al., 1993 | 80 | 93 | 92 |
| Kumar A. et al., 1992 | 98,5 | — | — |
| Sanchez R.B. et al., 1994 | 78 | — | — |
По данным В.О. Ольшанского и соавт. [14], цитoлогическое исследование пунктата из опухоли позволило верифицировать диагноз злокачественной опухоли у 91,1% больных.
Holm Н.Н. et al. [46] считают, что при пункции щитовидной железы частота неуверенного заключения на основании данных цитологического исследования достигает 33%. Почти половина из пунктированных узлов, признанных при цитологическом исследовании доброкачественными, оказалась злокачественными (18% солидных узлов и 27% кистозных).
Garib Н. et al. [42] сообщили о том, что при ТАП у 20% больных было получено цитологическое заключение, подразумевающее дифференциальный диагноз между различными патологическими процессами, при этом у 20% из этих пациентов на операции выявлен злокачественный процесс.
Takashima S. et al. [65] отметили, что при ТАП без визуального контроля диагностические ошибки возникают чаще (19,5%), чем при выполнении ТАП-УЗИ (0,04%).
При выполнении ТАП-УЗИ число ложноотрицательных заключений колеблется от 0,5 до 7,6% [34, 52]. При ТАП больших кистозно-солидных узлов щитовидной железы возрастает возможность ложноотрицательного ответа. По данным Meko J.B. и Norton J.А. [56], общее число ошибок при ТАП достигало 11%. ТАП больших (более 3 см), а также гетерогенных кистозно-солидных или больших солидных узлов дала ложноотрицательный результат в 17%, 25% и 30% случаев соответственно по сравнению с 0%, 9% и 17% при пункции мелких узлов (менее 3 см), мелких кистозно-солидных и солидных опухолей размерами менее 3 см соответственно. Meko J.В. и Norton J.А. [56] рекомендуют проводить оперативное лечение больным с большими солидно-кистозными узлами из-за большого числа ложноотрицательных результатов при ТАП.
Некоторые исследователи проводят трепан-биопсию, как более точное исследование (чувствительность до 90% и специфичность до 84,6%), но этот метод представляется излишне травматичным для щитовидной железы [19].
Анализ осложнений, возникающих после ТАП-УЗИ, показал, что при нем риск развития серьезных осложнений значительно ниже, чем после пункций без такого контроля [19, 23, 46]. Осложнения при выполнении ТАП-УЗИ встречаются редко; описаны гематомы, возникновение кратковременных болевых ощущений, воспалительные явления [23, 46, 65]. По данным Brom Ferral R. et al. [34], подобные осложнения возникают у 12% больных.
В щитовидной железе часто выявляются множественные узловые образования, в связи с чем возникает вопрос о необходимости пункции каждого конкретного узла [14, 20, 57]. Многие считают, что все выявленные узлы должны быть пунктированы [20].
Поскольку очагов опухолевого роста в щитовидной железе может быть много, решение о возможности выполнения органосохраняющей операции должно базироваться на точных данных о распространенности опухолевого процесса и его характере [14]. По данным Price R. et al. [60], у 25,9% больных выявляется рак контралатеральной доли щитовидной железы, о котором в 80% случаев до операции не подозревали. Было отмечено, что если больным проводили УЗИ до операции, то вновь выявляемые во время операции узлы контралатеральной доли не достигали и 5 мм, а у не обследованных с использованием УЗИ пациентов размер недиагностированных узлов достигал 15 мм [60].
В.А. Колосюк [8] всесторонне проанализировал течение первично-множественных опухолей у больных раком щитовидной железы за 20 лет. У этих больных были выявлены синхронные и метахронные доброкачественные заболевания щитовидной железы (узловой эутиреоидный зоб, токсический зоб, аутоимунный тиреоидит), а также сочетание доброкачественных заболеваний щитовидной железы с доброкачественными опухолями других локализаций.
Lagalla R. et al. [53] и Messina G. et al. [57] выделяют 4 типа васкуляризации. В 90,1% гиперфункционирующих автономных аденом ими выявлен сосудистый рисунок в узле, как и во всех случаях рака щитовидной железы. По данным Messina G. et al, [57], 90% узлов рака щитовидной железы являются васкуляризированными, что обнаружено при ультразвуковой допплерографии (УЗДГ). Lagalla R. et al. [53] считают, что уже на основании наличия сосудистого рисунка в узле можно заподозрить рак щитовидной железы и рекомендуют пунктировать (ТАП) только те узлы, в которых обнаружен сосудистый рисунок.
Erdem S. et al. [41] считают, что в выявлении злокачественных узлов УЗДГ имеет ограниченное значение, a Hubsch R et al. [49] полагают, что УЗДГ не помогает в диагностике рака щитовидной железы. Тем нe менее большинство авторов [1, 24, 53] убеждены, что УЗДГ имеет большое значение в выявлении патологии щитовидной железы и при дифференциальном диагнозе, особенно при обнаружении внутри узла извитых, ветвящихся сосудов, что характерно для рака.
По мнению Argalia С. et аl. [31], Castagnone D. et al. [36] а также Rommel О. и Tegcnthoff M. [61], УЗДГ имеет значение для оценки васкуляризации железы, но не имеет значения в дифференциальной диагностике узлов в ней.
По данным разных авторов, чувствительность УЗДГ в выявлении рака щитовидной железы колеблется от 16 и до 100% по самым оптимистичным оценкам [49, 68]. Тем не менее описаны узлы рака щитовидной железы, в которых при УЗДГ сосуды не определялись. При этом выявление сосудов в опухоли напрямую зависело от размера узла.
Многие считают, что определение параметров ЦДК не имеет существенного значения в дифференциальной диагностике опухолей щитовидной железы [22, 31, 49]. Li J. et al. [54] выявили ускорение максимальной систолической скорости (МСС) и снижение индекса резистентности (ИР) в верхней щитовидной артерии при раке щитовидной железы. Уровень кровотока в верхней щитовидной артерии у этих пациентов был в 8-10 раз выше, чем у здоровых.
Оценка показателей ЦДК при патологии щитовидной железы с единственным узлом показала, что первичные или вторичные злокачественные опухоли всегда хорошо васкуляризированы с широким разбросом показателей ЦДК, а МСС в узле не достигала 0,50 м/с при ИР более 0,75. Эти исследования подтвердили, что количественные показатели ЦДК не имеют самостоятельного значения в диагностике рака щитовидной железы, но способствуют отбору больных для проведения ТАП-УЗИ [31].
По данным В.П. Харченко и соавт. [24], в злокачественных новообразованиях МСС ниже, чем в аденомах, и составляет в среднем 0,39+/-0,11 м/с. Авторы считают, что даже при использовании УЗДГ с оценкой показателей ЦДК остаются трудности в проведении дифференциального диагноза между злокачественной опухолью и доброкачественными гиперваскулярными образованиями.
На субъективность в оценке изменений, выявленных при УЗДГ, и измерении показателей ЦДК указали Delorme S. et al. [39], отметив, что это может влиять на результат исследования и ведет к ошибочным заключениям.
Ошибки диагностики на дооперационном этапе приводят к необходимости выполнения реопераций на шее. В настоящее время у большого числа больных раком щитовидной железы приходится выполнять повторные операции. Сначала больных оперируют в учреждениях общей лечебной сети с предполагаемым диагнозом доброкачественного образования, а затем, после получения планового гистологического заключения, пациент попадает в онкологическое учреждение [12, 26]. По мнению С.В. Яйцева [29], неадекватно выполненные хирургические вмешательства обуславливают необходимость реоперации, так как в 38,8% случаев в оставшейся части щитовидной железы в отдаленные сроки обнаруживается опухоль. Рецидивы после неадекватных операций возникают у 17-28% больных. При реоперациях в 5 раз возрастает риск повреждения возвратного нерва и развития паратиреоидной недостаточности [12, 26].
Одним из основных параметров, определяющих прогноз онкологического заболевания, является степень распространенности опухолевого процесса на момент диагностики [26]. По мнению Snow G.В. et al. [64], состояние лимфатических узлов шеи является наиболее важным прогностическим фактором у больных раком щитовидной железы. Ультразвуковой метод имеет большое значение в обнаружении поражения регионарных лимфатических узлов, особенно в паратрахеальных зонах [12, 22, 67]. ТАП-УЗИ выявленных изменений позволяет уточнить характер поражения [23].
Известно, что лимфоотток из щитовидной железы осуществляется в глубокие шейные, паратрахеальные лимфатические узлы и в лимфатические узлы средостения. Регионарные метастазы в лимфатические узлы хорошо описаны, в большинствe своем они имеют типичную ультразвуковую картину; в них часто обнаруживаются мелкие гиперэхогенные включения. Специфичность УЗИ в выявлении и дифференциальной диагностике поражения лимфатических узлов колеблется от 30 до 100% во многом зависит от качества аппаратуры и опыта исследователя [4, 6, 22]. УЗИ позволяет обнаружить даже непальпируемые метастазы в лимфатические узлы шеи [17].
Choi М.Y. et al. [37] считают, что при оценке показателей ЦДК следует акцентировать внимание на достоверном различии МДС в лимфатическом узле при проведении дифференциального диагноза между метастатическим поражением лимфатического узла и его гиперплазией. Авторы полагают, что УЗДГ позволяет с высокой степенью достоверности различать доброкачественные и метастатически измененные лимфатические узлы. Между тем, они обращают внимание на то, что высокие значения показателей ЦДК в лимфатическом узле встречаются иногда и при гиперплазии лимфоидной ткани. Компьютерный анализ ультразвуковых признаков метастатически измененного лимфатического узла при исследовании в режиме серой шкалы и при УЗДГ показал, что в 82% лимфатических узлов можно провести дифференциальный диагноз между разными патологическими состояниями с чувствительностью в 84% и специфичностью в 80%. По мнению В.Р. Антонив с соавт. [2] и Choi М.Y. et аl. [37], 72% лимфатических узлов по ультразвуковой картине могут быть отнесены к трем группам (реактивное состояние, метастаз и злокачественная лимфома).
По мнению Noguchi Masakuni et al. [58], в настоящее время отсутствуют УЗ-критерии, позволяющие провести достоверную дифференциальную ультразвуковую диагностику между метастатическим поражением и гиперплазией лимфатического узла. Авторы рекомендуют осуществлять пункцию всех выявленных увеличенных лимфатических узлов. В ходе предоперационной диагностики они советуют производить УЗИ зон регионарного лимфооттока по ходу кивательных мышц с обеих сторон даже при выявлении узла в одной из долей щитовидной железы, поскольку считают, что у 24% больных выявляется метастатическое поражение контралатеральных лимфатических узлов [58].
Остается ряд трудностей как при первичной, так и уточняющей диагностике заболеваний щитовидной железы, даже при использовании УЗДГ и пункции под визуальным контролем. В то же время расширение показаний к функционально-щадящим операциям на шее требует высокой диагностической точности для определения лечебной тактики.
Перспективным является использование интраоперационного УЗИ у больных раком щитовидной железы. Оно позволяет провести осмотр после удаления железы (или ее части) и лимфоаденоэктомии, что снижает риск выполнения нерадикальной операции [67].
Таким образом, УЗИ, даже с использованием УЗДГ, не позволяет выявить рак щитовидной железы во всех случаях. Заключение на основе выполненных ТАП или ТАП-УЗИ также в ряде случаев недостоверно из-за ошибок забора материала или цитолога. Поэтому при увеличении размеров опухоли, особенно при одновременном изменении ее ультразвуковой структуры и выявлении микрокальцинатов, требуется взвешенный подход к проведению консервативной терапии, а при выполнении оперативного вмешательства необходимо срочное морфологическое исследование, которое может повлечь расширение объема операции.
Л.Е. Денисов и В.Л. Липин [5] рекомендуют осуществлять УЗИ для выявления рака щитовидной железы 1 раз в 2 года. По их мнению, это позволяет повысить выявляемость рака щитовидной железы I-II стадии с 67,8 до 80%.