Гинекологический мазок «на флору»: на что смотреть, и как понять
Большинству женщин мазок «на флору» знаком, как самый «простой» гинекологический анализ. Однако исследование куда «полезнее», чем может казаться. И всего несколько (а то и одно) отклонений способны подсветить значимые проблемы, еще до появления каких-либо симптомов. Так как же понять полученные результаты? Рассказываем по пунктам.
1. Эпителий
Как известно, любой живой объект в природе имеет ограниченный срок жизни, по истечении которого он погибает «от старости».
Эпителий в гинекологическом мазке – это и есть слущенные «старые» клетки слизистой оболочки влагалища, цервикального или уретры (в зависимости от оцениваемого локуса). Которые могут присутствовать в материале в умеренных количествах.
Превышение нормативных пределов («много» или «обильно») может указывать на:
Уменьшение или отсутствие эпителия в мазке – на атрофические изменения, недостаток эстрадиола или избыток андрогенов.
Кроме того, ввиду зависимости эпителия от уровня половых гормонов, его количество в материале может сильно меняться в зависимости от дня цикла, начиная с единичного «в поле зрения» в самом начале – до умеренного и даже большого количества ближе к овуляции и во время нее.
А появление в мазке так называемых «ключевых клеток» (эпителий, «облепленный» мелкими кокковыми бактериями) – является маркером бактериального вагиноза.
2. Лейкоциты
«Норма» лейкоцитов в мазке также сильно зависит от стадии цикла и уровня половых гормонов, а также исследуемого локуса.
Так, за «максимум» для:
Повышение показателя – очевидно, свидетельствует о воспалении, а полное отсутствие может иметь место в норме в самом начале цикла.
Слизь
Результат «отсутствует», «мало» или «умеренно» для этого показателя является нормой, что тоже связано с индивидуальными особенностями гормонального фона и циклом.
А вот «много» слизи в мазке – может свидетельствовать о том, что мазок взят в середине цикла, дисбиотических изменениях или избытке эстрогенов. Поэтому требует внимания специалиста или, как минимум, контроля в динамике.
Флора
Преобладающей флорой женских половых путей в норме у женщин репродуктивного возраста, как известно, являются лактобактерии (или палочки Дедерлейна). Количество которых может быть от умеренного до обильного, в том зависимости, в том числе, от фазы менструального цикла.
Патологические элементы
Присутствия мицелия грибов, трихомонад, диплококков (в том числе и возбудитель гонореи), лептотрикса, мобилункуса и прочих патогенных микроорганизмов в нормальном мазке не допускается, даже в минимальном количестве. А их выявление – серьезный повод незамедлительно обратиться за лечением.
Гистиоцитоз Х – это системное заболевание, характеризующееся образованием специфических клеточных гранулем в различных органах и тканях. Наиболее типичные клинические проявления включают кожные высыпания, кашель, односторонний экзофтальм. Также наблюдаются выпадение зубов, увеличение периферических лимфатических узлов, признаки несахарного диабета (полиурия, полидипсия). Диагноз верифицируется путем гистологического исследования кожи, легких или лимфатических узлов. В качестве лечения применяются противовоспалительные препараты (глюкокортикостероиды), химиотерапевтические средства. В случае выраженного поражения легких производится трансплантация органа.
МКБ-10
Общие сведения
Гистиоцитоз Х (гистиоцитоз из клеток Лангерганса, легочная эозинофильная гранулема) – системная патология, при которой происходит активная пролиферация клеток Лангерганса в тканях легких, костей, центральной нервной системы, ретикуло-эндотелиальной системы (в печени, селезенке, лимфатических узлах). Течение заболевания варьирует в зависимости от формы и может быть доброкачественным со спонтанной ремиссией или быстропрогрессирующим с высокой вероятностью летального исхода. Распространенность гистиоцитоза составляет 5 на 1 000 000 человек. Преимущественно страдают дети, подростки, взрослые в возрасте 20-30 лет. Гистиоцитоз встречается только у представителей белой расы, чаще у мужчин (соотношение с женщинами 2:1).
Причины
На сегодняшний день точная причина гистиоцитоза неизвестна. Предполагается роль иммунной аутоагрессии, вызванной инфицированием вируса герпеса 6-го типа. До сих пор ведутся научные дебаты о наследственной природе заболевания. У 50% пациентов в патологических клетках Лангерганса была обнаружена соматическая мутация гена V600E, кодирующего внутриклеточный сигнальный белок BRAF. Табакокурение рассматривается как один из основных факторов риска (более 90% больных являются курильщиками). Подтверждением этого служит тот факт, что симптоматика уменьшается после прекращения курения даже без применения какого-либо лечения.
Патогенез
Механизм развития гистиоцитоза изучен недостаточно. Основным звеном патогенеза считается накопление в тканях дендритных клеток (клеток Лангерганса, или гистиоцитов). Дендритные клетки синтезируются в костном мозге и мигрируют в дерму, паренхиму легких, ретикулоэндотелиальную систему и т.д. Их основная функция заключается в поглощении антигенов, поступающих из окружающей среды, и презентации Т и В-лимфоцитам для формирования иммунного ответа. После контакта с гистиоцитами лимфоциты начинают выделять провоспалительные цитокины и медиаторы, повышающие активность гистиоцитов и придающие им высокую подвижность.
При гистиоцитозе по неизвестным причинам у дендритных клеток нарушается процесс апоптоза (запрограммированной клеточной гибели). В сочетании с выделяемыми лимфоцитами факторами роста это приводит к их интенсивной пролиферации с последующим слиянием с эозинофилами. В результате образуются гигантоклеточные гранулемы, которые постепенно начинают замещать нормально функционирующую ткань того или иного органа. Присутствие большого количества Т-лимфоцитов в гранулемах позволяет предположить наличие специфического антигена.
Классификация
По локализации очагов выделяют моносистемную форму с единичным или множественным поражением одной анатомической области и мультисистемную форму с признаками нарушения функции органов или без них. Традиционно различают следующие клинические формы:
Симптомы гистиоцитоза
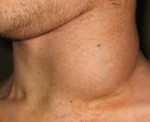
Клиническая картина крайне разнообразна. Заболевание начинается с появления общей слабости, повышения температуры тела, которая в основном бывает субфебрильной, но может достигать 40°С. Возможны диспепсические нарушения – тошнота, рвота, диарея. Кожа покрывается зудящими очагами гиперемии с чешуйками или корочками. Иногда наблюдаются геморрагические элементы, длительно незаживающие язвы. Высыпания присутствуют на коже головы, наружного слухового прохода, в области естественных складок (паховой, подмышечной). Увеличиваются лимфатические узлы по всему телу.
Возникает одышка, упорный сухой кашель и боли в грудной клетке. Затруднение дыхания может беспокоить только во время физической нагрузки или присутствовать даже в покое. Присоединяются тупые боли или тяжесть в правом подреберье из-за увеличения печени (гепатомегалии). При выраженном поражении печени кожа приобретает желтушный оттенок. Увеличение селезенки сопровождается болью в левом подреберье. Некоторые пациенты испытывают боль в костях. Деструкция костей глазницы ведет к образованию экзофтальма, чаще одностороннего. Боль в ухе ошибочно диагностируется как бактериальный или грибковый отит и безуспешно лечится антибактериальными и противогрибковыми препаратами. Остеолизис нижней челюсти приводит к периодонтитам и выпадению зубов.
При длительном течении гистиоцитоза больной начинает терять вес. В тяжелых случаях встречаются признаки костномозговой недостаточности – анемический синдром (бледность кожи, головокружение, учащенное сердцебиение), склонность к кровотечениям, сниженная сопротивляемость к инфекциям. Формирование гистиоцитарных гранулем в задней доле гипофиза вызывает угнетение выработки антидиуретического гормона. В результате развивается симптоматика несахарного диабета – сухость во рту, постоянная жажда (полидипсия) и повышенное мочеотделение (полиурия).
Осложнения
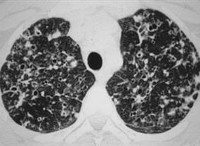
Широкая вариативность клинической картины при гистиоцитозе обусловливает разнообразие осложнений. Наиболее характерными считаются патологические переломы костей, особенно компрессионный перелом позвоночника. Типичные осложнения со стороны легких – легочная артериальная гипертензия вследствие диффузного фиброза легочной ткани, спонтанный пневмоторакс из-за разрыва тонкостенных булл. Массивная инфильтрация печени вызывает цирроз с печеночно-клеточной недостаточностью. К редким осложнениям относятся неблагоприятные последствия дефицита антидиуретического гормона (несахарного диабета) в виде гиперосмолярной гипогидратации, проявляющейся двигательным беспокойством, мышечными судорогами, нарушением сознания, вплоть до глубокой комы.
Диагностика
Пациентами с гистиоцитозом занимаются различные врачи – гематологи, пульмонологи, педиатры. Профиль специальности зависит от возраста больного и преимущественно пораженного органа. При общем осмотре отмечаются цианоз (синюшность) губ, участие в дыхании вспомогательной мускулатуры (при дыхательной недостаточности). При аускультации легких выслушивается жесткое дыхание, сухие хрипы по всем легочным полям. Дополнительное обследование включает:
Дифференциальный ряд включает большое количество нозологий и зависит от клинических симптомов гистиоцитоза. Кожные высыпания нужно дифференцировать с экземой, псориазом, атопическим дерматитом. Поражение легких следует отличать от туберкулеза, саркоидоза, лимфогранулематоза. Генерализованный гистиоцитоз дифференцируют с гематологическими заболеваниями (гемофагоцитарный синдром, острый лейкоз). Очаги деструкции костей требуют исключения гиперпаратиреоза, множественной миеломы, остеомиелита.
Лечение гистиоцитоза
Пациенты обязательно должны быть госпитализированы в стационар. При тяжелой дыхательной недостаточности показаны ингаляции кислорода или перевод на искусственную вентиляцию легких. При наличии признаков костномозговой недостаточности прибегают к переливанию компонентов крови и применению гранулоцитарного колониестимулирующего фактора.
Этиотропной терапии гистиоцитоза Х не существует. Наиболее важный этап в лечении – отказ от курения. Прекращение курения вызывает улучшение клинической, лабораторной, рентгенологической картины. В качестве патогенетической терапии используют глюкокортикостероиды (преднизолон, метилпреднизолон), химиотерапевтические средства (винбластин, меркаптопурин, этопозид).
Для лечения несахарного диабета назначается заместительная гормональная терапия аналогами вазопрессина (десмопрессин) в виде интраназального спрея или в таблетированной форме. При небольших остеолитических очагах выполняют кюретаж, при выраженной инфильтрации костей – резекцию или дистанционную гамма-терапию. При массивном деструктивном процессе в легочной ткани проводится трансплантация легких.
Прогноз и профилактика
Гистиоцитоз Х. Причины, симптомы и лечение
1. Общие сведения
Гистиоцитами называются блуждающие клетки рыхлой соединительной ткани, которые при определенных условиях (раздражение, воспаление) активизируются и выполняют функции иммунных макрофагов – «пожирателей» чужеродных клеток, микроорганизмов и вредоносных частиц. Гистиоциты называют также Х-клетками или клетками Лангерганса. Отсюда происходят синонимические названия заболевания, о котором речь пойдет ниже: гистиоцитоз Х, лангергансоклеточный гистиоцитоз, легочный гранулематоз X и т.п. Суть патологического процесса заключается в аномально интенсивном производстве гистиоцитов и пролиферации (разрастании) состоящих из них образований – гистиоцитарных гранулем.
Фактически, во внутренних структурах организма, никогда не подвергавшихся травматизации, образуются множественные рубцы, – подобные тем, которые затягивают тканевые дефекты после ранений, ожогов или гнойных воспалений. Такие Х-клеточные гранулемы развиваются преимущественно в костных структурах и легочной паренхиме, хотя могут быть обнаружены и в других тканях.
Гистиоцитоз Х относится к редким заболеваниям. Эпидемиологические оценки существенно расходятся – от 1,5 до 5 случаев на 1 миллион человек в общей популяции. Нет также достоверных сведений о зависимости заболеваемости от пола: в одних источниках говорится о равном риске для мужчин и женщин, в других сообщается о 24кратном преобладании мужчин – что, возможно, объясняется большей распространенностью главного фактора риска (см.ниже) среди представителей мужского пола.
2. Причины
Этиопатогенез лангергансоклеточного гистиоцитоза остается практически не изученным. Выдвигаются различные гипотезы (онкологическая, гематологическая, аутоиммунная и т.д.), однако ни одна из них пока не получила достаточно убедительного подтверждения.
Наиболее значимым фактором риска является табакокурение; известно, в частности, что практически любое лечение, – даже трансплантация легкого, – малоэффективно в тех случаях, когда пациент не отказывается от этой зависимости.
Кроме того, по неизвестным пока причинам заболевание (по крайней мере, некоторые его формы) зачастую манифестирует в раннем детском, подростковом или молодом возрасте. Логично предположить, что и в этих случаях провоцирующую, если не патогенетическую роль играет пассивное курение.
Неопределенность этиологии заболевания в сочетании с его редкостью приводят к разноголосице в трактовках. Так, в литературе встречается деление гистиоцитоза на три основные формы (см.ниже), реже на две; некоторые источники интерпретируют диагноз как собирательный, объединяющий группу разнородных по сути процессов.
В целом, необходимы дальнейшие глубокие исследования, – клинические, лабораторные и медико-статистические, – для установления истинных причин и механизмов развития гистиоцитоза Х.
3. Симптомы и диагностика
Как указано выше, большинство авторов различает три основные формы лангергансоклеточного гистиоцитоза.
Первично-острая (диссеминированная) форма, или болезнь Абта-Леттерера-Сиве. Встречается преимущественно у детей первых двух лет жизни. Развивается и протекает, по определению, остро, с одновременным поражением множества органов (печень, кожа, кости, слизистые, селезенка, органы слуха и т.д.). В легких формируются гистиоцитарные кисты и более крупные буллы, спонтанный прорыв которых приводит к повторным пневмотораксам. Отмечается общая слабость, лихорадочное состояние, анемия, прогрессирующая дыхательная и сердечная недостаточность. В совокупности данные клинические проявления обусловливают высокую летальность (по разным оценкам, от 60% до 100%).
Первично-хроническая (доброкачественная) форма, или болезнь Хенда-Шюллера-Крисчена. Проявляется клиникой несахарного диабета, поражением черепных костных структур, экзофтальмом. Нередко вследствие присоединившегося воспаления среднего уха развивается глухота. Увеличиваются печень, селезенка, лимфатические узлы. В некоторых случаях в процесс вовлекаются десны; примерно у трети больных поражаются легкие, однако встречаются случаи и изолированного легочного гистиоцитоза. Среди заболевающих преобладают дети дошкольного возраста, реже болезнь манифестирует среди подростков и молодых людей. Летальность оценивается на уровне 20-40%.
Локальная эозинофильная гранулема, легочный гистиоцитоз Х, в отечественной литературе – болезнь Таратынова. Процесс развивается, в основном, в костных структурах, как плоских, так и трубчатых. Легкие поражаются лишь в каждом пятом случае, хотя встречается, действительно, изолированное их поражение. Реже отмечается гепатоспленомегалия, увеличение лимфоузлов, кожные высыпания, симптоматика несахарного диабета. Данная форма развивается преимущественно в молодом возрасте или у взрослых. Иногда регистрируется бессимптомное течение и спонтанное излечение. Летальность до 2%.
Таким образом, общими признаками различных форм гистиоцитоза Х выступают образование гранулем в костных и легочных тканях, печени и других органах. Как следствие – сердечно-легочная недостаточность, слабость, лихорадка; при длительном течении – характерная деформация пальцевых фаланг и ногтевых пластин по типу, соотв., барабанных палочек и часовых стекол, деформация костей черепа, односторонний или двусторонний экзофтальм, гепатоспленомегалия, анемия.
Особо следует отметить такие симптомы легочного гистиоцитоза Х, как одышка, непродуктивный (сухой) кашель, боли в грудной клетке, спонтанный пневмоторакс.
Нередко гистиоцитоз Х выявляется случайно, на бессимптомной стадии, при флюорографическом исследовании, – и вызывает значительные диагностические сомнения. Как правило, больного направляют на КТ, МРТ, рентгенографию, бронхоскопию, бронхоальвеолярный лаваж («смыв» содержимого бронхов с последующим лабораторным анализом), исследования крови и мочи.
В ряде источников рекомендуется наиболее надежным способом подтверждения и уточнения диагноза считать биопсию и гистологический анализ образца.
4. Лечение
Поскольку терапевтические мишени до настоящего времени в точности не определены, все применяемые методы лечения являются эмпирическими паллиативами. Как правило, назначают глюкокортикостероидные препараты, цитостатики. При прогрессирующей дыхательной недостаточности показана пересадка легкого, однако такая операция весьма проблематична по ряду причин. Прогноз резко ухудшается в случаях, когда пациент продолжает курить, – прежде всего, из-за высокой вероятности малигнизации (озлокачествления). В противном случае пятилетняя выживаемость, согласно литературным данным, составляет порядка 75%.
Что такое гистиоциты в гинекологии
Клетки гистиоцитарного ряда, составляющие морфологический субстрат гистиоцитозов, включают два основных типа клеток, имеющих общее происхождение и функционально подразделяющихся на две большие группы:
1) антигенперерабатывающие гистиоциты — ординарные макрофаги;
2) антигенпрезентирующие гистиоциты — дендритические клетки.
Клетки 1-й группы имеют костно-мозговое происхождение, берут свое начало от общего с гранулоцитами предшественника и проходят все стадии созревания на уровне костного мозга. В эту группу входят также моноциты крови и все популяции тканевых макрофагов. К последним в зависимости от локализации относятся плевральные, перитонеальные и альвеолярные макрофаги, купферовские клетки печени, мезангиальные клетки почек, микроглиальные клетки головного мозга и т. д.
Морфология этих клеток весьма неоднородна, что обусловлено их адаптацией к различным функциям соответствующих органов. Иммунологическая функция макрофагов заключается в процессинге антигенов, запуске и координации ранних этапов иммунного ответа, а также в осуществлении ряда эффекторных функций.
Вторая группа клеток — это популяция дендритических клеток (ДК), основная роль которых — презентация антигенов Т-лимфоцитам. Клетки 2-й группы играют ключевую роль в запуске первичного иммунного ответа и формировании иммунологической толерантности. К группе дендритных клеток (ДК) относятся клетки Лангерганса, интерстициальные дендритные клетки, интердигитальные клетки и тимические дендритные клетки. Дендритические клетки имеют костно-мозговое происхождение.
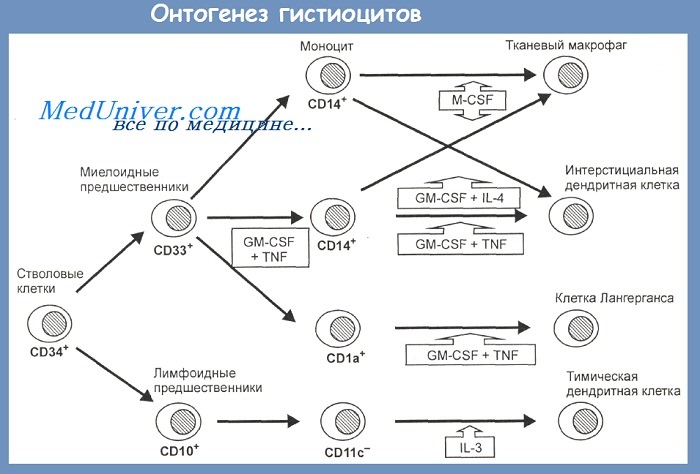
Интерстициальные дендритные клетки и эпидермальные дендритные клетки (клетки Лангерганса) происходят от общего с моноцитами миелоидного предшественника, ведущая роль в их дифференцировке принадлежит гранулоцитарно-макрофагальному колониестимулирующему фактору (GM-CSF). Тимические дендритные клетки (ДК) и, возможно, интердигитирующие дендритные клетки развиваются из коммитированных лимфоидных предшественников под влиянием ряда цитокинов, включая ИЛ-3.
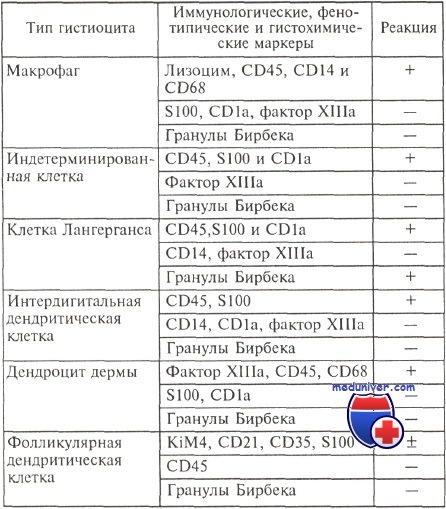
Иммуногистохимическая характеристика различных типов гистиоцитов
Близкое родство между макрофагами и дендритных клеток является результатом общности их функциональных, морфологических и фенотипических свойств. Клеточные характеристики гистиоцитов в процессе диф-ференцировки определяются не только стадией их развития, но и влиянием соответствующего микроокружения. Онтогенез гистиоцитов до настоящего времени остается объектом интенсивных исследований. Принятая схема онтогенеза гистиоцитов представлена на рисунке.
В клинической практике необходимо четко дифференцировать макрофаги, являющиеся фагоцитирующими клетками с преимущественными функциями обработки антигена, от дендритных клеток с преимущественными способностями презентации антигенов. Подобная дифференциация гистиоцитов сложна и решается с помощью цитоморфологических, иммунофенотипических и гистохимических методов. Следует подчеркнуть, что фолликулярная ДК имеет мезенхимальное происхождение и, согласно современным представлениям, не относится к гистиоцитарному ряду.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.