Химические формулы веществ
Химические формула – это изображение качественного и количественного состава вещества с помощью символов химических элементов.
Знаки химических элементов
Химический знак или химический символ элемента – это первая или две первые буквы от латинского названия этого элемента.
Таблица 1: Информация, которую дает химический знак
Название химического знака в большинстве случаев читается как название химического элемента. Например, К – калий, Са – кальций, Mg – магний, Mn – марганец.
Случаи, когда название химического знака читается иначе, приведены в таблице 2:
| Название химического элемента | Химический знак | Название химического знака |
(произношение)
Химические формулы простых веществ
Химическими формулами большинства простых веществ (всех металлов и многих неметаллов) являются знаки соответствующих химических элементов.
Таблица 3: Информация, которую дает химический знак
Химические формулы сложных веществ
Формулу сложного вещества составляют путем записи знаков химических элементов, из которых это вещество состоит, с указанием числа атомов каждого элемента в молекуле. При этом, как правило, химические элементы записывают в порядке увеличения их электроотрицательности в соответствии со следующим практическим рядом:
Исключение составляют:
Число атомов химического элемента в молекуле и сложном ионе определяется на основании понятия валентности или степени окисления и записывается индексом внизу справа от знака каждого элемента (индекс 1 опускается). При этом исходят из правила:
алгебраическая сумма степеней окисления всех атомов в молекуле должна быть равной нулю (молекулы электронейтральны), а в сложном ионе – заряду иона.
Этим же правилом пользуются при определении степени окисления химического элемента по формуле вещества или сложного иона. Обычно это элемент, имеющий несколько степеней окисления. Степени окисления остальных элементов, образующих молекулу или ион должны быть известны.
Заряд сложного иона – это алгебраическая сумма степеней окисления всех атомов, образующих ион. Поэтому при определении степени окисления химического элемента в сложном ионе сам ион заключается в скобки, а его заряд выносится за скобки.
При составлении формул по валентности вещество представляют, как соединение, состоящее из двух частиц различного типа, валентности которых известны. Далее пользуются правилом:
в молекуле произведение валентности на число частиц одного типа должно быть равным произведению валентности на число частиц другого типа.
Например:
Цифра, стоящая перед формулой в уравнении реакции, называется коэффициентом. Она указывает либо число молекул, либо число молей вещества.
Коэффициент, стоящий перед химическим знаком, указывает число атомов данного химического элемента, а в случае, когда знак является формулой простого вещества, коэффициент указывает либо число атомов, либо число молей этого вещества.
Например:
Химические формулы многих веществ были определены опытным путем, поэтому их называют «эмпирическими».
Таблица 4: Информация, которую дает химическая формула сложного вещества
1 моль (6,02·10 23 молекул) СаСО3 содержит 1 моль ионов Са 2+ и 1 моль ионов СО3 2- ;
1 моль (100г) карбоната кальция содержит 40г ионов Са 2+ и 60г ионов СО3 2-
Графические формулы
Для составления графической (структурной) формулы вещества необходимо:
Примеры графических формул:
Структурно-графические формулы веществ



Эмпирические формулы дают информацию о качественном и количественном составе соединений. Взаимное расположение атомов в молекуле вещества отражают структурно-графические формулы, однако они не показывают пространственное расположение атомов.
При составлении структурно-графических формул можно руководствоваться следующими правилами:
1. Элементы соединяются в соответствии с их валентностью.
2. Черточка в формуле обозначает единичную химическую связь, количество черточек соответствует валентности, например:
3. Состав кислот и оснований следует начинать изображать с центрального атома,
4. Если в молекуле кислоты содержится больше атомов кислорода, чем водорода, то «избыточные» атомы кислорода соединены с центральным атомом двойной связью,
| например: HClO4 | 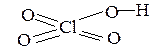 |
5. При написании графических формул солей исходят из графических формул кислот, заменяя атомы водорода на атомы металла, учитывая его валентность, например:
| Na3PO4 | 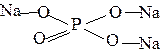 | Fe2(SO4)3 | 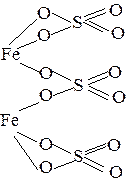 |
| KHCO3 | 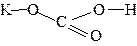 | ||
| CaOHNO3 | 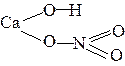 |
Структурно-графические формулы некоторых кислот приведены в табл. 5.
2.4. Общие химические свойства основных классов
неорганических веществ
Оксиды ‑ вещества, состоящие из атомов двух элементов, один из которых – кислород в степени окисления (–2). По химическим свойствам их подразделяют на индифферентные, или несолеобразующие (CO, NO), и солеобразующие, которые бывают основными, кислотными и амфотерными.
Химические свойства основных оксидов
1. Взаимодействуют с кислотами с образованием соли и воды, например:
2. Взаимодействие с кислотными оксидами с образованием солей:
3. Оксиды щелочных и щелочноземельных металлов взаимодействуют с водой с образованием растворимых в воде оснований – щелочей:
Химические свойства кислотных оксидов
1. Общим свойством всех кислотных оксидов является их способность взаимодействовать с основаниями с образованием соли и воды:
2. Кислотные оксиды взаимодействуют с основными оксидами с образованием солей.
3. Большинство кислотных оксидов взаимодействует с водой с образованием кислот:
Очень немногие кислотные оксиды не взаимодействуют с водой. Наиболее известный из них оксид кремния (SiO2).
Химические свойства амфотерных оксидов
1. Амфотерные оксиды взаимодействуют с кислотами с образованием солей и воды.
В этих реакциях амфотерные оксиды играют роль основных.
2. Амфотерные оксиды взаимодействуют с щелочами с образованием солей и воды.
ZnO + 2КОН 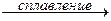
ZnO + 2КОН + H2O 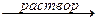
В этих реакциях амфотерные оксиды играют роль кислотных.
3. Амфотерные оксиды при нагревании взаимодействуют с кислотными оксидами с образованием солей:
4. Амфотерные оксиды при нагревании взаимодействуют с основными оксидами с образованием солей:
Оксиды могут быть получены различными способами:
1. Взаимодействием простых веществ с кислородом:
2. Разложением некоторых оксокислот:
H2SO3 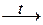
3. Разложением нерастворимых оснований:
Сu(OH)2 
4. Разложением некоторых солей:
СаСО3 
Основания ‑сложные вещества, при диссоциации которых в воде образуются гидроксид-ионы и никаких других анионов.
По растворимости в воде основания делятся на две группы: нерастворимые [Fe(OH)3, Си(ОН)2 и др.] и растворимые в воде [КОН, NaOH, Са(ОН)2, Ва(ОН)2 ], или щелочи.
Химические свойства оснований
1. Водные растворы щелочей изменяют окраску индикаторов.
Таблица 6 ‑ Изменение цвета индикаторов в растворах
| Индикатор | Цвет индикатора | Цвет индикатора в растворе щелочи (рН > 7) | Цвет индикатора в растворе кислоты (рН  3. Щелочи взаимодействуют с кислотными оксидами с образованием соли и воды: 4. Растворы щелочей взаимодействуют с растворами солей, если в результате образуется нерастворимое основание или нерастворимая соль. Например: 5. Нерастворимые основания при нагревании разлагаются на основный оксид и воду. 2Fе(ОН)3 6. Растворы щелочей взаимодействуют с металлами, которые образуют амфотерные оксиды и гидроксиды (Zn, Al и др.). 1. Получение растворимых оснований: а) взаимодействием щелочных и щелочноземельных металлов с водой: б) взаимодействием оксидов щелочных и щелочноземельных металлов с 2. Получение нерастворимых оснований действием щелочей на растворимые соли металлов: Кислоты ‑ сложные вещества, при диссоциации которых в воде, образуются ионы водорода (гидроксония) и никаких других катионов. Общие свойства кислот в водных растворах обусловлены присутствием ионов Н + (вернее H3O + ), которые образуются в результате электролитической диссоциации молекул кислот: 1. Кислоты одинаково изменяют цвет индикаторов (табл. 7). 2. Кислоты взаимодействуют с основаниями. Например: 3. Кислоты взаимодействуют с основными оксидам: 4. Кислоты взаимодействуют с амфотерными оксидами: 5. Кислоты взаимодействуют с некоторыми средними солями с образованием новой соли и новой кислоты, реакции возможны в том случае, если в результате образуется нерастворимая соль или более слабая (или более летучая) кислота, чем исходная. Например: 6. Кислоты взаимодействуют с металлами. Характер продуктов этих реакций зависит от природы и концентрации кислоты и от активности металла. Например, разбавленная серная кислота, хлороводородная кислота и другие кислоты‑неокислители взаимодействуют с металлами, которые находятся в электрохимическом ряду напряжения левее водорода. В результате реакции образуются соль и газообразный водород: Кислоты-окислители (концентрированная серная кислота, азотная кислота HNO3 любой концентрации) взаимодействуют и с металлами, стоящими в ряду напряжения после водорода с образованием соли и продукта восстановления кислоты. Например: 1. Бескислородные кислоты получают путем синтеза из простых веществ и последующим растворением продукта в воде. 2. Оксокислоты получают взаимодействием кислотных оксидов с водой. 3. Большинство кислот можно получить взаимодействием солей с кислотами. Химическая формула веществаЗнаки химических элементовХимический знак или химический символ элемента – это первая или две первые буквы от латинского названия этого элемента. Таблица 1: Информация, которую дает химический знакНа примере Cl Принадлежность элемента к данному классу химических элементов Один атом элемента Относительная атомная масса (Ar) данного элемента Ar (Cl) = 35,5 Абсолютная атомная масса химического элемента m = Ar · 1,66·10 -24 г = Ar · 1,66 · 10 -27 кг M (Cl) = 35,5 · 1,66 · 10 -24 = 58,9 · 10 -24 г Случаи, когда название химического знака читается иначе, приведены в таблице 2:Название химического элемента Название химического знака Химические формулы простых веществХимическими формулами большинства простых веществ (всех металлов и многих неметаллов) являются знаки соответствующих химических элементов. Таблица 3: Информация, которую дает химический знакУглерод (алмаз, графит, графен, карбин) Принадлежность элемента к данному классу химических элементов Один атом элемента Относительная атомная масса (Ar) элемента, образующего вещество Ar (C) = 12 Абсолютная атомная масса M (C) = 12 · 1,66 · 10-24 = 19,93 · 10 -24 г Один моль вещества 1 моль углерода, т.е. 6,02 · 10 23 атомов углерода Молярная масса вещества M (C) = Ar (C) = 12 г/моль Химические формулы сложных веществФормулу сложного вещества составляют путем записи знаков химических элементов, из которых это вещество состоит, с указанием числа атомов каждого элемента в молекуле. При этом, как правило, химические элементы записывают в порядке увеличения их электроотрицательности в соответствии со следующим практическим рядом: Me , Si , B , Te , H , P , As , I , Se , C , S , Br , Cl , N , O , F Число атомов химического элемента в молекуле и сложном ионе определяется на основании понятия валентности или степени окисления и записывается индексом внизу справа от знака каждого элемента (индекс 1 опускается). При этом исходят из правила: алгебраическая сумма степеней окисления всех атомов в молекуле должна быть равной нулю (молекулы электронейтральны), а в сложном ионе – заряду иона. 2Al 3 + +3SO 4 2- =Al 2 (SO 4 ) 3 Заряд сложного иона – это алгебраическая сумма степеней окисления всех атомов, образующих ион. Поэтому при определении степени окисления химического элемента в сложном ионе сам ион заключается в скобки, а его заряд выносится за скобки. При составлении формул по валентности вещество представляют, как соединение, состоящее из двух частиц различного типа, валентности которых известны. Далее пользуются правилом: в молекуле произведение валентности на число частиц одного типа должно быть равным произведению валентности на число частиц другого типа. · 3Fe – три атома железа, 3 моль атомов железа, · 2H – два атома водорода, 2 моль атомов водорода, · H 2 – одна молекула водорода, 1 моль водорода. Таблица 4: Информация, которую дает химическая формула сложного веществаНа примере CaCO3 Принадлежность элемента к определенному классу веществ Средняя (нормальная) соль Одна молекула вещества 1 молекула карбоната кальция Один моль вещества 6,02 · 10 23 молекул CaCO 3 Относительная молекулярная масса вещества (Мr) М r (CaCO3) = Ar (Ca) +Ar (C) +3Ar (O) =100 Молярная масса вещества (M) М (CaCO3) = 100 г/моль Абсолютная молекулярная масса вещества (m) M (CaCO3) = Mr (CaCO3) · 1,66 · 10 -24 г = 1,66 · 10 -22 г Качественный состав (какие химические элементы образуют вещество) кальций, углерод, кислород Количественный состав вещества:Число атомов каждого элемента в одной молекуле вещества: молекула карбоната кальция состоит из 1 атома кальция, 1 атома углерода и 3 атомов кислорода. Число молей каждого элемента в 1 моле вещества: В 1 моль СаСО 3 (6,02 ·10 23 молекулах) содержится 1 моль (6,02 ·10 23 атомов) кальция, 1 моль (6,02 ·10 23 атомов) углерода и 3 моль (3·6,02·10 23 атомов) химического элемента кислорода) Массовый состав вещества:Масса каждого элемента в 1 моле вещества: Массовые доли химических элементов в веществе (состав вещества в процентах по массе): Состав карбоната кальция по массе: W (Ca) = (n (Ca) ·Ar (Ca) )/Mr (CaCO3) = (1·40)/100= 0,4 (40%) W (C) = (n (Ca) ·Ar (Ca) )/Mr (CaCO3) = (1·12)/100= 0,12 (12%) W ( О ) = (n (Ca) ·Ar (Ca) )/Mr (CaCO3) = (3·16)/100= 0,48 (48%) Для вещества с ионной структурой (соли, кислоты, основания) – формула вещества дает информацию о числе ионов каждого вида в молекуле, их количестве и массе ионов в 1 моль вещества: Молекула СаСО 3 состоит из иона Са 2+ и иона СО 3 2- 1 моль ( 6,02·10 23 молекул) СаСО 3 содержит 1 моль ионов Са 2+ и 1 моль ионов СО 3 2- ; 1 моль (100г) карбоната кальция содержит 40г ионов Са 2+ и 60г ионов СО 3 2- Молярный объем вещества при нормальных условиях (только для газов) Графические формулыДля составления графической (структурной) формулы вещества необходимо:· Определить валентность всех химических элементов, образующих вещество. · Записать знаки всех химических элементов, образующих вещество, каждый в количестве, равном числу атомов данного элемента в молекуле. · Соединить знаки химических элементов черточками. Каждая черточка обозначает электронную пару, осуществляющую связь между химическими элементами и поэтому одинаково принадлежит обоим элементам. · Число черточек, окружающих знак химического элемента, должно соответствовать валентности этого химического элемента. · При составлении формул кислородсодержащих кислот и их солей атомы водорода и атомы металлов связываются с кислотообразующим элементом через атом кислорода. · Атомы кислорода соединяют друг с другом только при составлении формул пероксидов. |






