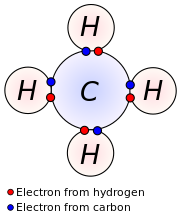
Атомы и электроны
Атомно-молекулярное учение
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.
Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Состоит из s-подуровня: одной «s» ячейки (2s 2 ) и p-подуровня: трех «p» ячеек (2p 6 ), на которых помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s 2 ), p-подуровня: трех «p» ячеек (3p 6 ) и d-подуровня: пяти «d» ячеек (3d 10 ), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s 2 ), p-подуровня: трех «p» ячеек (4p 6 ), d-подуровня: пяти «d» ячеек (4d 10 ) и f-подуровня: семи «f» ячеек (4f 14 ), на которых помещается 14 электронов
Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный «рисунок».
Правила заполнения электронных орбиталей и примеры
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
Внешний уровень и валентные электроны
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.
валентный электрон
СОДЕРЖАНИЕ
Обзор [ править ]
Электронная конфигурация [ править ]
Чем дальше вправо в каждой серии переходных металлов, тем ниже энергия электрона в подоболочке и тем меньше у такого электрона валентных свойств. Таким образом, хотя атом никеля в принципе имеет десять валентных электронов (4s 2 3d 8 ), его степень окисления никогда не превышает четырех. Для цинка подоболочка 3d является полной во всех известных соединениях, хотя она вносит вклад в валентную зону в некоторых соединениях. [4]
Подсчет д электронов является альтернативным инструментом для понимания химии переходного металла.
Число валентных электронов [ править ]
Количество валентных электронов элемента может быть определено группой периодической таблицы (вертикальный столбец), в которой этот элемент отнесен к категории. За исключением групп 3–12 ( переходные металлы ), цифра единиц номера группы указывает, сколько валентных электронов связано с нейтральным атомом элемента, указанного в этом конкретном столбце.
| Блок периодической таблицы | Группа периодической таблицы | Валентные электроны |
|---|---|---|
| s | Группа 1 (I) ( щелочные металлы ) | 1 |
| Группа 2 (II) ( щелочноземельные металлы ) и гелий | 2 | |
| ж | Лантаноиды и актиниды | 3–16 [а] |
| d | Группы 3-12 ( переходные металлы ) | 3–12 [b] |
| п | Группа 13 (III) ( группа бора ) | 3 |
| Группа 14 (IV) ( углеродная группа ) | 4 | |
| Группа 15 (V) ( пниктогены или азотная группа) | 5 | |
| Группа 16 (VI) ( халькогены или кислородная группа) | 6 | |
| Группа 17 (VII) ( галогены ) | 7 | |
| Группа 18 (VIII или 0) ( благородные газы ), кроме гелия | 8 |
Оболочка валентности [ править ]
Химические реакции [ править ]
Количество валентных электронов в атоме определяет его связывающее поведение. Следовательно, элементы, атомы которых могут иметь одинаковое количество валентных электронов, сгруппированы вместе в периодической таблице элементов.
Внутри каждой группы (каждого столбца периодической таблицы) металлов реакционная способность увеличивается с каждой нижней строкой таблицы (от легкого элемента к более тяжелому), потому что более тяжелый элемент имеет больше электронных оболочек, чем более легкий элемент; валентные электроны более тяжелого элемента существуют с более высокими главными квантовыми числами (они находятся дальше от ядра атома и, таким образом, имеют более высокие потенциальные энергии, что означает, что они менее тесно связаны).
Внутри каждой группы неметаллов реакционная способность уменьшается с каждой нижней строкой таблицы (от легкого элемента к тяжелому) в периодической таблице, потому что валентные электроны имеют все более высокие энергии и, следовательно, все менее прочно связаны. Фактически, кислород (самый легкий элемент в группе 16) является наиболее реакционноспособным неметаллом после фтора, хотя он и не является галогеном, потому что валентная оболочка галогена имеет более высокое главное квантовое число.
В этих простых случаях, когда соблюдается правило октета, валентность атома равна количеству электронов, полученных, потерянных или разделенных для формирования стабильного октета. Однако есть также много молекул, которые являются исключениями и для которых валентность менее четко определена.
Электропроводность [ править ]
Металл Металлоид Неметалл Неизвестные свойства Цвет фона показывает тенденцию металл – металлоид – неметалл в периодической таблице.
валентный электрон
СОДЕРЖАНИЕ
Обзор [ править ]
Электронная конфигурация [ править ]
Чем дальше вправо в каждой серии переходных металлов, тем ниже энергия электрона в подоболочке и тем меньше у такого электрона валентных свойств. Таким образом, хотя атом никеля в принципе имеет десять валентных электронов (4s 2 3d 8 ), его степень окисления никогда не превышает четырех. Для цинка подоболочка 3d является полной во всех известных соединениях, хотя она вносит вклад в валентную зону в некоторых соединениях. [4]
Подсчет д электронов является альтернативным инструментом для понимания химии переходного металла.
Число валентных электронов [ править ]
Количество валентных электронов элемента может быть определено группой периодической таблицы (вертикальный столбец), в которой этот элемент отнесен к категории. За исключением групп 3–12 ( переходные металлы ), цифра единиц номера группы указывает, сколько валентных электронов связано с нейтральным атомом элемента, указанного в этом конкретном столбце.
| Блок периодической таблицы | Группа периодической таблицы | Валентные электроны |
|---|---|---|
| s | Группа 1 (I) ( щелочные металлы ) | 1 |
| Группа 2 (II) ( щелочноземельные металлы ) и гелий | 2 | |
| ж | Лантаноиды и актиниды | 3–16 [а] |
| d | Группы 3-12 ( переходные металлы ) | 3–12 [b] |
| п | Группа 13 (III) ( группа бора ) | 3 |
| Группа 14 (IV) ( углеродная группа ) | 4 | |
| Группа 15 (V) ( пниктогены или азотная группа) | 5 | |
| Группа 16 (VI) ( халькогены или кислородная группа) | 6 | |
| Группа 17 (VII) ( галогены ) | 7 | |
| Группа 18 (VIII или 0) ( благородные газы ), кроме гелия | 8 |
Оболочка валентности [ править ]
Химические реакции [ править ]
Количество валентных электронов в атоме определяет его связывающее поведение. Следовательно, элементы, атомы которых могут иметь одинаковое количество валентных электронов, сгруппированы вместе в периодической таблице элементов.
Внутри каждой группы (каждого столбца периодической таблицы) металлов реакционная способность увеличивается с каждой нижней строкой таблицы (от легкого элемента к более тяжелому), потому что более тяжелый элемент имеет больше электронных оболочек, чем более легкий элемент; валентные электроны более тяжелого элемента существуют с более высокими главными квантовыми числами (они находятся дальше от ядра атома и, таким образом, имеют более высокие потенциальные энергии, что означает, что они менее тесно связаны).
Внутри каждой группы неметаллов реакционная способность уменьшается с каждой нижней строкой таблицы (от легкого элемента к тяжелому) в периодической таблице, потому что валентные электроны имеют все более высокие энергии и, таким образом, все менее прочно связаны. Фактически, кислород (самый легкий элемент в группе 16) является наиболее реакционноспособным неметаллом после фтора, хотя он и не является галогеном, потому что валентная оболочка галогена имеет более высокое главное квантовое число.
В этих простых случаях, когда соблюдается правило октета, валентность атома равна количеству электронов, полученных, потерянных или разделенных для формирования стабильного октета. Однако есть также много молекул, которые являются исключениями и для которых валентность менее четко определена.
Электропроводность [ править ]
Металл Металлоид Неметалл Неизвестные свойства Цвет фона показывает тенденцию металл – металлоид – неметалл в периодической таблице.