Что такое оксид азота
Оксид азота

Оксид азота или окись азота, а также известный как монооксид азота представляет собой молекулу с химической формулой NO. Это свободные радикалы, которые является важным промежуточным продуктом химических реакций.
В организмах млекопитающих и человека оксид азота является важной составляющей клеточных сигнальных молекул, участвующих во многих физиологических и патологических процессах. Это мощный вазодилататор с коротким, в несколько секунд, периодом полураспада в крови.
В конце 80-х годов было доказано, что особые ферментные системы организмов способны синтезировать газ оксида азота. Это происходит в результате окисления гуанидиновой группы аминокислоты L-аргинина с одновременным синтезом цитруллина.
Получение оксида азота
В лабораторных условиях получение оксида азота возможно путем проведения реакции разбавленной азотной кислоты с медью или восстановлением азотистой кислоты в виде нитрита натрия или нитрита калия.
Основным природным источником оксида азота являются электрические разряды молний в грозу. Оксид азота является побочным продуктом, возникающим при сгорании веществ в автомобильных двигателях и топлива на электростанциях.
Также получение оксида азота возможно из свободных элементов, для этого необходимо при температуре 1200-1300°C провести соединение азота с кислородом.
Применение оксида азота
Оксид азота используется в медицине для расширения кровеносных сосудов при ишемической болезни сердца путем уменьшения нагрузки на сердце.
Оксид азота используется при неотложной помощи для содействия капиллярному расширению легких для лечения первичной легочной гипертензии у новорожденных, связанной с врожденными дефектами. Терапия оксидом азота значительно повышает качество жизни и, в некоторых случаях, спасает жизнь детей с риском развития заболевания сосудов легких.
Оксид азота также вводится в виде спасительной терапии у больных с острой правожелудочковой недостаточностью, которая является вторичной по отношению к легочной эмболии.
В пищевой промышленности оксид азота известен под названием пищевая добавка Е942 и используется в качестве пропеллента и упаковочного газа.
Свойства оксида азота
Польза оксида азота

Вред оксида азота
Применение оксида азота у большинства людей не вызывает побочных эффектов, однако, в случаях передозировки он приводит к диарее, слабости, тошноте, головной боли, учащению пульса и сердцебиения, задержкам воды, усталости, раздражениям на коже и сухости во рту.
Также побочными эффектами применения оксида азота являются проблемы с дыханием, сильная аллергия или сыпь, крапивница, зуд, одышка, опасные для жизни осложнения астмы, внезапный озноб, потливость, тремор, рвота и обмороки. В некоторых случаях применение оксида азота приводит к вспышкам герпеса, расширению сосудов и кровотечениям.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Оксид азота I Для чего? I Полезные свойства
Фарида Сеидова
Врач и редактор / Опубликовано
Поделиться этой страницей
П риблизительно 30 лет назад ученые обнаружили природный газ, вырабатываемый в организме, который расслабляет гладкие мышцы в кровеносных сосудах, способствуя увеличению содержания кислорода в крови и усилению кровотока. С тех пор было опубликовано более 30000 научных работ, подтверждающих важную роль оксида азота в вазодилатации (расслаблении гладкой мускулатуры стенок кровеносных сосудов) и в клеточной коммуникации.
Что такое оксид азота?
Оксид азота (NO) представляет собой природный газ, вырабатываемый в организме под действием определенных ферментов, называемых синтазами оксида азота, которые разрушают аминокислоту аргинин. Оксид азота действует в качестве важной сигнальной молекулы в сосудистой системе, высвобождение в кровеносное русло которой способствует расширению кровеносных сосудов и увеличению их просвета, увеличению кровотока и доставки питательных веществ в мышечные клетки. Исходным материалом для выработки оксида азота в организме служит аргинин.
Полезные свойства
Оксид азота обладает рядом полезных свойств для организма: снижает пагубное воздействие стрессовых гормонов, повышает иммунитет, регулирует кислотно-щелочной баланс крови, обеспечивая клетки организма кислородом, ускоряет заживление ран. Ниже более подробно перечислены наиболее важные его свойства. Итак, оксид азота:
Вазодилатационный эффект оксида азота чрезвычайно важен для спортсменов, особенно для культуристов, потому что увеличение в крови количества питательных веществ и доставка большего количества кислорода к мышцам позволят дольше тренироваться, независимо от вида спорта.
Во время физической активности происходит возрастание сердечного выброса и перераспределение кровотока в мышечных волокнах. Когда вы тренируетесь, кислород в мышцах истощается. При недостатке кислорода организм начинает вырабатывать молочную кислоту, которая в конечном итоге приводит к мышечной усталости – до такой степени, что вы не можете больше продолжать тренировку. Оксид азота уменьшает количество молочной кислоты, вырабатываемой во время физических упражнений, и продлевает время до наступления истощения.
Улучшает результативность тренировок
Ускоряя доставку кислорода и питательных веществ в мышцы, оксид азота улучшает их реакцию на физические нагрузки и повышает спортивные результаты. Исследование, проведенное в 2010 году при Университете Небраски-Линкольна и опубликованное в Strength & Conditioning, изучало влияние добавок на основе аргинина на физическую работоспособность уставших людей. 1
Исследование показало, что у пациентов, принимавших аргинин, наблюдалось значительное повышение работоспособности, в то время как в группе, принимавшей плацебо, не отмечалось значительных изменений.
Известно также, что оксид азота ускоряет выделение из организма аммиака и способствует увеличению поглощения глюкозы клетками.
Улучшает восстановление после тренировок
Исследование китайских ученых, результаты которого были опубликованы в журнале Chinese Journal of Physiologyв 2009 году, показало, что прием L-аргинина приводит к увеличению в крови концентрации глюкозы и инсулина после тренировки. 2
Повышение уровня инсулина, в свою очередь, может помочь улучшить синтез мышечного белка а, следовательно, и улучшить восстановление после тренировок.
Может улучшать когнитивные функции
Результаты ряда исследований подтверждают, что оксид азота улучшает память и когнитивные функции мозга. Исследование, проведенное в 2011 году и опубликованное в Indian Journal of Medical Research, показало, что «оксид азота активирует вычислительную способность мозга». 3
Улучшает эректильную функцию
Оксид азота может улучшать эрекцию и бороться с эректильной дисфункцией. Это свойство препарата было подтверждено исследованием, проведенным в 1992 году доктором Бернеттом. Результаты выявили, что оксид азота играет решающую роль в эректильной функции, а добавка может помочь пациентам с эректильной дисфункцией). 4
Как увеличить выработку оксида азота
Для этого существует много естественных способов. Одним из них является выполнение физических упражнений. 5
Отличным способом увеличения содержания оксида азота является смех. Да, обычный смех! Исследование американских ученых, проведенное в 2009 году, показало, что смех высвобождает бета-эндорфины. Исследователи предположили, что «такие положительные эмоции приводят к прямому выбросу оксида азота и к связанным с его выработкой биологическим последствиям». 6
Еще один способ – это употребление в пищу продуктов с высоким содержанием нитратов, поскольку в кишечнике нитраты могут разлагаться, выделяя оксид азота. 7
Воздействие солнечного света также может способствовать увеличению выработки оксида азота. 8
Ну и наконец, если ваш организм не вырабатывает достаточное количество оксида азота, для удовлетворения его потребностей, вы можете воспользоваться добавками.
Добавки с оксидом азота
И все же, возможно, одним из наиболее важных для культуристов свойств добавок с аргинином, является его способность стимулировать выработку гормона роста. Научные исследования показывают, что уровень гормона роста повышается при пероральном приеме L-аргинина, сочетаемом с физической нагрузкой. В основном это связано со способностью аргинина подавлять секрецию соматостатина — гормона, который ингибирует гормон роста. Как известно, гормон роста ответственен за рост клеток и тканей: это делает его абсолютно необходимым для роста мышц.
Как видите, польза аргинина выходит далеко за рамки его способности стимулировать синтез NO. Как показали научные исследования, аргинин может непосредственно влиять на рост мышц. Цитруллин — еще одна аминокислота, которая, благодаря более высокой скорости всасывания по сравнению с аргинином, может успешно восстанавливать выработку оксида азота. Вы можете в ней нуждаться, если организм получает ограниченное количество этой аминокислоты.
Заключение
Теперь понятно, почему добавки с оксидом азота очень популярны среди спортсменов и культуристов — они способствуют вазодилатации и помогают организму доставлять необходимые питательные вещества в клетки мышц, улучшая таким образом спортивную результативность. Посетители тренажерных залов любят ощущать на себе эффект от пампинга, получаемый благодаря приему добавок с оксидом азота.
Аргинин и цитруллин – это два весьма полезных ингредиента, которые также включают в состав добавок. Они повышают выработку оксида азота, а иногда могут проявлять и другие полезные свойства, например, воздействовать напрямую на рост мышц. Вы можете выбирать для себя продукты с высокой степенью биодоступности, например, цитруллин малат или аргинин-альфа-кетоглютарат.
Статьи на нашем сайте представлены только в просветительских и информационных целях. Мы не рекомендуем использовать материалы статей в качестве медицинских рекомендаций. Если вы решили принимать биодобавки или внести основательные изменения в свой рацион, предварительно проконсультируйтесь со специалистом.
Переводчик, корректор и редактор: Фарида Сеидова
Окислы азота
Оксиды азота — соединения азота с кислородом.
Содержание
Список оксидов
Азот образует несколько соединений с кислородом:
Оксид азота N2O — бесцветный газ со слабым запахом, растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза.
Оксид азота NO — бесветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота (II) — очень реакционноспособное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO2. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
N2O3(III)
Оксид N2O3 (азотистый ангидрид) неустойчив при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
NО2, N2O4
Оксид азота NО2 — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NО2 находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
Сильный окислитель. Многие вещества (уголь, сера, фосфор, органические соединения) могут гореть в NО2. Этот оксид окисляет SО2 до SO3, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
N2O5(V)
Оксид N2O5 (азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NО2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
Воздействие на организм
Применение
Оксиды азота зарегистрированы в качестве пищевой добавки E918.
См.также
Полезное
Смотреть что такое «Окислы азота» в других словарях:
Окислы азота — Смесь различных окислов азота, кроме закиси NO2, образовавшихся в цилиндре дизеля в процессе сгорания Источник: ГОСТ 24585 81: Дизел … Словарь-справочник терминов нормативно-технической документации
Окислы азота — С кислородом азот образует ряд соединений N2O5 азотный ангидрид [О над азотной кислоте см. Крепкая водка.], N2O4 или NO2 азотноватый ангидрид или двуокись азота, N2O3 азотистый ангидрид, NO окись азота, N2O закись азота. Определения Фавра,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Окислы азота (NOх) — 5. Окислы азота (NOх) Смесь окиси и двуокиси азота, содержащихся в пробе газа Примечание. В расчетах условно предполагается, что окись азота находится в виде двуокиси азота Источник … Словарь-справочник терминов нормативно-технической документации
Окислы азота и азотная кислота — 4.6. Окислы азота и азотная кислота оказывают в основном вредное влияние на активную массу отрицательных электродов, окисляя свинец в окись. Окись свинца, в свою очередь, вступая в реакцию с оставшейся неиспользованной кислотой, образует… … Словарь-справочник терминов нормативно-технической документации
ОКИСЛЫ — ОКИСЛЫ, соединения элементов с кислородом. Кислород соединяется со всеми элементами кроме благородных газов. Недавно открытая юкись фтора заполняет существовавший в отношении фтора пробел. В зависимости от степени окисления и валентности элемента … Большая медицинская энциклопедия
Азота окислы — соединения азота с кислородом. Известны N2O, NO, N2O3, NO2 (и его димер N2O4), N2O5; есть сведения о существовании NO3, не выделенного в свободном состоянии. При высокой температуре в пламени вольтовой дуги, а в природе при электроразряде … Большая советская энциклопедия
Окислы — Оксид (окисел, окись) соединение химического элемента с кислородом, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам… … Википедия
Окислы — О. называются соединения простых тел с кислородом. Если придерживаться деления простых тел на две группы, на металлы и металлоиды (см.), то вообще в характере их О. можно заметить довольно ясную разницу. Тогда как типические представители первой… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Закись азота — химический состав см. Окислы азота. В медицине З. азота получила название веселящего газа: вдыхаемая в смеси с атмосферным воздухом или кислородом при обыкновенной температуре и давлении она вызывает особое состояние опьянения, уничтожающего… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Закись азота — веселящий газ, один из окислов азота (см. Азота окислы); в медицине применяют в смеси с кислородом как средство для ингаляционного Наркоза при хирургических операциях, родах, иногда при инфаркте миокарда. Назван веселящим газом английским … Большая советская энциклопедия
Окись азота
Окись азота
| Оксид азота(II) | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид азота(II) |
| Химическая формула | NO |
| Отн. молек. масса | 30.0061 а. е. м. |
| Молярная масса | 30.0061 г/моль |
| Физические свойства | |
| Плотность вещества | 0.00134 (газ) г/см³ |
| Состояние (ст. усл.) | бесцветный газ |
| Термические свойства | |
| Температура плавления | −163.6 °C |
| Температура кипения | −151.7 °C |
| Энтальпия (ст. усл.) | 81 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 0,01 г/100 мл |
| Классификация | |
| номер CAS | [10102-43-9] |
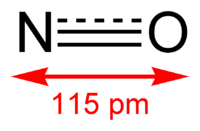
Окси́д азо́та (II) NO (моноксид азота, окись азота, нитрозил-радикал) — несолеобразующий оксид азота. Он представляет собой бесцветный газ, плохо растворимый в воде. Сжижается с трудом; в жидком и твёрдом виде имеет голубой цвет.
Наличие неспаренного электрона обусловливает склонность NO к образованию слабосвязанных димеров N2O2. Это непрочные соединения с ΔH° димеризации = 17 кДж. Жидкий оксид азота (II) на 25% состоит из молекул N2O2, а твердый оксид целиком состоит из них.
Содержание
Получение
Оксид азота(II) — единственный из оксидов азота, который можно получить непосредственно из свободных элементов соединением азота с кислородом при высоких температурах (1200—1300 °C) или в электрическом разряде. В природе он образуется в атмосфере при грозовых разрядах:
и тотчас же реагирует с кислородом:
При понижении температуры оксид азота(II) разлагается на азот и кислород, но если температура падает резко, то не успевший разложиться оксид существует достаточно долго: при низкой температуре скорость распада невелика. Такое резкое охлаждение называется «закалкой» и используется при одном из способов получения азотной кислоты.
В лаборатории его обычно получают взаимодействием 30%-ной HNO3 с некоторыми металлами, например, с медью:
Более чистый, не загрязнённый примесями NO можно получить по реакциям:
Промышленный способ основан на окислении аммиака при высокой температуре и давлении при участии Pt, Cr2O3 (как катализаторов):
Химические свойства
При комнатной температуре и атмосферном давлении окисление NO кислородом воздуха происходит мгновенно:
Для NO характерны также реакции присоединения галогенов с образованием нитрозилгалогенидов, в этой реакции NO проявляет свойства восстановителя:
В присутствии более сильных восстановителей NO проявляет окислительные свойства:
В воде NO мало растворим и с ней не реагирует, являясь несолеобразующим оксидом.
Физиологическое действие
Как и все оксиды азота (кроме N2O), NO — токсичен, при вдыхании поражает дыхательные пути.
За два последних десятилетия было установлено, что эта молекула NO обладает широким спектром биологического действия, которое условно можно разделить на регуляторное, защитное и вредное. NO, являясь одним из мессенджеров, участвует в регуляции систем внутри- и межклеточной сигнализации. Оксид азота, производимый клетками эндотелия сосудов, отвечает за расслабление гладких мышц сосудов и их расширение(вазодилатацию), предотвращает агрегацию тромбоцитов и адгезию нейрофилов к эндотелию, участвует в различных процессах в нервной, репродуктивной и иммунной системах. NO также обладает цитотоксическими и цитостатическими свойствами. Клетки-киллеры иммунной системы используют оксид азота для уничтожения бактерий и клеток злокачественных опухолей. С нарушением биосинтеза и метаболизма NO связаны такие заболевания, как ассенциальная артериальная гипертензия, ишемическая болезнь сердца, инфаркт миокарда, первичная легочная гипертензия, бронхиальная астма, невротическая депрессия, эпилепсия, нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона), сахарный диабет, импотенция и др.
Клиренс NO (скорость очищения крови от NO в процессе его химических превращений) происходит путем образования нитритов и нитратов и составляет в среднем не более 5 секунд. В клиренс могут быть вовлечены промежуточные ступени, связанные со взаимодействием с супероксидом или с гемоглобином с образованием пероксинитрита. Оксид азота может быть восстановлен NO-редуктазой – ферментом, тесно связанным с NO-синтазой.
Применение
Полезное
Смотреть что такое «Окись азота» в других словарях:
ОКИСЬ АЗОТА — ОКИСЬ АЗОТА, см. монооксид АЗОТА … Научно-технический энциклопедический словарь
окись азота — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN nitric oxide … Справочник технического переводчика
окись азота — azoto oksidas statusas T sritis ekologija ir aplinkotyra apibrėžtis Azoto junginys su deguonimi: N₂O, NO, NO₂, N₂O₃, N₂O₄, N₂O₅. atitikmenys: angl. nitric oxide; nitrogen monoxide vok. Stickoxid, n; Stickstoffmonoxid, n rus. окись азота, f … Ekologijos terminų aiškinamasis žodynas
Азота окислы — соединения азота с кислородом. Известны N2O, NO, N2O3, NO2 (и его димер N2O4), N2O5; есть сведения о существовании NO3, не выделенного в свободном состоянии. При высокой температуре в пламени вольтовой дуги, а в природе при электроразряде … Большая советская энциклопедия
азота окись — azoto(II) oksidas statusas T sritis chemija formulė NO atitikmenys: angl. nitrogen monoxide; nitrogen(II) oxide rus. азота окись; азота(II) оксид ryšiai: sinonimas – azoto monoksidas … Chemijos terminų aiškinamasis žodynas
азота(II) оксид — azoto(II) oksidas statusas T sritis chemija formulė NO atitikmenys: angl. nitrogen monoxide; nitrogen(II) oxide rus. азота окись; азота(II) оксид ryšiai: sinonimas – azoto monoksidas … Chemijos terminų aiškinamasis žodynas
Окись этилена — Окись этилена … Википедия
Окись — Оксид (окисел, окись) соединение химического элемента с кислородом, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам… … Википедия
Окись углерода — Монооксид углерода Общие Систематическое наименование Монооксид углерода Химическая формула … Википедия
Окислы азота — С кислородом азот образует ряд соединений N2O5 азотный ангидрид [О над азотной кислоте см. Крепкая водка.], N2O4 или NO2 азотноватый ангидрид или двуокись азота, N2O3 азотистый ангидрид, NO окись азота, N2O закись азота. Определения Фавра,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона