Что такое остеобласты и остеокласты
Что такое остеобласты и остеокласты
Репаративная регенерации костной ткани представляет собой восстановление после повреждения. Этот процесс имеет большое значение для практической медицины. Костная ткань уникальна, поскольку кость способна полностью восстанавливать даже значительные дефекты в отличие от всех других тканей, в которых регенерация завершается образованием соединительнотканного рубца или гипертрофией органа.
Единого определения термина «репаративная регенерация» не существует. Одни авторы утверждают, что это разновидность физиологической регенерации, которая происходит в условиях экстремальных воздействий на организм, но отличается большей интенсивностью. Другие характеризуют ее как сложный процесс, который вызван разрушением костных структур, количественно превышающий допустимые пределы физиологической регенерации и направленный на восстановление целостности и обеспечения функции.
Процессы регенерации костной ткани челюстно-лицевой области представляют собой сложное переплетение ряда общих воздействий на системном уровне и локальных изменений тканевого метаболизма, включая изменения на молекулярном уровне. В основе репаративной регенерации лежат дифференцировки клеток, их пролиферация, резорбция поврежденной ткани и новообразования кости в ходе ремоделирования, а также формирования органического внеклеточного матрикса с последующей его минерализацией.
Стадии заживления костной ткани челюстно-лицевой области
При заживлении переломов выделяют следующие четыре стадии: репаративная реакция, формирования сращений костных отломков, сращение костных отломков, функциональная перестройка костной мозоли и отломков с формированием органной структуры.
В настоящее время исследователи выделяют несколько стадий репаративной регенерации:
Катаболизм тканей, дифференциация и пролиферация клеточных элементов.
Образование и дифференциация новых тканевых структур.
Формирование сосудистых образований для питания новой ткани.
Перестройка первичного регенерата.
В первой стадии, репаративной реакции кости, различают такие фазы, как острое посттравматическое нарушение тканевого кровоснабжения, некроз клеток с дезорганизацией клеточных структур, пролиферацию нежизнеспособных мезенхимальных стволовых клеток и дифференциацию пролиферирующих клеток в направлении образования костного дифферона (мезенхимальная стволовая клетка — преостеобласт — остеобласт — остеоцит).
Острые посттравматические нарушения тканевого кровоснабжения в области перелома сопровождаются разрывом периоста, эндоста, каналов остеонов, а также костного мозга, сосудов и нервов, мышечной и соединительной тканей, окружающих кость. Данные процессы сопровождаются кровоизлияниями, отеком, макрофагальной инфильтрацией и развитием диффузных ишемических дегенеративнонекротичних изменений в тканях. Указанная фаза продолжается порядка 6-18 часов с момента перенесенной травмы.
Вторая фаза, длительностью 10-24 часов после травмы, сопровождается дезорганизацией структур костной ткани, признаками некроза и макрофагальной клеточной инфильтрацией.
В третьей фазе, которая приходится на промежуток 24-72 часа с момента перелома, на фоне восстановленного кровоснабжения наблюдается пролиферация мезенхимальных стволовых клеток, перицитов микроциркуляторного русла, периоста, эндоста с формированием остеогенной ткани. В зависимости от расположения пролиферирующих клеток выделяют периостальные (клетки периоста), эндостальные (клетки костного мозга) и интермедиарные (клетки костного мозга и сосудов центральных каналов) костные образования.
Четвертая фаза репаративной реакции сопровождается пролиферацией и дифференциацией остеогенных клеток в преостеобласты и остеобласты. Они синтезируют остеоид, который после минерализации превращается в грубоволокнистую костную ткань. Наблюдается активация остеокластов, что резорбируют некротизированную костную ткань.
На стадии формирования сращений костных отломков, которая наступает на 3-5 сутки с момента травмы, образуется костный регенерат, или мозоль, который распространяется в проксимальном и дистальном направлениях. Спустя 2-6 недель этот процесс приводит к слиянию и консолидации костных отломков.
Последняя стадия заживления перелома характеризуется образованием костных сращений, которые могут быть нескольких типов. Первичное костное сращение сопровождается прямым сращиванием отломков на уровне кортикального слоя с формированием новых остеонов. Фиброзно-хрящевое сращение характеризуется развитием в зоне перелома некроза костной и мягких тканей, вялой репаративной реакцией, развивающейся на значительном расстоянии от места перелома, и преимущественным развитием фиброзной, реже хрящевой ткани.
Сложившееся фиброзно-хрящевое сращение кости в результате длительной оссификации может замещаться костной тканью, образуя вторичное сращение костных отломков. В четвертой стадии происходит функциональная перестройка костной мозоли и сросшихся отломков с формированием органной структуры кости.
Клетки и вещества, участвующие в репаративной регенерации костной ткани
Процесс регенерации костной ткани челюстно-лицевой области происходит при участии таких клеток, как остеобласты, остеокласты или остеоциты. Ниже приведена краткая характеристика этих клеточных элементов с указанием особенностей их структуры и функций.
Остеобласты представляют собой костеобразующие клетки, которые происходят из мезенхимальных стволовых клеток. Они округлой формы, размером 20-30 мкм, с эксцентрично расположенным ядром. Эти клетки располагаются в остеогенном слое надкостницы и в периваскулярных пространствах остеонов.
Выделяют четыре типа остеобластов, участвующих в заживлении костной ткани: преостеобласты, пролиферирующие функционально активные остеобласты, созревающие с гипертрофированной эндоплазматической сетью остеобласты, а также дифференцированные малоактивные остеобласты. Основная часть остеобластов синтезируют костную ткань, пока не наступит остановка их функции с последующим превращением их в неактивные клетки.
Эти клетки выстилают поверхность вновь созданной костной ткани, и при помощи системы канальцев соединяется с остеоцитами. Определенная часть остеобластов инкапсулируется в остеоидный матрикс и дифференцируются в остеоциты.
Остеобласты имеют развитый аппарат Гольджи и митохондрии, благодаря чему синтезируют огромное количество межклеточного вещества, в частности протеины и коллагеновые волокна, которые образуют органический костный матрикс — остеоид. Остеобласты синтезируют коллаген I типа из проколлагена, который состоит из одной α2- и двух α1-полипептидных цепочек, образующих спиральную структуру.
Молекула проколлагена содержит два конечных пептида: амино- и карбокситерминальные пропептиды. После секреции проколлагена остеобластами в экстрацеллюлярное пространство эти два пропептида под влиянием энзимов отщепляются от проколлагена, который трансформирутеся в тропоколлаген.
Свободные конечные пропептиды костной ткани попадают в циркулирующую кровь, где можно определить их концентрацию иммуноферментным методом. Этот анализ очень точно указывает на количество синтезированного коллагена I типа, причем уровень аминотерминального пропептида наиболее точно характеризует его метаболизм.
Также остеобласты синтезируют неколлагеновую фракцию белков костного матрикса, которым принадлежит ведущая роль в его минерализации. Это остеокальцин, остеопонтин, остеонектин, и костный сиалопротеин.
Остеокальцин — основной неколлагеновых белок кости, который участвует в связывании кальция и гидроксиапатитов. Он оказывает хемотаксическое воздействие на остеокласты и принимает участие в резорбции кости.
Остеонектин связывает коллаген I типа и гидроксиапатит, принимает участие в образовании начального кристалла (нуклеации) при минерализации кости. Остеопонтин также связывает костные клетки с гидроксиапатитом внеклеточного пространства, но исследования последних лет указывают на участие этого белка в метастазировании опухолей путем облегчения адгезии опухолевых клеток в процессе инвазии.
Костный сиалопротеин содержит сиаловые кислоты. Он является кальцийсвязывающим гликопротеином, обеспечивающим минерализацию и стабилизации структуры коллагена.
Остеоциты, или «звездчатые клетки», имеют большое количество длинных и тонких отростков. Они делятся на три типа, характеристики которых кратко перечислены ниже:
Остеоциты I типа, продуцирующие клетки, синтезируют компоненты костного матрикса.
Остеоциты II типа, зрелые или резорбирующие клетки, участвуют в процессе остеолиза.
Остеоциты III типа, дегенерирующие клетки, располагаются на периферии остеона. Вследствие их деструкции высвобождается значительное количество лизосомальных ферментов и происходит остеолизис костной ткани.
Остеоциты имеют рецепторы к паратгормону, синтезируют остеокальцин, матриксные протеины и склеротин, который является ингибитором Wnt-сигнала в остеобластах. Главной их функцией является передача механического и химического сигналинга остеобластам, покровным клеткам и через них — остеокластам. Эта цепочка играет важную роль для запуска процессов ремоделирования кости в физиологических и в патологических условиях.
Остеокласты представляют собой многоядерные гигантские клетки, которые обеспечивают резорбцию компонентов костного матрикса. Они расположены на поверхности кости в небольших углублениях (эрозионные лакуны или лакуны Хаушипа). В местах контакта с участками резорбции кости цитоплазма остеобластов образует выросты в виде гофрированной каймы, что увеличивает площадь контакта с костью и облегчает поступление в зону резорбции биологически активных клеточных продуктов.
Также остеокласты секретируют в зону резорбции протоны и протеолитические ферменты (катепсин К, цистеинпротеазу, матриксные металлопротеиназы) и удаляют через базолатеральную мембрану продукты распада в окружающее пространство. Для осуществления такого транспорта необходимо присутствие тартратрезистентной кислой фосфатазы (ТРКФ). Существует 5 видов кислых фосфатаз, которые производятся костной тканью, селезенкой, эритроцитами, тромбоцитами и макрофагами. Все виды кислых фосфатаз ингибируются тартратом, кроме пятой изоформы, которая называется ТРКФ-5.
Остеокластогенез, остеобластогенез и ремоделирование кости
Различают следующие функциональные типы остеокластов: молодые, зрелые, функционально активные и неактивные, а также погибающие. Источником происхождения всех остеокластов являются макрофагально-моноцитарные клетки костного мозга.
Важная роль в остеокластогенезе принадлежит системе RANK / RANKL / OPG, которая была открыта в 1997 году. RANKL, экспрессируемый на поверхности остеобластов, связывается с RANK-рецептором, который расположен на мембранах клеток-предшественников остеокластов. Это запускает дифференциацию и активацию остеокластов. Взаимодействие RANKL и RANK происходит в присутствии макрофагального колониестимулирующего фактора (M-CSF), который при помощи высокоафинных трансмембранных рецепторов (c-fms) активирует внутриклеточную тирозинкиназу и стимулирует пролиферацию и дифференциацию предшественников остеокластов, мононуклеаров.
Было доказано, что активность M-CSF значительно повышается при воздействии на остеобласты паратиреоидного гормона, витамина Д3 и фактора некроза опухолей (TNF), однако снижается при воздействии OPG и эстрогенов.
Обнаружено, что продукцию остеокластов стимулирует паратиреоидный гормон. Он синтезируется паращитовидными железами. Гормон поддерживает гомеостаз кальция путем вымывания из кости во внеклеточную жидкость и усиление реабсорбции в канальцах почек. Этот гормон активирует синтез кислой фосфатазы, лактата и цитрата, и подавляет синтез коллагена и щелочной фосфатазы.
При резком повышении уровня паратгормона в крови наблюдается активация зрелых остеоцитов и резорбция кости (остеоцитарный остеолиз). При длительной гиперсекреции паратгормона усиливается остеокластогенез и снижается активность остеобластов, что также подавляет синтез коллагена. Доказано, что длительное введение малых доз паратгормона вызывает анаболический эффект, а это, наоборот, способствует созреванию хрящевой ткани. Он способствует синтезу в почках 1,25-(ОН)-2D3 под влиянием циклического АМФ из 25-(ОН)-2D3.
В отличие от паратгормона, кальцитонин, который секретируется в межфолликулярных клетках щитовидной железы, уменьшает количество и активность остеокластов в костной ткани, подавляет остеоцитарный остеолиз и уменьшает уровень кальция в крови. Кальцитонин стимулирует созревание хондроцитов в эпифизарном хряще.
Согласно зарубежным исследованиям последних лет, ведущая роль в регуляции остеобластогенеза принадлежит костным морфогенетических белкам (BMP, bone morphogenetic protein). Это группа сигнальных факторов роста (цитокины), которыеактивно стимулируют формирование энхондральной костной ткани и регулируют различные клеточные процессы (пролиферацию, дифференцировку, апоптоз, хемотаксис, ангиогенез или продукцию внеклеточного матрикса в тканях).
BMP запускают процесс образования костной ткани за счет экспрессии генов, регулирующих процессы дифференциации мезенхимальных стволовых клеток с последующим образованием клеток-остеобластов. Нарушение регуляции сигнальной системы BMP очень часто обнаруживаются при онкологических заболеваниях.
В настоящее время были описаны 47 белков подсемейства BMP, взаимодействующих со специфическими BMP-рецепторами (BMPs). В процессе межклеточных взаимодействий в костной ткани челюстно-лицевой области особенно важны следующие:
BMP2: стимулируют дифференцировку остеобластов.
BMP3: способствуют образованию новой костной ткани.
BMP7: активируют дифференцировку остеобластов и продукцию SMAD1.
BMP8a: принимают непосредственное участие в развитии кости и хряща.
В практической медицине BMP используют для стимуляции процессов заживления кости. Их вводят в костный имплантат, откуда они попадают в места перелома для улучшения остеогенеза.
Костные клетки интенсивно выделяют в межкостный матрикс трансформирующий фактор роста β1 (ТGFβ1), который активирует дифференциацию мезенхимальных стволовых клеток по остеобластическому и хондральному типу, стимулируют процессы репаративной регенерации костей, усиливают пролиферацию и синтез коллагена.
Процессы, связанные с морфогенезом клеток, регулирует также Wnt-сингалинг. Этот процесс включает белки, открытые в начале 1980-х годов как маркеры некоторых видов онкологических заболеваний. Они являются также ключевыми регуляторами процессов ремоделирования и регенерации костной ткани, дифференцировки мезенхимальных стволовых клеток.
В основе канонического пути Wnt-сигналинга в костной ткани лежит стабилизация белка цитоплазмы β-катенина. При отсутствии сигнала он неактивен и быстро разрушается. При активации β-катенина через Wnt, сам Wnt связывается с поверхностными рецепторами клеток, в качестве которых выступает трансмембранный белок Фрайзленда. В результате этого тормозится разрушения β-катенина, он накапливается в цитоплазме и после проникает в ядро. Там он взаимодействует с белками TCF / LEF, которые избирательно связываются с определенными белками-активаторами и последовательностями ДНК.
Таким путем происходит активация определенных генов, отвечающих за регенерацию костной ткани. Другой, или неканонический (β-катениннезависимый) путь Wnt-сигналинга регулирует полярность клеток, стимулирует метаболизм кальция и реорганизацию цитоскелета. Передача Wnt-сигналов стимулирует продукцию OPG. Доказано, что у человека в активации Wnt-сигналинга привлечено как минимум 22 Wnt-лигандов.
Антагонистом Wnt / β-катенинсигнального пути является склеротингликопротеид, который производится остеоцитами неповрежденной кости. Он препятствует дифференцировке MSC. При возникновении повреждений костной ткани челюстно-лицевой области остеоциты передают сигнал покровным клеткам, которые выстилают поверхность трабекулы. Под влиянием простагландинов и факторов роста, которые при этом выделяются, покровные клетки отслаиваются от поверхности кости, образуя специфический навес. Клетки навеса сочетаются с остеоцитами, с капилляром и образуют компартмент костного ремоделирования.
Недавно были открыты такие регуляторы межклеточных взаимодействий между остеобластами и остеокластами, как семафорины и их рецепторы плексины. Cемафорины образуют семейство молекул из 8 основных классов секреторных и трансмембранных белков, которые отвечают за передачу сигналов по аксонам. Они регулируют рост, развитие и функционирование клеток нервной, сердечно-сосудистой, иммунной, дыхательной, а также опорно-двигательной систем.
В частности, Semaphorin 4D (Sema4D), который является производным остеокластов, действует на мембранный рецептор Plexin-B1 на поверхности остеобластов, подавляя функцию последних. В результате наблюдается активация резорбции костной ткани. Семафорин 3В способствует активации остеокластов, а семафорин 3А, наоборот, стимулирует остеогенез. Исходя из этого, для лечения остеопении важное значение имеет ингибирование семафоринов 4D и 3В.
Важным секреторным производным остеокластов является белок SLIT3. Он стимулирует пролиферацию клеток-остеобластов благодаря активации β-катенинового пути. Аутокринная сигнализация SLIT3 ингибирует резорбцию костной ткани путем подавления дифференцировки преостеокластов. В экспериментальных исследованиях было показано, что модифицированные животные с отсутствием SLIT3 или его рецептора Robo 1 имеют низкие показатели образования костной ткани и высокую скорость ее резорбции.
Практическая оценка процессов регенерации костной ткани
Маркеры синтеза костной ткани косвенно характеризует активность остеобластов. Эти клетки принимают активное участие в формировании костной ткани, производят коллаген I типа плюс другие компоненты остеоида, участвуют в минерализации остеоида гидроксиапатитом.
Первым биохимическим маркером костного ремоделирования является фермент щелочная фосфатаза, который в 1929 году был введен в клиническую практику и сегодня применяется. Существует 4 изоформы этого фермента: костная, печеночная, кишечная и плацентарная.
Лабораторным показателем активности остеобластов является костная щелочная фосфатаза. Это гликопротеин, который принимает участие в минерализации костного матрикса. Одновременное повышение КЩФ и паратгормона может указывать на развитие остеодистрофии с высоким уровнем костного ремоделирования, а снижение этих показателей может свидетельствовать об адинамическом состоянии костной ткани челюстно-лицевой области.
Наиболее информативным маркером формирования кости является остеокальцин. Этот неколлагеновый белок костного матрикса, содержащий гидроксиапатит, может считаться специфическим для костной ткани и дентина. Он синтезируется преимущественно остеобластами и формирует внеклеточный матрикс кости.
Фракция вновь синтезированных остеокластов высвобождается в кровоток, поэтому именно этот маркер указывает на скорость ремоделирования костной ткани. Повышенный уровень паратгормона в крови подавляет активность остеобластов, продуцирующих остеокластов, и снижает концентрацию остеокластов в крови и костной ткани.
В процессе синтеза коллагена I типа остеобластами с проколлагена I типа от него в результате действия специфических ферментов отделяются амино- и карбокситерминальные фрагменты. Соотношение между количеством зрелого коллагена, откладывающегося в костный матрикс, и количеством терминальных молекул, которые поступают в кровеносное русло, должно быть равно единице. Благодаря этому по показателям АКФ, ККФ в сыворотке крови можно судить о синтетической активности остеобластов по синтезу коллагена I типа.
Следующая группа показателей костного ремоделирования — это маркеры резорбции костной ткани. Следует отметить, что они в течение суток меняют свой уровень, поэтому определять их необходимо в одно и то же время суток, лучше утром. К маркерам резорбции костной ткани относятся ферменты, участвующие в разрушении костного матрикса под влиянием остеобластов, и продукты разрушения коллагена I типа.
Это, например, тартратрезистентная кислая фосфатаза (TRAP) — металлосодержащий энзим, один из 6 изоферментов кислой фосфатазы. Он секретируется остеобластами в внеклеточную среду во время резорбции. Существуют формы TRAP-5а и 5в, но TRAP-5в синтезируется остеобластами, а TRAP-5а имеет макрофагальное происхождение. Активность TRAP-5в в плазме крови является показателем процессов резорбции кости.
Гидроксипролин является основной аминокислотой в составе коллагена. Он не считается аутоспецифичным маркером костной ткани, ведь только 50% этой аминокислоты находится в костях, а остальные 50% являются компонентом других белков, в частности эластина, ацетилхолинэстеразы и фактора комплемента С1q.
Большая часть его после разрушения коллагена окисляется в печени и только 15% выводится с мочой. Содержание гидроксипролина зависит от характера питания, возраста человека, наличия опухоли с распадом и демонстрирует циркадный ритм с пиком между 0.00 и 8.00 утра.
14% аминокислотного состава коллагена составляет оксипролин. Он синтезируется остеобластами и также является маркером костной резорбции. В наше время используют более специфические маркеры костной резорбции, такие как продукты распада коллагена I типа. К ним относятся пиридинолин (ПИД) и дезоксипиридинолин (ДПИД). Они находятся в тканях, содержащих коллаген I, II, III типа. ПИД является важным химическим соединением, но ДПИД встречается только в коллагене, поэтому его оценивают как селективный костный маркер.
Также широко применяют в медицинской практике определение показателей пептидов коллагена I типа, NTX и СTX. Уникальность этих показателей заключается в быстром росте их уровня при заболеваниях, сопровождающихся высокой резорбцией костной ткани (например, при остеопорозе, метастазах в кости), а также быстрому их снижению (в течение нескольких недель) на фоне антирезорбтивной терапии.
Следующий маркер резорбции костной ткани — это костный сиалопротеин (BSP). В процессе остеолиза (физиологического или патологического) происходит разрушение костного матрикса ферментами остеобластов с выделением в кровь сиалопротеина с соответствующим ростом лабораторных показателей BSP. Костный сиалопротеин присутствует только в зрелых остеобластах и не обнаруживается в их предшественниках, поэтому BSP может служить маркером поздней дифференцировки клеток кости.
Репаративная регенерация костной ткани челюстно-лицевой области связана с деятельностью остеогенных клеток. В основе локальной регуляции репаративной регенерации лежат несколько сигнальных путей, такие как молекулярная система RANK / RANKL / OPG, костные морфогенетические белки, Wnt-сигналинг и другие.
Остеобластогенез и остеокластогенез характеризует биохимические маркеры костного ремоделирования, определение которых позволяет установить скорость обменных процессов в костной ткани, выявлять пациентов с повышенным риском и проводить раннюю оценку эффективности назначенного лечения, прогнозировать риск возникновения осложнений, диагностировать на ранних сроках появление костных метастазов и др.
Что такое остеобласты и остеокласты
Развитие костной ткани на месте хряща протекает несколько сложнее, чем остеогистогенез, совершающийся непосредственно в мезенхиме. В этом случае развитию костной ткани предшествует образование хрящевой модели трубчатой кости, выполняющей опорную функцию на докостной стадии формирования скелета. Исходными клетками являются камбиальные клетки надхрящницы — адвентициальные. При подрастании к надхрящнице кровеносных сосудов и улучшении условий трофики и оксигенации эти клетки дифференцируются не в хондробласты, а в остеобласты, вырабатывающие межклеточное вещество ретикулофиброзной костной ткани. Они образуют подобие костной манжетки, окружающей хрящевую модель будущей трубчатой кости. Так возникает перихондральная костная ткань и надкостница. Окруженные костной тканью хрящевые клетки, утратившие связь с источником питания, подвергаются дегенерации. В возникшие полости дегенерирующего хряща из надкостницы врастают кровеносные сосуды с расположенными вокруг них камбиальными клетками. Некоторые из них превращаются в остеобласты, обусловливающие энхондральное развитие ретикулофиброзной костной ткани. Клетки, которые замуровываются в межклеточное вещество, дифференцируются в остеоциты, а периферически расположенные клетки — остеобласты — размножаются и продолжают синтез и секрецию компонентов межклеточного вещества. Все эти процессы первоначально протекают в середине хрящевой модели трубчатой кости (диафизе) и распространяются в проксимальном и дистальном направлениях.
В зоне контакта хрящевой и костной тканей можно выделить зоны неизмененного хряща, размножающихся хондроцитов, формирующих клеточные колонки, зону дегенерации и замещения хряща костной тканью. Зона размножающихся хрящевых клеток определяет зону роста будущей кости и важна для формирования вектора роста кости.
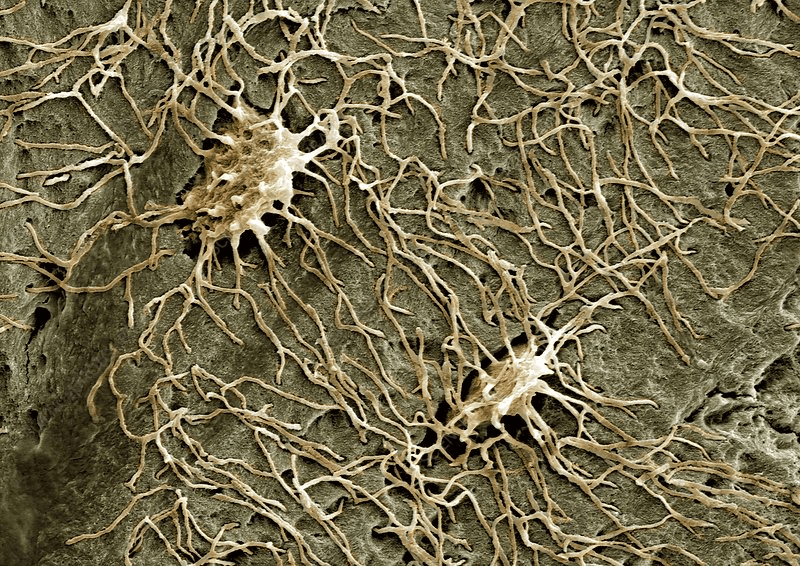
Одновременно с формированием ретикулофиброзной костной ткани, содержащей остеобласты и остеоциты, возникает другой гистогенетический тип клеток — остеокласты. Это крупные многоядерные (до 20-100 ядер) клетки размером до 100 мкм в диаметре являются производными стволовой кроветворной клетки. Цитоплазма остеокластов оксифильна со слабо развитой эндоплазматической сетью. Хорошо развит комплекс Гольджи. В цитоплазме много лизосом, содержащих кислую фосфатазу, коллагеназу, карбоангидразу и другие ферменты. Особенно много лизосом в той части цитоплазмы остеокластов, которая обращена к разрушаемой ткани. На этой поверхности имеются многочисленные выросты цитоплазмы, образующие подобие «щеточной (гофрированной) каемки». Остеокласты специализированы на «внеклеточной работе» лизосом: гидролитические ферменты из них выходят и резорбируют межклеточное вещество. Методами микрокиносъемки показано, что остеокласты подвергают деминерализации и разрушению оссеиновые волокна и аморфное вещество, а затем макрофаги фагоцитируют остатки органического субстрата. Остеокласты разрушают хрящевую ткань и ретикулофиброзную костную ткань, формируя каналы для врастающих сосудов и проникновения остеобластов.
Последующие стадии гистогенеза складываются из процессов новообразования костной ткани, ее разрушения остеокластами и перестройки — ремоделирования. Важным фактором гистогенеза пластинчатой костной ткани, входящей в состав трубчатой кости, является вектор роста кости. Он определяет направление движения остеокластов, следовательно, формирования каналов и врастание в них кровеносных сосудов (по вектору роста). Кровеносный сосуд, в свою очередь, определяет упорядоченное (концентрическое) расположение остеобластов вокруг себя. При этом остеобласты синтезируют межклеточное вещество, оссеиновые волокна которого упорядоченно (параллельно) располагаются возле остеобласта и при минерализации формируют костную пластинку, толщиной 3-10 мкм. Соседняя костная пластинка содержит оссеиновые фибриллы, которые располагаются под углом по отношению к первым.
На протяжении гистогенеза и всей возрастной динамики костной ткани в ней происходит непрерывная перестройка благодаря согласованной деятельности остеобластов и остеоцитов, образующих межклеточное вещество, а также остеокластов, разрушающих костную ткань, что необходимо для процессов ее самообновления. Так происходит смена генераций костных пластинок и формирующихся структурно-функциональных единиц — остеонов, достигается упорядоченность расположения последних, следовательно, высокая механическая прочность костной ткани и кости как органа (см. кость).
Дентиноидная костная ткань отличается отсутствием тел костных клеток в толще межклеточного вещества. Дентин — это вещество, состоящее из коллагеновых волокон и основного аморфного вещества, пропитанного минеральными солями. Образующие дентин зуба клетки — одонтобласты (точнее — их ядросодержащая часть) — расположены вне дентина в пульпе зуба. Дентин пронизан дентинными канальцами, в которых проходят отростки одонтобластов. Сходное строение имеет цемент зуба.
Ретикулофиброзная (грубоволокнистая) костная ткань характеризуется беспорядочным расположением оссеиновых фибрилл в виде толстых, плотных пучков волокон и основного аморфного вещества. Такая костная ткань образует кости в зародышевом и раннем постнатальном периодах. У взрослого человека она сохраняется лишь на месте прикрепления сухожилии к кости, в зарастающих швах черепа, а также в составе тканевого регенерата на месте переломов костей.
Пластинчатая костная ткань отличается упорядоченным расположением оссеиновых фибрилл в составе костных пластинок. Последние образуют расположенные один за другим слои пропитанного солями кальция фибрилл, образованных остеобластами. Слои имеют толщину от 3-7 до нескольких сотен микрометров. Каждая костная пластинка состоит из параллельно ориентированных тонких оссеиновых (коллагеновых) волокон (коллаген 1-го типа). Но коллагеновые волокна двух прилежащих друг к другу костных пластинок ориентированы под разными углами. Костная пластинка соединяется с соседней пластинкой коллагеновыми фибриллами. Так создается прочная волокнистая основа кости. Костные пластинки располагаются концентрически вокруг сосудов, то есть формируют остеоны — структурно-функциональные единицы пластинчатой кости как органа. Кроме этого существуют наружные и внутренние окружающие и вставочные пластинки трубчатой кости (см. ниже).
Регенерация. В регенерации костной ткани участвуют детерминированные остеогенные элементы в составе надкостницы, механоциты костного мозга, которые размножаются и дифференцируются в остеобласты. Продуцируя межклеточное вещество, остеобласты дифференцируются в остеоциты и образуют ретикулофиброзную костную ткань. Кроме того, адвентициальные клетки волокнистой соединительной ткани надкостницы также принимают участие в регенерации костной ткани. Однако дифференцировка их во многом зависит от микроокружения, внетканевых и внеорганных факторов (например, от репозиции отломков, неподвижности отломков, оксигенации места перелома и др.).
Дифференцировка адвентициальных клеток возможна в трех направлениях: остеогенном, хондрогенном, фибробластическом. Этим определяется соотношение различных видов тканей в регенерате. При преимущественно остеобластическом гистогенезе формируется ретикулофиброзная костная ткань, которая постепенно ремоделируется с образованием костной ткани, напоминающей по своему строению пластинчатую.