Микрофлора влагалища. Зачем нам нужны бактерии?
Что представляет микрофлора влагалища в норме?
Какие микроорганизмы относятся к условно-патогенным?
Если в массе микрофлоры уменьшается количество лактобацилл, то условно- патогенные микроорганизмы начинают вести себя агрессивно и способны вызвать следующие заболевания в зависимости от того, какие микробы более активны:
Заболевания, ассоциированные с условно-патогенными микроорганизмами – так принято называть данную группу болезней.
Почему нарушается микрофлора влагалища?
Чем опасно нарушение микрофлоры влагалища?
Нарушения микрофлоры могут проявляться выделениями белого или сероватого цвета, иногда с неприятным запахом. Возможны зуд и жжение при мочеиспускании. А могут вообще не проявляться. Но в любом случае нарушение баланса микрофлоры может вызвать следующие состояния:
Как можно выявить нарушения влагалищной микрофлоры?
Самый точный метод – ПЦР. Но здесь присутствует важный момент: для комплексной и полной оценки микрофлоры нужны специальные анализы, определяющие уровень лактобацилл как самых главных и нужных; и уровень условно-патогенных микроорганизмов по отношению к лактобациллам. К таким тестам относят:
Как понять результат исследования?
Рашифровкой занимается врач. Ответ может быть в виде графика (Фемофлор) и заключения (Флороценоз)
Если лактобациллы преобладают – значит, всё хорошо. Если лактобацилл мало или их нет, а преобладает любой тип УПМ – врач сопоставляет данные осмотра, жалоб и лабораторного заключения, ставит диагноз и назначает лечение.
Обследуйтесь своевременно с лабораторией KDL и будьте здоровы!
Нужно ли избавляться от условно-патогенной флоры?
Мы – дом для бактерий, вирусов и грибов. Это не хорошо и не плохо, просто данность. Оставить только хорошие микроорганизмы, поднять иммунитет при помощи БАДов, избавиться выборочно только от условных патогенов не получится. Главное правило здорового человека в вопросе микрофлоры – «если все работает – не трогай».Разбираемся с условными патогенами и рассказываем, когда все-таки надо обращаться к врачу.
Что значит условно-патогенная
Патоген – это микроорганизм или чужеродный белок, который может вызвать заболевание. Словосочетание «условно-патогенный» означает то, что этот белок может вызвать болезнь только в определенных условиях:
Условно-патогенная флора есть у всех людей: и здоровых и больных. Мы не можем сделать так, чтобы на нашей коже и слизистых оболочках жили только хорошие бактерии: выбрать не получится.
Микроорганизмы заселяют человека с рождения: они передаются по родовым путям от матери, после контакта кожа-к-коже в первые месяцы жизни. Условные патогены хорошо уживаются с остальными и формируют уникальную микробиоту – индивидуальный набор бактерий каждого человека. Состояние иммунитета отчасти зависит от баланса видов бактерий, в норме хороших микроорганизмов больше. А условно-патогенные микроорганизмы размножаются медленно, они не дают иммунитету расслабиться.
К ним относятся: грибки кандиды, стафилококки, энтеробактерии, живущие в кишечнике, например, энтерококк фекальный, кожный клещ демодекс.
Где обитает
Условно-патогенные микроорганизмы живут:
Эти микроорганизмы есть у всех: на коже одни, в кишечнике другие, во влагалище третьи.
Лаборатории предлагают сдавать тесты (образцы кала, соскобы со слизистых оболочек или кожи) на микрофлору. Если у человека нет специфических жалоб – то делать этого не нужно. Баланс между хорошими микроорганизмами и патогенными динамичен: сегодня результат один, а завтра может быть другой.
Эти анализы не показывают полное соотношение хороших и плохих микроорганизмов, не дают возможность увидеть весь микробиом, а отображают его в ограниченном варианте (только из места, где взяли соскоб, например). Такие исследования без обоснованного назначения путают человека, они бесполезны для грамотного врача.
«Часто пациенты на приеме говорят, что у них высеялась кишечная палочка в секрете простаты, которую они хотят устранить, – комментирует Риназ Камалетдинов. – Но без клинических проявлений, без воспалительных изменений это состояние не нуждается в лечении».
Можно ли избавиться
Но после убийства условных патогенов:
В результате настоящим патогенам будет проще проникнуть в ослабленный организм и вызвать заболевание.
«Самолечение антибиотиками и другими препаратами для уничтожения условно-патогенных микроорганизмов приводит к антибиотикорезистентности, – предупреждает Мария Волкова. – Это означает, что бактерии становятся невосприимчивыми к препарату. Чем больше таких стойких или резистентных бактерий будет в мире, тем сложнее будет лечить инфекционные болезни».
Нужно ли лечение
Здоровому человеку не стоит вмешиваться в деятельность микроорганизмов. Лечение условно патогенной флоры только «по анализам» не проводят.
«Навсегда избавиться от условно-патогенной микрофлоры не удастся, – дополняет Риназ Камалетдинов. – И не нужно ставить перед собой такую цель. Задача врача – помочь справиться с воспалительным процессом, который появился из-за избытка бактерий или грибков».
Нужно лечить условно-патогенную микрофлору, которая размножилась, вышла из-под контроля и вызвала воспалительный процесс.
«Воспалительные заболевания органов малого таза у женщин, вызванные условно патогенной флорой, могут потребовать оперативного вмешательства, приводить к бесплодию, быть причиной неудачных попыток ЭКО, – объясняет Мария Волкова. – В случае наступления беременности повышается вероятность её прерывания, преждевременного излития околоплодных вод, преждевременных родов, инфицирования новорожденного и осложнений в послеродовом периоде для матери».
Примеры болезней, вызванных условно-патогенной флорой:
«Мужчинам стоит помнить, что простатит, вызванный кишечной палочкой, может повлиять на потенцию, – предупреждает Риназ Камалетдинов. – Если появились боли и трудности с мочеиспусканием – нужно обратиться к врачу, а не начинать самостоятельное лечение антибиотиками».
Когда лечить обязательно
Условно-патогенная флора опасна для людей с иммунодефицитами. Они бывают первичными (врожденные патологии) и вторичными: на фоне тяжелой болезни.
Состояния, которые приводят ко вторичным иммунодефицитам:
Если у человека есть одно из вышеперечисленных состояний, это не значит, что нужно сдавать анализы на флору, делать посевы кала, пить антибиотики для профилактики. Нужно более пристально следить за здоровьем и не игнорировать любые неприятные симптомы. С ними можно обратиться к семейному врачу, терапевту или напрямую к узкому специалисту, который занимается основным лечением.
Патогенные микроорганизмы и их основные характеристики
Инфекция – сложный биологический процесс, возникающий в результате проникновения патогенных микробов в организм и нарушения постоянства его внутренней среды. Возникновение инфекции зависит от нескольких факторов: степени патогенности (вирулентности) микроба, состояния макроорганизма и условий внешней среды.
Патогенность – это способность микроба определенного вида при соответствующих условиях вызывать характерное для него инфекционное заболевание. Следовательно, патогенность есть видовой признак.
Токсичность – способность патогенного микроба вырабатывать и выделять ядовитые вещества, вредно действующие на организм. Токсины бывают двух видов – экзотоксины и эндотоксины.
Экзотоксины – выделяются в окружающую среду при жизни микробов в организме или на искусственных питательных средах, а также в пищевых продуктах. Они очень ядовиты. Например, 0,005 мл жидкого столбнячного токсина или 0,0000001 мл ботулинического токсина убивает морскую свинку. Микробы, способные образовывать токсины, получили название токсигенных Под влиянием нагревания и света экзотоксины легко разрушаются, а под действием некоторых химических веществ теряют токсичность. Эндотоксины прочно связаны с телом микробной клетки и освобождаются только после ее гибели и разрушения. Они весьма устойчивы при действии высоких температур и не разрушаются даже после нескольких часов кипячения. Ядовитое действие многих бактерийных экзотоксинов связано с ферментами – лецитиназой (разрушает эритроциты), коллагеназой, гиалуронидазой (расщепляет гиалуроновую кислоту) и рядом других ферментов, которые производят в организме разрушение жизненно важных соединений. Условленно также, что некоторые патогенные бактерии (дифтерийные стафилококки и стрептококки) продуцируют фермент дезоксирибонуклеазу В процессе жизнедеятельности патогенные микробы выделяют и другие вещества, обусловливающие их вирулентность.
Пути внедрения патогенных микробов в организм
Место проникновения патогенных микробов в организм называется входными воротами инфекции. В естественных условиях заражение происходит через пищеварительный тракт (алиментарный путь), когда в пищу или в воду попадают патогенные микроорганизмы. Болезнетворное начало может проникать через поврежденные, а при некоторых инфекционных болезнях (бруцеллез) и неповрежденные слизистые оболочки рта, носа, глаз, мочеполовых путей и кожу. Судьба патогенных микробов, попавших в организм, может быть различной – в зависимости от состояния организма и вирулентности возбудителя. Некоторые микробы, попав с током крови в определенные органы, оседают (задерживаются) в их тканях, размножаются в них, выделяют токсины и вызывают заболевание. Например, возбудитель туберкулеза в легочной ткани. Любая инфекционная болезнь, независимо от клинических признаков и локализации микроба в организме, представляет собой заболевание всего организма. Если патогенные микробы проникли в кровеносные сосуды и начинают размножаться в крови, то они очень быстро проникают во все внутренние органы и ткани. Такую форму инфекции называют септицемией. Она характеризуется быстротой и злокачественностью течения и нередко заканчивается смертельным исходом. Когда микробы находятся в крови временно и не размножаются в ней, а посредством ее только переносятся в другие чувствительные ткани и органы, где затем уже размножаются, инфекцию принято называть бактериемией. Иногда микробы, проникнув в организм, остаются только в поврежденной ткани и, размножаясь выделяют токсины. Последние, проникая в кровь, вызывают общее тяжелое отравление (столбняк, злокачественный отек). Такой процесс называется токсемией. Пути выделения патогенных микробов из организма также различны: со слюной, мокротой, мочой, калом, молоком, выделениями из родовых путей.
Условия возникновения инфекций и значение состояния организма в этом процессе
Для возникновения инфекционного процесса требуется минимально заражающая доза микроба; однако чем больше проникло в организм микробов, тем скорее развивается болезнь. Чем вирулентнее микроб, тем быстрее наступают все клинические признаки болезни. Имеют значение и ворота инфекций. Например, после введения в легкие морской свинки 1 – 2 туберкулезных микробов может возникнуть заболевание, а чтобы вызвать заболевание путем подкожной инъекции микробов, надо ввести не меньше 800 живых туберкулезных палочек.
Одно из необходимых условий для возникновения заболевания – восприимчивость организма к данной инъекции очень восприимчивы, а к другим устойчивы. Например, крупный рогатый скот не заражается сапом лошадей, а чума свиней совершенно неопасно в смысле заражения для человека. Исключительно важное значение для возникновения инфекционного процесса имеет состояние организма. И.И.Мечников писал: «Болезнь, помимо внешних причин – микробов, обязана своим происхождением еще и внутренним условиям самого организма. Болезнь наступает тогда, когда эти внутренние причины оказываются бес сильными помешать развитию болезнетворных микробов; когда они, наоборот, успешно борются с микробами, то организм оказывается невосприимчивым. Проникновение патогенного микроба в чувствительный организм вовсе не обязательно вызывает соответствующее заболевание». Устойчивость организма против инфекции снижается при плохом питании. Влияет также простудный фактор, перегревание, радиация, отравление алкоголем и пр. Течение инфекционного заболевания Инфекционный процесс проявляется не сразу после внедрения патогенного микроба в организм, а спустя некоторый срок. Время от внедрения микробов в организм до появления первых клинических признаков заболевание называют скрытым, или инкубационным, периодом. Продолжительность его определяется вирулентностью и количеством внедрившихся микробов, воротами инфекции, состоянием организма и окружающими условиями. За период инкубации внедрившиеся микробы размножаются, производят качественные биологические изменения в организме, в результате чего появляются клинические признаки. По длительности течения инфекции бывают острые, кратковременно протекающие (ящур, холера, сибирская язва и многие др.). Большинство инфекций относится к острым. Инфекционные болезни людей и животных могут наблюдаться в виде единичных случаев, именуемых спорадическими. Когда инфекция быстро распространяется среди людей и охватывает населенные пункты значительной территории, такое распространение инфекции принято называть – эпидемия, соответственно инфекция среди животных – эпизоотия. Инфекционные болезни по природе отличаются от других заболеваний следующими свойствами: наличием живого возбудителя, заразительностью (передаются от больных здоровым), инкубационным периодом, иммунитетом (невосприимчивостью) переболевших. Последний наступает не всегда.Источники и пути распространения инфекции Основной источник и переносчик заразного начала – больной организм. От больного могут заражаться люди, животные. Зараженная почва может быть источником заражения. Болезни, при которых заражение происходит в результате попадания патогенных микробов из почвы, получили название почвенных инфекций (сибирская язва, газовая гангрена и др.)
Автор: Тайша Әсем Шарафиқызы
ГП на ПХВ Областная инфекционная больница
бактериологическая лаборатория –бак лаборантка
Условно-патогенная микрофлора
В организме существует множество бактерий, которые находятся с человеком в разных взаимоотношениях. Большую часть микрофлоры (микробиоценоза) представляют микроорганизмы, которые сосуществуют с человеком на основе симбиоза. Иными словами, основная масса микробов получает от человека пользу (в виде постоянной температуры и влажности, питательных веществ, защиты от ультрафиолета и так далее). В то же время эти бактерии сами приносят пользу, синтезируя витамины, расщепляя белки, соперничая с болезнетворными микроорганизмами и выживая их со своей территории. И одновременно с такими полезными бактериями у человека есть «сожители», которые в небольших количествах не приносят существенного вреда, но при определенных условях становящиеся болезнетворными. Такую часть микробов называют условно-патогенной микрофлорой.
Условно-патогенные микроорганизмы (УПМ) желудочно-кишечного тракта борются за свое выживание, поэтому их поколения вырабатывают устойчивость к конкурентной нормальной флоре. Лакто– и бифидобактерии в процессе жизнедеятельности производят вещества, сходные с антибиотиками по своему действию. Кроме того, сам организм, благодаря иммунной системе сдерживает размножение болезнетворных бактерий. Прием алкоголя и табакокурение, не говоря уже о наркомании, нервные стрессы, физические перегрузки, возрастные изменения, физиологическое несовершенство лимфатической системы (у маленьких детей), различные заболевания (в первую очередь – вирусного происхождения) – все это нарушает нормальный баланс микрофлоры в желудочно-кишечном тракте, приводит к гибели полезных микроорганизмов. Природа не терпит пустоты, и на смену погибшим полезным бактериям приходят условно-патогенные. С этого момента начинается развитие дисбиоза и дисбактериоза. Если же бывшие условно-патогенными, а теперь ставшие болезнетворными, бактерии покидают свое привычное место жительства, проникая через тканевые барьеры, то развивается оппортунистическая инфекция.
Состав условно-патогенной микрофлоры
Нормофлора у каждого человека индивидуальна по своему составу. То же самое касается и условно-патогенной микрофлоры, как части нормального биоценоза. Да-да! Несмотря на свою пагубную деятельность, условно-патогенные микроорганизмы нужны нормальной микрофлоре. Бактерии живут по принципу: «Что нас не убивает, то делает сильнее». То есть, постоянно соперничая за место, наши полезные бактерии становятся более выносливыми, вырабатывают «навыки» борьбы с УПМ на генном уровне. То же самое происходит и с остальной иммунной системой. Так что, можно сказать, что даже условно-патогенные микробы нужны нашему организму в качестве своеобразного «тренера» иммунитета.
К условно-патогенным микроорганизмам желудочно-кишечного тракта относится практически все семейство Enterobacteriaceae. Сюда входят клебсиелла пневмония, энтеробактеры (аэрогенес и клоацеа), цитробактер фреунди, протеи. Предельно допустимой нормой для семейства энтеробактерий в ЖКТ является показатель в 1000 микробных единиц. Из семейства стафилококков в кишечнике обитают на постоянной основе негемолитические формы стафилококка, количество которого может достигать в норме 10 000 микроорганизмов на 1 гкала. Гемолитических форм, то есть растворяющих эритроциты, в кишечнике в норме быть не должно вообще. Из УПМ очень большое количество бактероидов (фрагилис, например), можно встретить в толстом отделе кишечника. Эти бактерии принимают участие в жировом (липидном) обмене. Но их количество не должно выходить за пределы 10 9 колониеобразующих единиц, то есть отдельных особей, в1 г кала. В кишечнике можно также встретить небольшое количество стрептококков, которые помимо антагонистических (враждебных) свойств несут также и полезную нагрузку в нашем организме – они стимулируют выработку иммуноглобулинов, а также активно подавляют патогенных бактерий типа сальмонелл, шигелл.
Среди представителей нормофлоры также есть микроорганизмы, способные вызывать дисфункции кишечника. То есть, собственно эти бактерии относят к условно-патогенным, но тем не менее, их полезные свойства преобладают над патогенными. Такими бактериями являются энтерококки фекалис и фециум.
Из представителей условно-патогенной микрофлоры желудочно-кишечного тракта есть и такие, которые весьма редко, но все же могут вызывать заболевания. К таким можно отнести вейлонелл и фузобактерий. Их локализация, преимущественно, ограничена ротовой полостью. Но при попадании в кишечник, по данным некоторых ученых, они могут вызывать разного рода воспаления. Сведения о роли этих микробов в возникновении заболеваний ЖКТ весьма разрозненные и поэтому врачи, в лабораторных исследованиях причин дисбактериозов, особого внимания на них не обращают.
В отличие от вейлонелл и фузобактерий, хеликобактер пилори изучен довольно неплохо. Ему было отведено большое внимание в последнее время в связи с тем, что средой обитания он избрал желудок. Гастриты, язвенная болезнь желудка инфекционной природы в первую очередь связывается именно с хеликобактером. Лечение и приведение концентрации этого микроба к норме – довольно сложный процесс. Основная сложность терапии – высокая устойчивость хеликобактера к антимикробным препаратам. Еще бы – ведь он обитает в среде с повышенной кислотностью и через него проходят все лекарственные препараты. Какие должны быть защитные механизмы у бактерии, чтобы не только выживать, но и прекрасно себя чувствовать в подобных условиях!
Для того чтобы сдерживать патогенные свойства УПМ организму необходима помощь. Человек должен понимать, что его здоровье – в его же руках. Какими бы замечательными антагонистическими свойствами ни обладали наши эшерихии, бифидобактерии и лактобактерии, им нужна наша помощь, которая заключается в разумном подходе к образу жизни, и в первую очередь – к питанию.
Что такое патогенные и условно патогенные микроорганизмы
В настоящее время исследование качества пищевых продуктов путем выявления в них неспецифической микрофлоры является актуальным для современной биологии и медицины. Размножение некоторых микроорганизмов приводит к непригодности пищевых продуктов к употреблению. Многие из производимых в мире продуктов не доходят до потребителя в связи с их порчей (в большинстве случаев микробами) [1–3].
Содержание в пищевых продуктах белков, углеводов, витаминов и других питательных веществ благоприятствует не только сохранению, но и размножению различных микроорганизмов [4, 5]. В молочнокислых и полученных путем брожения пищевых продуктах находятся в большом количестве микробы, которые придают им вкусовые качества и определенную консистенцию (специфическая микрофлора). Кроме того, в продуктах могут содержаться микроорганизмы или их споры, попавшие из внешней среды (неспецифическая микрофлора) [6–8].
В отдельных случаях пищевые продукты могут быть обсеменены сальмонеллами, шигеллами, стафилококками, клостридиями ботулизма, E. coli, B. cereus, Cl. perfringens и другими бактериями, приводящими к возникновению у людей пищевых токсикоинфекций и других заболеваний [9–11]. Поэтому актуально выявление и исследование культуральных, биохимических свойств микрофлоры пищи.
Целью нашего исследования явилось изучение биохимических свойств выявленных неспецифических микроорганизмов пищевых продуктов.
Материалы и методы исследования
Исследование проводилось в бактериологической лаборатории Департамента профилактики заболеваний и госсанэпиднадзора Кыргызской Республики. Объекты исследования – выявленная патогенная и условно-патогенная микрофлора пищевых продуктов.
Во время исследования использовали биохимические методы микробиологии (бродильный метод, методы определения лецитоветиллазы, индикаторные бумажные тесты) [12]. Определение бактерий группы кишечных палочек (БГКП) в пищевых продуктах производили бродильным методом посевом на среды Кесслера, – 37 °С – 18–24 ч., высев на Эндо – 37 °С – 24 ч. (ГОСТ 30518-97, ГОСТ 10444.15-94). Определение семейства Enterobacteriacea производили с помощью системы индикаторные бумажные (СИБ) тесты – индолообразования (СТ 28560-90, ГОСТ 30726-2001). А идентификацию Staphylococcus aureus – определением лецитоветиллазы (лецитиназа), реакцией плазмокоагуляция (ГОСТ 9225-84).
Результаты исследования и их обсуждение
Из молочных продуктов, кондитерских изделий и готовых кулинарных изделий выделены бактерии группы кишечных палочек. Характерные биохимические свойства бактерии группы кишечных палочек мы описываем ниже.
Для определения биохимических свойств БГКП 0,1 г продукта (разведение 1:10) высевали на 9 мл среды Кесслера с поплавками при температуре 37 °С и инкубировали на 16–24 ч. После инубации наблюдали выделение газа и изменение цвета среды. Цвет среды Кесслера изменился с красного на желтый. Это доказывает, что БГКП ферментировал среды Кесслера с образованием газа (рис. 1).
Рис. 1. Биохимические свойства семейства Enterobacteriaceae: а) отрицательный, б) положительный (ферментировали среды Кесслера с образованием газа)
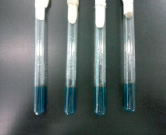
Рис. 2. Биохимические свойства семейства Enterobacteriaceae: а) среда лактоза до посева, б) среда лактоза после посева
Затем, чтобы дальше исследовать биохимические свойства БГКП, производили посев на лактозную среду. После инкубации при температуре 37 °С на 24 ч на лактозной среде наблюдали выделение пузырьков и изменение цвета среды. Как видно на рис. 2, изменился цвет среды с темно-зеленого на желтый, выделение пузырьков доказывает, что эти микроорганизмы, ферментируя лактозную среду, образуют кислоту и газы.
Чтобы определить биохимические свойства E. coli, 0,1 г продукта (разведение 1:10) высевали на 9 мл среды Кесслера с поплавками при температуре 44 °С, инкубировали на 16–24 ч. После инкубации наблюдали выделение газа и изменение цвета среды. Цвет среды Кесслера изменился с красного на желтый. Это доказывает, что E. coli ферментировал среды Кесслера с образованием газа (рис. 1). Для дальнейщего исследования биохимических свойств E. coli производили посев на лактозную среду. После инкубации при температуре 37 °С на 24 ч на среде лактоза наблюдали выделение пузырьков и изменение цвета лактозной среды. Цвет лактозной среды изменялся с темно-зеленого на желтый и выделялись газы. Эти свойства характерны для семейства Enterobacteriaceae (рис. 2).
Для межродовой и видовой биохимической дифференциации энтеробактерий определяли с помощью системы индикаторные бумажные тесты (СИБ-тесты).
Биохимические свойства группы Proteus определяются с помощью СИБ-тестов. После инкубации наблюдали следующие изменения. Результат анализа регистрировался визуально. При определении оксидазной активности группы Proteus СИБ тест меняет свой цвет на синий. Это доказывает, что эти выросшие культуры на поверхности агара группы Proteus.
Из колонии группы Proteus vulgaris брали бактериологической петлей и посевали штрихом по косяку и уколом в столбик комбинированной среды для первичной биохимической идентификации микробов на среду Клиглера (1) и Симонса (2) (Проба № 2118-2121, рис. 3). На рис. 4 видно, что идет почернение среды Клиглера, образование сероводорода, ферментация глюкозы с изменениями окраски столбика среды, кислотообразования. А среда Симонса не изменилась. Почернение среды Клиглера, появляющееся в средней или нижней части столбика, происходит при образовании выделенным микробом сероводорода, что свойственно представителям рода Рroteus vulgaris, Р. mirabilis.
Рис. 3. Биохимические свойства Proteus vulgaris. Среда Клиглера (1) и Симонса (2) до пересева
Рис. 4. Биохимические свойства Proteus vulgaris. Среда Клиглера (1) и Симонса (2) после пересева
При проведении дополнительного биохимического анализа Proteus vulgaris определяли индолообразование. Для выявления индола в пробирки разливали 6 мл среды и засевали суспензией бактерий. Инкубировали при температуре 37 °С в течение 18–24 ч. Затем для определения индола складывали по намеченной на ней линии вдвое и пинцетом опускали на дно пробирки. Контроль произвели СИБ-диской, помещенной в пробирку со стерильным натрия хлорида раствором 0,9 %. Обе пробирки инкубировали при температуре (37 ± 1) °С. На пробе индолообразования подтверждено, что конец индола окрашивался в розово-малиновый цвет.
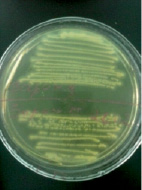
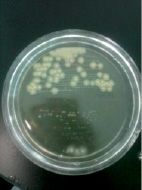
Staphylococcus aureus в анаэробных условиях ферментирует маннит. Биохимические свойства Staphylococcus aureus определяли с помощью лецитоветиллазы и плазмокоагуляции. При определении лецитоветиллазы (лецитиназа) посевали на среду желточно-солевой агар – хлористый натрий является элективным фактором, он подавляет рост большинства представителей другой микрофлоры, главным образом грамотрицательной. Одним из компонентов яичного желтка является лецитовителлин. Лецитовителлин является субстратом для фермента лецитовителлазы (лецитиназы), относящегося к группе липаз и продуцируемого некоторыми стафилококками. На желточно-солевом агаре (рис. 5) колонии Staphylococcus aureus – S-формы, выпуклые, круглые и блестящие. Наличие пигмента легко определяется на глаз. Вокруг колонии S. аureus образовался радужный венчик. Это доказывает, что S. aureus обладает лецитовителлазной активностью.
Рис. 5. Биохимическая идентификация Staphylococcus aureus
Для окончательной идентификации Staphylococcus aureus определяли фермент плазмокоагулазы. В пробирку, содержащую цитратную плазму крови, вносили с петлей суточной агаровой культуры исследуемого штамма и штатив с пробирками инкубировали на 4 часа в термостат при 37 °С. После инкубации учитывали результат, в пробирке (рис. 6) появился студнеобразный сгусток. Под действием фермента плазмокоагулазы активируется естественная система свертывания крови (плазминоген протромбин). Появление студнеобразного сгустка любого размера считается положительным результатом реакции. Положительным результатом следует считать наличие плазмокоагуляции в первые 4 часа инкубации. Отсутствие свертывания плазмы в течение 18 ч расценивается как отрицательный результат. В качестве контроля рекомендуется ставить реакцию с заведомо коагулирующим и некоагулирующим штаммами, а также оставлять одну пробирку с плазмой незасеянной (рис. 6).
Рис. 6. Биохимические свойства Staphylococcus aureus. Реакция плазмокоагуляции
Выводы
1. Показано, что семейства Enterobacteriaceae ферментируют углеводы с кислотообразованием и выделяют сероводород.
2. Установлено, что Staphylococcus aureus ферментирует лецитовителлин и активирует естественную систему свертывания крови и вызывает плазмокоагуляцию.
3. Показано, что Proteus vulgaris обладает сахаролитической и протеолитической активностью.