Физическая сущность и механизм процесса кристаллизации
Главная > Документ
| Информация о документе | |
| Дата добавления: | |
| Размер: | |
| Доступные форматы для скачивания: |
Физическая сущность и механизм процесса кристаллизации
Кристаллизация – это процесс образования участков кристаллической решетки в жидкой фазе и рост кристаллов из образовавшихся центров.
Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию с минимумом свободной энергии.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура. Кривая охлаждения чистого металла представлена на рис. 1.
Рис.1. Кривая охлаждения чистого металла


Процесс кристаллизации чистого металла:
Механизм кристаллизации металлов.
Переход из жидкого состояния в кристаллическое требует затраты энергии на образование поверхности раздела жидкость – кристалл. Процесс кристаллизации будет осуществляться, когда выигрыш от перехода в твердое состояние больше потери энергии на образование поверхности раздела. Зависимость энергии системы от размера зародыша твердой фазы представлена на рис. 2.
Зародыши с размерами равными и большими критического растут с уменьшением энергии и поэтому способны к существованию.
Рис.2. Зависимость энергии системы от размера зародыша твердой фазы
Механизм кристаллизации представлен на рис.3.
Рис.3. Модель процесса кристаллизации
Центры кристаллизации образуются в исходной фазе независимо друг от друга в случайных местах. Сначала кристаллы имеют правильную форму, но по мере столкновения и срастания с другими кристаллами форма нарушается. Рост продолжается в направлениях, где есть свободный доступ питающей среды. После окончания кристаллизации имеем поликристаллическое тело.
Качественная схема процесса кристаллизации может быть представлена количественно кинетической кривой (рис. 4).
Рис. 4. Кинетическая кривая процесса кристаллизации
Процесс вначале ускоряется, пока столкновение кристаллов не начинает препятствовать их росту. Объем жидкой фазы, в которой образуются кристаллы уменьшается. После кристаллизации 50 % объема металла, скорость кристаллизации будет замедляться.
Таким образом, процесс кристаллизации состоит из образования центров кристаллизации и роста кристаллов из этих центров.
В свою очередь, число центров кристаллизации (ч.ц.) и скорость роста кристаллов (с.р.) зависят от степени переохлаждения (рис. 5).
Рис. 5. Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) от степени переохлаждения
Размеры образовавшихся кристаллов зависят от соотношения числа образовавшихся центров кристаллизации и скорости роста кристаллов при температуре кристаллизации.
При равновесной температуре кристаллизации Т S число образовавшихся центров кристаллизации и скорость их роста равняются нулю, поэтому процесса кристаллизации не происходит.
Если жидкость переохладить до температуры, соответствующей т. а, то образуются крупные зерна (число образовавшихся центров небольшое, а скорость роста – большая).
При переохлаждении до температуры соответствующей т. в – мелкое зерно (образуется большое число центров кристаллизации, а скорость их роста небольшая).
Если металл очень сильно переохладить, то число центров и скорость роста кристаллов равны нулю, жидкость не кристаллизуется, образуется аморфное тело. Для металлов, обладающих малой склонностью к переохлаждению, экспериментально обнаруживаются только восходящие ветви кривых.
Рекристализационный отжиг (Рекристаллизация) – отжиг I-го рода, процесс зарождения и роста новых недеформированных зерен при нагреве наклепанного металла до определенной температуры.
Нагрев металла до температур рекристаллизации сопровождается резким изменением микроструктуры и свойств. Нагрев приводит к резкому снижению прочности при одновременном возрастании пластичности. Также снижается электросопротивление и повышается теплопроводность.
1 стадия – первичная рекристаллизация (обработки) заключается в образовании центров кристаллизации и росте новых равновесных зерен с неискаженной кристаллической решеткой. Новые зерна возникают у границ старых зерен и блоков, где решетка была наиболее искажена. Количество новых зерен постепенно увеличивается и в структуре не остается старых деформированных зерен.
Движущей силой первичной рекристаллизации является энергия, аккумулированная в наклепанном металле. Система стремится перейти в устойчивое состояние с неискаженной кристаллической решеткой.
2 стадия – собирательная рекристаллизация заключается в росте образовавшихся новых зерен.
Движущей силой является поверхностная энергия зерен. При мелких зернах поверхность раздела большая, поэтому имеется большой запас поверхностной энергии. При укрупнении зерен общая протяженность границ уменьшается, и система переходит в более равновесное состояние.
Температура начала рекристаллизации связана с температурой плавления

для металлов
для твердых растворов
для металлов высокой чистоты
На свойства металла большое влияние оказывает размер зерен, получившихся при рекристаллизации. В результате образования крупных зерен при нагреве до температуры t 1 начинает понижаться прочность и, особенно значительно, пластичность металла.
Основными факторами, определяющими величину зерен металла при рекристаллизации, являются температура, продолжительность выдержки при нагреве и степень предварительной деформации (рис. 6).
Рис. 6. Влияние предварительной степени деформации металла на величину зерна после рекристаллизации
С повышением температуры происходит укрупнение зерен, с увеличением времени выдержки зерна также укрупняются. Наиболее крупные зерна образуются после незначительной предварительной деформации 3…10 %. Такую деформацию называют критической. И такая деформация нежелательна перед проведением рекристаллизационного отжига.
Практически рекристаллизационный отжиг проводят для малоуглеродистых сталей при температуре 600…700 o С, для латуней и бронз – 560…700 o С, для алюминиевых сплавов – 350…450 o С, для титановых сплавов – 550…750 o С.
Превращения в железоуглеродистых сплавах
Диаграмма состояния Fe-Fe 3 C (рис. 7) показывает фазовый состав и превращения в сплавах с концентрацией от чистого железа до цементита.
Превращения в железоуглеродистых сплавах происходит как при кристаллизации (затвердевании) жидкой фазы (Ж), так и в твердом состоянии.
Рис. 7. Диаграмма состояния Fe – Fe 3 C (в упрощенном и полном виде).
Первичная кристаллизация идет в интервале температур, ограни-ченных линиями ликвидус (ACD) и солидус (AECF).
Вторичная кристаллизация происходит за счет превращения железа одной аллотропической модификации в другую и за счет изменения растворимости углерода в аустените и феррите, которая уменьшается с понижением температуры. Избыток углерода выделяется из твердых растворов в виде цементита. В сплавах системы Fe-Fe 3 C происходят следующие изотермические превращения:
Эвтектическое превращение на линии ECF (1147 °C)
Эвтектоидное превращение на линии PSK (727 °C)
Эвтектическая смесь аустенита и цементита называется ледебуритом (Л), а эвтектоидная смесь феррита и цементита – перлитом (П). Ледебурит содержит 4,3 % углерода. При охлаждении ледебурита ниже линий PSK входящий в него аустенит превращается в перлит и при нормальной температуре ледебурит представляет собой смесь перлита и цементита и называется ледебуритом превращенным (Л пр). Цементит в этой структурной составляющей образует сплошную матрицу, в которой размещены колонии перлита. Такое строение ледебурита объясняет его большую твердость (HB 700) и хрупкость.
Перлит содержит 0,8 % углерода. В зависимости от формы частичек цементит бывает пластинчатый и зернистый. Является прочной структурной составляющей с твердостью (HB210).
Линии диаграммы состояния Fе – Fе 3 C
Линии диаграммы представляют собой совокупность критических точек сплавов с различным составом, характеризующих превращения в этих сплавах при соответствующих температурах.
Рассмотрим значение линий диаграммы при медленном охлаждении.
ACD – линия ликвидус. Выше этой линии все сплавы находятся в жидком состоянии.
AECF – линия солидус. Ниже этой линии все сплавы находятся в твердом состоянии.
АС – из жидкого раствора выпадают кристаллы аустенита.
CD – линия выделения первичного цементита.
AE – заканчивается кристаллизация аустенита.
ECF – линия эвтектического превращения.
GS – определяет температуру начала выделения феррита из аустенита (910-727 °C).
GP – определяет температуру окончания выделения феррита из аустенита.
PSK – линия эвтектоидного превращения.
ES – линия выделения вторичного цементита.
PQ – линия выделения третичного цементита.
Области диаграммы состояния Fe – Fe 3 C
Линии диаграммы: делят все поле диаграммы на области равновесного существования фаз. Каждой области диаграммы соответствует определенное структурное состояние, сформированное в результате происходящих в сплавах превращений.
I – Жидкий раствор (Ж).
II –Жидкий раствор (Ж) и кристаллы аустенита (А).
III – Жидкий раствор (Ж) и кристаллы цементита первичного (Ц I ).
IV – Кристаллы аустенита (А).
V – Кристаллы аустенита (А) и феррита (Ф).
VI – Кристаллы феррита (Ф).
VII – Кристаллы аустенита (А) и цементита вторичного (Ц II ).
VIII – Кристаллы феррита (Ф) и цементита третичного (Ц III ).
IX – Кристаллы феррита (Ф) и перлита (П).
X – Кристаллы перлита (П) и цементита вторичного (Ц II ).
XI – Кристаллы аустенита (А), ледебурита (Л) и цементита вторичного (Ц II ).
XII – Кристаллы перлита (П), цементита вторичного (Ц II ) и ледебурита превращенного (Л пр).
XIII –Кристаллы ледебурита и цементита первичного (Ц I ).
XIV – Кристаллы цементита первичного (Ц I ) перлита (П) и ледебурита превращенного (Л пр).
Сталь эвтектоидного состава – содержание углерода 0,8 % (рис.8, сплав Ш).
А s 
Подсчет ведется по правилу рычага, несколько ниже эвтектоидной линии:
При комнатной температуре – состав феррит и перлит
Рис. 8. Левый нижний участок диаграммы состояния железо-цементит. Вторичная кристаллизация сплавов:
а) диаграмма, б), в), г), д), е) кривые охлаждения сплавов
9. Кристаллизация металлов; зарождение кристаллов, критический зародыш; гомогенное и гетерогенное зарождение кристаллов; рост кристаллов. Кривые Таммана
9. Кристаллизация металлов; зарождение кристаллов, критический зародыш; гомогенное и гетерогенное зарождение кристаллов; рост кристаллов. Кривые Таммана
Кристаллизация – это процесс перехода металла из жидкого состояния в твердое с образованием кристаллической структуры. В природе все самопроизвольно протекающие превращения, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии.
Переход металла из жидкого или парообразного состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. Процесс кристаллизации состоит из двух одновременно идущих процессов зарождения и роста кристаллов. Кристаллы могут зарождаться самопроизвольно – самопроизвольная кристаллизация или расти на имеющихся готовых центрах кристаллизации – несамопроизвольная кристаллизация.
Проследить процесс кристаллизации металла можно с помощью счетчика времени и термоэлектрического пирометра. Две разнородные проволоки, которые спаянны концами, погружают в расплавленный металл и при этом возникающий термоток пропорционален температуре металла, а стрелка милливольтметра отклоняется, она указывает температуру по специально градуированной шкале. Показания пирометра записывают во времени и по полученным данным строят кривые охлаждения в координатах температура – время. Критической точкой называется температура, которая соответствует какому-либо превращению в металле.
При охлаждении переход из жидкого состояния в твердое сопровождается образованием кристаллической решетки, т. е. кристаллизацией. Для того чтобы вызвать кристаллизацию, жидкий металл нужно переохладить до температуры ниже температуры плавления. При затвердевании и при аллотропическом превращении в металле вначале образуются центры кристаллизации, вокруг которых группируются атомы, образуя соответствующую кристаллическую решетку. Процесс кристаллизации складывается из двух этапов: образования центров кристаллизации и роста кристаллов. У каждого из возникающих кристаллов кристаллографические плоскости ориентированы случайно, кроме того, при первичной кристаллизации кристаллы могут поворачиваться, так как они окружены жидкостью. Смежные кристаллы растут навстречу друг другу, и точки их столкновения определяют границы кристаллитов (зерен).
У аморфных веществ кривые охлаждения плавные, без площадок и уступов: понятно, что аллотропии у этих веществ быть не может. Механизм кристаллизации металла состоит в том, что при соответствующем понижении температуры внутри тигля с жидким металлом начинают образовываться мелкие кристаллики, называемые центрами кристаллизации или зародышами.
Для начала роста кристаллов из жидкого металла необходимо, чтобы свободная энергия металла
уменьшилась. Если же в результате образования зародыша свободная энергия металла увеличивается, то зародыш растворяется. Минимальный размер способного к росту зародыша называется критическим размером зародыша, а такой зародыш – устойчивым.
Чем больше степень переохлаждения, понижающая свободную энергию металла, тем меньше критический размер зародыша.
Вокруг образовавшихся центров начинают расти кристаллы. По мере роста кристаллов в металле, оставшемся еще в жидком состоянии, продолжают возникать новые центры кристаллизации. Каждый из растущих новых кристаллов ориентирован в пространстве произвольно.
Кристаллы с неправильной формой называются зернами или кристаллами. Твердые тела, в том числе и металлы, состоящие из большого количества зерен, называют поликристаллическими.
Д.В. Черновым установлено, что процесс кристаллизации состоит из двух элементарных процессов: зарождения центров кристаллизации и роста кристаллов из этих центров. Гораздо позже Тамман, изучая процесс кристаллизации, установил зависимость числа центров кристаллизации и скорости роста кристаллов от степени переохлаждения.
Пока образовавшиеся кристаллы растут свободно, они имеют более или менее правильную геометрическую форму. Однако при столкновении растущих кристаллов их правильная форма нарушается, так как в этих участках рост граней прекращается. Рост продолжается в тех направлениях, где есть свободный доступ «питающей» жидкости. В результате растущие кристаллы, имеющие сначала геометрически правильную форму, после затвердевания получают неправильную внешнюю форму и поэтому называются кристаллитами или зернами.
Рост зародышей происходит в результате перехода атомов из переохлажденной жидкости к кристаллам. Кристалл растет послойно, каждый слой имеет одноатомную толщину. Различают два элементарных процесса роста кристаллов.
Образование двумерного зародыша.
Рост двумерного зародыша путем поступления атомов из переохлажденной жидкости. После образования на плоской грани двумерного зародыша дальнейший рост нового слоя протекает сравнительно легко, так как появляются участки, удобные для закрепления атомов, переходящих из жидкости.
Размер зерен, образующихся в процессе кристаллизации, зависит не только от числа самопроизвольно зарождающихся центров кристаллизации, но и от числа частичек нерастворимых примесей, всегда имеющихся в жидком металле, которые играют роль готовых центров кристаллизации.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Читайте также
Глава первая. Зарождение идеи
Глава первая. Зарождение идеи История любой идеи- это почти всегда история многих вещей и событий. Идеи в своем становлении похожи на большие реки: их питают разные источники. Как берега реки близ устья наполнены водами ее многочисленных притоков, так и всякая идея в
Глава I. ЗАРОЖДЕНИЕ ВОЗДУШНОГО БОЯ (первая мировая война)
Глава I. ЗАРОЖДЕНИЕ ВОЗДУШНОГО БОЯ (первая мировая война) 1. Как вести бой в воздухе? Сентябрь 1913 года. В разгаре маневры войск Киевского военного округа. На одной из «действующих» сторон X корпус, на другой — XXI, каждому из них придано по два авиационных отряда.…Над
ГЛАВА 1 Зарождение идеи
5.15. Подготовка совещания. Кривые пути электронов и тупики источников направленного РЧЭМИ
14.3. Рост науки
14.3. Рост науки Наука растет и растет стремительно — по экспоненциальному закону, т. е. таким образом, что за каждые сколько-то лет ее количественные характеристики возрастают во столько-то раз. Общее число статей в научных журналах всего мира удваивается за 12–15 лет1. Число
2. Кристаллизация и структура металлов и сплавов
2. Кристаллизация и структура металлов и сплавов Порядок расположения атомов – тип кристаллической решетки – природное свойство металла, форма кристаллов и их размеры зависят от процесса перехода металла из жидкого состояния в твердое. Процесс образования кристаллов
Долой рост!
Долой рост! В свое время сельскохозяйственное отделение фирмы КОШМАР занималось выращиванием вьющихся бобов на дугообразных подпорках, надеясь выяснить, станут ли побеги загибаться вниз, к земле. Бобы, однако, упрямо стремились вверх, хотя и испытывали некоторое
Тема I. ЗАРОЖДЕНИЕ И ВЫЗРЕВАНИЕ ИНЖЕНЕРНОЙ ДЕЯТЕЛЬНОСТИ. ЕЕ СУЩНОСТЬ И ФУНКЦИИ
Тема I. ЗАРОЖДЕНИЕ И ВЫЗРЕВАНИЕ ИНЖЕНЕРНОЙ ДЕЯТЕЛЬНОСТИ. ЕЕ СУЩНОСТЬ И ФУНКЦИИ В истории становления и развития производительных сил общества на различных этапах проблема инженерной деятельности занимает особое место. Инженерное дело прошло довольно непростой,
ЗАРОЖДЕНИЕ ПРОЕКТА «СУ-27»
ЗАРОЖДЕНИЕ ПРОЕКТА «СУ-27» Павел ПЛУНСКИЙК концу 1960-х годов ОКБ П.О. Сухого являлось одним из ведущих конструкторских бюро МАП, специализирующимся на самолетах тактического назначения. В коллективе успела сложиться собственная школа проектирования, а в активе КБ было
2.8. ЗАРОЖДЕНИЕ ТЕОРЕТИЧЕСКИХ ОСНОВ ЭЛЕКТРОТЕХНИКИ
2.8. ЗАРОЖДЕНИЕ ТЕОРЕТИЧЕСКИХ ОСНОВ ЭЛЕКТРОТЕХНИКИ Как известно, процессы в электрической цепи определяются скалярными величинами — электродвижущей силой (или напряжением) и током. Напомним, что понятие об электродвижущей силе ввел в обращение А. Вольта. После первых
2.11. ЗАРОЖДЕНИЕ ЭЛЕКТРОАВТОМАТИКИ, ЭЛЕКТРОПРИБОРОСТРОЕНИЯ И ИНФОРМАЦИОННОЙ ЭЛЕКТРОТЕХНИКИ
2.11. ЗАРОЖДЕНИЕ ЭЛЕКТРОАВТОМАТИКИ, ЭЛЕКТРОПРИБОРОСТРОЕНИЯ И ИНФОРМАЦИОННОЙ ЭЛЕКТРОТЕХНИКИ Длительное время электрическая энергия не могла получить широкого практического применения вследствие отсутствия экономичных генераторов. Но это относится к так называемым
7.4.1. ЗАРОЖДЕНИЕ И РАЗВИТИЕ ЭЛЕКТРОХИМИЧЕСКОЙ ТЕХНОЛОГИИ
7.4.1. ЗАРОЖДЕНИЕ И РАЗВИТИЕ ЭЛЕКТРОХИМИЧЕСКОЙ ТЕХНОЛОГИИ Создание первого источника тока — вольтова столба — привело к зарождению новой технологии, которая позднее получила название электрохимической.Уже в 1800 г. В. Никельсон и А. Карлейль (Англия) разложили воду с
Диалог с заказчиком и зарождение идеи
Диалог с заказчиком и зарождение идеи Как вы поняли, проект обладает сложной структурой, которую непросто понять с первого раза. Это под силу лишь небольшому числу заказчиков. Разрозненность посвященной этой теме информации в сети Интернет в виде бесплатных советов
32. Отжиг 1-го рода. Неравновесная кристаллизация
32. Отжиг 1-го рода. Неравновесная кристаллизация Этот вид термической обработки возможен для любых металлов и сплавов. Его проведение не обусловлено фазовыми превращениями в твердом состоянии. Нагрев при отжиге 1 рода, повышая подвижность атомов, частично или полностью
Кристаллизация и осаждение
Оптимизация размера кристаллов, выхода реакции и чистоты продукта на специализированном оборудовании
Что такое кристаллизация?
Кристаллизация — процесс выстраивания атомов и молекул в жесткую кристаллическую решетку с хорошо определенной энергетически устойчивой структурой. Мельчайший структурный элемент кристаллической решетки — ячейка. Она способна принимать атомы и молекулы, и благодаря этому свойству формируется макроскопический кристалл. В процессе кристаллизации атомы и молекулы соединяются между собой под определенными углами, образуя характерную форму кристалла с гладкими поверхностями и гранями. Хотя кристаллизация происходит в природе, у нее также есть широкое промышленное применение. Она используется на этапе разделения и очистки при производстве фармацевтических и химических продуктов.
Условия процесса кристаллизации напрямую влияют на размер и форму кристаллов и чистоту кристаллического продукта. Важно понимать сущность процесса кристаллизации и правильно подбирать его параметры. Это позволит получать однородные кристаллы нужного размера, формы и чистоты, а также предотвратить проблемы на последующих этапах, такие как слишком долгое время фильтрации или недостаточная сушка.
Почему кристаллизация так важна?
Кристаллизация широко применяется для производства различных необходимых нам продуктов — начиная от пищи и лекарств и заканчивая топливом. Большинство продуктов агрохимической и фармацевтической промышленности в ходе разработки и производства подвергается нескольким этапам кристаллизации. С помощью этого процесса получают такие ключевые пищевые ингредиенты, как лактоза и лизин. Однако нежелательная кристаллизация может быть опасна — например, кристаллизация газовых гидратов в глубоководных трубопроводах.
Основные понятия кристаллизации
Кристаллизация
— это процесс образования твердой фазы в виде кристаллов из растворов или расплавов.
Кристалл
— тело, частицы которого (атомы, ионы или молекулы) расположены в трехмерной периодической структуре, принимающей естественную форму многогранника.
Осаждение
— синоним кристаллизации, однако этот термин чаще всего употребляется в отношении кристаллизации, которая происходит очень быстро в результате химической реакции.
Растворимость
— свойство вещества, его количество, которое способно раствориться в данном растворителе при данной температуре.
Насыщенный раствор
— раствор, содержащий максимальное количество вещества, которое способно раствориться в данном растворителе при данной температуре. Кристаллизация происходит в насыщенном растворе. Количество растворенного на тот момент вещества определяется его растворимостью.
Пересыщение
— разница между реальной и равновесной концентрациями растворенного вещества при данной температуре.
Виды кристаллизации
Кристаллизация происходит, когда растворимость вещества в растворе понижается каким-либо способом. Стандартные методы снижения растворимости:
b) добавление антирастворителя;
d) реакция (осаждение).
Выбор метода кристаллизации зависит от имеющегося оборудования, целей процесса кристаллизации, растворимости и стабильности растворенного вещества в выбранном растворителе.
Типичные сложности при кристаллизации
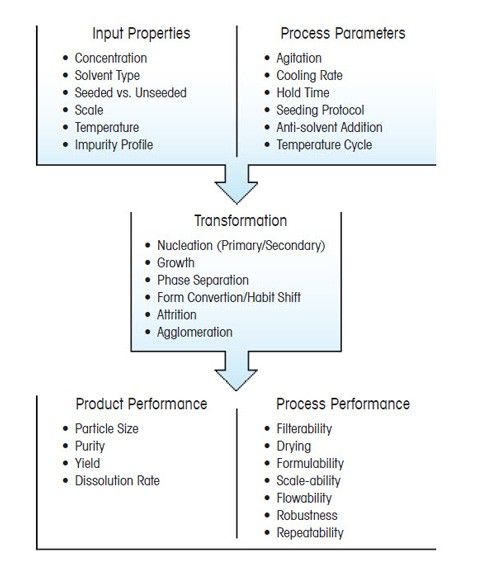
Кристаллизация происходит за счет нескольких взаимосвязанных процессов, на протекание которых влияют выбранные параметры. Основные этапы:
Данные процессы, которые часто протекают в скрытом виде, оказывают ключевое влияние на результат кристаллизации.
Этапы кристаллизации
Публикации по теме кристаллизации
Ознакомьтесь с подборкой статей по теме кристаллизации:
Классическая работа по нуклеации кристаллов из растворов
Jaroslav Nývlt, Kinetics of nucleation in solutions, Journal of Crystal Growth, Volumes 3–4, 1968.
Исследование механизмов выращивания кристаллов из раствора
Crystal Growth Kinetics, Material Science and Engineering, Volume 65, Issue 1, July 1984.
Описание причин, по которым в системах «растворенное вещество — растворитель» вместо кристаллизации происходит образование новой жидкой фазы
Kiesow et al., Experimental investigation of oiling out during crystallization process, Journal of Crystal Growth, Volume 310, Issue 18, 2008.
Подробное исследование причин агломерации кристаллов в процессе кристаллизации
Brunsteiner et al., Toward a Molecular Understanding of Crystal Agglomeration, Crystal Growth & Design, 2005, 5 (1), pp 3–16.
Исследование механизмов распада агломератов в процессе кристаллизации
Fasoli & Conti, Crystal breakage in a mixed suspension crystallizer, Volume 8, Issue 8, 1973, Pages 931–946.
Обзор алгоритмов разработки эффективных процессов кристаллизации в высокотехнологичных сегментах химической промышленности
Paul et al., Organic Crystallization Processes, Powder Technology, Volume 150, Issue 2, 2005.
Технологии, которые гарантируют получение нужной полиморфной формы в процессе кристаллизации
Kitamura, Strategies for Control of Crystallization of Polymorphs, CrystEngComm, 2009,11, 949–964.
Основные параметры и превращения в процессе кристаллизации
Кристаллы обладают множеством характеристик, но, пожалуй, важнейшая из них — это распределение кристаллов по размерам. От этого параметра в значительной степени зависят качество конечного продукта и эффективность процесса его получения. Размер и форма кристаллов непосредственно влияют на основные технологические этапы, следующие за кристаллизацией, — фильтрацию и сушку. Конечный размер кристаллов также определяет качество кристаллического продукта. Например, биологическая доступность и эффективность фармацевтических составов тем выше, чем мельче получаемые кристаллы, так как они лучше растворяются.
Оптимизировать дисперсность кристаллов можно путем тщательного подбора условий и параметров процесса кристаллизации. Чтобы кристаллический продукт приобрел нужные свойства, важно понимать, как параметры процесса влияют на основные превращения в ходе кристаллизации — образование зародышей (нуклеацию), рост и распад кристаллов.
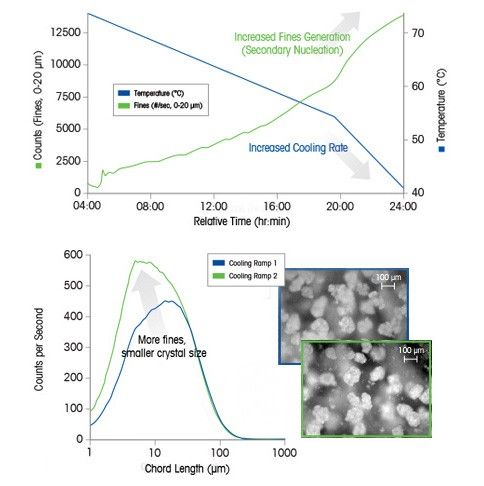
Практический пример: значение скорости охлаждения для кристаллизации
В этом примере охлаждение в конце цикла вызывает вторичную нуклеацию, которая приводит к образованию множества мелких частиц. Исследование проведено с использованием анализаторов размера частиц.
Увеличение скорости охлаждения раствора ведет к более быстрому пересыщению, в результате скорость образования зародышей кристаллов будет выше скорости их роста. Следовательно, чтобы получить нужное распределение кристаллов по размеру, чрезвычайно важно контролировать скорость охлаждения.
Дисперсность кристаллов льда, например, влияет на вкус и консистенцию мороженого: так, кристаллы размером менее 50 мкм предпочтительнее кристаллов, которые больше 100 мкм. Она влияет и на технологические свойства распыляемых агрохимикатов: их частицы должны быть малы настолько, чтобы не засорять сопла при распылении, но при этом достаточно большими, чтобы их не уносило на соседние поля.
При масштабировании получить кристаллический продукт нужного размера и формы с наименьшими издержками возможно лишь в случае понимания всех нюансов кристаллизации.
Оборудование для кристаллизации
Процессно-аналитическая технология для разработки процессов кристаллизации
Рабочая станция кристаллизации позволяет ученым получать максимум информации из каждого эксперимента с помощью централизованного программного решения. Средства процессно-аналитической технологии (PAT):
Автоматизированные реакторы
Точное регулирование критических параметров процесса
В дисперсных системах такие параметры, как температура, интенсивность перемешивания или режим дозирования, непосредственно влияют на качество процесса и конечного продукта. Приборы EasyMax, OptiMax, RC1 и RX-10 обеспечивают точное регулирование и регистрацию условий процесса для гибкого конструирования дисперсных систем.
Определение характеристик частиц
Изучение частиц в технологической среде
Размер, форма и концентрация — это важнейшие свойства частиц на каждой стадии процесса кристаллизации и на всех этапах масштабирования, поэтому они считаются критическими показателями качества (CQA). Анализаторы размера частиц оперативно отображают и количественно характеризуют частицы и важнейшие механизмы их формирования, что существенно облегчает разработку процессов кристаллизации.
Химический и структурный анализ
Достижение заданной конечной точки — в каждом эксперименте
Такие характеристики среды, как концентрация раствора, степень пересыщения и кристаллическая (полиморфная) модификация, часто связаны между собой и в совокупности определяют успех разработки технологического процесса кристаллизации. Системы ReactIR и ReactRaman анализируют состояние раствора и дисперсии для безошибочного достижения заданной конечной точки процесса.
Как разработать процесс кристаллизации
Разработка процесса кристаллизации для получения чистого продукта с оптимальным выходом и размером частиц включает в себя ряд важных элементов: