Что такое подслизистое образование желудка
Доброкачественные опухоли желудка
Доброкачественные опухоли желудка – это группа новообразований эпителиального и неэпителиального гистогенеза, исходящих из разных слоев желудочной стенки, характеризующихся медленным развитием и относительно благоприятным прогнозом. Могут проявляться болями в эпигастрии, симптомами желудочного кровотечения, тошнотой, рвотой. Основными методами диагностики являются рентгенография желудка и фиброгастроскопия, гистологическое исследование опухолевой ткани. Лечение заключается в удалении неоплазий эндоскопическим методом или хирургическим путем.
Общие сведения
Доброкачественные опухоли желудка составляют в современной гастроэнтерологии 2-4% от общего числа всех опухолевых новообразований органа. Опухоли желудка могут исходить из его слизистого, подслизистого, мышечного или подсерозного слоя; из эпителиальных, нервных, сосудистых, жировых структур. По типу роста различают эндогастральные новообразования (растущие в сторону просвета желудка), экзогастральные (растущие в сторону соседних органов) и интрамуральные (с внутристеночным ростом).
Причины
Причины развития доброкачественных опухолей желудка окончательно не выяснены. С точки зрения дисрегенераторной теории, развитие полипов может быть связано с нарушением регенерации слизистой оболочки желудка, дискоординацией процессов пролиферации и дифференцировки ее клеток при хроническом гастрите. Аденомы желудка возникают на фоне атрофического гастрита в результате перестройки желез и покровного эпителия, появления кишечной метаплазии.
Гиперпластические полипы развиваются при нарушении обновления и увеличения продолжительности жизни клеток, из-за избыточной регенерации покровно-ямочного эпителия. Также отмечено, что чаще всего полипы желудка возникают в зонах со сниженной секрецией соляной кислоты (нижняя треть желудка), у больных с гипо- и ахлоргидрией. Источником неэпителиальных опухолей может быть гетеротопированная эмбриональная ткань, сохранившаяся в слизистой оболочке при нарушении внутриутробного развития.
Классификация
В зависимости от происхождения доброкачественные новообразования желудка разделяются на эпителиальные и неэпителиальные. Среди эпителиальных опухолей встречаются единичные или множественные аденоматозные и гиперпластические полипы, диффузный полипоз. Полипы представляют собой опухолевидные эпителиальные выросты в просвете желудка с ножкой или широким основанием, шаровидной и овальной формы, с гладкой или грануляционной поверхностью, плотной или мягкой консистенцией.
Аденомы опасны в плане малигнизации и часто приводят к развитию рака желудка. До 75% доброкачественных эпителиальных опухолей желудка составляют гиперпластические (опухолеподобные) полипы, возникающие вследствие очаговой гиперплазии покровного эпителия, имеющие относительно низкий риск озлокачествления (около 3%). При диффузном полипозе желудка выявляются и гиперпластические, и аденоматозные полипы.
Также в желудке могут наблюдаться дермоиды, остеомы, хондромы, гамартомы и гетеротопии из тканей поджелудочной железы, дуоденальных желез. Неэпителиальные доброкачественные неоплазии чаще возникают у женщин и иногда могут достигать значительных размеров. Они имеют четкие контуры, обычно округлую форму, гладкую поверхность.
Лейомиомы – наиболее часто встречающиеся доброкачественные неэпителиальные опухоли могут оставаться в мышечном слое, расти в направлении серозной оболочки или прорастать сквозь слизистую желудка, приводя к изъязвлению и желудочному кровотечению. Неэпителиальные новоообразования желудка предрасположены к малигнизации.
Симптомы
В половине случаев полипы желудка протекают без клинических проявлений. Симптомы в основном определяются фоновым заболеванием (хроническим гастритом) и осложнениями (изъязвлением верхушки полипа, кровотечением, пролапсом полипа в двенадцатиперстную кишку и непроходимостью привратника). Боли при полипах желудка обусловлены воспалительным процессом в окружающей его слизистой оболочке, локализуются в эпигастральной области и имеют тупой, ноющий характер. Сначала они возникают после приема пищи, затем становятся постоянными.
Клинические признаки неэпителиальных опухолей зависят от их локализации, характера и скорости роста, наличия изъязвления поверхности. Чаще всего неэпителиальные опухоли желудка сопровождаются кратковременными и постоянными болями, возникающими натощак, после приема пищи, при изменении положения тела. При невриномах болевой синдром сильный, жгучего характера. Изъязвление опухоли (особенно, гемангиомы) может вызывать скрытые или обильные желудочные кровотечения с угрозой для жизни больного.
При большом размере опухоли могут пальпироваться через переднюю брюшную стенку. Доброкачественные неэпителиальные неоплазии могут осложняться перитонитом при некрозе новообразований; острой или хронической непроходимостью привратника в случае ущемления в нем опухоли и ее злокачественным перерождением.
Диагностика
Диагностировать опухоли позволяют данные анамнеза, рентгенологического и эндоскопического исследований. На наличие полипов при рентгенографии желудка может указывать дефект наполнения, повторяющий очертания опухоли: четкие, ровные контуры, круглую или овальную форму, его смещаемость при наличии ножки или неподвижность – при полипе с широким основанием.
В случае полипоза желудка выявляют большое число разных по величине дефектов наполнения. Перистальтика стенок желудка при этом сохраняется. Признаки отсутствия перистальтики, увеличение размера, изменение формы, появление нечеткости контуров дефекта наполнения при динамическом наблюдении могут говорить о малигнизации полипа.
Диагноз уточняется при фиброгастродуоденоскопии (ФГДС), которая позволяет провести визуальный осмотр состояния слизистой оболочки желудка, распознавание и дифференциацию полипов от других заболеваний. Визуальная дифференциация доброкачественного полипа от малигнизированного затруднена. Обычно об озлокачествлении могут свидетельствовать наличие полипа размером более 2 см, с бугристой дольчатой поверхностью, неправильными изъеденными контурами. Для точного определения характера полипа во время ФГДС выполняется биопсия подозрительных участков с морфологическим исследованием биоптатов.
Диагноз неэпителиальной неоплазии в большинстве случаев можно установить только после операции и морфологического исследования данного новообразования. Наличие клинических проявлений (например, кровотечения) указывает на возможность опухолевого процесса. ФГДС более информативна при эндогастральном росте неэпителиальных опухолей. При интрамурально или экзогастрально расположенных новоообразованиях при эндоскопическом исследовании определяется сдавление желудка извне.
Рентгенография желудка при неэпителиальных объемных процессов помогает обнаружить округлые или неправильные контуры дефекта наполнения с сохранением перистальтики и складок на подслизистом слое; экзогастральный рост новообразования с оттягиванием стенки желудка; изъязвление с образованием ниши на верхушке опухоли и др. Для обнаружения экзогастральных опухолей могут быть использованы УЗИ и КТ брюшной полости.
Лечение доброкачественных опухолей желудка
Лечение патологии только хирургическое; метод оперативного вмешательства зависит от вида, характера опухоли и ее локализации. В отсутствии надежных критериев малигнизации необходимо проводить удаление всех выявленных новообразований. Основными методами удаления доброкачественных опухолей в настоящее время являются малоинвазивная эндоскопическая электроэксцизия (или электрокоагуляция), энуклеация, резекция желудка, редко – гастрэктомия.
При множественных полипах или подозрении на малигнизацию выполняют ограниченную или субтотальную резекцию желудка. После полипэктомии и резекции существует риск неполного удаления, рецидива и малигнизации опухоли, возможно развитие послеоперационных осложнений и функциональных расстройств. Гастрэктомия может быть показана при диффузном полипозе желудка.
Доброкачественные опухоли желудка
Доброкачественная опухоль желудка – это новообразование, которое не имеет признаков злокачественного процесса. В некоторых случаях остается небольшой риск перерождения при отсутствии соответствующего лечения. Доброкачественные новообразования желудка составляют до 5% от числа всех опухолевых заболеваний желудка, могут развиваться из эпителия, нервной ткани, жировых структур или сосудистых. Рост может быть быстрый или замедленный. По направлению роста выделяют опухоли, движущиеся в сторону просвета желудка, в сторону органов брюшной полости и новообразования, которые разрастаются внутри стенки. По локализации они с одинаковой частотой возникают в теле желудка, антральном отделе или в других местах.
Разновидности и особенности желудочных опухолей
По происхождению все новообразования, локализованные в области желудка, разделяют на две большие группы: эпителиальные и неэпителиальные.
Среди первой группы встречаются аденомы и полипы (одиночные или группами). Разница в том, что полипы – это выросты в просвет органа, они обычно округлой формы и имеют широкое основание, могут располагаться на ножке. Развитие полипов ассоциировано с возрастными изменениями – чаще встречаются в возрасте после 40 лет, болезнь поражает мужчин чаще, чем женщин. Гистологически полип представляет собой разросшиеся железистые и эпителиальные ткани с соединительнотканными элементами и развитой сетью сосудов.
Аденомы – это истинные доброкачественные новообразования, состоящие преимущественно из железистой ткани. В отличие от полипов, аденома может чаще перерождаться. Но встречаются реже, чем полипы.
Неэпителиальные опухоли встречаются редко. Они формируются в стенке желудка и могут состоять из самых разных тканей.
К неэпителиальным новообразованиям относят:
В отличие от полипов, которые чаще встречаются у мужчин, опухоли неэпителиальной природы чаще диагностируют у женщин. У всех подобных новообразований есть отличительные особенности: как правило, они имеют четкий контур, гладкую поверхность, округлую форму. Могут разрастаться до значительных размеров.
Особо выделяют неэпителиальную опухоль лейомиому – она встречается с более высокой частотой, чем другие новообразования из этой группы. Эта опухоль может вызывать желудочные кровотечения или потенцировать образование язв за счет прорастания в слизистую оболочку желудка. Все неэпителиальные новообразования отличаются достаточно высоким риском онкологического перерождения – малигнизации.
Симптомы
Симптомы опухоли желудка, как правило, слабо выражены. Если новообразование не растет, то практически не проявляется и никак не наблюдается. Очень часто доброкачественные опухоли определяют по косвенным признакам или выявляют случайно при эндоскопическом обследовании.
Клиническая картина включает в себя:
При абсолютно спокойном течении могут наблюдаться боли тупого и ноющего характера, локализованные, как правило, в эпигастрии. Боль нередко возникает после приема пищи. Достаточно часто больные ассоциируют эти симптомы с гастритом.
При опухолях достаточно большого размера могут наблюдаться более выраженные проявления. Появляется тяжесть, возникают приступы тошноты, появляется частая отрыжка. В рвотных массах и стуле больные обнаруживают примеси крови. В лабораторных анализах определяют пониженный гемоглобин. Пациенты испытывают слабость и головокружения. Вне зависимости от сохранности нормального аппетита начинается потеря веса. Всего различают более сотни видов доброкачественных новообразований – с разным течением и клинической картиной. Выраженность симптомов зависит от локализации, размера и скорости роста опухоли. Классической клинической картиной, позволяющей заподозрить опухоль, считается кровотечение, сопровождаемое общими нарушениями работы ЖКТ.
Причины
На сегодняшний день все причины образования доброкачественных опухолей желудка неизвестны. Поэтому правильно говорить о факторах риска – факторах, которые провоцируют патологические процессы, приводящие к появлению новообразований. В их числе наличие других заболеваний ЖКТ.
Наиболее актуальная теория гласит, что полипы появляются в результате нарушений естественной регенерации слизистой желудка. Поэтому полипы часто развиваются на фоне гастрита. Аденомы чаще сопровождаются атрофическим гастритом. При этом отмечено, что более 70% всех новообразований развивается в нижней трети желудка – то есть в зоне с пониженной концентрацией соляной кислоты.
Причиной развития неэпителиальной опухоли могут быть эмбриональные нарушения или наличие хронических заболеваний. Так как конкретных причин выявить не удается, не существует и специфической профилактики доброкачественных опухолей. Нельзя забывать и о наследственной предрасположенности – пациентам, чьи родственники имели новообразования желудка, необходимо даже при отсутствии каких-либо симптомов заболевания желудка выполнять эндоскопическое исследование. В любом случае, при подозрении на наличие полипа или полиповидного образования желудка следует обратиться к хирургу.
Неэпителиальные доброкачественные опухоли желудка
Неэпителиальные доброкачественные опухоли желудка
К этой категории новообразований относятся опухоли, растущие из мышечной, жировой, нервной, соединительной и сосудистой ткани. Их процент невелик – всего 0,5 – 3% от числа новообразований желудка. В 6-10 % опухолевый процесс переходит в рак, поэтому неэпителиальные новообразования желудка нужно выявлять и удалять.
Причины развития неэпителиальных опухолей желудка
Точная причина возникновения опухолей неизвестна, но считается, что предрасполагающими факторами являются:
Какие опухоли встречаются чаще всего
Большинство желудочных неэпителиальных новообразований составляют миомы (лейомиомы), растущие из мышечной ткани. Они выглядят, как плотные узлы и бывают двух типов:
Миомы характеризует медленный рост и способность разрастаться до внушительных размеров. В медицине описаны миомы весом 5 кг и размером 20 см. Крупные опухоли затрудняют работу желудка и сдавливают другие органы. У женщин они образуются чаще, чем у мужчин. Эти новообразования перерождаются в миосаркому, приводящую к быстрой гибели больного.
Невриномы желудка – опухоли, растущие из нервной ткани. Они медленно растут, но могут перерождаться в злокачественные нейросаркомы.
Фибромы и нейрофибромы желудка разрастаются в соединительной ткани нижней части желудка. Болезнь чаще регистрируется в пожилом возрасте. В рак желудка опухоль перерождается всего в 1,3% случаев.
Липомы – мягкие опухоли, растущие из жировой ткани. В рак перерождаются крайне редко, но могут мешать продвижению пищи и работе соседних органов.
Лимфангиомы и гемангиомы – сосудистые новообразования, которые практически не растут, но могут воспаляться, вызывая боль, повышение температуры и кровотечения.
Симптомы неэпителиальных опухолей желудка
Более половины новообразований не дают выраженных симптомов, потому что имеют небольшой размер и не мешают работе органов. Жалобы у больных возникают по мере роста опухолей:
Опухоли вызывают тупые или жгучие боли в верхней части живота при перемене положения тела, натощак или после еды. Вначале боль слабая и кратковременная, но по мере роста образования она усиливается. Опухолевые процессы могут осложняться прободением стенки желудка, опасным для жизни больного.
Диагностика и лечение
Опухоли обнаруживаются при рентгенографии желудка. На рентгене новообразования выглядят, как дефекты заполнения с темными контурами правильной или неправильной формы. Если привратник не закрыт, орган функционирует нормально. Слизистая желудка растянута, поэтому его складки уплощены.
Изъязвление выглядит на рентгенограмме как очаг неправильной формы. Иногда наблюдается отек слизистой, заметный на снимке.
Опухоли мягкой консистенции, например, липомы, на рентгене не видны. Для их обнаружения используется МРТ, КТ и УЗИ-диагностика.
Диагноз подтверждается на фиброгастроскопии со взятием фрагмента образования на анализ. Однако не всегда расположение опухоли позволяет это сделать. В этом случае диагноз ставится только после операции.
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Фиброгастроскопия-1.jpg?fit=450%2C289&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Фиброгастроскопия-1.jpg?fit=858%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/%D0%A4%D0%B8%D0%B1%D1%80%D0%BE%D0%B3%D0%B0%D1%81%D1%82%D1%80%D0%BE%D1%81%D0%BA%D0%BE%D0%BF%D0%B8%D1%8F-1.jpg?resize=900%2C577&ssl=1″ alt=»Фиброгастроскопия» width=»900″ height=»577″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Фиброгастроскопия-1.jpg?w=900&ssl=1 900w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Фиброгастроскопия-1.jpg?w=450&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Фиброгастроскопия-1.jpg?w=858&ssl=1 858w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Фиброгастроскопия-1.jpg?w=768&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″ /> Фиброгастроскопия
Неоперационные методы лечения опухолей не существуют, поэтому образование приходится удалять. В зависимости от размера и места расположения опухоль вырезают эндоскопическим методом или с помощью частичной (клиновидной) резекции.
После операции больной находится под наблюдением, чтоб не пропустить образование рака.
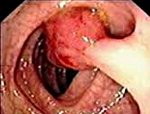
Что такое подслизистое образование желудка
Подслизистые новообразования желудочно-кишечного тракта представляют собой гетерогенную группу заболеваний, общим признаком которых является локализация патологического очага под слизистой стенки полого органа. Наиболее часто они выявляются при эндоскопическом исследовании в виде округлой или овоидной формы образований, деформирующих просвет органа и в большинстве наблюдений покрытых неизмененной слизистой.
Подслизистые новообразования составляют 5% всех образований верхних отделов желудочно-кишечного тракта и включают разные опухоли мышечного, неврогенного, сосудистого и смешанного происхождения, а также пороки развития в виде эктопии поджелудочной железы и дупликационных кист (табл. 1) [1]. 
Длительное время подслизистые новообразования рассматривались хирургами в качестве доброкачественных опухолей, преимущественно подлежащих динамическому наблюдению. Исключение составляли новообразования больших размеров, имеющие клинические проявления, которые определяли показания к оперативному вмешательству. Однако выделение в структуре подслизистых опухолей ГИСО, которые считаются потенциально злокачественными, заставило кардинально изменить тактические подходы к лечению. В связи с возросшим за последнее время интересом врачей к этим новообразованиям все большее число исследований посвящено их морфологии, методам диагностики и тактике лечения.
Материал и методы
В нашей работе проведен анализ эндоскопической диагностики и результатов лечения 38 пациентов с 39 подслизистыми новообразованиями верхних отделов желудочно-кишечного тракта, которые были госпитализированы в Институт хирургии им. А.В. Вишневского в период с 2005 по 2009 г. (табл. 2). 
Результаты и обсуждение
Все пациенты обследованы по стандартному протоколу, включающему общеклинические и биохимические исследования, ультразвуковое исследование, компьютерную томографию, магнитно-резонансную томографию, эзофагогастродуоденоскопию. Эндоскопическая ультрасонография (ЭУС) как самый точный метод диагностики подслизистых новообразований была выполнена 37 (97,4%) пациентам.
Дупликационные кисты обычно исходят из 4-го (мышечного) или реже 3-го (подслизистого) эхослоя и нередко достигают больших размеров. При других лучевых методах исследования их нередко принимают за кисты поджелудочной железы или печени. С учетом доброкачественного характера этих образований своевременная и точная диагностика позволяет при доступной локализации использовать различные варианты малоинвазивного хирургического лечения (эндоскопическая, лапароскопическая или робот-ассистированная операция). В одном из наших наблюдений было выявлено кистозное новообразование верхнего отдела брюшной полости, которое на основании данных ультразвукового исследования и компьютерной томографии было расценено как киста поджелудочной железы или неорганная забрюшинная опухоль. Только проведение эндосонографии позволило установить, что киста, имеющая размер более 4 см, связана со стенкой желудка и исходит из 4-го эхослоя (мышечный слой стенки, рис. 4). 
Гиперэхогенные новообразования в большинстве наблюдений являются липомами. Обычно они локализуются в 3-м эхослое, однако в 2 наших наблюдениях липомы выявлялись и во 2-м слое. Наиболее часто липому необходимо дифференцировать с нейроэндокринной опухолью, эктопированной поджелудочной железой, а также с ГИСО.
Гипоэхогенные новообразования вызывают наибольшие сложности в диагностике, так как такую структуру могут иметь все остальные подслизистые опухоли, включая эктопированную поджелудочную железу.
Все остальные пациенты были оперированы. Выбор объема оперативного вмешательства определяли на основании предположительного характера новообразования, его размера, топической принадлежности к определенному слою стенки органа и распространенности за его пределы.
При ГИСО отдавали предпочтение клиновидной резекции желудка с использованием лапароскопического или традиционного доступа, а при локализации опухоли в двенадцатиперстной кишке выполняли ее изолированную сегментарную резекцию или панкреатодуоденальную резекцию открытым способом. При выборе хирургического доступа также принимали во внимание прогнозируемую степень злокачественности опухоли. Признаками злокачественного потенциала по данным ЭУС являлись:
— размер опухоли более 3-4 см;
— неровный контур новообразования;
— наличие внутренних фокусов повышенной эхогенности или кист;
— инвазия опухоли в слизистую или выход ее за пределы стенки полого органа;
— быстрый рост при динамическом наблюдении [4, 6].
При дупликационной кисте пищевода проводили пункцию образования под эндосонографическим контролем с аспирацией содержимого. После морфологического исследования с подтверждением предоперационного диагноза выполняли эндоскопическое иссечение «крыши» кисты, выступающей в просвет органа, с полным удалением содержимого и аргоноплазменной коагуляцией эпителиальной выстилки остающейся части.
Во всех наблюдениях после эндоскопического удаления новообразования производили тщательную ревизию зоны резекции с обязательной электро- или аргоноплазменной коагуляцией сосудов.
Среди осложнений наиболее вероятны перфорация полого органа и кровотечение. В одном наблюдении небольшое подслизистое новообразование, локализующееся в дне желудка, подвижное при инструментальной пальпации, с несмещаемой слизистой над ним было ошибочно расценено как исходящее из 2-го эхослоя. Эндоскопическую ультрасонографию не производили. Однако при его удалении произошла перфорация стенки желудка. Дефект был клипирован со стороны слизистой желудка. В послеоперационном периоде проводили консервативную терапию. Оперативное вмешательство не потребовалось. При гистологическом исследовании выявлена лейомиома, исходящая из мышечной стенки желудка. Это наблюдение еще раз подчеркивает роль эндосонографии в выборе метода хирургического лечения. Еще в одном наблюдении после удаления липомы бульбодуоденального перехода двенадцатиперстной кишки в послеоперационном периоде при КТ брюшной полости в забрюшинном пространстве выявлено небольшое скопление воздуха без клинических проявлений, характерных для перфорации полого органа (рис. 10). 
Трансабдоминальное УЗИ, как правило, малоинформативно, так как новообразования располагаются в стенке воздухсодержащих органов и визуализация их затруднена вследствие экранирования ультразвуковых волн воздухом. КТ и МРТ выявляют крупные новообразования, однако часто возникают трудности с определением органной принадлежности опухоли (подслизистые образования расцениваются как опухоли печени, поджелудочной железы, неорганные забрюшинные опухоли). Точная топическая диагностика опухоли возможна только при проведении эндоскопической ультрасонографии, на основании результатов которой определяют тактику хирургического лечения и выбирают оптимальный оперативный доступ. Этот метод позволяет не только достоверно различать новообразования стенки и экстраорганные структуры, но и определять слой, из которого происходит новообразование, а также, оценивая его эхогенную характеристику, четко дифференцировать неэпителиальные опухоли и неопухолевые образования желудочно-кишечного тракта [1]. При выявлении неэпителиальных опухолей перед эндосонографическим исследованием встает задача определения признаков их злокачественности.
По нашему мнению, все подслизистые новообразования, при которых сохраняется даже малый процент вероятной ошибки в дифференциальной диагностике их с ГИСО, подлежат оперативному лечению с последующим гистологическим и иммуногистохимическим исследованием.
Задачами эндосонографического исследования являются определение органной принадлежности новообразования, его структуры и локализации в стенке полого органа, т.е. из какого именно слоя оно происходит. Тактику лечения таких пациентов следует определять, основываясь преимущественно на данных, полученных при эндосонографии [2], за исключением наблюдений, в которых развиваются осложнения, требующие оперативного лечения независимо от размеров и локализации опухоли.
При опухолях, не выходящих за пределы органа и не имеющих признаков злокачественности, возможно выполнение малоинвазивных операций. При локализации опухоли в мышечной пластинке слизистой и подслизистом слое целесообразно эндоскопическое удаление. При локализации образования в мышечном слое необходимо выполнение лапароскопической резекции стенки органа, несущего опухоль. Опухоли большого размера, выходящие за пределы органа и имеющие дооперационные признаки высокого риска злокачественности, требуют резекции из лапаротомного доступа с соблюдением всех онкологических принципов.
Таким образом, современный взгляд на диагностику и лечебную тактику предусматривает необходимость удаления подслизистых образований независимо от их вида и размера, что объясняется невозможностью точной дифференциальной диагностики с гастроинтестинальной стромальной опухолью без проведения иммуногистохимических исследований. Эндоскопическая ультрасонография является ведущим методом диагностики подслизистых новообразований и позволяет определить тактику лечения и выбрать оптимальный оперативный доступ.