Что такое пограничная опухоль
Кафедра общей хирургии ФГБОУ ВО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава РФ, Рязань, Россия
ГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
Московский научно-исследовательский онкологический институт им. П.А. Герцена Росмедтехнологий, Москва
Клинико-морфологические факторы прогноза при пограничных опухолях яичников
Журнал: Онкология. Журнал им. П.А. Герцена. 2014;3(3): 22-25
Виноградов И. И., Андреева Ю. Ю., Новикова Е. Г., Шевчук А. С., Завалишина Л. Э., Франк Г. А. Клинико-морфологические факторы прогноза при пограничных опухолях яичников. Онкология. Журнал им. П.А. Герцена. 2014;3(3):22-25.
Vinogradov I I, Andreeva Yu Yu, Novikova E G, Shevchuk A S, Zavalishina L É, Frank G A. Clinical and morphological predictors in borderline ovarian tumors. P.A. Herzen Journal of Oncology. 2014;3(3):22-25.
Кафедра общей хирургии ФГБОУ ВО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава РФ, Рязань, Россия
Высокий удельный вес в структуре заболеваемости пограничными опухолями яичников составляют женщины репродуктивного возраста. В этой связи часто встает вопрос об органосохраняющих методах лечения, что в свою очередь диктует необходимость оценки риска развития рецидива. Цель исследования — оценка влияния на развитие рецидива таких морфологических факторов, как гистологический тип, наличие имплантов, псаммомных телец и микрососочковых структур в пограничной опухоли. Материал и методы. Материалом для исследования служили гистологические препараты опухолей от 101 женщины в возрасте от 18 до 63 лет (средний возраст 32,14 года), проходившей лечение или консультированной в МНИОИ им. П.А. Герцена с диагнозом пограничной опухоли яичников. Результаты. Выявлено, что импланты, псаммомные тельца и микрососочковая архитектура чаще ассоциированы с рецидивными опухолями.
Кафедра общей хирургии ФГБОУ ВО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава РФ, Рязань, Россия
ГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
Московский научно-исследовательский онкологический институт им. П.А. Герцена Росмедтехнологий, Москва
История изучения пограничных опухолей яичников (ПОЯ) насчитывает уже около 100 лет, однако многие вопросы до настоящего времени не находят своего ответа. Впервые ПОЯ были описаны в 1929 г. гинекологом из США Говардом Тэйлором [1]. Он назвал эти опухоли «полузлокачественными», подчеркивая тем самым особенности их клинического течения, существенно отличающегося как от классического рака яичников, так и от доброкачественных образований.
В структуре неоплазий яичников доля пограничных опухолей составляет около 10—15%, показатели заболеваемости варьируют в различных странах от 1,8 до 4,8‰. ПОЯ развиваются из поверхностного эпителия яичников и кист-включений. С морфологических позиций эти новообразования характеризуются умеренно выраженными пролиферативной и митотической активностью, стратификацией эпителия, ядерной и клеточной атипией. Принципиальным отличием пограничных опухолей от рака яичников является отсутствие стромальной инвазии и характерного для аденокарцином инфильтративного деструктивного роста. Именно эти морфологические характеристики ПОЯ предопределяют их особенное положение в спектре биологической агрессивности опухолей яичников [2, 3].
Соответственно различным видам эпителия, представленного в женской половой системе, выделяют следующие гистологические типы пограничных опухолей: серозные, муцинозные, эндометриоидные, опухоли Бреннера, светлоклеточные и смешанные. Наиболее часто встречаются серозная (50—55%) и муцинозная формы (40—45%), на долю остальных типов ПОЯ приходится 4—5% наблюдений [4, 5]. Характерной особенностью серозных ПОЯ является высокая частота двустороннего поражения яичников, варьирующая от 28 до 66%. Билатеральные муцинозные опухоли наблюдаются не более чем в 10% наблюдений [6, 7].
Экстраовариальные очаги пограничных опухолей на брюшине получили название «имплантов», которые классифицируют на неинвазивные и инвазивные. Чаще выявляют неинвазивные импланты (75%), характеризующиеся торпидным доброкачественным течением. К особенностям этих имплантов следует отнести возможность злокачественной трансформации, способность формировать обширные очаги фиброза в брюшной полости в результате десмоплазии, нередко приводящие к развитию кишечной непроходимости и, как это ни парадоксально, возможность спонтанной регрессии после удаления первичного очага. Инвазивные импланты обнаруживаются в 25% наблюдений и только при серозном варианте ПОЯ. Клинические и морфологические особенности инвазивных имплантов аналогичны таковым при метастазах рака яичников. Учитывая эти обстоятельства, многие патоморфологи предлагают рассматривать серозные пограничные опухоли с инвазивными имплантами как высокодифференцированные серозные аденокарциномы. В целом, перитонеальная диссеминация на момент установки диагноза определяется у 35—38% пациенток с серозными ПОЯ и у 10—15% с муцинозными [8].
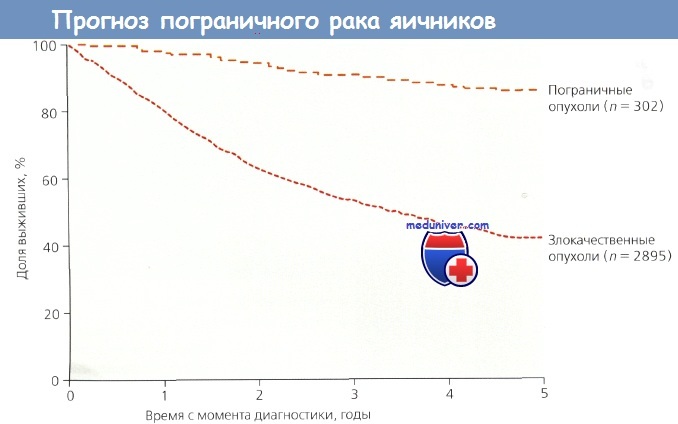
Благодаря длительному торпидному течению, ПОЯ в большинстве случаев (60—85%) диагностируют в I стадии процесса. Частота выявления III стадии заболевания составляет 10—35%, при раке яичников — 60—70%. Особенности биологии ПОЯ и преобладание начальных форм заболевания предопределяют хороший прогноз для больных. Если в течение последних десятилетий в результате применения новейших схем лечения удалось приблизить показатели общей 5-летней выживаемости пациенток с раком яичников к 50%, то выживаемость больных с пограничными опухолями остается достаточно стабильной и превышает 90% [7].
Поскольку удельный вес женщин репродуктивного возраста в структуре заболеваемости ПОЯ достаточно высок (более 30%), вопросы сохранения фертильности занимают центральное место в лечении этой категории больных. Благоприятный прогноз, низкая частота рецидивирования и впечатляющие показатели выживаемости, безусловно, создают предпосылки для более широкого применения органосохраняющих и репродуктивных технологий при ПОЯ, чем при раке яичников [9].
Несмотря на высокие показатели выживаемости, поиск новых и оценка существующих прогностических факторов при ПОЯ имеют существенное значение, особенно при планировании органосохраняющего лечения у молодых пациенток.
Как и при раке яичников, при ПОЯ стадия опухолевого процесса является наиболее важным прогностическим фактором. Известно, что у больных с начальными формами болезни рецидивы развиваются в среднем у 5%, при распространенных стадиях — в 25% случаев, а 5-летняя выживаемость при I—II и III—IV стадиях составляет 98 и 82—90% соответственно [7].
Наличие перитонеальных имплантов, особенно инвазивных, является вторым по значимости фактором прогноза. По своему строению и клиническому течению инвазивные импланты очень схожи с метастазами рака яичников и могут служить маркером злокачественной трансформации пограничной опухоли. По данным P. Morice [10], рецидивы при инвазивных имплантах наблюдаются в 2 (45% против 24%) раза чаще, чем при неинвазивных. Десятилетняя выживаемость пациенток с неинвазивными имплантами пограничных опухолей составляет 90—95%, с инвазивными — 60—70%.
В настоящее время в литературе активно обсуждается прогностическая значимость некоторых морфологических особенностей пограничных опухолей. Так, в серозных пограничных опухолях могут быть обнаружены очаги хрупкой микропапиллярной архитектуры (рис. 1, 2,). Результаты проведенных исследований показали, что рост по поверхности яичника и наличие имплантов больше характерны для микрососочковых серозных пограничных опухолей, чем для типичных [11, 12]. Помимо этого, имеются данные об увеличении частоты рецидивов (до 36%) при микрососочковой структуре пограничной опухоли, выявляемой у 12—18% больных [7].

Много споров ведется вокруг присутствия в ПОЯ кальцификатов, именуемых псаммомными тельцами. Предпринятые попытки определить их возможное прогностическое значение пока не принесли конкретных результатов. Ряд авторов [13] предполагают, что наличие псаммомных телец в высокодифференцированных аденокарциномах обусловлено хорошим прогнозом, объясняя этот факт тем, что их образование связано с повышенным апоптозом в опухоли. Другие [14] считают, что псаммомные тельца не имеют прогностической значимости.
Некоторые авторы [6, 15] связывают высокую частоту рецидивов с наличием микроинвазии, имеющей место у 10—13% больных, и рассматривают фокусы микроинвазии в качестве мелких очагов инвазивного серозного рака, развивающегося на фоне пограничной опухоли. Считается, что это обстоятельство должно служить поводом к изменению диагноза в пользу рака яичников с применением более агрессивной лечебной тактики.
Определенное прогностическое значение при ПОЯ может иметь ДНК-плоидность опухоли. Так, в работах J. Kaern (1993, 2009) было показано, что при анеуплоидии риск умереть от пограничной опухоли в 19 раз выше, чем при диплоидных образованиях [8].
Убедительных данных о том, что гистологический тип опухоли или вовлечение в опухолевый процесс лимфатических узлов является независимым прогностическим фактором, получено не было. Так, проведенный метаанализ 97 исследований, включавший более 4000 больных с ПОЯ, показал, что 6-летняя выживаемость больных с поражением лимфатических узлов составила 98% [16].
Цель настоящего ретроспективного исследования — оценка влияния на развитие рецидива таких морфологических факторов, как гистологический тип, наличие имплантов, псаммомных телец и микрососочковых структур в пограничной опухоли яичников.
Материал и методы
Материалом для исследования служили гистологические препараты пациенток, проходивших лечение или консультированных в МНИОИ им. П.А. Герцена с диагнозом: пограничная опухоль яичников. Исследованы образцы опухолей 101 женщины в возрасте от 18 до 63 лет (средний возраст 32,14 года).
Пациентки были разделены на две группы: 1-я — больные без рецидивов ПОЯ (83 человека — 82,2%); 2-я — больные с рецидивами ПОЯ (18 человек — 17,8%).
Материал фиксировали в 10% забуференном формалине в течение 24 ч, обрабатывали по стандартной методике с использованием ксилола и заливали в парафин. Из блоков изготавливали срезы толщиной 4 мкм, окрашивали гематоксилином и эозином.
Препараты изучали при помощи светового микроскопа Axioskop «OPTON» со стандартным набором оптики. Анализ результатов проводили при помощи пакета программ Statistica 6.0, используя метод процентилей описательной статистики, U-тест Манна—Уитни. Уровень значимости (р) принимали равным 0,05.
Результаты и обсуждение
Нами было выявлено, что подавляющее большинство (78,2%) исследованных ПОЯ были представлены серозным типом. Муцинозные опухоли имели место в 13,8% случаев, смешанные — в 5%, эндометриоидные — в 3%. Однако при изучении распределения типов ПОЯ в исследуемых группах статистически значимых различий обнаружено не было (р>0,05).
Неинвазивные импланты в группе больных без рецидивов отмечены в 15,7% случаев, а в группе с рецидивами — в 77,8%. При этом были выявлены статистически значимые различия по частоте встречаемости имплантов в исследуемых группах (р
Пограничные опухоли яичников
Диагностируют пограничные опухоли у женщин в возрасте от тридцати до сорока пяти лет, и именно они выступают причиной, из-за которой пациентки не могут забеременеть.
Высокая вероятность рецидива в случае не радикального лечения не дает отнести их к доброкачественным новообразованиям, но и к злокачественным отнести их не представляет возможным. Более чем в шестидесяти процентов случаев диагностируют пограничные опухоли яичников на начальной стадии, а это один из залогов благоприятного прогноза.
Проблема пограничной опухоли яичника состоит как раз в том, что женщины хотят сберечь фертильную функцию, а органосохраняющие методы лечения несут высокую вероятность рецидивирования.
Специалисты Юсуповской больницы разрабатывают план лечения для каждой пациентки индивидуально и максимально учитывают ее потребности. Врачи следят за новинками в медицине, внедряют новые методы и технологии. За годы работы в Юсуповской больнице диагностика и лечение пограничных опухолей яичников проводилась тысячам женщин, и каждая из них выбрала оптимальный для себя метод.
Лучшая больница Москвы с удобным расположением, ведущими специалистами разных отраслей медицины, современным оборудованием, компетентным персоналом и комфортабельными палатами оказывает помощь населению в круглосуточном режиме. Диагностику можно пройти амбулаторно, без очередей и заминок. Лечение подбирается с учетом особенностей каждой пациентки, а также разрабатывается курс реабилитации и в благоприятных условиях восстановление происходит в максимально короткие сроки. Записаться на консультацию необходимо в онлайн режиме и по телефону. Во время личного разговора с врачом можно получить ответы на вопросы о этиологии, патогенезе, диагностике, лечению и реабилитации данного заболевания, решить вопросы госпитализации и дальнейшей тактики.
В случае пограничных опухолей яичников очень важно в начальной стадии правильно расставить приоритеты и не допустить распространению заболевания. На сайте Юсуповской больницы большое количество информации, касающееся данной патологии, а также многих других. Сайт по праву считается одним из лучших информационных сайтов сети.
Причины пограничных опухолей яичников
Пограничные опухоли яичников по морфологическим, клиническим и прогностическим критериям занимают некое срединное положение между злокачественными и доброкачественными новообразованиями. Но, как и в их случае, достоверных причин их возникновения на данное время не установлено. Многочисленные проведенные исследования свидетельствуют о том, что значительно повышают вероятность возникновения пограничных опухолей яичников следующие факторы:
Не опровергается также и инфекционно-вирусная теория возникновения пограничных опухолей яичников.
Достоверным считается тот факт, что беременность, роды и кормление грудью значительно снижают риски возникновения пограничных опухолей яичников.
Классификация пограничных опухолей яичников
От злокачественных новообразований пограничные опухоли яичников отличаются тем, что для них нехарактерна стромальная деструктивная инвазия. Согласно цитологической классификации, пограничные опухоли яичников разделяют на наиболее распространённые – серозная и муцинозная, и более редкие – эндометриоидные, опухоль Бреннера, метанефроидные и смешанные формы.
Также их принято разделять на инвазивные и неинвазивные. Опухоли, которые имеют форму узла и располагаются на ножке, называют поверхностными, а кистовидные злокачественные новообразования – внутрияичниковыми.
Метастазы пограничных опухолей яичников могут располагаться как в толще, так и на поверхности малого и большого сальников.
Симптомы пограничных опухолей яичников
На ранних стадиях пограничные опухоли яичников не имеют не то что специфических признаков, а не дают клиники вообще. Очень часто их диагностируют случайно во время профилактических осмотров или проведения ультразвукового исследования.
Также заподозрить пограничную опухоль яичника может специалист в случае проблемы первичного бесплодия, ведь именно данная опухоль является причиной невозможности забеременеть. Если беременность все-таки наступает, пограничная опухоль яичника может выступить причиной невынашивания.
Хоть в начале заболевания клинических симптомов практически нет, но в дальнейшем могут возникнуть тянущие боли внизу живота и дискомфорт в пояснице, который вначале носит односторонний характер, но вскоре охватывает и вторую сторону. Эти симптомы неинтенсивные и редко становятся причиной обращения к специалисту.
Увеличение размера пограничной опухоли яичника к увеличению живота, что очень часто пациентки объясняют себе набором веса или беременностью.
В дальнейшем присоединяются симптомы, связанные с прогрессированием процесса:
Диагностика пограничных опухолей яичников
Сбор жалоб и анамнеза дополняется гинекологическим осмотром, а также лабораторными и инструментальными методами исследования.
Лабораторные методы включают следующие анализы:
Из инструментальных методов могут быть использованы следующие:
Проведение данных физикальных, лабораторных и инструментальных методов позволит не только определить доброкачественное, пограничное или злокачественное новообразование, а и даст представление о локализации, стадии и распространенности, а также поможет определиться с дальнейшей тактикой ведения пациентки.
Лечение пограничных опухолей яичников
Поскольку основная масса пациенток – женщины репродуктивного возраста, вполне обоснованным их желанием является сохранение матки как органа и, хотя бы, части яичника, которая бы и продолжала функционировать.
Эффективным и оправданным методом лечения пограничных опухолей яичников является хирургический метод.
Щадящая операция подразумевающая одностороннее удаление яичника и брюшины с сохранением второго яичника и матки несет за собой определенный риск. Каждая женщина должна понимать, что пограничная опухоль яичника после такой операции может, а как показывает практика скорее всего и будет, рецидивировать.
Если пациентка все-таки настаивает на органосохраняющей операции, она должна понимать серьезность ситуации и наблюдаться у гинеколога, регулярно обследоваться.
Важно знать, что есть возможность сохранить яйцеклетки путем криоконсервации, таки образом сохраняется возможность выполнения репродуктивной функции даже после двухстороннего удаления яичников.
Женщинам в менопаузе наиболее правильным считается обширное оперативное вмешательство, которое подразумевает удаление матки с придатками, большим сальником с последующей множественной биопсией брюшины. Такой объем вмешательства оправдан значительным улучшением прогноза при пограничной опухоли яичника после операции.
Многочисленные исследования свидетельствуют в пользу неэффективности применения химиотерапевтических препаратов для профилактики рецидивов.
Важно понимать, что несвоевременное лечение, или вовсе отказ от него несет за собой тяжелые последствия в виде перехода в злокачественную форму, так называемая малигнизация, сдавление соседних органов и структур, нарушение репродукции, некроз, перфорация, пенетрация, кровотечение и др.
Юсуповская больница – это не просто рядовая больница Москвы. Она изначально создавалась, чтоб каждый пациент мог в комфортных условиях, в окружении тепла и заботы, получить все необходимые медицинские услуги.
Диагностика и лечение в Юсуповской больнице выполняются с использованием современной техники. Все оборудование высокоточное, качественное. Доктора, которые работают в Юсуповской больнице, обладают не только наивысшими профессиональными, но и прекрасными человеческими качествами, такими как сочувствие и поддержка.
Персонал Юсуповской больницы работает двадцать четыре часа в сутки, чтобы каждый пациент мог получить высокопрофессиональную помощь в любое время суток.
Пограничные опухоли яичников хоть и очень часто долгое время не приносят никакого дискомфорта пациенткам, но требуют обязательного лечения. Опыт наших специалистов, современные технологии и совместная работа врачей Юсуповской больницы помогают найти подход к каждой пациентке, выбрать наиболее эффективную тактику лечения, обезопасить женщину от рецидива и дают возможность вновь почувствовать себя здоровой.
Не стоит откладывать проблему, необходимо немедленно ее решить. Обсудить и объяснить то, что раньше казалось пациенту недостижимым – важная часть работы хорошего специалиста. Вылеченная на ранней стадии пограничная опухоль яичника, не несет за собой никаких последствий для здоровья женщины. Записаться на консультацию можно по телефону или в онлайн режиме в любое время дня и ночи. В Юсуповской больнице всегда рады помочь пациенту.
Что такое пограничная опухоль
За последние 40 лет появились убедительные доказательства существования эпителиальных опухолей яичников с гистологическими и биологическими характеристиками, промежуточными между явно доброкачественными и явно злокачественными. Эти пограничные опухоли составляют приблизительно 15 % всех злокачественных эпителиальных новообразований яичников; их часто называют пролиферирующими цистаденомами. Они чаще возникают в молодом возрасте, а РЯ — в пожилом. При I стадии пограничных опухолей 10-летняя выживаемость составляет примерно 95 %. Однако у некоторых пациенток рецидив и летальный исход могут наступить через 20 лет после лечения, поэтому эти опухоли правильнее называть раком низкой степени злокачественности.
Пограничные серозные эпителиальные опухоли по гистологическому строению и прогнозу для жизни действительно занимают промежуточное положение между доброкачественными серозными цистаденомами и цистаденокарциномами. Внешний вид их напоминает серозные цистаденомы с папиллярными разрастаниями. Однако по сравнению с доброкачественными аналогами пограничные серозные опухоли чаще двусторонние и имеют большее количество сосочковых разрастаний. Выживаемость при злокачественных и пограничных серозных эпителиальных опухолях значительно различается.
Гистологические критерии пограничных опухолей:
• Стратификация эпителия папиллярных разрастаний.
• Образование микроскопических сосочковых выростов или ворсин из эпителия папиллярных разрастаний.
• Полиморфизм эпителия.
• Атипия.
• Митотическая активность.
• Отсутствие инвазии стромы.
По мнению Janovski и Paramananthon, в пограничной опухоли должно быть не менее двух из перечисленных выше признаков. Хотя пограничные серозные эпителиальные опухоли яичников детально изучены и признаны Международной федерацией акушеров и гинекологов (FIGO) в 1964 г., согласия по этому вопросу до сих пор нет. Например, среди серозных цистаденокарцином, несомненно, существует группа опухолей низкой степени злокачественности. В связи с этим непонятно, можно ли считать классификационный термин «пограничные» всегда конкретным. К сожалению, у некоторых врачей термин «пограничные» может создавать иллюзию благополучия. Наблюдение при этих опухолях должно быть таким же тщательным, как и при раке яичников (РЯ).
В 1973 г. Hart и Norris сообщили о больных с пограничными муцинозными опухолями одного или обоих яичников с корректированным показателем 10-летней выживаемости 96 %. Несмотря на то что происхождение серозных опухолей из зародышевого эпителия ни у кого не вызывает сомнений, гистогенез муцинозных опухолей до конца не выяснен. Внешний вид пограничных муцинозных опухолей практически не отличается от их доброкачественных прототипов: они многокамерные, кистозные, часто большие по объему, с гладкой наружной поверхностью. То же относится и к внутренней оболочке: она гладкая, как и удоброкачественных муцинозных цистаденом, хотя в 25—50 % случаев описаны папиллярные структуры и солидное утолщение капсулы.
При микроскопическом исследовании в пограничной опухоли в отличие от доброкачественной имеется 2 или 3 слоя эпителия. В доброкачественных поражениях нет полиморфизма и атипии клеток, а в эпителии пограничных образований обнаруживают неровные гиперхромные ядра, увеличенные ядрышки и фигуры митоза.
Пограничные опухоли подлежат полному удалению. При одностороннем поражении после тщательного обследования другого яичника (биопсия при необходимости) выполняют аднексэктомию или цистэктомию с цитологическим исследованием смывов из брюшной полости и резекцией сальника. Julian и Woodruff представили результаты лечения 65 пациенток с папиллярным серозным РЯ низкой степени злокачественности. 5-летняя выживаемость 50 пациенток после односторонней аднексэктомии составила 100 %, а в группе из 10 пациенток после радикальной операции (абдоминальная гистерэктомия с двусторонней аднексэктомией) — 90 %. Lim-Tan и соавт. наблюдали 35 пациенток с пограничными серозными опухолями яичников после одно- или двусторонней цистэктомии.
Персистенция или рецидив опухоли после цистэктомии отмечены у 2 (6 %) из 33 пациенток: в обоих яичниках у 1 (3 %) пациентки с I стадией заболевания и в противоположном яичнике также у 1 (3 %) пациентки. После операции все больные жили без признаков заболевания 3—18 лет, средний период наблюдения составил 7,5 года. Согласно результатам отдельных небольших исследований, у пациенток, планирующих иметь детей, приемлемый объем операции — цистэктомия, при условии небольшого риска.
При двустороннем поражении яичников, особенно с папиллярными разрастаниями на наружной поверхности опухоли или вовлечением в процесс брюшины, показано радикальное хирургическое лечение — абдоминальная гистерэктомия с двусторонней аднексэктомией и полным удалением пораженной брюшины таза. У пациенток с распространенными стадиями заболевания дополнительно выполняют цитологическое исследование, частичную оментэктомию и селективную тазовую и парааортальную лимфаденэктомию. Хотя для этой стадии заболевания (III) характерны метастазы в лимфоузлах, выживаемость довольно велика. Другие виды лечения I стадии пограничных опухолей яичников, за исключением хирургического, пока еще не разработаны.
Kolstad и соавт. разделили пациенток с I стадией пограничных опухолей на две группы: одним проводили адъювантную ЛТ на область таза, а у других комбинировали ее с и/п введением коллоидного радиоактивного золота. Показатели выживаемости составили 92 и 87,2 % соответственно; несколько пациенток умерли от осложнений, связанных с лечением золотом. По сравнению с тремя другими наблюдениями такая терапия, очевидно, привела к значительному снижению выживаемости.
Интраперитонеальное введение радиоактивного фосфора ( 32 Р) без ЛТ сопровождается меньшим числом осложнений и поэтому лучше подходит для лечения данной патологии.
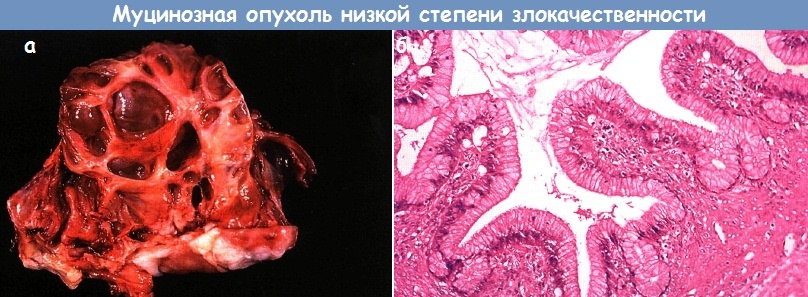
а — внешний вид;
б — микрофотография той же опухоли
Creasman наблюдал 55 пациенток с I стадией пограничных опухолей яичников или раком низкой степени злокачественности. Он сделал вывод об одинаковой эффективности послеоперационного тазового облучения и адъювантной XT после хирургического лечения. Gershenson и соавт., Bell и соавт. сообщили о результатах лечения больных с перитонеальными имплантатами, возникшими из пограничных серозных опухолей яичника. По данным Gershenson, 5-летняя безрецидивная выживаемость составила 95 %, а 10-летняя — 91 %. Согласно Bell, эти опухоли были непосредственной причиной смерти 13 % пациенток; 1 больная продолжала жить, несмотря на распространенное прогрессирующее заболевание.
Через 5 лет от основной болезни умерло 4 % женщин, через 10 лет — 23 %. Drescher и соавт. определяли содержание ДНК и изучали морфологию ядер в этих опухолях. По их мнению, оценка плоидности ДНК методом проточной цитометрии и анализ морфологии ядер у пациенток с пограничными опухолями может дать важную прогностическую информацию. Работы, подобные этой, крайне важны, т. к. при прогрессировании пограничных опухолей яичников онкогинекологи часто поднимают вопрос о назначении XT. Было бы хорошо идентифицировать признаки, позволяющие отличать злокачественные опухоли низкой степени злокачественности по биологическому поведению — агрессивные от находящихся в состоянии покоя, которые не представляют угрозу для здоровья и благополучия пациенток.
Некоторые экстраовариальные имплантаты состоят из неправильной формы железистых структур, погруженных в незрелую десмопластическую или воспаленную строму, что создает трудности в диагностике. Во многих случаях присутствуют инвазия подлежащих структур и клеточные признаки злокачественности. В отличие от поражений яичников они способны к инвазии и могут иметь независимое или аутохтонное происхождение. Другие умеренные скопления клеток в десмопластической грануляционной ткани без инвазии подлежащих структур названы неинвазивными имплантатами. Russell и Merkur сообщили о худшем прогнозе при инвазивных имплантатах по сравнению с неинвазивными.
Gershenson и соавт. обследовали 7 пациенток с инвазивными имплантатами после XT и последующей плановой повторной хирургической ревизии (операция «second-look»). Ответ на лечение обнаружен у 4 женщин. Наиболее активный цитостатик выявить не удалось. В практике авторов встретилось 39 больных с инвазивными имплантатами; в 12 (31 %) случаях развился рецидив или заболевание прогрессировало.
Trimble и Trimble в 1994 г. представили подробный обзор эпителиальных опухолей яичников с низким потенциалом злокачественности. Средний возраст выявления серозных и муцинозных опухолей низкой степени злокачественности был 40 лет, инвазивного РЯ — 60 лет. Проводя метаанализ 12 исследований по типу «случай-контроль», выполненных в США, Harris и соавт. установили, что средний возраст женщин с опухолями низкой степени злокачественности составлял 44 года, а при инвазивном РЯ — 52,9 года. Метаанализ Collaborative Ovarian Cancer Group позволил выявить защитные факторы против развития опухолей низкой степени злокачественности: беременность, кормление грудью и прием пероральных контрацептивов. Бесплодие в анамнезе увеличивает риск этих новообразований (отношение шансов 1,9), прием препаратов для лечения бесплодия увеличивает его еще больше, до показателя значительно выше, чем у женщин без бесплодия (отношение шансов 4,0).
Kurman и Trimble проанализировали выживаемость больных на основании обзора 22 исследований серозных опухолей низкой степени злокачественности без инвазивных перитонеальных имплантатов. У 538 пациенток с I стадией заболевания выживаемость составляла 99 %, средний период наблюдения — 7 лет. В группе 415 пациенток со II и III стадиями заболевания выживаемость за тот же промежуток времени составила 92 %. Анализ причин смерти показал, что 3 пациентки умерли от осложнений ЛТ, 9 — от XT, 8 — от кишечной непроходимости, 8 — от инвазивного рака, 18 — от основного заболевания (без дополнительного указания причин). Можно сказать, что большинство женщин умерли «с болезнью, но не от нее». Причиной смерти в основном были осложнения, связанные с лечением, а не кишечная непроходимость, характерная для прогрессирования заболевания.
Kurman выявил агрессивную подгруппу пролиферативных серозных поражений, которые назвал микропапиллярным серозным раком яичников (РЯ). Seidman и Kurman наблюдали 11 пациенток с микропапиллярными разрастаниями, причем, согласно их классификации, эти опухоли можно было отнести как к раку, так и к серозным пограничным опухолям с инвазивными имплантатами. Плохой прогноз при этих новообразованиях заставляет некоторых врачей назначать XT в дополнение к хирургическому лечению.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021





