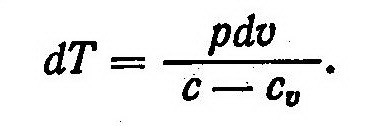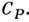Политропный процесс
Здравствуйте! В процессах изменения состояния газа переменными часто являются все параметры состояния (температура, давление, удельный объем), причем в некоторых процессах может изменяться и теплоемкость. Для того чтобы рассчитать такой процесс, необходимо знать зависимость теплоемкости от параметров процесса. Расчет значительно упрощается, если теплоемкость считать постоянной. Политропным называют процесс, происходящий при постоянной теплоемкости и вызываемый подводом тепла к рабочему телу или отводом тепла от него (название происходит от греческих слов «поли» — много и «тропос» — путь). В политропном процессе в общем случае могут изменяться все параметры и функции состояния.
Для вывода уравнения политропного процесса продифференцируем уравнение Клапейрона :
Из выражений dq=du+pdυ и du=cudT найдем
Подставив в это соотношение равенство dq = cdT, будем иметь
Из выражения (3) найдем
После подстановки этого равенства в выражение (1) получим
Величину газовой постоянной определим из уравнения Майера cp = cυ + R.
Подставив величину R в выражение (4), и выполнив некоторые преобразования, найдем
Разделив уравнение (5) на pυ и введя обозначение
Интегрирование этого выражения возможно при условии n = const, то есть c=const. После интегрирования уравнения (7) получим
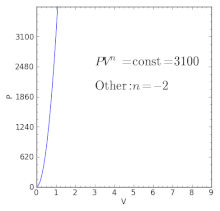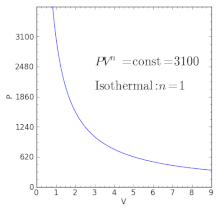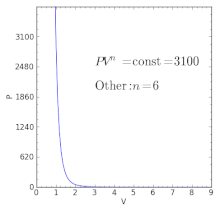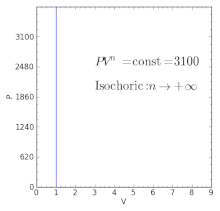
Выражение (8) называют уравнением политропы. Оно определяет связь между параметрами состояния p и υ в политропном процессе. Величина n, которая находится из соотношения (6), называется показателем политропы. Показатель n является функцией теплоемкости и, как и теплоемкость зависит от характера процесса. Для анализа частных случаев процесса требуется знать соответствующий показатель политропы n.
При изохорном процессе (c=cυ) функция (6) претерпевает бесконечный разрыв, изменяясь от n = +∞ до n — ∞. При изобарном процессе (с = ср) показатель n = 0. Следовательно, показатель политропы n в зависимости от характера процесса может изменяться в широких пределах, принимая любые значения от —∞ до +∞.
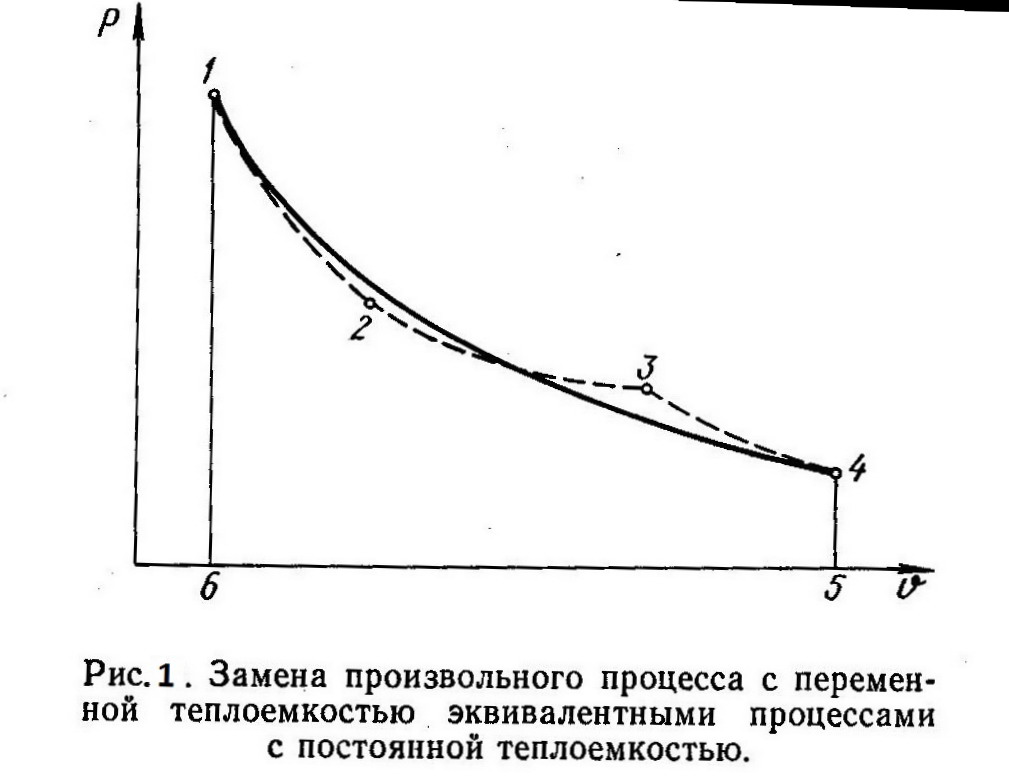
С помощью политропного процесса можно приближенно описать и рассчитать любой процесс изменения состояния 1—4 (рис. 1), для которого теплоемкость является переменной величиной. При этом произвольный процесс 1—4 необходимо заменить несколькими эквивалентными политропными процессами (процессы 1—2, 2—3 и 3—4), которые отличаются друг от друга постоянными значениями теплоемкости.
Замена должна производиться таким образом, чтобы работа в процессе 1—4 была равна работе на пути 1—2 — 3—4, то есть, чтобы были равны площади, ограниченные соответствующими кривыми процессов и ординатами 1—6 и 4—5. Так как изменение внутренней энергии ∆u на участке 1—4 не зависит от пути процесса (∆u=const), то, согласно уравнению q = ∆u + l первого закона термодинамики, количество теплоты в обоих случаях будет также одинаково. Погрешности, обусловленные такой заменой, окажутся тем меньшими, чем большим числом эквивалентных политропных участков будет заменен произвольный процесс 1—4, протекающий при переменной теплоемкости. Исп. литература: 1) Теплотехника, под общей ред. И.Н. Сушкина, Москва, «Металлургия», 1973. 2) Теплотехника, Бондарев В.А., Процкий А.Е., Гринкевич Р.Н. Минск, изд. 2-е,»Вышейшая школа», 1976.
ПОЛИТРОПА
Полезное
Смотреть что такое «ПОЛИТРОПА» в других словарях:
ПОЛИТРОПА — (от поли. и греч. tropos поворот направление), кривая на диаграммах состояния, изображающая политропный процесс … Большой Энциклопедический словарь
политропа — сущ., кол во синонимов: 1 • кривая (56) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
политропа — (от поли. и греч. trópos поворот, направление), кривая на диаграммах состояния, изображающая политропный процесс. * * * ПОЛИТРОПА ПОЛИТРОПА (от поли. (см. ПОЛИ. (часть сложных слов)) и греч. tropos поворот, направление), кривая на… … Энциклопедический словарь
политропа — politropė statusas T sritis Standartizacija ir metrologija apibrėžtis Termodinaminės diagramos pastovios šiluminės talpos kreivė. atitikmenys: angl. polytrope vok. Polytrope, f rus. политропа, f pranc. courbe polytropique, f … Penkiakalbis aiškinamasis metrologijos terminų žodynas
политропа — politropė statusas T sritis chemija apibrėžtis Termodinaminės diagramos pastovios šiluminės talpos kreivė. atitikmenys: angl. polytrope rus. политропа … Chemijos terminų aiškinamasis žodynas
политропа — politropė statusas T sritis fizika atitikmenys: angl. polytrope vok. Polytrope, f rus. политропа, f pranc. courbe polytropique, f; polytrope, f … Fizikos terminų žodynas
политропа — politropa statusas T sritis Energetika apibrėžtis Linija, vaizduojanti būsenos diagramoje politropinį procesą. atitikmenys: angl. curve of polytropic process; polytrope vok. Polytrope, f; polytropische Linie, f rus. политропа, f pranc. courbe… … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
Политропа — (от Поли. и греч. trópos поворот, направление) линия, изображающая на любой термодинамической диаграмме Политропический процесс. Уравнение П. идеального газа (См. Идеальный газ) имеет вид pV n = const, где р давление газа, V его объём,… … Большая советская энциклопедия
ПОЛИТРОПА — линия, изображающая на диаграмме состояния политропич. процесс … Большой энциклопедический политехнический словарь
ПОЛИТРОПНЫЙ ПРОЦЕСС
Частные 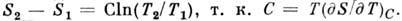
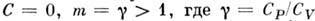
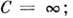
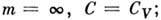
Для неидеальных газов показатель т можно приближённо считать постоянным лишь в нек-ром интервале термодинамич. параметров, поэтому П. п. в техн. термодинамике лишь приближённо представляет реальные термодинамич. процессы.
Лит.: Жуковский В. С., Термодинамика, М., 1983; Новиков И. И., Термодинамика, М., 1984.
Полезное
Смотреть что такое «ПОЛИТРОПНЫЙ ПРОЦЕСС» в других словарях:
ПОЛИТРОПНЫЙ ПРОЦЕСС — (политропический процесс) термодинамический процесс, характеризующийся постоянной теплоемкостью; для идеального газа описывается уравнением pVn=const, где n постоянная, называемая показателем политропы … Большой Энциклопедический словарь
политропный процесс — Термодинамический процесс, удовлетворяющий соотношению pvn = const, где п — показатель политропы есть величина постоянная. [Сборник рекомендуемых терминов. Выпуск 103. Термодинамика. Академия наук СССР. Комитет научно технической… … Справочник технического переводчика
политропный процесс — (политропический процесс), термодинамический процесс, характеризующийся постоянной теплоёмкостью; для идеального газа описывается уравнением pVn = const, где n постоянная, называется показателем политропы. * * * ПОЛИТРОПНЫЙ ПРОЦЕСС ПОЛИТРОПНЫЙ… … Энциклопедический словарь
политропный процесс — politropinis vyksmas statusas T sritis Standartizacija ir metrologija apibrėžtis Termodinaminės sistemos grįžtamasis būsenos pakitimas, kurio metu nesikeičia sistemos savitoji šiluminė talpa. atitikmenys: angl. polytropic process vok. polytrope… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
политропный процесс — politropinis procesas statusas T sritis chemija apibrėžtis Termodinaminės sistemos grįžtamasis būsenos kitimas, kurio metu nesikeičia sistemos savitoji šiluminė talpa. atitikmenys: angl. polytropic process rus. политропический процесс;… … Chemijos terminų aiškinamasis žodynas
политропный процесс — Процесс в идеальном газе, характеризующийся постоянной теплоемкостью … Политехнический терминологический толковый словарь
ПОЛИТРОПНЫЙ ПРОЦЕСС — (политропический процесс), термодинамич. процесс, характеризующийся пост, теплоёмкостью; для идеального газа описывается ур нием pVn = const, где п постоянная, наз. показателем политропы … Естествознание. Энциклопедический словарь
Процесс — (Process) Определение процесса, виды и типы процессов Информация об определении процесса, виды и типы процессов Содержание Содержание Определение Исторический Бизнес процесс Тепловой процесс Адиабатический процесс Изохорный процесс Изобарный… … Энциклопедия инвестора
Характеристики политропных процессов в зависимости от значения показателя n
Характеристики политропных процессов в зависимости от значения показателя n
В некоторых производственных процессах, особенно в области химических технологий, вполне возможен процесс с отрицательным политропным индексом. Процесс исследования расположен в верхнем левом и нижнем правом углу рисунка. Все кривые справа от рисунка(используя точку 1 в качестве начального состояния газа) характеризуют процесс, связанный с расширением газа, и процесс слева (процесс, связанный со сжатием газа).как видно из рисунка 5.8, все политропные процессы, которые мы изучили, зависят от их положения по отношению к основному процессу. Можно разделить на 3 группы 1.
Графический метод определения температурного поля плоской стенки при нестационарном режиме по Шмидту. Людмила Фирмаль
Значения показателей указывают на то, что эти политропные процессы лежат между изобарической и изотермой, ход которых можно определить по слепующим характеристикам: а) расширение газа; все процессы в этой секции осуществляются с повышением температуры, в результате чего повышается внутренняя температура Уменьшить* Энергия газа; увеличивает объем газа. То есть газ будет расширяться и создавать рабочие места. Таким образом, этот процесс осуществляется путем подвода тепла к газу, тепло которого частично расходуется на нагревание газа, а частично на работу расширения.
Когда значение индикатора приближается к 1, температура снижается, когда часть тепла, затрачиваемого на изменение внутренней энергии газа, приближается к 0. б) сжатие газа; совершенно очевидно, что все явления происходят при сжатии газа с противоположным знаком. Объем.—…………— Сжатие газа требует больших усилий. Температура газа снижается, а внутренняя энергия падает. Таким образом, он должен быть снабжен теплом от газа, в результате чего внутренняя энергия, затрачиваемая на работу, будет уменьшаться Тепловая мощность процесса измеряется от cp(n = 0) до (n = 1).Коэффициент изменяется от 1 / k(если n = 0) до 0 (если n = 1). 2. 1.
Эти процессы расположены между изотермами и теплоизоляцией. а) расширение газа; при изотермическом расширении работа получается за счет тепла, подаваемого извне. При адиабатическом расширении работа выполняется только за счет внутренней энергии В процессе, расположенном между изотермами и теплоизоляцией, газ работает частично за счет внутренней энергии газа, частично за счет тепла, подаваемого извне. чем ближе значение l к 1, тем больше процент работы на E. величина внешнего тепла, n, приближается к значению K. чем больше процент работы за счет уменьшения внутренней энергии газа, тем больше газ охлаждается.
Но нагревание может производиться не только при подаче тепла, но и в процессе сжатия газа. В политропном процессе, который расположен между изотермами и теплоизоляцией, когда газ расширяется, внутренняя энергия частично вызывает работу и снижает температуру газа. Остальное поступает из окружающей среды с необходимым теплом для work. So, при расширении, несмотря на подачу тепла, газы охлаждаются, что возможно только при отрицательной теплоемкости. Это видно из уравнения. Где 0, и. То же самое происходит и при сжатии газа. Работа сжатия превращается в тепло, но часть этого тепла выделяется в окружающую среду, и только часть его нагревает воздух.
Исходя из известного начального распределения температур, последовательным применением этого уравнения можно постепенно установить изменение температурного поля. Людмила Фирмаль
В результате температура газа повышается с отводом тепла, а при приведенных выше уравнениях 0 это возможно только при отрицательной теплоемкости. значение изменяется от L-k до L-1 d°0.Эти процессы расположены между диабатом и изохорой. Кривая процесса увеличивается быстрее по мере увеличения значения l, приближаясь к пределу предела а) расширение газа; работа газа всегда уменьшается и приближается к 0 (Изокор).С уменьшением внутренней энергии количество отводимого тепла увеличивается, и поэтому температура газа снижается быстрее.
Сжатие газа; несмотря на то, что работа сжатия газа уменьшается, из-за увеличения количества тепла, подаваемого извне, температура повышается по мере приближения значения l к ОО. Увеличение внутренней энергии газа вызвано работой сжатия, эквивалентной суммарной теплоте, подаваемой извне. Как видно из Формулы(5.13), теплоемкость процесса возрастает от 0 до cn при увеличении индекса политропы от k до oo. значение p от oo (для n = k>, оно уменьшается до 1 (для n = oo).Формула (5.14), полученная путем деления числителя и знаменателя на n, выражается в виде: * ±oo 1. Н-k_1_±_ Посмотрите на картинки.
Можно сделать следующие выводы: изотерма, имеющая расстояние от начала координат、 За счет повышения температуры все процессы от начальной точки 1 справа от изотермы осуществляются с повышением температуры газа, то есть с увеличением внутренней энергии. Процесс перемещения от начальной точки влево к нижней сопровождается снижением температуры газа, в результате чего внутренняя энергия decreases. So, изотерма-это граница процесса, который осуществляется с внутренним увеличением и уменьшением Газовая энергетика.
Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
А политропный процесс это термодинамический процесс который подчиняется соотношению:
куда п давление, V является объем, п это политропный индекс, и C является константой. Уравнение политропного процесса может описывать множественные процессы расширения и сжатия, которые включают теплопередачу.
Содержание
Частные случаи
Некоторые конкретные значения п соответствуют частным случаям:
Кроме того, когда закон идеального газа применяется:
Эквивалентность коэффициента политропы и отношения передачи энергии
Для идеальный газ в закрытая система проходит медленный процесс с незначительными изменениями в кинетический и потенциальная энергия процесс политропный, так что
Отношение к идеальным процессам
Для определенных значений индекса политропы этот процесс будет синонимом других общих процессов. Некоторые примеры влияния различных значений индекса приведены в следующей таблице.
Когда индекс п находится между любыми двумя из первых значений (0, 1, γ, или ∞), это означает, что кривая политропы будет прорезать (быть ограничен) кривые двух ограничивающих индексов.
Для идеального газа 1 γ = c п c v = c v + р c v = 1 + р c v = c п c п − р 
Другой
Решение проблемы Уравнение Лейна – Эмдена использование политропной жидкости известно как политроп.