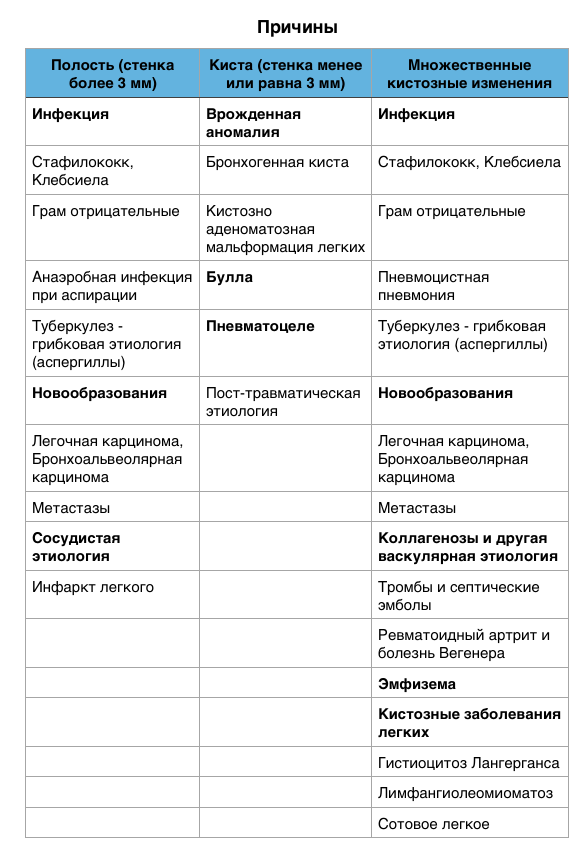
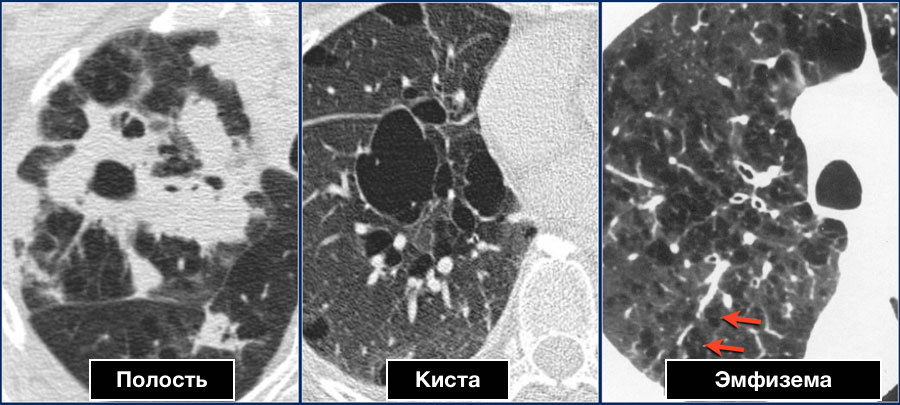
Кисты, полости, эмфизема — дифференциальный диагноз
Радиологи используют множество терминов для характеристики изменений легких низкой плотности или участков просветлений таких, как кисты, полости, пневматоцеле, эмфизема, булла, сотовое легкое и других.
Большое количество терминов затрудняет общее понимание патологического процесса в легких, поэтому более практичнее использовать следующие термины.
Полости возникают по причине некроза в образованиях или участках консолидации. Порой трудно отличить кисту от полости. Также после лечения пациента полость в легком превращается в кисту, и наоборот киста может инфицироваться и визуализироваться, как полость. Бывают случае, когда эмфизематозные буллы имеют видимые стенки, толщина которых составляет до 1 мм. Для проведения дифференциального диагноза в данном случае следует оценить окружающую легочную паренхиму. При визуализации легочных кист сопутствующей эмфиземы не выявляется. Кисты обычно содержат воздух, реже жидкость и солидный компонент. Данный термин наиболее часто используют при описании тонкостенных воздушных полостей в легких у пациентов с лимфангиолейомиоматозом или гистиоцитозом. Более толстые стенки кист определяются у пациентов с сотовым легком, что является признаком далеко зашедшего фиброза.
ПОЛОСТИ
Пневмония
In virulent pyogenic infections an abscess may form within the consolidated lung as a result of necrosis due to vasculitis and thrombosis.
Когда у пациентов гной откашливается, то полости можно выявить на рентгенограмме. Как правило состояние данных пациентов оценивается, как плохое.
При таких гранулематозных заболеваниях, как туберкулез, полости также выявляются, но пациент чувствует себя чаще удовлетворительно.
Полости не выявляются при пневмониях вирусной этиологии и микоплазменной, а также редко визуализируются при стрептококковых пневмониях.
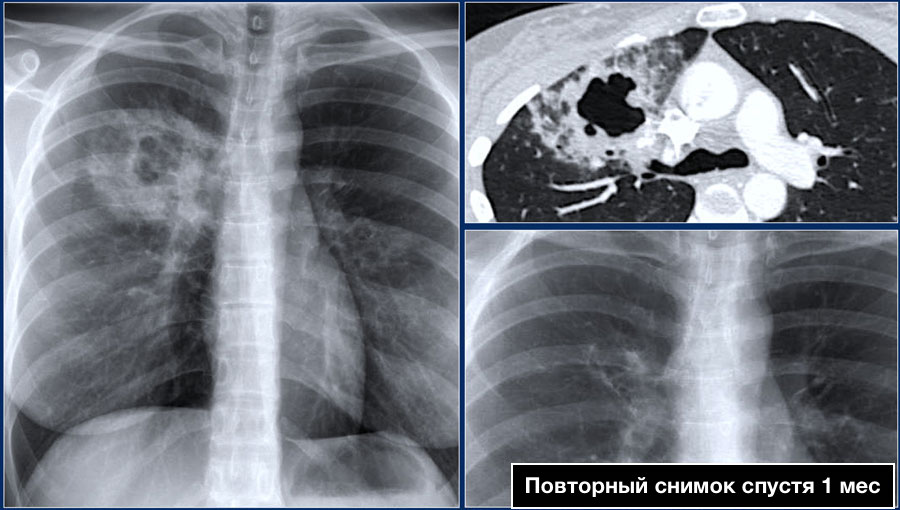
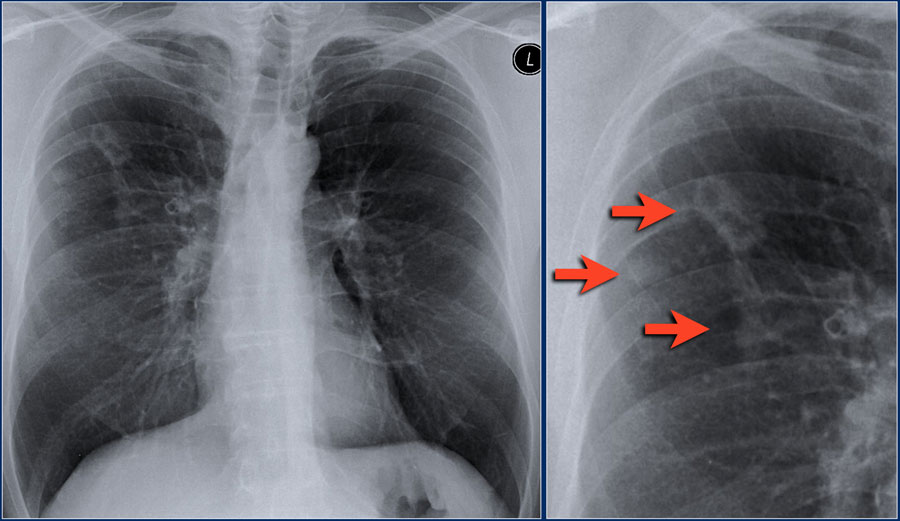
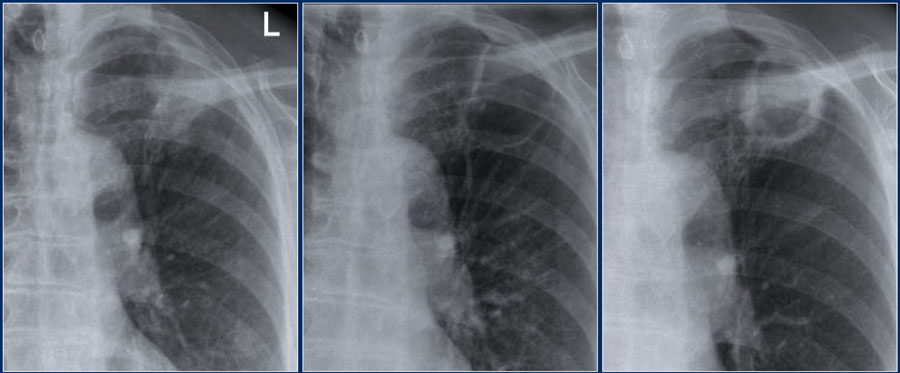
Ниже представленные изображения молодого пациента с пневмонией. Спустя месяц после лечения на повторных снимках видно, что консолидация и полость разрешились.
Пневмония
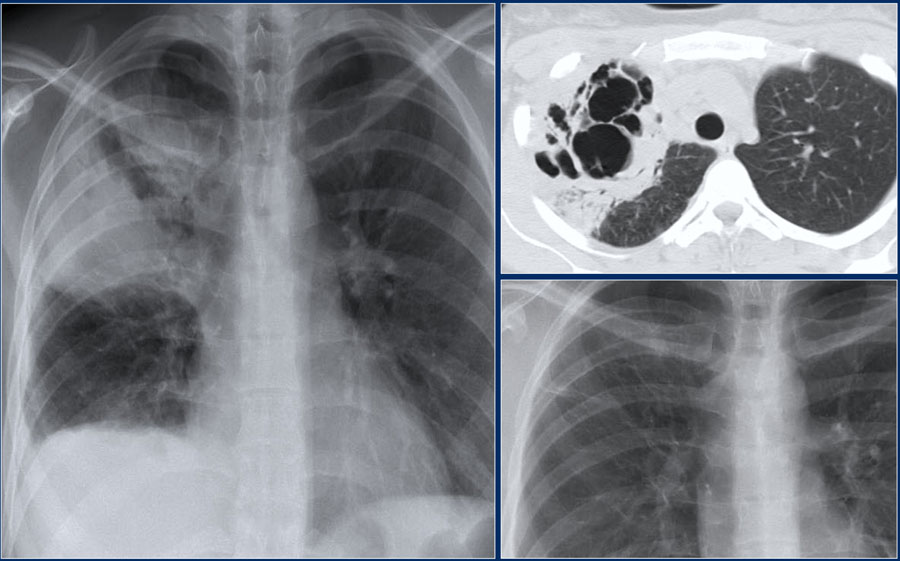
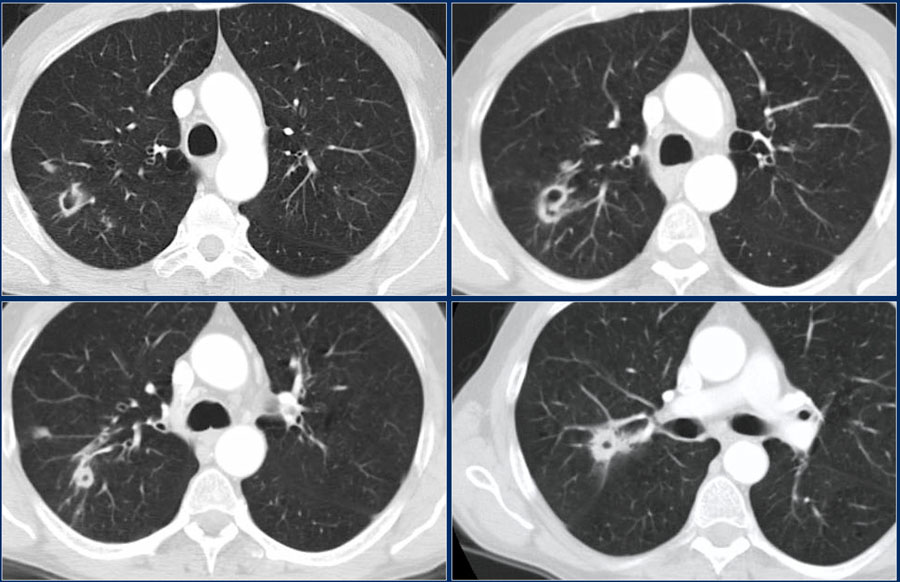
Ниже представлен еще один пример пневмонии с полостью.
Обратите внимание на поражение паренхимы легких, которое хорошо определяется на КТ.
На последующих изображениях спустя год визуализируются минимальные изменения на рентгенограмме.
Туберкулез
Первичный туберкулез клинически обычно протекает бессимптомно и малосимптомно длительное время.
Иммунитет 5% инфицированных людей справляется недостаточно, что благоприятно для развития заболевания.
Вторичный туберкулез развивается в 5% случаях у латентных носителей, что на рентгенограмме чаще проявляется, как консолидация с полостью распада преимущественно в верхних и нижних долях легких. Миллиарный туберкулез является результатом гематогенного распространения заболевания.
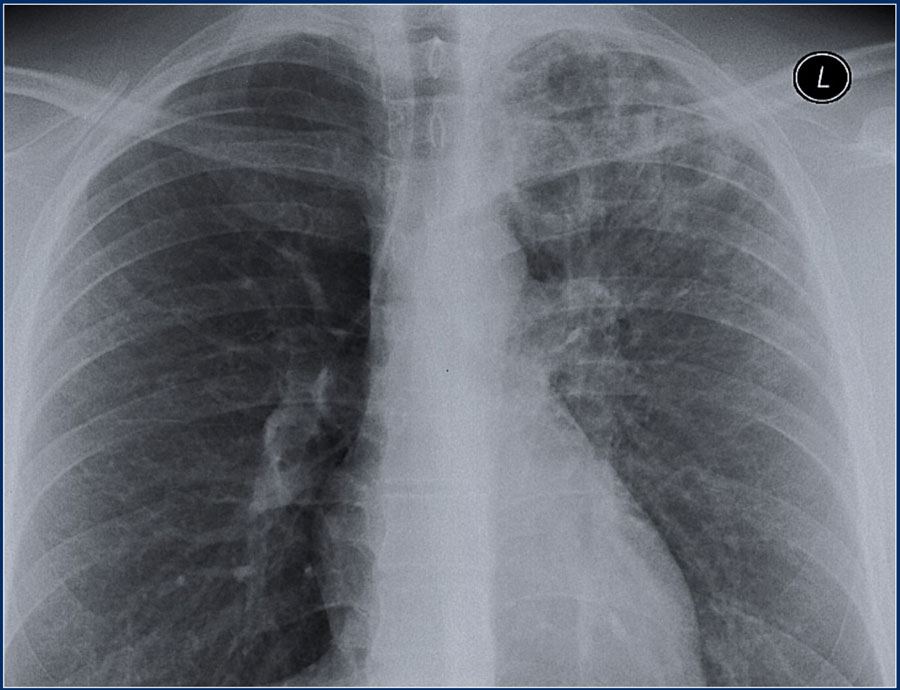
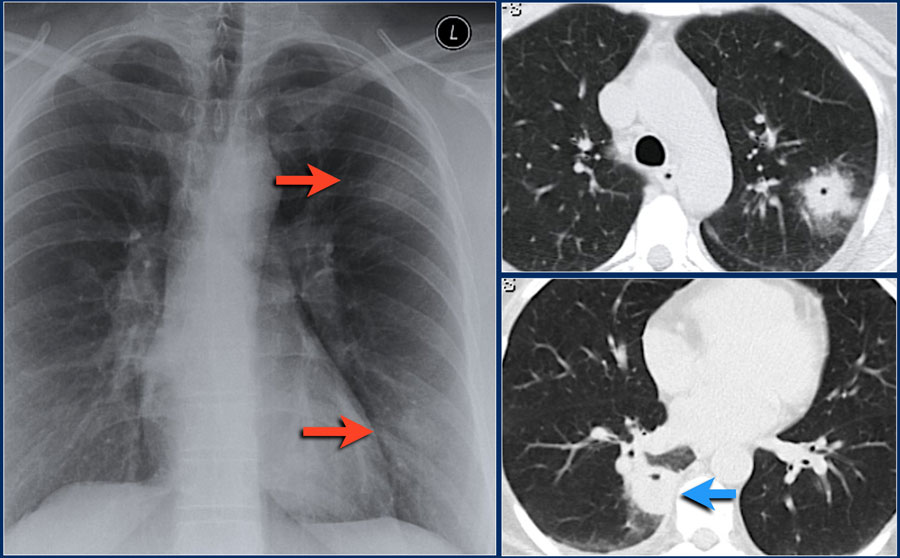
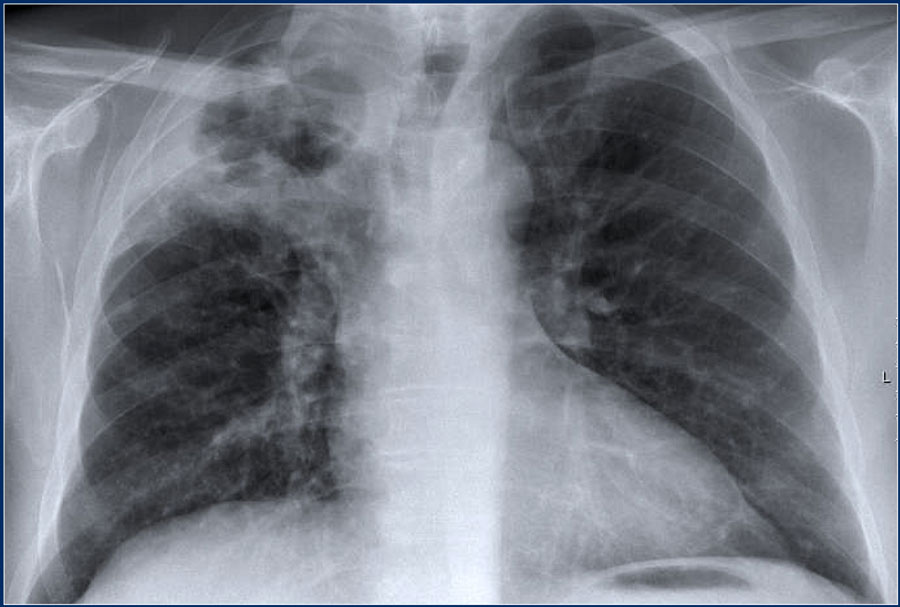
Ниже представлен пациент со вторичным туберкулезом с полостью распада в верхней доле левого легкого.
Туберкулез
Сперва оцените изображения, а потом продолжите чтение.
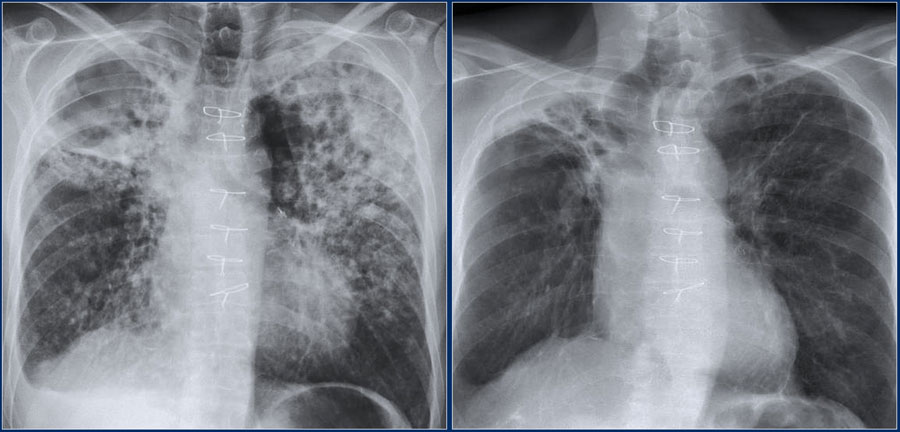
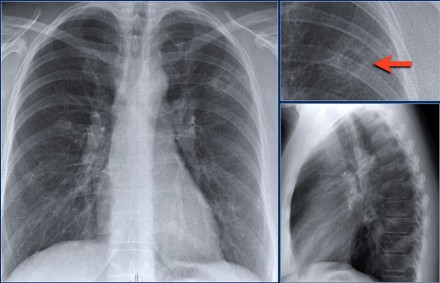
Рентгенограмма того же пациента несколько лет спустя.
Изменения лучше оценить на КТ.
Ниже представлен тот же пациент, что и выше.
Обратите внимание на полость в правом легком. В левом легком, вероятнее всего, тракционные бронхоэктазы вследствие фиброза.
Нетуберкулезный микобактериоз
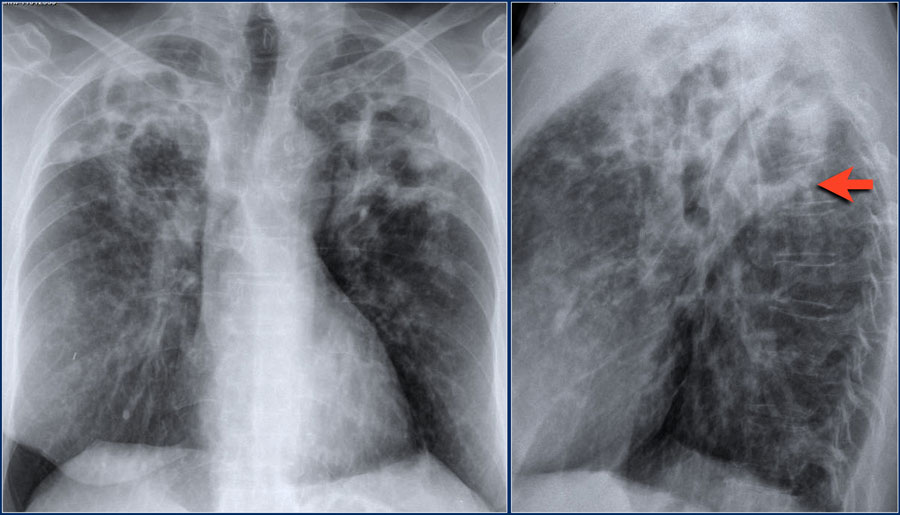
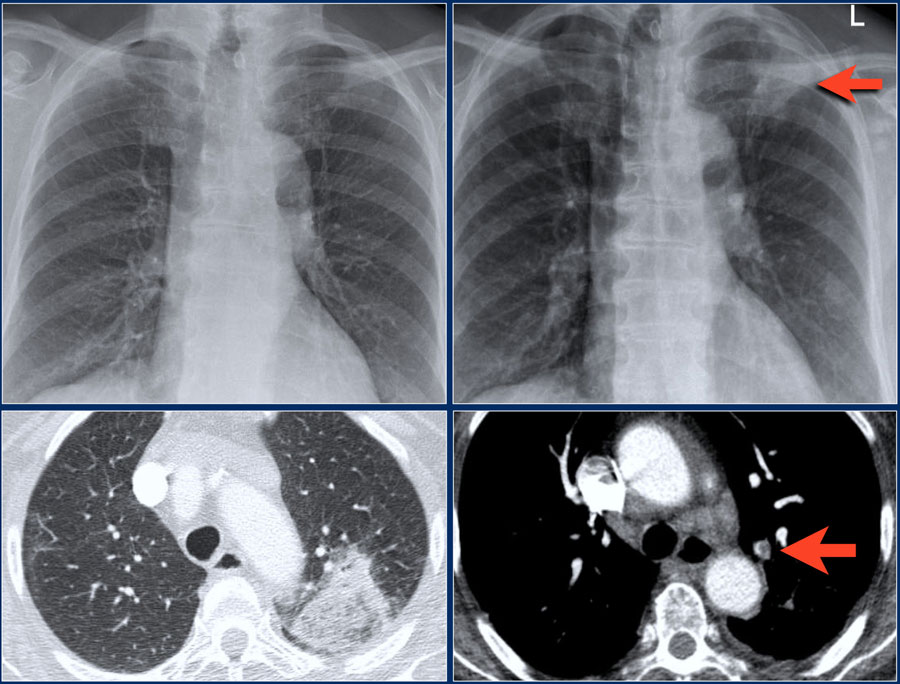
Нетуберкулезная микобактерия, также известная, как атипичная микобактерия. Ниже представлен пациент с двухсторонним патологическим двухсторонним процессом в верхних долях легких, который обусловлен инфицированием нетуберкулезной микобактерией. Обратите внимание на содержание жидкости (гной) в полости (указано стрелкой).
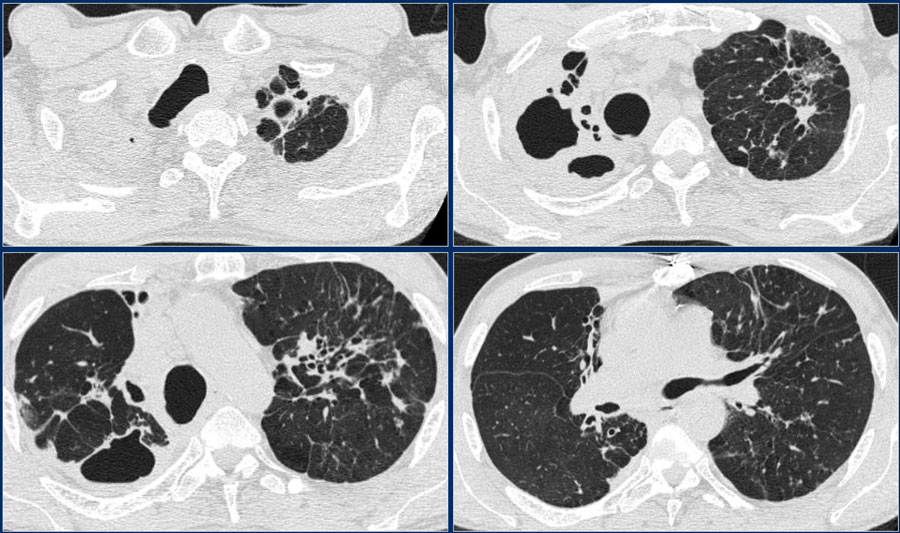
Ниже представлен еще один пациент с поражением легких атипичной микобактерией. Обратите внимание на узлы и полость и продолжите оценку КТ-снимка.
На КТ визуализируются множественные полости небольших размеров.
Септическая пневмония
Септическая пневмония визуализируется, как множественные слабо выраженные очаги. В 50% выявляются полости. На КТ изображениях выявляется намного больше патологических изменений, чем на рентгенограмме. Обычно данные изменения локализуются по периферии легких, примыкая к плевре. Также визуализируются симптом воздушной бронхограммы и симптом питающего сосуда. Хотя многие спорят насчет последнего.
Ниже представлен пациент с септической пневмонией. На рентгенограмме визуализируется две слабовыраженных изменений высокой плотности в левой легкого, что по всей вероятности являются консолидацией.
Ниже представлены повторные изображения того же пациента, на которых визуализируются мелкие кисты.
Легочный рак
В 10% случаях легочного рака образуются полости, что наиболее характерно для плоскоклеточного рака.
При мелкоклеточном раке полости не образуются. При бронхоальвеолярном раке (аденокарцинома in situ) редко образуются полости.
Ниже представлена рентгенограмма с большой полостью распада у пациента с раком легких.
Инфаркт легкого
При легочном эмболизме не характерно проявление на рентгенограмме в виде легочной консолидации. Консолидация обычно — это результат инфаркта легкого и кровоизлияний в альвеолы. В таком случае киста формируется в области инфаркта.
Ниже представлена рентгенограмма, которая соответствует норме. Стрелкой указано трехгранное изменение легочной паренхимы высокой плотности, причиной которой является легочная эмболия. На КТ данные изменения являются сегментной консолидацией.
Ниже представлен тот же пациент на снимках спустя год, которого выявляются кисты. Толстые стенки предположительно вследствие инфицирования кисты.
ПНЕВМАТОЦЕЛЕ
Пневматоцеле это тонкостенные, наполненные воздухом кисты легкого, при которых хирургическое вмешательство обычно не требуется, если не возникает затруднения дыхания, связанного со сдавлением легкого или прорывом кист в плевральную полость. Пневматоцеле наиболее часто развивается у очень маленьких детей при пневмонии, вызванной золотистым стафилококком.
Патология. К развитию пневматоцеле приводит некроз и расплавление легочной паренхимы. Стафилококковая пневмония вызывает тяжелый воспалительный процесс, связанный отчасти с мощным деструктивным воздействием стафилококкового экзотоксина на легочную ткань. Воздух выходит через разрушенные стенки альвеол субплеврально в результате чего и образуется типичная тонкостенная киста.
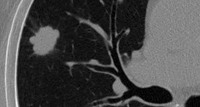
Ниже приведена илюстрация механизма образования пневматоцеле при травме. Из-за жидкости в кисте при визуализации данные изменения будут схожи с одиночным легочным очагом (узлом).
Доброкачественные опухоли легких
МКБ-10
Общие сведения
Опухоли легких составляют большую группу новообразований, характеризующихся избыточным патологическим разрастанием тканей легкого, бронхов и плевры и состоящих из качественно измененных клеток с нарушениями процессов дифференцировки. В зависимости от степени дифференцировки клеток различают доброкачественные и злокачественные опухоли легких. Также встречаются метастатические опухоли легких (отсевы опухолей, первично возникающих в других органах), которые по своему типу всегда являются злокачественными.
Доброкачественные опухоли легких составляют 7-10% от общего числа новообразований данной локализации, развиваясь с одинаковой частотой у женщин и мужчин. Доброкачественные новообразования обычно регистрируются у молодых пациентов в возрасте до 35 лет.
Причины
Причины, приводящие к развитию доброкачественных опухолей легкого, до конца не изучены. Однако, предполагают, что этому процессу способствует генетическая предрасположенность, генные аномалии (мутации), вирусы, воздействие табачного дыма и различных химических и радиоактивных веществ, загрязняющих почву, воду, атмосферный воздух (формальдегид, бензантрацен, винилхлорид, радиоактивные изотопы, УФ-излучение и др.). Фактором риска развития доброкачественных опухолей легких служат бронхолегочные процессы, протекающие со снижением локального и общего иммунитета: ХОБЛ, бронхиальная астма, хронический бронхит, затяжные и частые пневмонии, туберкулез и т. д.).
Патанатомия
Доброкачественные опухоли легких развиваются из высокодифференцированных клеток, схожих по строению и функциям со здоровыми клетками. Доброкачественные опухоли легких отличаются относительно медленным ростом, не инфильтрируют и не разрушают ткани, не метастазируют. Ткани, расположенные вокруг опухоли, атрофируются и образуют соединительнотканную капсулу (псевдокапсулу), окружающую новообразование. Ряд доброкачественных опухолей легкого имеет склонность к малигнизации.
По локализации различают центральные, периферические и смешанные доброкачественные опухоли легких. Опухоли с центральным ростом исходят из крупных (сегментарных, долевых, главных) бронхов. Их рост по отношению к просвету бронха может быть эндобронхиальным (экзофитным, внутрь бронха) и перибронхиальным (в окружающую ткань легкого). Периферические опухоли легких исходят из стенок мелких бронхов или окружающих тканей. Периферические опухоли могут расти субплеврально (поверхностно) или внутрилегочно (глубоко).
Доброкачественные опухоли легких периферической локализации встречаются чаще, чем центральные. В правом и левом легком периферические опухоли наблюдаются с одинаковой частотой. Центральные доброкачественные опухоли чаще располагаются в правом легком. Доброкачественные опухоли легких чаще развиваются из долевых и главных бронхов, а не из сегментарных, как рак легкого.
Классификация
Доброкачественные опухоли легких могут развиваться из:
Среди доброкачественных опухолей легких чаще встречаются гамартомы и аденомы бронхов (в 70% случаев).
К редким доброкачественным опухолям легких относятся фиброзная гистиоцитома (опухоль воспалительного генеза), ксантомы (соединительнотканные или эпителиальные образования, содержащие нейтральные жиры, холестеринэстеры, железосодержащие пигменты), плазмоцитома (плазмоцитарная гранулема, опухоль, возникающая вследствие расстройства белкового обмена). Среди доброкачественных опухолей легкого также встречаются туберкуломы – образования, являющиеся клинической формой туберкулеза легких и образованные казеозными массами, элементами воспаления и участками фиброза.
Симптомы
Клинические проявления доброкачественных опухолей легких зависят от локализации новообразования, его размера, направления роста, гормональной активности, степени обтурации бронха, вызываемых осложнений. Доброкачественные (особенно периферические) опухоли легких длительно могут не давать никаких симптомов. В развитии доброкачественных опухолей легких выделяются:
Периферические опухоли легких
При периферической локализации в бессимптомной стадии доброкачественные опухоли легких ничем себя не проявляют. В стадии начальной и выраженной клинической симптоматики картина зависит от размеров опухоли, глубины ее расположения в легочной ткани, отношения к прилежащим бронхам, сосудам, нервам, органам. Опухоли легких больших размеров могут достигать диафрагмы или грудной стенки, вызывая боли в груди или области сердца, одышку. В случае эрозии сосудов опухолью наблюдаются кровохарканье и легочное кровотечение. Сдавление опухолью крупных бронхов вызывает нарушение бронхиальной проходимости.
Центральные опухоли легких
Клинические проявления доброкачественных опухолей легких центральной локализации определяются выраженностью нарушений бронхиальной проходимости, в которой выделяют III степени. В соответствии с каждой степенью нарушения бронхиальной проходимости различаются клинические периоды заболевания.
В 1-ый клинический период, соответствующий частичному бронхиальному стенозу, просвет бронха сужен незначительно, поэтому течение его чаще бессимптомное. Иногда отмечаются кашель, с небольшим количеством мокроты, реже с примесью крови. Общее самочувствие не страдает. Рентгенологически опухоль легкого в этом периоде не обнаруживается, а может быть выявлена при бронхографии, бронхоскопии, линейной или компьютерной томографии.
Во 2-ом клиническом периоде развивается клапанный или вентильный стеноз бронха, связанный с обтурацией опухолью большей части просвета бронха. При вентильном стенозе просвет бронха частично открывается на вдохе и закрывается на выдохе. В части легкого, вентилируемой суженным бронхом, развивается экспираторная эмфизема. Может происходить полное закрытие бронха вследствие отека, скопления крови и мокроты. В ткани легкого, расположенной по периферии опухоли, развивается воспалительная реакция: у пациента повышается температура тела, появляется кашель с мокротой, одышка, иногда кровохарканье, боли в груди, утомляемость и слабость. Клинические проявления центральных опухолей легких во 2-ом периоде носят перемежающийся характер. Противовоспалительная терапия снимает отек и воспаление, приводит к восстановлению легочной вентиляции и исчезновению симптомов на определенный период.
Скорость и выраженность нарушений проходимости бронхов зависит от характера и интенсивности роста опухоли легкого. При перибронхиальном росте доброкачественных опухолей легких клинические проявления менее выраженные, полная окклюзия бронха развивается редко.
Осложнения
При осложненном течении доброкачественных опухолей легкого могут развиться пневмофиброз, ателектаз, абсцедирующая пневмония, бронхоэктазы, легочное кровотечение, синдром сдавления органов и сосудов, малигнизация новообразования. При карциноме, являющейся гормонально активной опухолью легких, у 2–4% пациентов развивается карциноидный синдром, проявляющийся периодическими приступами жара, приливов к верхней половине туловища, бронхоспазмом, дерматозом, диареей, психическими расстройствами вследствие резкого повышения в крови уровня серотонина и его метаболитов.
Диагностика
В стадии клинической симптоматики физикально определяются притупление перкуторного звука над зоной ателектаза (абсцесса, пневмонии), ослабление или отсутствие голосового дрожания и дыхания, сухие или влажные хрипы. У пациентов с обтурацией главного бронха грудная клетка асимметрична, межреберные промежутки сглажены, соответствующая половины грудной клетки отстает во время совершения дыхательных движений. Необходимые инструментальные исследования:
Лечение
Все доброкачественные опухоли легких, независимо от риска их малигнизации подлежат оперативному удалению (при отсутствии противопоказаний к хирургическому лечению). Операции выполняют торакальные хирурги. Чем ранее диагностирована опухоль легкого и проведено ее удаление, тем меньше объем и травма от оперативного вмешательства, опасность осложнений и развития необратимых процессов в легких, в т. ч. малигнизации опухоли и ее и метастазирования. Применяются следующие виды оперативных вмешательств:
Оперативное лечение доброкачественных опухолей легких обычно производят методом торакоскопии или торакотомии. Доброкачественные опухоли легкого центральной локализации, растущие на тонкой ножке, можно удалить эндоскопическим путем. Однако, данный метод сопряжен с опасностью развития кровотечения, недостаточно радикальным удалением, необходимостью проведения повторного бронхологического контроля и биопсии стенки бронха в месте локализации ножки опухоли.
При подозрении на малигнизированную опухоль легких, во время проведения операции прибегают к срочному гистологическому исследованию тканей новообразования. При морфологическом подтверждении злокачественности опухоли объем оперативного вмешательства выполняется как при раке легкого.
Прогноз и профилактика
При своевременных лечебно-диагностических мероприятиях отдаленные результаты благоприятные. Рецидивы при радикальном удалении доброкачественных опухолей легких наблюдаются редко. Менее благоприятен прогноз при карциноидах легких. С учетом морфологической структуры карциноида пятилетняя выживаемость при высокодифференцированном типе карциноида составляет 100%, при умеренно дифференцированном типе –90%, при низкодифференцированном — 37,9%. Специфическая профилактика не разработана. Минимизировать риски возникновения новообразования позволяет своевременное лечение инфекционно-воспалительных заболеваний легких, исключение курения и контакта с вредными веществами-поллютантами.
Синдром внутрилегочного полостного образования
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В структуре острой и хронической бронхолегочной патологии первое место занимают пневмонии, их частота составляет 30,4% [1–3]. Несмотря на значительные достижения в изучении проблемы пневмоний, данная патология продолжает характеризоваться устойчиво высокой заболеваемостью с тенденцией к затяжному течению, увеличением числа тяжелых форм с риском развития осложнений и форм с атипичным течением [4]. Это связано как с ростом антибиотикорезистентности возбудителей пневмоний, так и с увеличением числа пациентов с иммунодефицитными состояниями различного генеза.
В структуре острой и хронической бронхолегочной патологии первое место занимают пневмонии, их частота составляет 30,4% [1–3]. Несмотря на значительные достижения в изучении проблемы пневмоний, данная патология продолжает характеризоваться устойчиво высокой заболеваемостью с тенденцией к затяжному течению, увеличением числа тяжелых форм с риском развития осложнений и форм с атипичным течением [4]. Это связано как с ростом антибиотикорезистентности возбудителей пневмоний, так и с увеличением числа пациентов с иммунодефицитными состояниями различного генеза.
Пациентов, поступающих в стационар с диагнозом «абсцедирующая пневмония», следует дифференцировать с достаточно большой группой пациентов, у которых рентгенологический синдром внутрилегочного полостного образования ложно трактуется именно как абсцесс легкого. Синдром внутрилегочного полостного образования рентгенологически определяется как участок просветления в пределах легочной ткани, которая может содержать или не содержать жидкость, окружена стенкой разной толщины и сохраняется во всех проекциях [5]. Патологически этот синдром определяется как наличие газосодержащего пространства внутри участка легочной консолидации либо узла, появившегося в результате эвакуации определенного объема некротизированной легочной ткани через бронхиальное дерево.
Синдром внутрилегочного полостного образования следует также дифференцировать с внелегочной патологией, имеющей сходную рентгенологическую картину, такой, например, как ограниченный пневмоторакс или грыжа пищеводного отверстия диафрагмы [5].
Несмотря на все более совершенные методики диагностики внутрилегочных полостных образований, процент ошибок остается жизненно значимым. До настоящего времени не выявлено 100% патогномоничных клинико-рентгенологических признаков ни для одного заболевания, проявляющегося в виде полостей в легком. Наличие полости в легком часто свидетельствует о неблагоприятном течении заболевания. Это диктует необходимость неотложной диагностики, поскольку в ряде случаев единственно рациональной тактикой лечения является хирургическое вмешательство. Объективные показатели трудности диагностики – это расхождения первоначального диагноза, установленного в клинике, и окончательного, подтвержденного в процессе обследования или после хирургического лечения [6].
Появление полостного образования в легком возможно при периферическом раке легкого (причем бессимптомное развитие болезни наблюдается почти в 60% случаев). По разным данным, распад в опухолевом узле встречается в 10% случаев [7], более чем в 30% случаев [8], в 10–25% [9], в 2–5% случаев периферического рака [10]. Некроз и распад в центре обычно наблюдаются при размере опухоли более 5 см. По мнению Ю.Б. Альтшулера и соавт., распад опухоли зависит по меньшей мере от 3-х факторов: различия в темпах роста и распада; наличия и степени дренажа; характера воспалительного процесса. Преобладание одного из этих факторов на разных стадиях процесса, по-видимому, оказывает решающее влияние на форму полости, толщину ее стенок, характер самого распада. По данным литературы, эта форма встречается в 3–50% случаев. Большой разброс в оценке полостной формы рака объясняется тем, что одни авторы такой формой считают появление на рентгенограмме просветления в раковом узле, другие – только те случаи, когда имеется полный распад с образованием тонкостенной полости.
Наличие полости в опухолевом узле обусловливает ряд особенностей клинического течения заболевания и создает благоприятные условия для вторичного инфицирования, что существенно затрудняет дифференциальную диагностику полостной формы рака и других заболеваний, сопровождающихся распадом легочной ткани.
Любая форма туберкулеза легких может перейти в деструктивную с формированием полости от малых (до 2 см в диаметре) до гигантских (свыше 6 см в диаметре) размеров [11]. Существуют публикации, отмечающие сочетание туберкулеза с раком в одном сегменте или возникновение рака в стенке туберкулезной каверны даже при активном туберкулезном процессе.
Синдромом внутрилегочного полостного образования могут проявляться кисты различного генеза. Кисты подразделяются на паразитарные и непаразитарные. Последние в свою очередь делятся на врожденные (истинные) и приобретенные (ложные). Одиночные приобретенные легочные кисты являются следствием какого-то заболевания воспалительной этиологии с вовлечением в процесс легочной ткани и бронхиального дерева. К паразитарным кистам относятся эхинококковые кисты, кисты легочной двуустки.
Рентгенологическая картина
При оценке рентгенологической картины полостного внутрилегочного образования рекомендуется оценивать от 9 [9] до 15 [12] основных признаков, не считая оценки параметров полости в течение времени, что бывает диагностически малодостоверно и задерживает начало лечения. Основные рентгенологические симптомы:
1. Количество полостей (1 и более).
2. Локализация и расположение полости. При этом рассматриваются центральное и эксцентрическое расположение полости, ее локализация в 1, 2 аксиллярном, 6 и прочих сегментах легкого.
3. Форма полости. Рассматриваются округлая, щелевидная и неправильная формы полостей.
4. Максимальный размер полости:
– менее 3 см;
– от 3 до 6 см;
– более 6 см.
5. Внутренний контур полости:
– ровный;
– бугристый.
6. Внешний контур полости:
– четкий на всем протяжении;
– нечеткий на ограниченном участке;
– нечеткий на большем протяжении.
7. Толщина стенки полости:
– равномерная;
– неравномерная на ограниченном участке;
– неравномерная на большем протяжении.
8. Минимальная толщина стенки полости:
– менее 2 мм;
– от 2 до 10 мм;
– более 10 мм.
9. Содержимое полости:
– отсутствует;
– в небольшом количестве;
– в большом количестве.
10. Характер содержимого:
– однородное;
– неоднородное.
11. Кальцификация узла:
– есть;
– нет.
12. «Дорожка» к корню легкого:
– есть;
– нет.
13. Увеличение лимфоузлов корня легкого:
– есть;
– нет.
14. Отношение площади полости к площади узла:
– полость занимает менее 5% площади узла;
– полость занимает от 5 до 25% площади узла;
– полость занимает более 25% площади узла.
15. Наличие очагов в окружающей ткани:
– есть;
– нет.
Рентгенологическая картина наиболее часто встречающихся полостных внутрилегочных образований
При сравнении рентгенологических картин по указанным признакам отмечено, что для абсцесса легкого характерно одностороннее поражение в 92% случаев [13] (8% приходится на двусторонние септические пневмонии у пациентов с хронической экзогенной интоксикацией, аспирационными пневмониями), преимущественно отмечается поражение 2, 6, 10-го сегментов [14].
В начальном периоде формирования полость острого абсцесса легкого имеет неправильную округлую форму с неровными внутренними контурами, что объясняется быстрым расплавлением легочной паренхимы, опережающим расплавление сосудов и бронхов в очаге поражения [15]. Полость округлая, размерами от 2 до 6 см, с четкими наружными контурами, инфильтрацией окружающей легочной ткани, большим количеством жидкости, чаще с четким горизонтальным уровнем (88,6%) [13, 14]. Некоторые авторы указывают, что верхняя стенка абсцесса бывает значительно тоньше нижней [16]. При наличии широкой зоны перифокальной инфильтрации (более 3–4 см) следует подозревать наличие мелких гнойников по периферии основного гнойника [15].
При хроническом абсцессе легкого зона перифокального затемнения, как правило, неравномерна как по интенсивности тени, так и по распространению за счет сочетания паренхиматозных и интерстициальных изменений с поражением бронхов [15]. Полость с неровным, бахромчатым внутренним контуром, независимо от формы и величины зоны перифокального затемнения, характерна для гангренозного абсцесса. Этот контур свидетельствует о наличии неотторгшихся некротизированных участков легочной ткани [15].
Как и всякий гнойно-воспалительный процесс, абсцесс легкого сопровождается реактивными изменениями в регионарных (бронхопульмональных) лимфатических узлах, которые гиперплазируются до значительных размеров. Рентгенологически эти изменения проявляются расширением корня легкого, смазанностью его нормальной структуры. При наличии дренирующего бронха выявляется «отводящая дорожка», идущая от полости к легочному корню [15].
Нельзя не отметить существование гигантских абсцессов легкого, размеры которых могут превышать 10 см в диаметре. При эксцентрическом расположении таких полостей возникает необходимость дифференциальной диагностики с эмпиемой плевры, причем на первое место выходит полипозиционное рентгеноскопическое исследование.
Одностороннее поражение встречается в 97% случаев периферического рака легкого с распадом. По данным различных авторов, периферический распадающийся рак в 55–62% локализуется в правом легком, в 38–45% – в левом легком, наиболее часто поражаются 3 и 4 сегменты [8].
По мнению А.Х. Трахтенберга и К.И. Колбанова [17], при диаметре опухоли более 5 см за счет недостаточного кровоснабжения всего ее массива могут наблюдаться некроз и распад в центре узла и образование полости. Однако в литературе рассматривается и малый периферический рак до 2 см в диаметре, имеющий картину полигональной тени. Если имеется просветление в центре, то оно обусловлено либо легочной паренхимой, еще не занятой тканью опухоли, либо полостью распада в опухолевом узле. Наружные контуры полости нечеткие с лучистостью по периферии, тяжами, уходящими в окружающую легочную ткань. Внутренние контуры неровные и нечеткие, с неравномерностью в различных отделах [14].
При локализации опухоли вблизи плевры выявляется симптом втяжения ее на уровне опухоли. При полостной форме периферического рака легкого от 3 до 5 см размер полости соответствует размеру узла в 70% случаев [9]. Форма узла обычно неправильно шаровидная с четким бугристым наружным контуром [11], нечетким лучистым контуром за счет инфильтративного опухолевого роста в окружающую легочную паренхиму. Внутренний контур выглядит по-разному: от серповидного просветления до неровного, бухтообразного, изъеденного, бугристого. Толщина стенок полости различная на разных участках, это зависит от отделившегося опухолевого секвестра. При полном отторжении ракового секвестра рентгенологически выявляется кольцевидная тень с тонкими стенками. Раковые полости могут содержать жидкость.
Сложность для дифференциальной диагностики представляют случаи развития параканкрозной пневмонии, причем появляется инфильтрация окружающей узел легочной ткани, регрессирующая при назначении стандартной антибактериальной терапии (АБТ). По данным Д.И. Мурзенко [9], при полостной форме рака легкого отмечаются наличие «дорожки» к корню легкого в 28% случаев, увеличение бронхопульмональных лимфоузлов корня ипсилатерального легкого в 57% случаев.
Не следует забывать о том, что в ряде случаев при центральном раке, если опухоль не полностью обтурирует бронх, наблюдается вентильная эмфизема, которая рентгенологически может ошибочно трактоваться как тонкостенная полость неправильной овоидной формы. Необходимо учитывать и то, что появление рентгенологического синдрома внутрилегочного полостного образования может быть связано не только непосредственно с наличием распадающейся опухоли легкого, но и с деструктивными пневмониями, вызванными нарушением пассажа воздуха в системе трахеобронхиального дерева при центральных неопроцессах. Недостаток внимания к этому важному аспекту, недообследованность больного и отсутствие АБТ могут оказаться фатальными.
Туберкулез легких. Рентгенологическая картина сформированной каверны зависит от исходной формы туберкулеза. При инфильтративной форме каверна неправильно округлой формы, очертания наружных и внутренних контуров зависят от длительности процесса [10]. Внутренний контур полости четкий, наружные очертания нечеткие за счет инфильтративных изменений. Фиброзные изменения в стенке полости и окружающей легочной ткани отсутствуют, но определяются специфические очаговые тени вокруг полости. При кавернозной форме туберкулеза полость часто локализуется субплеврально. Она округлой формы с одинаковыми по толщине стенками, с очаговыми тенями в окружности и «дорожкой» к корню легкого. Наружные очертания соответствуют внутренним.
При фиброзно-кавернозном туберкулезе каверна может иметь различную форму, с неровными контурами, вокруг в легочной ткани фиброзные и очаговые изменения. Если в полости находятся казеозные массы, то внутренний контур неровный, ланктообразный, а наружный – с перифокальным воспалением и очагами в окружности. При нарушении функции дренирующего каверну бронха в полости может быть жидкость. При обострении туберкулемы выделяются следующие варианты распада: эксцентричный (в любой точке туберкулемы), центральный, возможно появление множественных распадов. Также в процессе распада возникает секвестр.
Наиболее частый вариант распадающейся туберкулемы – это эксцентричный распад вблизи дренирующего бронха. В окружности видны очаговые тени и «дорожка» к корню легкого в виде парных полосок, что является отражением воспаления бронха. При наличии распадающейся туберкулемы с наличием секвестра возникают диагностические затруднения, вызывая ассоциацию с абсцессом или аспергилломой, требуется морфологическая верификация. Кортикальный и субплевральный слои легкого, наиболее богато снабженные лимфатическими сосудами, играют важную роль в развитии легочного туберкулеза. Патологически измененные туберкулезным процессом лимфатические сосуды кортикального слоя в связи со своеобразным анатомическим строением дают целый ряд необычных теневых изображений на рентгенограммах. Речь идет о кольцевидных тенях различной величины. Иногда они имеют форму неправильной, незамкнутой окружности. Контуры колец нежны, тонки, в некоторых случаях унизаны мелкими круглыми четкими очагами – «нить с бусинами». Иногда кольца достигают достаточной степени плотности, что может симулировать каверны [18].
Рентгенологическая картина аспергилломы характеризуется наличием округлой тонкостенной полости свыше 1,5 см в диаметре с четкими контурами и расположенным внутри клубком мицелия, окаймленным тонким ободком (серпом) воздуха [19]. Затемнение имеет однородную структуру и четкие очертания. Воздушная прослойка полностью окаймляет клубок, что может помочь дифференцировать аспергиллому от распадающейся туберкулемы, содержащей внутри секвестр. В ряде случаев грибковое образование не фиксировано к стенке полости и перемещается внутри нее при переводе больного из одного положения в другое. Этот симптом облегчает дифференциальную диагностику в ходе использования полипозиционной рентгеноскопии. В то же время наличие клубка мицелия внутри полости не может свидетельствовать об отсутствии активности основного процесса, которому обязана своим происхождением полость. Известны случаи заселения гриба в активную туберкулему с распадом [11].
Для поликистоза легких характерно наличие нескольких тонкостенных круглых полостей с четкими наружными и внутренними контурами, сохраняющимися при присоединении вторичного воспаления. Фокусы и очаги в окружающей легочной ткани отсутствуют [13]. В 54,2% случаев отмечается уменьшение пораженной части легкого в объеме [14]. Скиалогическая картина при буллах легкого характеризуется изменениями 3-х типов: аваскулярные участки, изменения в сосудистой сети, гиперпрозрачность [14].
Для саркоидоза легких также характерны тонкостенные небольшие и средних размеров полости. Однако при этом заболевании поражение в 50% случаев носит двусторонний симметричный или несимметричный характер, поражается окружающая легочная ткань. Расположены полости преимущественно по периферии [20], их наружные и внутренние контуры четкие. При отсутствии вторичной инфекции полости не содержат жидкость. При саркоидозе в 35% случаев отмечается увеличение внутригрудных лимфоузлов [13].
Эхинококковые кисты одинаково часто поражают как правое, так и левое легкие, также было отмечено значительное (в 2 раза) преобладание поражения нижних долей по сравнению с верхними [21]. Рентгенологическая картина зависит от фазы заболевания. В большинстве случаев кисты имеют овальную или яйцевидную форму, причем отмечается зависимость формы кисты от ее расположения в легочной ткани. При расположении кисты в центральной или средней зонах форма ее преимущественно неправильная, что связано с влиянием на стенки кисты сосудисто-бронхиальной системы; в литературе описываются характерные формы «почки» и «карточного сердца». При расположении кисты на периферии с равномерным влиянием легочной паренхимы на стенки кисты ее форма преимущественно правильная, округлая. При значительных размерах кисты и ее близком расположении к грудной стенке, позвоночнику, диафрагме, средостению отмечается уплощение кисты. Структура кисты в закрытой фазе однородна, контуры при отсутствии перикистозного воспаления четкие.
Рентгенологическая картина эхинококковой кисты в переходной фазе характеризуется уменьшением размеров кисты, сопровождающимся нечеткостью ее контуров. Одиночная вскрывшаяся эхинококковая киста дает рентгенологическую картину с симптомом отслоения хитиновой оболочки от фиброзной капсулы в виде воздушной полости в форме серпа в любом участке тени. При спавшейся хитиновой оболочке в полости фиброзной капсулы рентгенологически определяются газ и жидкость. При падении внутрипузырного давления возможно попадание воздуха как в перикистозное пространство, так и в полость самой кисты. Такая рентгенологическая картина является патогномоничной для эхинококковой кисты в легком. Cumbo в 1921 г. назвал ее симптомом «двойной арки». При неполном опорожнении кисты и достаточном количестве жидкости на поверхности могут определяться волнистость и выпуклость, обусловленные наличием на поверхности сморщенной хитиновой оболочки эхинококка. Этот симптом носит название «водяной лилии» [Rubin, 1954]. Полость заполняется контрастным веществом при бронхографии. После полного очищения кисты исходом ее является пневмокиста в форме кольцевидной тени неправильной округлой формы.
Парагонимоз – заболевание, возникающее в результате инвазии легочной двуустки. Ее цисты выявляются в виде множественных полостей, содержащих воздух, до 1–2 см в диаметре с толстыми стенками.
При гистиоцитозе Х (форма Абта – Леттерера – Сиве) в 94,3% случаев поражение носит двусторонний характер [13]. Характерным рентгенологическим признаком является наличие большого количества мономорфных [20] толстостенных, но мелких полостей (57% случаев). Дифференциальную диагностику этого заболевания облегчает специфическая клиническая картина с внелегочным поражением.
Кисты легких, как уже было отмечено, могут быть как первичными, так и вторичными. Одиночные приобретенные легочные кисты являются следствием какого-то заболевания воспалительной этиологии с вовлечением в процесс легочной ткани и бронхиального дерева. Кисты бывают размерами от 0,5 до 20 см в диаметре, различной формы. Неосложненные кисты имеют правильно округлую форму. Стенки полости тонкие, ровные, с резко очерченным как внутренним, так и наружным контуром. Окружающая легочная ткань не изменена или фиброзно изменена. Осложненные кисты содержат жидкость на дне. По периферии кист имеется перифокальное воспаление.
Рентгенологические исследования с применением контрастных веществ. При бронхографии иногда удается выявить признаки, помогающие отличить туберкулему от периферического рака и абсцесса легкого. Бронхография при определении полостей гнойников малоэффективна. Полости острых абсцессов, как правило, не заполняются контрастным веществом вследствие отечности слизистой оболочки дренирующих бронхов, наличия гноя и секвестров в них. При абсцессе часто в патологический фокус входит несколько бронхов, что при раке не наблюдается [15]. При туберкулеме сегментарные бронхи поражаются редко, образуя деформированную культю; субсегментарные бронхи также образуют культю, но обрывающуюся у капсулы туберкулемы или на некотором расстоянии от нее. При периферическом раке бронх чаще всего входит в патологическое образование и, обрываясь, образует культю внутри самой опухоли.
При бронхографии у пациентов с очаговым распадом опухоли в зоне поражения обычно выявляются сужение и узурация мелких бронхиальных ветвей, при массивном распаде более характерной оказывается ампутация концевых бронхов, подходящих к опухоли [19]. Использование бронхографии позволяет изучить состояние бронхиального дерева в зоне поражения, что имеет большое значение для определения путей катетеризации опухоли и выбора оптимального способа получения биопсийного материала [19]. Контрастирование пищевода и желудка, диагностический пневмоперитонеум, пневмомедиастинография применяются для исключения полостных образований внелегочной локализации, вдающихся в гемиторакс из прилежащих к легким отделов, которые проецируются на легочное поле.
Абсцесс легкого
Как уже было отмечено, наибольший процент среди пациентов с синдромом внутрилегочного полостного образования, поступающих в стационар, составляют пациенты с острыми и хроническими абсцессами легкого. Абсцессы легкого – наиболее часто встречающиеся заболевания, которые проявляются клинико-рентгенологическим симптомокомплексом – синдромом внутрилегочного полостного образования. Количество тяжелых форм острых инфекционных деструкций легких (ОИДЛ), несмотря на достижения современной медицины как в консервативном, так и в хирургическом лечении заболеваний, которые осложняются ОИДЛ, не снижается. В основном это обусловлено появлением высоковирулентных, антибиотикорезистентных штаммов микроорганизмов, снижением общей резистентности макроорганизма вследствие неблагоприятных экологических факторов, несовершенством традиционных методов диагностики [22].
В последние десятилетия расширились представления об этиологической значимости различной микрофлоры, участии вирусов в развитии ОИДЛ. Проводятся исследования механизмов развития ОИДЛ, связанных с изменениями гомеостаза, патологии иммунной системы [22].
Сложное строение легких определяет специфическое течение воспалительного процесса в легочной ткани. Вирусное поражение снижает сопротивляемость легочной паренхимы, способствует некробиотическим изменениям бронхиального и альвеолярного эпителия, вызывает токсическое поражение сосудистого эпителия, изменяет нормальную трофику, нарушает нервную регуляцию и местное кровообращение.
При воспалительном процессе в легочной паренхиме нарушается проходимость мелких бронхов из-за спазма, отека или обтурации секретом, в результате чего возникает ателектаз участка легкого. Прогрессирование инфекционного процесса вызывает расстройство легочного кровообращения в таком участке легкого, что в конечном итоге приводит к некрозу легочной паренхимы. Кровоток в системе легочной артерии в зоне гнойного воспаления практически не осуществляется, а жизнедеятельность воспаленной легочной ткани поддерживается за счет усиления кровообращения в бронхиальных артериях [22].
Высокая протеолитическая активность продуктов жизнедеятельности микроорганизмов иногда приводит к аррозии стенок сосудов, расплавлению тромботических масс и поступлению большего или меньшего количества крови в пораженное легкое. Пораженная легочная паренхима подвергается отграничению от жизнеспособной легочной ткани, происходят ее распад, полное или частичное гнойное расплавление и отторжение. Течение этого процесса зависит как от патогенности микроорганизма, так и от реактивности макроорганизма. При адекватном лечении происходят очищение полости от гнойного содержимого, спадение стенок полости, ее облитерация и рубцевание. Это расценивается как полное выздоровление.
У части больных успешное лечение может завершиться формированием и сохранением остаточной полости – «ложной кисты». С течением времени она покрывается изнутри эпителием, растущим из просвета дренирующего бронха, а по периферии отграничивается от здорового легкого рубцовой тканью. Это расценивается как клиническое выздоровление.
Если в полости деструкции в течение длительного времени находятся секвестры некротизированной ткани, а по периферии рано начинают формироваться пневмосклеротические изменения и рубцовая капсула, то внутренняя поверхность покрывается грануляционной тканью, острый абсцесс переходит в хронический [22].
Собственные данные
811 больных в возрасте от 18 до 85 лет поступили в отделение гнойной торакальной хирургии городской клинической больницы № 61 (Москва) в период с 2000 по 2013 г. Большинство больных поступали в отделение с подозрением на абсцедирующую пневмонию. Пациентов доставляла служба скорой медицинской помощи или переводили из других стационаров г. Москвы. Подавляющее большинство поступивших (528 человек, 65,1%) были наиболее трудоспособного возраста – от 20 до 55 лет. Полостные образования легких у мужчин встречаются значительно чаще, чем у женщин: 653 случая (80,51%) и 158 случаев (19,48%) соответственно. 674 пациента по результатам проведенного обследования страдали от острого и хронического абсцесса легкого.
В общих хирургических и терапевтических стационарах нет четкого алгоритма обследования больных с синдромом внутрилегочного полостного образования, что приводит к несвоевременной, неправильной диагностике и неадекватному лечению. При патологиях отмечалось острое, постепенное, а порой и бессимптомное начало. Такие симптомы, как одышка, продуктивный кашель, кровохарканье, боли в грудной клетке были отмечены и при неспецифических гнойно-деструктивных поражениях легочной ткани, и при специфических процессах, таких как туберкулез и полостная форма рака легкого, что соответствует данным литературы.
Симптомы интоксикации, отклонения от нормы при физикальном исследовании, изменения общего и биохимического анализа крови не являются патогномоничными для той или иной патологии и должны оцениваться в динамике. Однако всем пациентам, поступающим в стационар, было проведено биохимическое исследование крови, включавшее в себя оценку основных показателей (общий белок, аланинаминотрансфераза, аспартатаминотрансфераза, мочевина, креатинин, глюкоза). При наличии отклонений от нормальных показателей при базовом исследовании проводилась оценка дополнительных параметров, более часто выполнялось и само базовое исследование в динамике на фоне лечения.
Обязательным исследованием в настоящее время является выполнение коагулограммы (фибрин, тромбиновое время, протромбиновое время, международное нормализованное отношение, активированное частичное тромбопластиновое время). Учитывая высокую вероятность наличия у пациента с внутрилегочным полостным образованием коагулопатии, мы считаем недопустимым отсутствие указанного исследования.
Методы диагностики
Рентгенологическое исследование является базовым в диагностике внутрилегочных полостных образований. Для общего представления о состоянии легких, локализации патологического процесса, наличии дополнительных патологических теней, вовлеченности рядом расположенных органов всем 811 пациентам были выполнены рентгенография грудной клетки и полипозиционная рентгеноскопия. На обзорных рентгенограммах проявлялись тонко- и толстостенные полости.
При компьютерной томографии представляется возможным более четко оценить стенки полости, изменения окружающей ткани, увеличение регионарных лимфоузлов. Наиболее информативным это исследование является при постановке диагноза у пациентов с тонкостенными внутрилегочными полостными образованиями. Однако при дифференциальной диагностике толстостенных внутрилегочных полостных образований это исследование недостаточно эффективно.
Для исключения экзофитной патологии бронхиального дерева у пациентов с внутрилегочными полостными образованиями в 606 случаях (74,7%) была выполнена фибробронхоскопия. Диффузный двусторонний бронхит был выявлен у 98,7% пациентов, что, очевидно, связано с общей неблагоприятной экологической ситуацией. Эндоскопическое исследование в 23,07% случаев позволило выявить у пациентов с полостной формой рака прямые или косвенные признаки опухолевого роста. При абсцессе легкого в 97,3% случаев выявлены более выраженные признаки бронхита на стороне поражения (дренажный бронхит). Бронхоскопическое исследование было дополнено проведением фибробрашбиопсии, щипцовой биопсии.
Состояние легочного кровотока, диффузионная способность легких, вентиляция окружающих полость тканей играют немаловажную роль в диагностике заболевания, оценке компенсаторных способностей бронхолегочной системы, формировании лечебной тактики, определении объема хирургического вмешательства. Для этих целей мы применяли радионуклидный метод исследования – перфузионную пульмоносцинтиграфию. Когда речь шла об опухоли центральной локализации, практически всегда отмечалось отсутствие кровообращения или его выраженное диффузное снижение. Изменения на сцинтиграмме, как правило, превышали объем нарушений, выявляемый при рентгенологическом исследовании. При периферической локализаций опухоли имело место некоторое снижение прозрачности легочных полей и разрежение или даже полное отсутствие накопления изотопа в зоне расположения опухоли.
Всем пациентам были выполнены трехкратное микроскопическое исследование мокроты, посев мокроты, обследование соответствующими методами при подозрении на наличие внелегочной патологии. Если установить точный диагноз или распространенность патологических изменений не представляется возможным, особенно в случаях, когда совокупность результатов обследования не позволяет исключить специфический характер процесса, показано проведение диагностического оперативного вмешательства.
Методики консервативного лечения пациентов с неспецифическими внутрилегочными полостными образованиями (абсцессы легких)
Лечение проводилось по принятой в клинике методике: АБТ, сочетающаяся с различными типами дренирования и санации полости гнойника, бронхоскопические катетеризации и санации. Специфическая противовирусная терапия в нашей клинике не используется. На этапе назначения стартовой АБТ проводится посев мокроты, по результатам которого происходит смена АБТ.
Для улучшения дренирующей функции бронхов применяются бронхолитики, отхаркивающие средства, ингаляции. Повторные лечебные бронхоскопии при достаточно близком расположении абсцесса к главному бронху проводятся 1–3 раза с интервалом 4–5 дней по методике Г.И. Лукомского. При расположении абсцесса в нижних долях легкого проводится дренаж. Для этого ножной конец кровати приподнимается на 20–30 см, и пациент принимает соответствующее положение. В комплексной терапии используется стимулирование защитных сил организма (высококалорийное питание, белки, витамины, физиотерапия, ультрафиолетовое облучение крови).
В течение длительного времени в клинике применяется методика длительной трансназальной катетеризации полости абсцесса, внедренная М.В. Филипповым. Под рентгенологическим контролем через канал фибробронхоскопа в полость абсцесса вводится катетер (мы используем катетер типа Pigtale), проводятся введение в полость антибактериальных препаратов и промывание растворами антисептиков (гидроксиметилхиноксилиндиоксид, хлоргексидин). После удаления фибробронхоскопа катетер фиксируется к коже носа и остается в полости абсцесса. Ежедневно 2–3 р./сут полость абсцесса санируется введением антисептиков, продолжается интракавитальное введение антибактериальных препаратов. Длительность проведения трансназальной катетеризации зависит от изменений клинико-рентгенологической и эндоскопической картин, динамики клинического анализа крови.
Возможно проведение чрескожной пункции с последующим трансторакальным дренированием полости абсцесса по Мональди. Проводится рентгенологическое исследование легких с наложением метки на область предполагаемой пункции. Затем таким же способом, как и при торакоцентезе, проводится пункция, в полость абсцесса заводится дренажная трубка. Эта манипуляция была выполнена 13 пациентам с острым абсцессом легкого, что составило 1,93%. В 97,1% случаев применение консервативной терапии по вышеописанной методике привело к выздоровлению пациентов (рис. 1).
Лечение пациентов с неспецифическими внутрилегочными полостными образованиями невоспалительной природы (преимущественно кисты легких паразитарной и непаразитарной природы) было (при отсутствии противопоказаний) оперативным.