Значение проведения пострегистрационных клинических исследований
Пострегистрационные исследования лекарственных препаратов являются важным жизненным этапом любого медикамента даже несмотря на то, что регулятор не считает их обязательными. Главная цель проведения подобных испытаний — это обеспечение полноценного сбора дополнительной информации, связанное с выяснением эффективности и безопасности медицинского препарата на довольно большой популяции, в реальных условиях и на протяжении длительного времени. Для того чтобы обеспечить однородную выборку, клинические исследования проводятся на ограниченный популяции, исходя из довольно жестких критериев отбора, что в некоторых случаях не позволяет до регистрации качественно оценить поведение препарата у пациентов, имеющих различные сопутствующие заболевания или принимающих другие лекарства.
Учитывая ограниченное число людей, проходящих клинические исследования на этапе дорегистрационного изучения лекарственного средства, очень редко встречающиеся побочные эффекты могут оказаться незарегистрированными по причине того, что у конкретных добровольцев они не встретились, однако это не означает, что при более широком, массовом употребления, какие-либо противопоказания не проявятся. Увидеть их и идентифицировать по всем параметрам можно только тогда, когда препарат уже выйдет на рынок и будет использоваться большим количеством пациентов.
Как только лекарственное средство поступает на реализацию, за ним начинают тщательно следить специалисты в стремлении оценить и изучить самые важные параметры терапии медикамента, его взаимодействие с остальными препаратами и воздействие на организм пациента при длительном использовании либо наличии заболевания других систем и органов.
Дополнительно проводится анализ эффективности применения у людей различного возраста с выявлением редких побочных эффектов и др. Все перечисленные данные спустя некоторое время вносятся в инструкцию по применению медикамента в определенном порядке, который подробно обозначен на https://www.oct-clinicaltrials.com/ru/services/drug_registration_russia.php.
Кроме того, в пострегистрационном периоде могут обнаружиться и новые положительные качества препарата, которые далее потребуют дополнительных клинических испытаний и могут выступить в качестве основы для расширения показаний исследуемого лекарственного средства.
Если в препарате таким образом будут обнаружены ранее неизвестные, но являющиеся опасными побочные эффекты, то его использование может быть ограничено, а регистрация приостановлена или отозвана вовсе.
Пострегистрационные исследования лекарственных средств и БАД
Успешно пройдя все этапы исследований, лекарственное средство регистрируется в государственном реестре, а разработчик получает регистрационное свидетельство. Лекарственный препарат выводится на рынок. На данном этапе в процесс включаются маркетологи для продвижения лекарственного средства. Тем не менее также остается необходимость и у компании-производителя получать информацию об использовании лекарственного средства с целью сбора важных сведений, таких как:
-получение более полной информации об эффективности и безопасности препарата;
-анализ данных о препарате при его применении в рутинной медицинской практике;
-выявление новых, ранее не возникающих побочные действий;
-выявление новых потенциальных свойств и показаний к применению препарата.
Таким образом, при проведении пострегистрационных исследований компания-производитель, спонсор ставят перед собой задачу более полно и глубоко изучить действие препарата после его попадания на рынок и широком назначении врачами и применения пациентами.
Такие исследования, так же, как и клинические, проводятся на группах людей. Но вовлекаются значительно большее количество пациентов. Такой подход имеет неоспоримые плюсы.
1. Нивелируются случайные совпадения
2. Задействуются значительные возрастные и другие характеристики испытуемых, что дает более широкую информацию об эффективности препарата при его использовании в разных группах пациентов.
3. Могут охватывать те группы пациентов, которые не участвовали в клинических исследованиях, что потенциально может выявить новые данные по безопасности и эффективности лекарственного препарата.
Вдобавок пострегистрационные исследования несут на себе и маркетинговые задачи:
-вовлекают в исследование лиц – экспертов в области фармакотерапии, национальных координаторов программ исследования, лидеров мнений;
-по результатам исследований способствуют включению препарата в льготные листы, списки, списки жизненно необходимых средств;
-получают данные для публикаций, презентаций, рекламных кампаний.
Все пострегистрационные исследования можно распределить на несколько групп.
1. В зависимости от степени вмешательства («интервенции») в лечебный процесс:
-Интервенционные исследования. Предполагают ситуацию, заданную экспериментально, т.е. вмешательство в лечебный процесс, его упорядочивание, рандомизацию испытуемых в группы по определенным признакам, назначение препарата в вариантах, отличных от инструкции по применению;
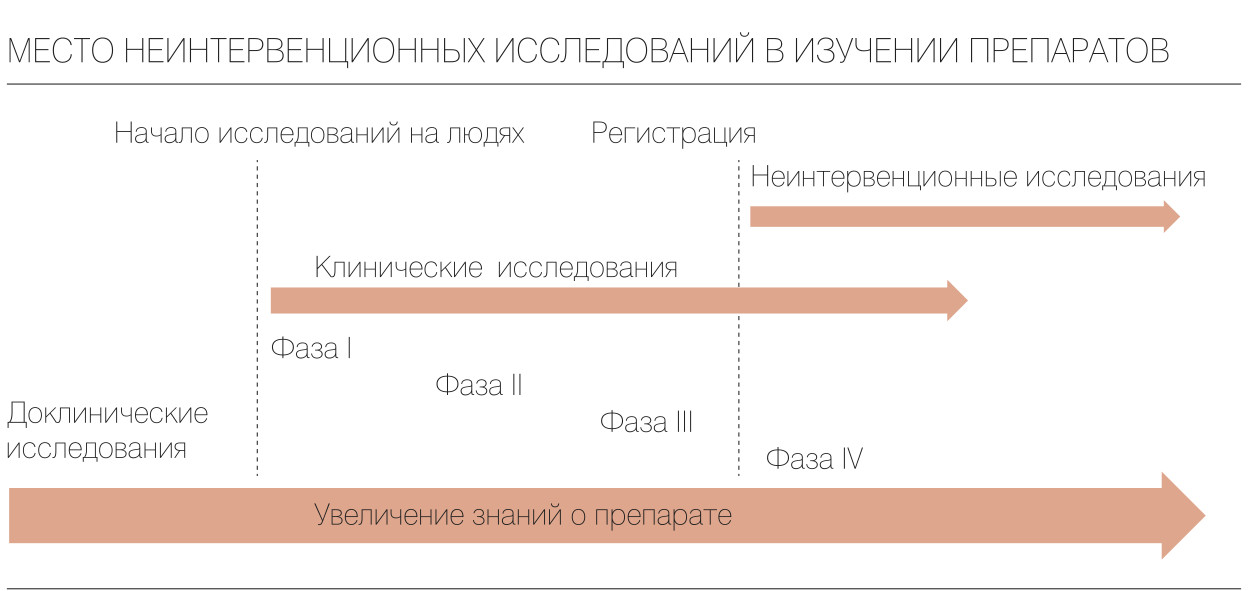
-Неинтервенционные исследования. Имеют более значимую объективность, так как проводятся без вмешательства в лечебный процесс, а проходят в рамках общей медицинской практики. То есть препарат назначается по прописанным показаниям, и не назначается какое-либо дополнительное лечение и контрольные мероприятия, связанные непосредственно с исследованием. Использование лекарственного средства в повседневной жизни, в рамках разрешенной терапии, дает бесценную информацию по соотношению предполагаемой пользы к возможному риску применения, дает возможность оценить взаимодействие с другими препаратами, получить более широкие данные о препарате.
Компания Clinical Research Laboratory (CRLab) обладает опытом большим проведения обоих типов исследований, что имеет особое значение для наших спонсоров.
2. В зависимости от принципов организации:
— исследования в рамках GCP. GCP- это международный этический и научный стандарт планирования и проведения клинических исследований с участием человека в качестве субъекта исследования. Он принят во многих странах, что позволяет странам участникам принимать результаты партнеров как достоверные.
— Неклинические исследования – фармакоэпидемиологические, неинтервенционные, инициативные исследователем и другие.
3. По локализации места проведения:
-локальные (проводящиеся в одной стране)
4. По дизайну исследования:
-открытые или слепые (простые слепые или двойные слепые) исследования;
-проспективные (в начале составляется план исследования и порядок сбора и обработки данных, а затем проводится само исследование по ранее запланированным этапам) или ретроспективные (оценка проводится по уже пошедшим событиям, например, историям болезни);
— сравнительные (имеющие группы сравнения или контроля) или несравнительные исследования;
-параллельные или перекрестные (по дизайну исследования);
-рандомизированные или нерандомизированные (рандомизация – способ распределения пациентов в исследуемые группы с использованием методов статистики и элементов случайности).
5. В зависимости от источника получения препарата под исследование:
— от Спонсора – производителя фармпрепарата;
— от Учреждения (например, научно-исследовательского института – НИИ).
По завершении экспериментальной части исследования происходит сбор, группировка и анализ полученных результатов. Полученные данные подтверждают или задают новый вектор в развитии продвижения лекарственного препарата и предлагают варианты доработки, усовершенствования, увеличения эффективности без снижения безопасности лекарственного средства.
Одним словом, пострегистрационные исследования являются важным этапом в жизненном цикле препарата, используемого в медицинских целях.
Чем на самом деле является вакцина от коронавируса? Испытания, скрытые компоненты и правда о сроках разработки «Спутник V»
Чем на самом деле является вакцина от коронавируса? Испытания, скрытые компоненты и правда о сроках разработки «Спутник V»

Институт им. Гамалеи, где и был синтезирован «Спутник V», создавал вакцины на основе аденовируса с 2015 г., поэтому ученым в относительно небольшие сроки удалось создать вакцину от коронавируса. Она защищает организм от заражения следующим образом: в аденовирусный вектор (вирус), который искусственно лишили возможности размножаться, вшили ген, кодирующий S-белок шипа коронавируса. Вектор доставляет кусочек РНК-вируса в клетку, а та, в свою очередь, реагирует на это так же, как реагировала бы на вторжение SARS-CoV-2. Начинают вырабатываться специфические антитела, которые и создают иммунитет против коронавируса.
Что входит в состав вакцины от коронавируса и содержатся ли в ней опасные «ингредиенты»?
Аденовирусный вектор – основное действующее вещество вакцины. Это главное составляющее, но, для работы прививки необходимы и другие компоненты. Они помогают сохранить эффект действующего вещества и облегчают его проникновение в клетки человека.
Помимо самого аденовирусного вектора в состав «Спутник V» входят:
Каждый «ингредиент» прививки от коронавируса абсолютно безвреден. Для того чтобы проверить, формируют ли в связке все эти компоненты устойчивый иммунитет к коронавирусу, проводятся испытания.
Какие испытания прошла вакцина от коронавируса?
Сразу после синтеза нового препарата, ученые провели доклиническое тестирование на хомячках и приматах. Проверяли токсичность, безопасность и эффективность новой вакцины. Никаких осложнений, побочных реакций у животных не возникло, поэтому ученые приступили к клиническим испытаниям на людях.
Первая фаза испытаний обычно проводится на небольшой группе здоровых добровольцев. Для тестирования российской вакцины «Спутник V» было привлечено 76 военных возрастом от 18 до 60 лет. Фаза была разделена на два этапа.
Первый этап длился 28 дней. Девятнадцати добровольцам поставили первую часть вакцины, основанной на ослабленном аденовирусе 26 типа, другим девятнадцати – вторую, с аденовирусом 5 типа. Так была проверена безопасность обоих компонентов вакцины. Результатом этапа стала хорошая переносимость препарата всеми добровольцами. Побочные эффекты были легкими или умеренными:
Опасных для жизни побочных эффектов обнаружено не было.
Во время второго этапа исследовался уже формирующийся после вакцинации иммунитет. Все добровольцы получили обе части вакцины с разницей в 21 день между ними. На 28 день после введения второй дозы, с помощью высокоточных тестов, у 100% добровольцев были обнаружены антитела к SARS-CoV-2. Более того, было доказано формирование другого – клеточного иммунитета. Обычно он сохраняется в «памяти» организма несколько лет.
Спустя три месяца после старта третьей фазы клинических испытаний в декабре 2020 г. российский Минздрав принял решение совместить последний этап исследований с массовой вакцинацией населения прививкой «Спутник V». Решение приняли оперативно, основываясь на предварительных результатах, опубликованных разработчиками вакцины в ноябре 2020 г.
В основе проведенных расчетов лежат случаи заболевания COVID-19 среди уже привитых добровольцев. Из общего числа участников испытаний, получивших обе положенные инъекции вакцины или плацебо (18 794), к концу третьей недели после второго укола вирус был диагностирован у 39 человек.
31 случай заражения был выявлен у тех, кто получил плацебо. В группе волонтеров, привитых настоящей вакциной, COVID-19 был диагностирован у восьмерых (группа получивших вакцину – в три раза больше группы плацебо). Сопоставление результатов по двум группам дает результат эффективности вакцины в 95%.
«Набранная группа участников исследований позволяет в полной мере исследовать профиль безопасности и профилактической эффективности вакцины на длительном промежутке времени», – пояснили в Минздраве.
Несмотря на то, что прививка «Спутник V» стала доступна всем желающим (за исключением группы с противопоказаниями), ученые продолжили наблюдение за добровольцами, принявшими участие в третьей фазе клинических испытаний. Второго февраля 2021г. разработчики вакцины представили результаты исследования в авторитетном медицинском издании The Lancet.
Результаты последней третьей фазы клинических испытаний вакцины «Спутник V»
Третья фаза испытаний вакцины «Спутник V» длилась с 7 сентября по 24 ноября. В ней приняли участие 21 977 человек, из них 16 427 были привиты, а 5435 – получили плацебо (раствором, в который входят все ингредиенты «Спутник V», кроме самого аденовирусного вектора).
Согласно выводам ученых специфические антитела против коронавируса вырабатывались через 42 дня после первой прививки или через 21 день после второй у 95,8% добровольцев. Более того, в день первой инъекции и через 28 дней после второй у добровольцев уже определялся клеточный иммунитет.
Что касается побочных эффектов, они проявились у 7966 привитых, при этом у 94% из них были легкими и включали повышение температуры, неприятные ощущения в месте инъекции, головную боль и слабость. Лишь 0,3% привитых имели серьезные побочные эффекты, однако, независимая комиссия не доказала связи между ними и вакцинацией.
Эффективность вакцины при таких показателях составляет 91.6%.
«Спутник V» также исследовали на добровольцах старше 60 лет – всего 2144 человека. Эффективность вакцины в этой группе практически не отличается от общей и составляет 91.8%.
Таким образом, вакцина показала свою эффективность и безопасность как у людей от 18 до 60 лет, так и у пожилых добровольцев. При этом серьезных побочных эффектов, связанных с вакциной, обнаружено не было.
Быстро не значит плохо: почему вакцину от коронавируса разработали за короткие сроки?
Разработка и тестирование вакцины заняли около года. Это уникальный, но объяснимый, случай. Прежде всего, ускорило создание «Спутник V» то, что вакцина была сделана на основе аденовирусного вектора. Такая технология уже давно известна ученым, а сам центр им. Гамалеи имел опыт в выпуске подобных вакцин. Ранее была разработана вакцина от ближневосточного респираторного синдрома. Вирус, который его вызывает – MERS, также относится к группе коронавирусов.
Быстрое распространение и способность к мутации вируса требовали кардинальных решений. При этом безопасность и эффективность вакцины на первом месте. Именно поэтому первые фазы исследования были проведены с соблюдением всех международных правил: количество добровольцев на каждой фазе, критерии оценки их состояния здоровья после вакцинации. Только после того, как вакцина показала свою безопасность и способность защищать от коронавируса, было принято решение о массовой вакцинации.
Как изменится мир после массовой вакцинации?
Идея коллективного иммунитета заключается в том, что, когда достаточно большое число людей в популяции уже обладает иммунитетом, инфекция лишается каналов распространения. Из-за этого вспышки заболевания быстро сходят на нет. Добиться коллективного иммунитета против коронавируса можно только путем вакцинации.
После массовой вакцинации будет снижена нагрузка на медицинский персонал и больницы, многие люди, особенно те, которые находятся в группе риска, смогут вернуться к привычной жизни. Вакцинация не только положит конец пандемии, но и поможет не бояться новых вспышек коронавируса.
Что такое пострегистрационные испытания вакцины
Зачем проводят пострегистрационные исследования?
После доклинических исследований на животных каждый препарат проходит клинические испытания, чтобы получить разрешение на государственную регистрацию.
Успешно пройдя исследования, которые требуют регуляторные органы, лекарственное средство выходит на рынок, и компания-производитель занимается лишь продвижением своего продукта. При этом сохраняется необходимость в получении информации о результатах применения ЛС в рутинной клинической практике, в уточнении профиля рисков препарата, в изучении его взаимодействия с другими назначаемыми пациенту лекарственными средствами. Такие данные пришлось бы собирать долгие годы, если бы не велись неинтервенционные исследования, которые могут предоставить нужные сведения об использовании препарата в массовом порядке.
Неинтервенционные исследования лекарственных препаратов могут проводиться компаниями-производителями или научными коллективами в рамках проведения научно-исследовательских работ. Несмотря на то что эти исследования имеют важное медико-социальное значение, далеко не каждый производитель препарата готов оправдать доверие своих потребителей и выступить в качестве инициатора и спонсора такого рода исследований, так как этого не требуют регуляторные органы, а продукт уже выведен на рынок. Но в чем же научная значимость и преимущества наблюдательных исследований?
Неинтервенционные исследования – исследования без вмешательств, т.е. лекарственное средство назначается врачом обычным способом в соответствии с инструкцией к препарату. Применение препарата в реальной жизни, в рутинной клинической практике и в рамках разрешенной терапии предоставляет наиболее достоверные данные об эффективности и безопасности ЛС. Также появляется возможность оценить отношение пациентов к схеме приема и самому препарату, что более точно отражает результаты исследования.
В регистрационных клинических исследованиях эффективность изучаемого препарата определяется на пациентах, которые были выбраны согласно строгим критериям включения. Неинтервенционные исследования позволяют изучить ЛС на большой популяции пациентов без возрастных ограничений, что нивелирует фактор случайности при изучении вариаций оцениваемых параметров. В том числе дается возможность изучения эффективности и безопасности препарата у пациентов с сопутствующими заболеваниями и патологиями. Также необходимо учитывать, что сроки наблюдения за пациентами определяются спонсором исследования, поэтому за больными можно наблюдать длительное время, соответственно легче отследить процесс лечения по некоторым дополнительным параметрам, например по сезонности заболевания.
Еще одна ключевая особенность неинтервенционных исследований – возможность оценить использование в комплексной терапии, т.е. в сочетании с другими лекарственными средствами и процедурами, что не предусматривается в клинических исследованиях. Это позволяет собрать не только информацию о конкретном препарате, но и проследить течение заболевания и оценить существующие методики лечения. Также в пострегистрационном периоде могут быть обнаружены и новые положительные свойства препарата, которые в дальнейшем потребуют дополнительных клинических исследований и могут стать основой для расширения показаний для лекарственного средства.
Для реальной клинической практики огромное значение имеет комплаентность пациента, т.е. приверженность пациента к лечению, на которую напрямую влияют факторы информированности, скорости ожидаемого эффекта и удобства приема лекарственного препарата. Неинтервенционные исследования позволяют наладить обратную связь с пациентами: получить оценку назначаемой терапии, соблюдения курса лечения и определить степень удовлетворенности лекарственным препаратом.
Примером того, как компания-производитель ЛС сама инициирует и проводит пострегистрационное исследование для подтверждения эффективности, безопасности своего препарата и получения новых данных о течении заболевания, является международное многоцентровое проспективное когортное наблюдательное исследование «Лечение ОРВИ и гриппа в рутинной клинической практике» (FLU-EE). Результаты этого проекта уже вызвали интерес у профессионального сообщества, так как данные, полученные в исследовании FLU-EE, позволяют более точно прогнозировать течение и исход ОРВИ, улучшить результаты лечения и повысить качество жизни пациента в целом. Неинтервенционное исследование компании «Ниармедик» не только подтвердило эффективность и безопасность противовирусного препарата «Кагоцел», но и предоставило новые научные и статистические данные, которые крайне важны для понимания течения гриппа и ОРВИ, а также анализа применяемых в повседневной клинической практике схем терапии.
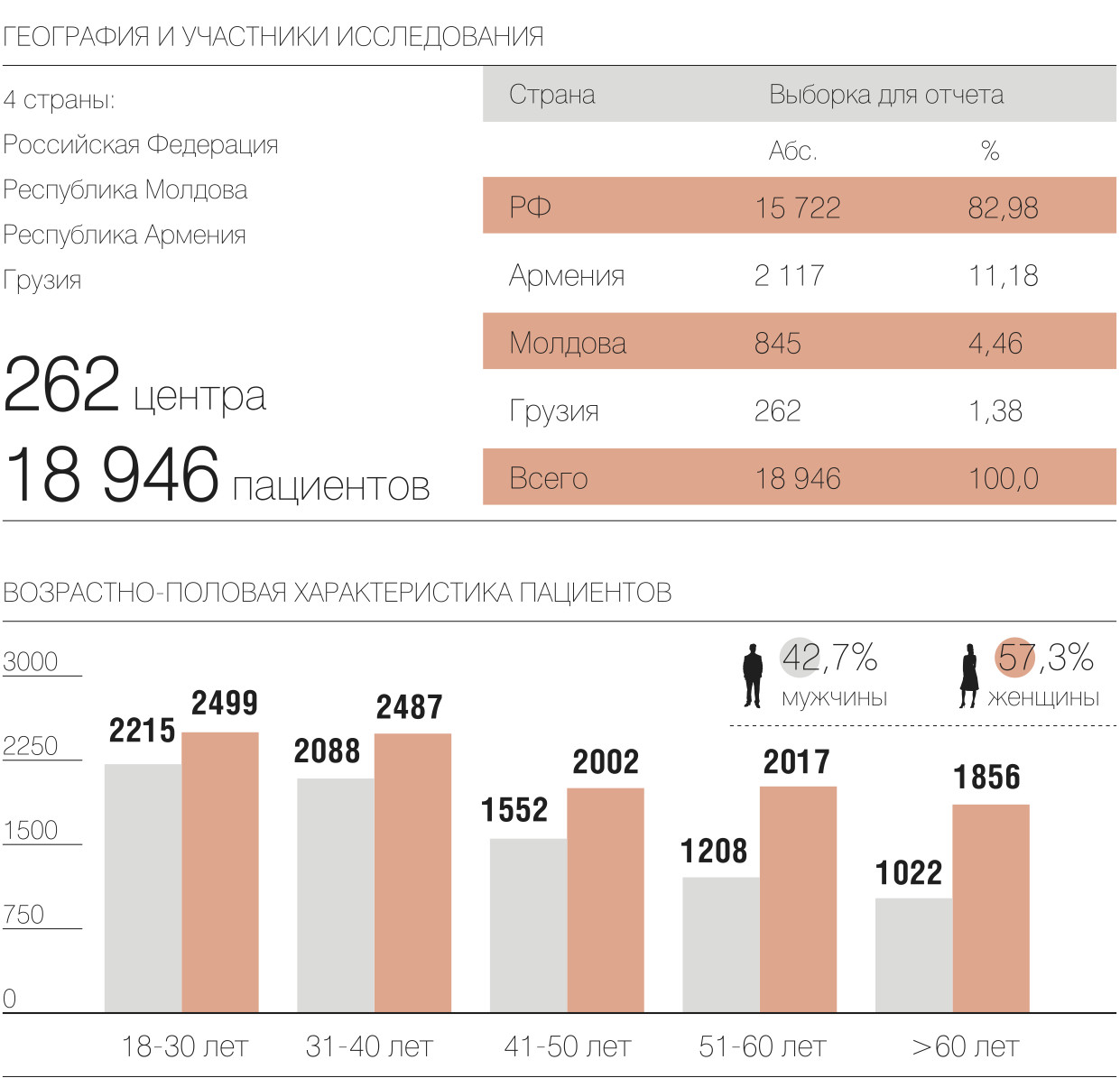
В исследовании FLU-EE приняли участие 18 946 пациентов в возрасте от 18 до 93 лет с установленными диагнозами ОРВИ и грипп. Компания сотрудничала с 262 медицинскими центрами России, Молдовы, Армении и Грузии. Врачами-исследователями стали специалисты первичного звена, терапевты, семейные врачи и врачи общей практики. К проекту также привлекли специалистов из Первого МГМУ им. И. М. Сеченова, которые проводили статистическую обработку данных и их клиническую интерпретацию.
В исследовании FLU-EE было предусмотрено три визита пациента к врачу, промежутки между визитами не регламентировались, и врачи придерживались принятой в каждой стране клинической практики лечения больных ОРВИ и гриппом. Общее количество получаемых пациентами препаратов на протяжении всего исследования варьировалось от 1 до 11, в среднем – 3 препарата. Наиболее часто назначали противомикробные средства для системного использования (это и противовирусные препараты, и антибактериальные) – 93,3%, а также лекарственные средства для лечения патологии дыхательной системы – 58,8%. Так как это неинтервенционное исследование, дополнительные процедуры не проводились. Врачи сами назначали необходимые, на их взгляд, препараты, в том числе и «Кагоцел».
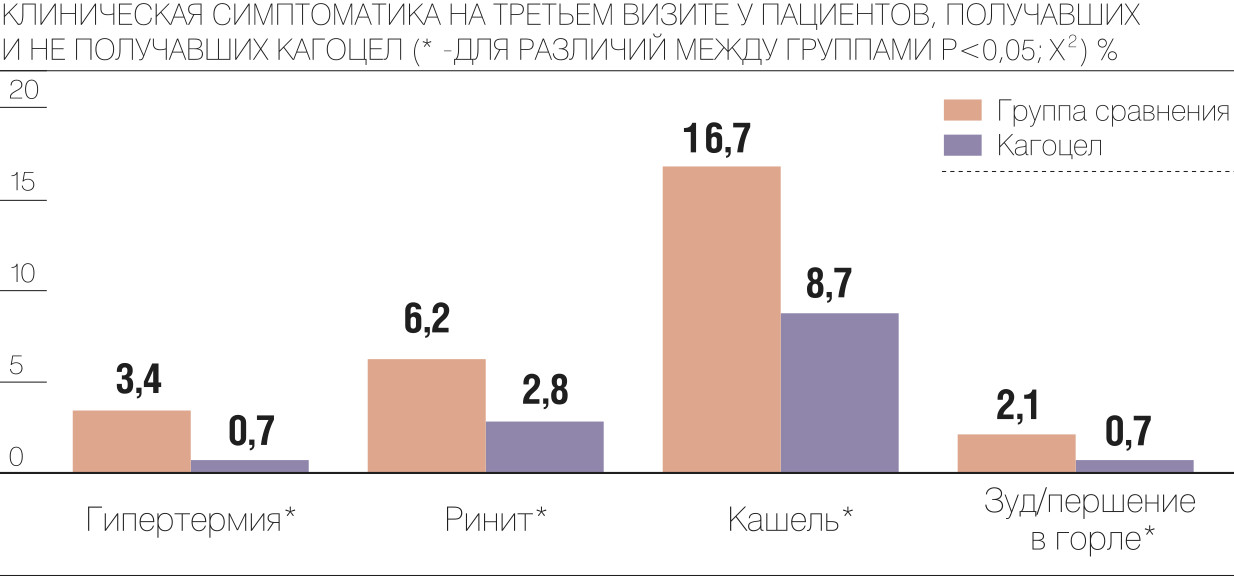
По окончании исследования для анализа результатов пациентов разделили на две группы, одной из которых в составе комплексного лечения был назначен противовирусный препарат «Кагоцел». Исследование FLU-EE доказало, что применение этого препарата в составе комплексной терапии улучшает клиническую картину заболевания: регистрировалось более быстрое купирование клинических симптомов (как интоксикации, так и катаральных) и происходила нормализация температуры, а также сокращались сроки выздоровления больных, в том числе с тяжелым течением заболевания. «Кагоцел» продемонстрировал эффективность у пациентов разного возраста и степени тяжести заболевания вне зависимости от времени назначения, в том числе при запоздалом лечении, на фоне высокого уровня безопасности.
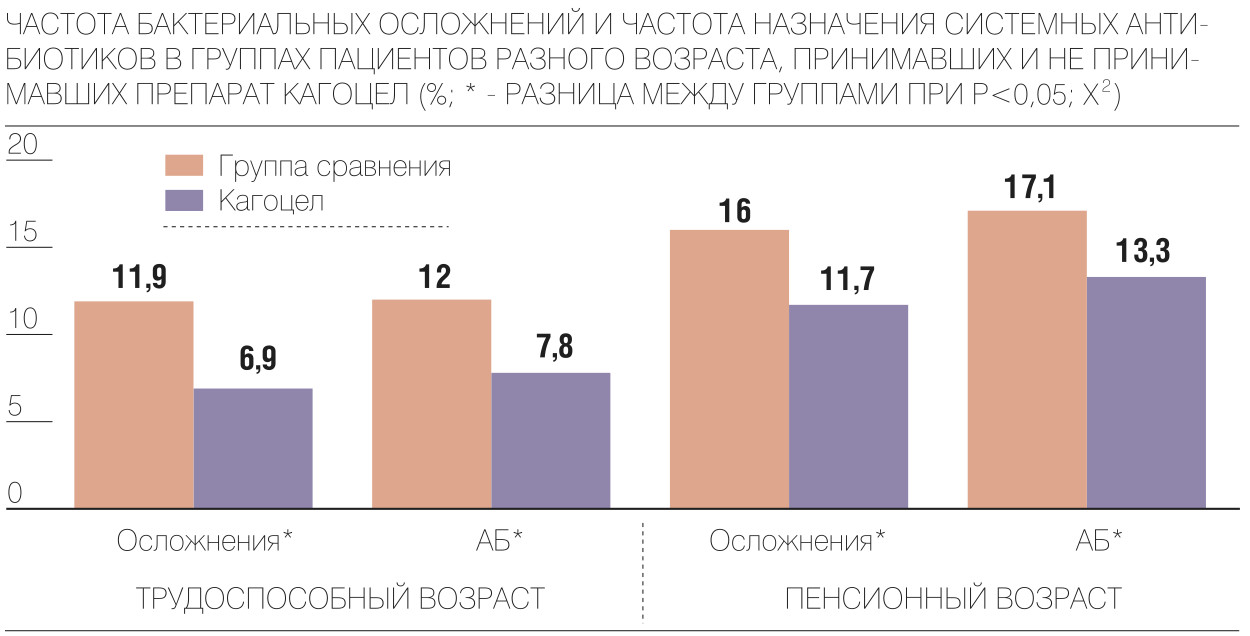
В ходе исследования FLU-EE удалось получить очень важные для специалистов данные. Например, для борьбы с бактериальными осложнениями в клинической практике используют антибиотики, но они не рекомендуются при легком и среднетяжелом течении ОРВИ, так как это грозит развитием лекарственной устойчивости возбудителей и замедлением процесса выздоровления организма. Даже возможно ухудшение исхода заболевания из-за побочных свойств антибактериальной терапии. В исследовании FLU-EE сравнили количество пациентов с зарегистрированными осложнениями и количество пациентов, которым были назначены антибактериальные препараты для терапии бактериальных осложнений, развивающихся на фоне ОРВИ и гриппа. Исследование FLU-EE наглядно показало, что антибактериальную терапию врачи рекомендовали 9,3% пациентов, при этом осложнения, действительно требующие назначения препаратов этой группы, зарегистрировали только у 8,3%. Учитывая огромный размер исследуемой популяции (почти 19 тысяч пациентов), за этим 1% разницы стоят реальные больные, т.е. такому большому количеству пациентов необоснованно прописали антибактериальную терапию. Некоторые пациенты получали антибиотики с профилактической целью. Были также зарегистрированы осложнения, которые требовали назначения антибактериальных препаратов, но пациенты не принимали их, в основном по причине добровольного отказа.
Эти данные наглядно демонстрируют, что, несмотря на растущую резистентность к антибиотикам и доказанную нецелесообразность их применения при ОРВИ, они активно рекомендуются врачами для лечения пациентов, что может ухудшить исход заболевания. Также исследование FLU-EE доказало, что «Кагоцел» в составе комплексного симптоматического лечения ОРВИ и гриппа достоверно способствует сокращению числа осложнений и, как следствие, снижает частоту назначения антибиотиков на 51%.
Кроме того, исследование показало, что применение «Кагоцела» сокращает частоту и длительность употребления жаропонижающих средств в 1,5 раза и позволяет справиться с лихорадкой нелекарственными методами. В группе «Кагоцела» существенно уменьшилась частота приема парацетамола (в 3,5 раза) и ибупрофена (в 3,7 раза), что, несомненно, положительно влияет на качество жизни пациентов и является весомым аргументом в пользу включения в комплексную терапию ОРВИ и гриппа индукторов интерферонов.
Для реальной клинической практики огромное значение имеет комплаентность пациента (приверженность пациента к лечению), на которую напрямую влияют факторы информированности, скорости ожидаемого эффекта и удобства приема лекарственного препарата, поэтому в ходе исследования была организована обратная связь с пациентами.
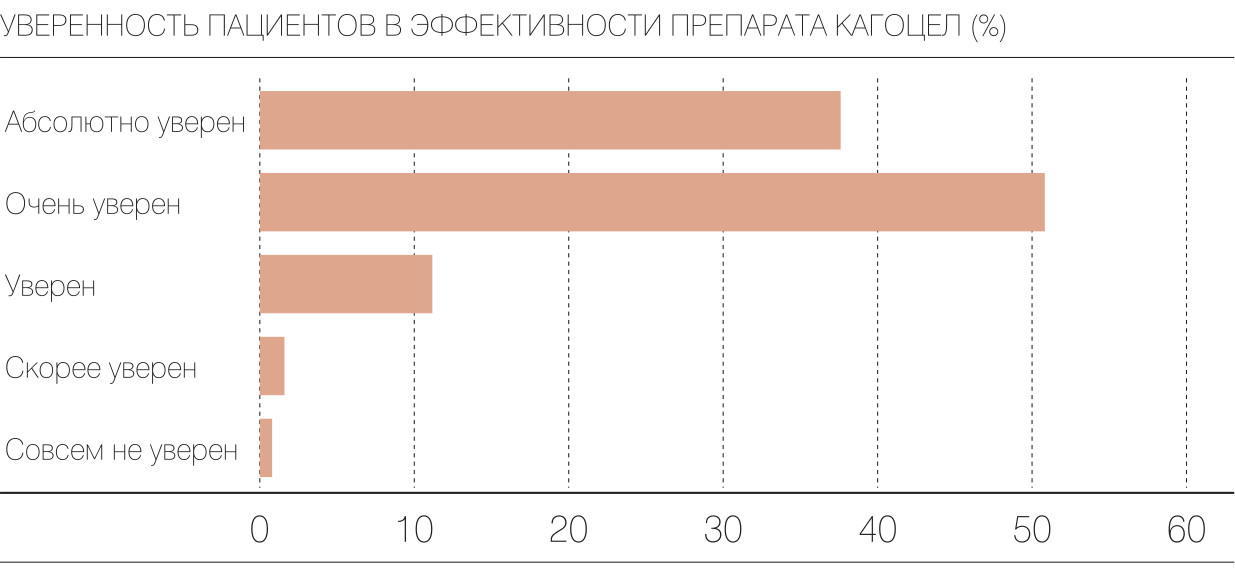
На третьем визите к врачу пациентам было предложено заполнить опросник удовлетворенности лечением TSQM (Treatment Satisfaction Questionnaire for Medication). В результате получены уникальные данные: 99% пациентов, получавших «Кагоцел», были уверены в пользе препарата. Более того, по результатам анализа субъективной оценки удовлетворенности терапией по таким параметрам, как результаты лечения, купирование симптоматики, сроки выздоровления, пациенты, которые получали в составе терапии «Кагоцел», были на 70% более довольны результатами лечения. Большинство пациентов отметили удобство формы, времени и схемы приема. Как мы видим, сами пациенты очень высоко оценивают эффективность препарата.
Доказанная эффективность в реальной клинической практике для врача, порой, может иметь большее значение, чем эффективность, показанная в ходе чистых клинических исследований. Зачастую неинтервенционные исследования, как продолжение клинических испытаний, служат единственным методом изучения редких нежелательных явлений препарата и дают максимально подробную информацию об эффективности ЛС в реальных условиях. Полученные данные в ходе исследования FLU-EE очень важны для понимания течения гриппа и ОРВИ, а также особенностей применения препарата «Кагоцел» в рутинной клинической практике. Исследование компании «Ниармедик» позволит более точно прогнозировать течение и исход ОРВИ, что, разумеется, существенно скажется на качестве жизни пациентов.
Научно доказанная безопасность
Рынки обращения лекарственных средств стран Евразийского экономического союза (ЕАЭС) объединяются и начинают работу в формате единого пространства. Создается единая фармакопея ЕАЭС. До 2025 года досье всех лекарственных препаратов стран-участниц необходимо привести в общий формат в рамках экономического союза. Компания «Ниармедик» уже сейчас начала подготовку к переходу на новый стандарт и актуализирует данные о противовирусном препарате «Кагоцел».
«Кагоцел» – противовирусный препарат компании «Ниармедик» для лечения и профилактики гриппа, ОРВИ и герпеса. Он способствует образованию в организме человека так называемых поздних интерферонов (ИНФ), которые обладают противовирусной активностью.
В настоящее время «Кагоцел» является одним из самых назначаемых в России противовирусных лекарственных средств. Эффективность и высокий профиль безопасности «Кагоцела» отмечают как врачи, так и пациенты. Несмотря на то что препарат имеет в полном объеме все необходимые для подтверждения эффективности и безопасности препарата доклинические и клинические исследования, проведенные согласно требованиям Министерства здравоохранения Российской Федерации, компания «Ниармедик» продолжает заниматься дополнительными пострегистрационными исследованиями «Кагоцела». Так как препарат разрешен к применению у детей с 3 лет, особое внимание уделяется маленьким пациентам: значительное количество научно-исследовательских работ компании «Ниармедик» посвящено изучению различных аспектов безопасности препарата на неполовозрелых животных. Вопрос репродуктивной безопасности любого лекарственного средства является важнейшим и масштабным, так как определяет развитие страны на десятилетия вперед.
Действующее вещество противовирусного препарата «Кагоцел» является продуктом химического синтеза, в котором к полимерной полисахаридной матрице (карбоксиметилцеллюлозе) ковалентно присоединены молекулы госсипола (природного полифенольного пигмента хлопчатника). В многочисленных исследованиях, проводимых в ведущих исследовательских лабораториях в различных странах мира, доказано, что в результате прочной химической связи госсипола с различными веществами по его альдегидным группам он утрачивает свои токсические свойства, но при этом сохраняется его противовирусная и иммуномодулирующая активность.
Именно этот метод был использован при разработке препарата «Кагоцел». Ковалентное связывание молекулы госсипола с полимерным носителем – карбоксиметилцеллюлозой – позволило создать эффективный и безопасный лекарственный препарат. В разработанной технологии синтеза за счет использования избытка окисленной карбоксиметилцеллюлозы и проведения многократных стадий очистки продукта обеспечивается максимально полное удаление остаточных примесей свободного госсипола в препарате.
Сейчас в мировой практике фармацевтического производства для контроля конкретной примеси рекомендуется метод высокоэффективной жидкостной хроматографии (ВЭЖХ), который позволяет проводить одновременное разделение сложных проб на составляющие их компоненты и измерение концентрации одного или нескольких соединений.
Для контроля примесей свободного госсипола в лекарственном препарате «Кагоцел» компания «Ниармедик» совместно с МГУ имени
М. В. Ломоносова разработала и валидировала собственную высокочувствительную методику ВЭЖХ, которая отвечает современным требованиям и обладает высокой чувствительностью. С помощью данного метода подтверждено, что содержание остаточных примесей свободного госсипола в препарате после изготовления, а также после хранения в течение установленного срока годности находится на уровне от 0, 0002 до 0,0030% от массы субстанции. Для сравнения: основные мировые фармакопеи установили максимальный порог, при котором необходимо строго контролировать содержание примесей в веществе при производстве лекарственных средств – 0,05%. Соответственно, такой низкий уровень содержания примесей госсипола гарантирует отсутствие неблагоприятных воздействий препарата «Кагоцел» на организм человека.
Научное подразделение компании «Ниармедик» совместно со специалистами ФИЦ Биотехнологии РАН провели исследование на предмет исключения высвобождения свободного госсипола из препарата «Кагоцел» в среде, которая имитирует физико-химические условия пищеварительного тракта. В ходе проведенных работ доказано, что содержание микропримесей свободного госсипола в среде после 24-часового инкубирования в известных стандартных имитаторах желудочного и кишечного соков не увеличивается. Более того, количество примесей госсипола уменьшается, что говорит об их деградации. Важно, что при применении препарата по инструкции поступление в организм госсипола в виде содержащихся в препарате остаточных примесей не превысит 0,0007 мг в сутки. А это практически в 10 000 раз ниже допустимой суточной дозы госсипола, поступающего с некоторыми продуктами питания (согласно постановлениям Европейской комиссии по безопасности питания для взрослого человека негативные эффекты в отношении репродуктивной сферы способны вызвать дозы, превышающие 7–8 мг в сутки).
Для очередного подтверждения этих выводов о безопасности препарата в отношении репродуктивной функции в случае его применения у детей были проведены эксперименты на животных с использованием как терапевтических доз, так и многократно их превышающих. Все дополнительные научно-исследовательские работы были проведены в ведущих научно-исследовательских учреждениях нашей страны под руководством специалистов высокой квалификации в области оценки репродуктивной функции.
В ходе экспериментов были разработаны уникальные дизайны исследований, призванные еще раз убедительно показать полную безопасность препарата для репродуктивной системы организма, в том числе для развития потомства.
В рамках исследования на тему «Экспериментальная оценка влияния препарата «Кагоцел» на генеративную функцию крыс-самцов пубертатного возраста» было доказано отсутствие токсического действия противовирусного препарата «Кагоцел» на репродуктивную систему неполовозрелых крыс-самцов ювенильного возраста. Препарат «Кагоцел» вводился в терапевтической дозе и в дозе, в 10 раз ее превышающей, ежедневно в течение 48 дней (период сперматогенеза у крыс), что не привело к статистически значимому снижению способности животных к оплодотворению и зачатию. Морфологический анализ половых желез крыс-самцов установил, что в семенниках крыс всех групп отмечалось наличие активного процесса созревания мужских половых клеток. Полученные данные подтвердили, что препарат не вызывает в мужских половых клетках генетических нарушений.
Аналогичное исследование проведено также на крысятах самого маленького возраста. «Кагоцел» в течение 12 дней вводили в инфантильном периоде развития (начиная с 10-дневного возраста, что соответствует возрасту 1–2 года у человека) в терапевтической дозе и в дозе, в 10 раз превышающей. Введение препарата в таких дозах не привело к нарушению репродуктивной функции по достижении половой зрелости: индексы фертильности (способность к оплодотворению и зачатию) крыс-самок и крыс-самцов в экспериментальных группах находились на уровне групп контроля, морфологических патологических изменений не обнаружено. Число новорожденных, один из родителей которых получал «Кагоцел», соответствует группам контроля.
Противовирусный препарат «Кагоцел» рекомендуется не только для лечения, но и для профилактики ОРВИ и гриппа, поэтому был разработан специальный дизайн эксперимента на животных, моделирующий длительный профилактический прием, например, для категории часто болеющих детей, начиная с раннего детского возраста и до периода полового созревания. В ходе эксперимента «Кагоцел» вводили неполовозрелым животным (в том числе в дозе, в 10 раз превышающей норму по инструкции) короткими курсами в течение всего периода полового созревания – это можно считать экспериментальной моделью применения препарата «Кагоцел» у детей раннего детского возраста (2–3 года) и до периода полового созревания. Способность животных к зачатию не изменилась. Применение «Кагоцела» такими повторными курсами не приводит к нарушению морфологического состояния половых желез и не оказывает токсического действия на потомство.
В заключение отметим, что противовирусный препарат «Кагоцел» обладает широким профилем репродуктивной безопасности и может быть использован в педиатрической практике для детей раннего возраста, что было в очередной раз подтверждено циклом пострегистрационных экспериментальных работ.
По материалам “Коммерсант. Наука”