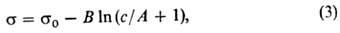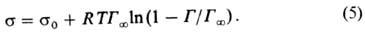ПОВЕРХНОСТНАЯ АКТИВНОСТЬ
, способность в-ва при адсорбции на границе раздела фаз понижать поверхностное натяжение (межфазное натяжение). Адсорбция Гв-ва и вызванное ею понижение поверхностного натяжения s связаны с концентрацией св-ва в фазе, из к-рой в-во адсорбируется на межфазную пов-сть, ур-нием Гиббса (1876):

где R- газовая постоянная, Т-абс. т-ра (см. Адсорбция). Производная 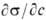
Смотреть что такое «ПОВЕРХНОСТНАЯ АКТИВНОСТЬ» в других словарях:
поверхностная активность — Способность вещ ва понижать поверхностное натяжение на границе фаз в результате адсорбции. [http://metaltrade.ru/abc/a.htm] Тематики металлургия в целом EN surface activity … Справочник технического переводчика
поверхностная активность — – способность веществ вследствие своего строения адсорбироваться на поверхности раздела фаз и снижать межфазное поверхностное натяжение. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
поверхностная активность — paviršinis aktyvumas statusas T sritis Standartizacija ir metrologija apibrėžtis Medžiagos gebėjimas dėl įgerties sumažinti fazės paviršinę energiją. atitikmenys: angl. surface activity vok. Grenzflächenakitvität, f; Oberflächenakitvität, f rus.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
поверхностная активность — paviršinis aktyvumas statusas T sritis chemija apibrėžtis Medžiagos gebėjimas dėl adsorbcijos sumažinti fazės paviršinę energiją. atitikmenys: angl. surface activity rus. поверхностная активность … Chemijos terminų aiškinamasis žodynas
поверхностная активность — paviršinis aktyvumas statusas T sritis fizika atitikmenys: angl. surface activity vok. Oberflächenaktivität, f rus. поверхностная активность, f pranc. activité superficielle, f … Fizikos terminų žodynas
поверхностная активность — [surface activity] способность вещества понижать поверхностное натяжение на границе фаз в результате адсорбции. Смотри также: Активность флотационная активность реагента … Энциклопедический словарь по металлургии
поверхностная активность радионуклида в источнике ; AS — 3.4 поверхностная активность радионуклида в источнике ; AS : Отношение активности радионуклида А в плоском источнике к площади источника S Источник … Словарь-справочник терминов нормативно-технической документации
Активность радиоактивного источника — У этого термина существуют и другие значения, см. Активность. Активность радиоактивного источника ожидаемое число элементарных радиоактивных распадов в единицу времени. Содержание 1 Производные величины 2 … Википедия
активность порошков — [powder activity] способность порошков к уменьшению свободной поверхности под действием приложенного внешнего давления и температуры; характеризуется скоростями уплотнения и усадки при спекании. Смотри также: Активность флотационная активность… … Энциклопедический словарь по металлургии
главная > справочник > химическая энциклопедия:
Поверхностная активность
Поверхностная активность, способность вещества при адсорбции на границе раздела фаз понижать поверхностное натяжение (межфазное натяжение). Адсорбция Г в-ва и вызванное ею понижение поверхностного натяжения s связаны с концентрацией с в-ва в фазе, из которой вещество адсорбируется на межфазную поверхность, уравнением Гиббса (1876):
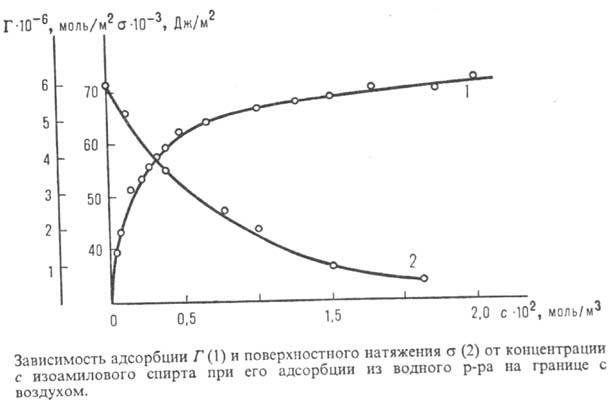
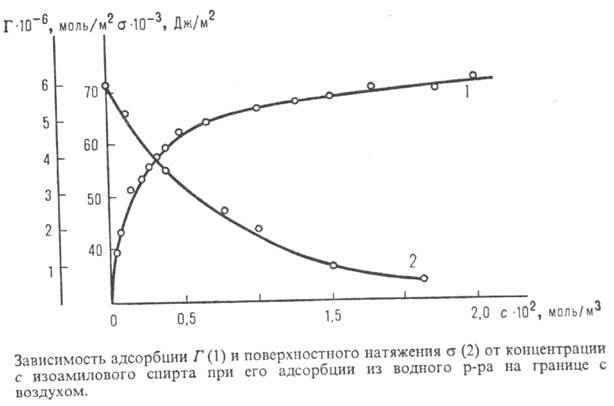
Поверхностную активность определяют с помощью изотерм адсорбции, на которых можно выделить линейный участок роста Г с увеличением с и предельное значение 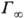

В случае адсорбции вещества из раствора поверхностная активность определяется на основании эмпирич. уравнения Шишковского (1908):
Уравнение Шишковского позволяет определять поверхностную активность данного вещества более строго, чем уравнение Ленгмюра, из-за отсутствия концентрационных ограничений. Третьим уравнением, используемым для определения поверхностной активности, является уравнение изотермы адсорбции Фрумкина (1949):
При прочих равных условиях (температура, состав раствора) поверхностная активность вещества зависит в первую очередь от состава и строения молекул.
Осн. параметры адсорбц. слоя ПАВ, помимо уже упоминавшейся поверхностной активности 
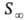
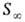
где d- плотность вещества в адсорбц. слое, равная его плотности в чистом состоянии. Из (6) и (7) следует:
Для растворов ПАВ в неполярных растворителях на границе с воздухом, в отличие от водных растворов, с увеличением длины углеводородного радикала растворимость ПАВ возрастает. При адсорбции из углеводородного растворителя на границе с водой размер углеводородного радикала практически не влияет на поверхностную активность. Например, для жирных кислот работа адсорбции определяется переносом главным образом группы COOH из объема неполярной среды на границу раздела фаз. Аналогично протекает адсорбция жирных кислот из неполярных растворителей на твердых полярных адсорбентах, например силикагеле. С увеличением мол. массы кислоты адсорбция даже уменьшается, т. к. высшие жирные кислоты лучше растворимы в неполярной среде, чем в воде. Адсорбция ПАВ из воды на неполярных адсорбентах подчиняется правилу Дюкло-Траубе. Отсюда следует, что чем меньше растворимость вещества в к.-л. среде, тем больше его поверхностная активность на границе с этой средой. Так, поверхностная активность анилина на границе вода-толуол, вычисленная с водной стороны: G H2O = = 

С повышением температуры поверхностная активность любых веществ уменьшается вследствие десорбции.
Лит.: Абрамзон А. А., Поверхностно-активные вещества. Свойства и применение, 2 изд., Л., 1981; Успехи коллоидной химии, под ред. П.А. Ребиндера и Г. И. Фукса, M., 1973; то же, под ред. Ф. Д. Овчаренко, К., 1983; то же, под ред. И. В. Петрянова-Соколова и К. С. Ахмедова, Ташкент, 1987. © В. П. Тихонов.
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ, способность в-ва при адсорбции на границе раздела фаз понижать поверхностное натяжение (межфазное натяжение). Адсорбция Г в-ва и вызванное ею понижение поверхностного натяжения s связаны с концентрацией с в-ва в фазе, из к-рой в-во адсорбируется на межфазную пов-сть, ур-нием Гиббса (1876):

где R-газовая постоянная, Т-абс. т-ра (см. Адсорбция). Производная 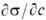
П оверхностную активность определяют с помощью изотерм адсорбции, на к-рых можно выделить линейный участок роста Г с увеличением с и предельное значение 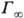
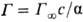
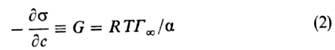
В случае адсорбции в-ва из р-ра поверхностная активность определяется на основании эмпирич. ур-ния Шишковского (1908):
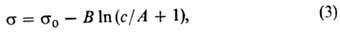

Ур-ние Шишковского позволяет определять поверхностную активность данного в-ва более строго, чем ур-ние Ленгмюра, из-за отсутствия концентрац. ограничений. Третьим ур-нием, используемым для определения поверхностной активности, является ур-ние изотермы адсорбции Фрумкина (1949):
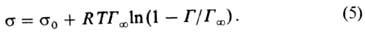
При прочих равных условиях (т-ра, состав р-ра) поверхностная активность в-ва зависит в первую очередь от состава и строения молекул.


где d- плотность в-ва в адсорбц. слое, равная его плотности в чистом состоянии. Из (6) и (7) следует:
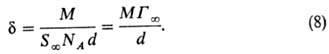
Для р-ров ПАВ в неполярных р-рителях на границе с воздухом, в отличие от водных р-ров, с увеличением длины углеводородного радикала р-римость ПАВ возрастает. При адсорбции из углеводородного р-рителя на границе с водой размер углеводородного радикала практически не влияет на поверхностную активность. Напр., для жирных к-т работа адсорбции определяется переносом гл. обр. группы COOH из объема неполярной среды на границу раздела фаз. Аналогично протекает адсорбция жирных к-т из неполярных р-рителей на твердых полярных адсорбентах, напр. силикагеле. С увеличением мол. массы к-ты адсорбция даже уменьшается, т. к. высшие жирные к-ты лучше растворимы в неполярной среде, чем в воде. Адсорбция ПАВ из воды на неполярных адсорбентах подчиняется правилу Дюкло-Траубе. Отсюда следует, что чем меньше р-римость в-ва в к.-л. среде, тем больше его поверхностная активность на границе с этой средой. Так, поверхностная активность анилина на границе вода-толуол, вычисленная с водной стороны: G H2O = = 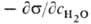
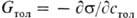
С повышением т-ры поверхностная активность любых в-в уменьшается вследствие десорбции.
Лит.: Абрамзон А. А., Поверхностно-активные вещества. Свойства и применение, 2 изд., Л., 1981; Успехи коллоидной химии, под ред. П. А. Ребиндера и Г. И. Фукса, M., 1973; то же, под ред. Ф. Д. Овчаренко, К., 1983; то же, под ред. И. В. Петрянова-Соколова и К. С. Ахмедова, Ташкент, 1987. В. П. Тихонов.
Поверхностно-активные вещества
Однако, ПАВ имеет предел растворимости (так называемую критическую концентрацию мицеллообразования или ККМ), с достижением которого при добавлении ПАВ в раствор концентрация на границе раздела фаз остается постоянной, но в то же время происходит самоорганизация молекул ПАВ в объёмном растворе (мицеллообразование или агрегация).
В результате такой агрегации образуются так называемые мицеллы.
Отличительным признаком мицеллообразования служит помутнение раствора ПАВ.
Водные растворы ПАВ, при мицеллообразовании также приобретают голубоватый оттенок (студенистый оттенок) за счёт преломления света мицеллами.
Теоретически любое химическое соединение, имеющее в молекуле гидрофильные и гидрофобные участки, будет поверхностно активным.
Однако в действительности только некоторые из них являются эффективными моющими средствами, стабилизаторамиэмульсий и пен, пленкообразователями и т. д.
По своему применению ПАВ данного класса делятся на смачиватели, солюбилизаторы, эмульгаторы, моющие агенты, пенообразователи.
Упрощенно действие поверхностно активных веществ можно описать следующим образом.
Благодаря тому, что ПАВ обладают поверхностной активностью, они снижают поверхностное натяжение воды, поэтому загрязнение лучше отстает от поверхности (кожи, волос).
Что и обеспечивает перевод загрязнений в раствор, т. е. отмывку загрязнений.
Происходит это благодаря тому, что молекула ПАВ имеете двойственную структуру один ее конец гидрофильный (т.е. любит воду) другой липофильный (т.е. любит жир).
Анионные ПАВ, отвечают за моющую способность любого щелочного мыла (детского, ручной работы, банного, туалетного и т.п.), а также большинства шампуней и жидких мыл.
В моющих средствах жирорастворимая часть молекулы анионного ПАВ связывает и обволакивает частицы грязи в секрете сальных желез, которые затем вымываются водой.
Одновременно водорастворимая часть молекулы ориентирует эти частицы в сторону от кожи, несущей отрицательный заряд.
При этом жирные загрязнения попадают внутрь молекулы ПАВ, благодаря чему не оседают на поверхности снова.
А уходят вместе с водой, удерживаясь в ней благодаря гидрофильной части.
Тем не менее, в мире потребляется ежегодно 9 млн. т мыла.
Таким образом, мыло остается наиболее распространенным в мире ПАВ.
Что такое поверхностная активность
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ, способность вещества при адсорбции на границе раздела фаз понижать поверхностное натяжение (межфазное натяжение). Адсорбция Г вещества и вызванное ею понижение поверхностного натяжения s связаны с концентрацией с вещества в фазе, из которой вещество адсорбируется на межфазную поверхность, уравением Гиббса (1876):

где R-газовая постоянная, Т-абс. температура (см. Адсорбция). Производная 
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. определяют с помощью изотерм адсорбции, на которых можно выделить линейный участок роста Г с увеличением с и предельное значение 


В случае адсорбции вещества из раствора ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. определяется на основании эмпирическая уравения Шишковского (1908):


Уравнение Шишковского позволяет определять ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. данного вещества более строго, чем уравение Ленгмюра, из-за отсутствия концентрац. ограничений. Третьим уравением, используемым для определения ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а., является уравение изотермы адсорбции Фрумкина (1949):

При прочих равных условиях (температура, состав раствора) ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. вещества зависит в первую очередь от состава и строения молекул.



где d- плотность вещества в адсорбционного слое, равная его плотности в чистом состоянии. Из (6) и (7) следует:

Для растворов ПАВ в неполярных растворителях на границе с воздухом, в отличие от водных растворов, с увеличением длины углеводородного радикала растворимость ПАВ возрастает. При адсорбции из углеводородного растворителя на границе с водой размер углеводородного радикала практически не влияет на ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. Например, для жирных кислот работа адсорбции определяется переносом главным образом группы COOH из объема неполярной среды на границу раздела фаз. Аналогично протекает адсорбция жирных кислот из неполярных растворителей на твердых полярных адсорбентах, например силикагеле. С увеличением молекулярной массы кислоты адсорбция даже уменьшается, т. к. высшие жирные кислоты лучше растворимы в неполярной среде, чем в воде. Адсорбция ПАВ из воды на неполярных адсорбентах подчиняется правилу Дюкло-Траубе. Отсюда следует, что чем меньше растворимость вещества в к.-л. среде, тем больше его ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. на границе с этой средой. Так, ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. анилина на границе вода-толуол, вычисленная с водной стороны: G H2O = = 

С повышением температуры ПОВЕРХНОСТНАЯ АКТИВНОСТЬ а. любых веществ уменьшается вследствие десорбции.
Литература: Абрамзон А. А., Поверхностно-активные вещества. Свойства и применение, 2 изд., Л., 1981; Успехи коллоидной химии, под ред. ПОВЕРХНОСТНАЯ АКТИВНОСТЬ А. Ребиндера и Г. И. Фукса, M., 1973; то же, под ред. Ф. Д. Овчаренко, К., 1983; то же, под ред. И. В. Петрянова-Соколова и К. С. Ахмедова, Ташкент, 1987. В. ПОВЕРХНОСТНАЯ АКТИВНОСТЬ Тихонов.
Химическая энциклопедия. Том 3 >> К списку статей