Преаналитический этап лабораторных исследований и его влияние на результаты анализов.
Опубликовано 23 ноября 2015 пользователем roman.l
Это этап, предшествующий непосредственному выполнению лабораторного исследования пробы пациента, который включает в себя:
Согласно данным статистики по разным источникам, до 70% процентов ошибок в результатах лабораторных исследованийявляются следствием нарушений правил работы именно на преаналитическом этапе. Современное оборудование, используемое в лабораториях, полностью автоматизировано, что исключает влияние человеческого фактора на процесс выполнения исследований. В связи с этим на аналитический этап лабораторных исследований (непосредственно исследование биоматериала в лаборатории) приходится лишь малая доля ошибок в исследованиях.
Так как цель каждого пациента, заказывающего лабораторные исследования – получить точные результаты этих исследований от лаборатории, и, соответственно, правильный диагноз от врача, то в работе лаборатории необходимо обратить особое внимание именно на преаналитический этап исследований.
Перед тем как идти в лабораторию, обязательно обратитесь к ееконсультантам и уточните, какой подготовки требует те анализы, которые Вам необходимы. Тщательно соблюдайте все рекомендации, которые получите у консультантов, и не забывайте, что на этом этапе качество проводимых исследованийнаходится непосредственно в Ваших руках.
Забор материала должен производиться специально обученной процедурной медсестрой с соблюдением всех правил и норм, предъявляемых современными стандартами. Взятый на исследование биоматериал должен быть правильно промаркирован и в кратчайшие сроки доставлен в лабораторию, при этом должны соблюдаться все необходимые правила хранения и транспортировки (такие как температурный режим, влажность и т.д.).
Сроки транспортировки биоматериала– это очень важный критерий при выборе лаборатории. Ведь, как известно, некоторые исследования очень «капризны», и сроки стабильности определяемых в биоматериале показателей невелики. Например, при исследовании свертывающей системы крови, некоторых электролитов (K, Na, Cl), а также некоторых гормонов, биоматериал должен быть доставлен в лабораторию, и его исследование должно быть выполнено в кратчайшие сроки с момента забора, иначе диагностическая точность полученных результатов сводится к нулю.
Только в сети КДЛ «ОЛИМП» лаборатории расположены вгородах республиканского значения (Астана и Алматы), а также вкаждом областном центре, что позволяет обеспечить транспортировку биоматериала из процедурного кабинета в лабораторию вкратчайшие сроки, и тем самым обеспечитьмаксимальную точность результата исследования. Кроме этого, в наших лабораториях вероятность ошибки на преаналитическом этапе сводится к минимуму, благодаря работе тщательно обученного персонала,применению современныходноразовых систем забора крови и других биоматериалов,штрих-кодированию проб сразу по месту забора, а также выполнениювсех современных требований к забору на основе международных принятых стандартов и рекомендаций.
Перед тем как заказать у нас исследования,Вы можете позвонить в наш контакт-центр по номеру 59-79-69 ( для г. Астана и регионов) или 259-79-69(для г. Алматы) и получить консультацию по всем интересующим Вас вопросам. Вы получите информацию о том, как необходимо подготовиться к сдаче каждого анализа, а также сведения о ближайших процедурных кабинетах и времени их работы.
Также Вы всегда можете зайти на наш сайт kdlolymp.kz и ознакомиться с режимом работы процедурных кабинетов в разделе «Где сдать?»
О том, как правильно подготовиться к сдаче анализов читайте здесь.
Кроме того, рекомендуем Вам ознакомиться с видеоинструкциями от нашей лаборатории по подготовке к сдаче анализов:
Как подготовиться к анализам крови:
Как подготовиться к анализам мочи:
Что такое преаналитический этап лабораторной диагностики
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Технологии лабораторные клинические
ОБЕСПЕЧЕНИЕ КАЧЕСТВА КЛИНИЧЕСКИХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ
Правила ведения преаналитического этапа
Clinical laboratory technologies. Quality assurance of clinical laboratory tests. Part 4. Rules for conducting of preanalytical stage
Дата введения 2010-01-01
Сведения о стандарте
1 РАЗРАБОТАН Лабораторией проблем клинико-лабораторной диагностики Московской медицинской академии им. И.М.Сеченова Росздрава, кафедрой биохимии Российской медицинской академии последипломного образования Росздрава
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 466 «Медицинские технологии»
1 Область применения
Настоящий стандарт устанавливает требования к условиям и процедурам ведения преаналитического этапа клинических лабораторных исследований с целью исключения или ограничения влияния эндогенных, экзогенных, ятрогенных и иных факторов, мешающих правильному отражению состояния внутренней среды обследуемых пациентов в результатах клинических лабораторных исследований.
Настоящий стандарт может использоваться всеми организациями, учреждениями и предприятиями, а также индивидуальными предпринимателями, деятельность которых связана с оказанием медицинской помощи.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие национальные стандарты:
ГОСТ Р ИСО 15189-2006 Лаборатории медицинские. Специальные требования к качеству и компетентности
ГОСТ Р ИСО 15190-2007* Лаборатории медицинские. Требования к безопасности
3 Правила ведения преаналитического этапа клинических лабораторных исследований
3.1 Общие положения
Достоверность отражения в результатах лабораторных исследований состояния внутренней среды пациента, содержания искомых компонентов биологических материалов в значительной степени зависит от условий, в которых пациент находился в период, предшествовавший взятию у него образца биоматериала, от условий и процедур взятия образца, его первичной обработки и транспортирования в лабораторию, то есть от факторов преаналитического этапа клинического лабораторного исследования.
С целью исключения или ограничения влияния внелабораторных факторов преаналитического этапа на результаты лабораторных исследований настоящий стандарт регламентирует:
а) условия периода, предшествующего взятию у пациента образца биологического материала (приложение А);
б) условия и процедуры взятия образца биологического материала у пациента;
в) процедуры первичной обработки образца биологического материала;
г) условия хранения и транспортирования образцов биоматериалов в клинико-диагностические лаборатории.
Требования стандарта основаны на:
а) научных данных о постоянных и переменных факторах физического, химического и биологического характера, способных оказать влияние на содержание веществ и клеток в биологических материалах пациентов;
б) обобщенных данных о стабильности компонентов в образцах биологических материалов после их взятия при различных условиях хранения (приложения Б, В, Г);
в) обобщенных данных о влиянии принимаемых пациентом лекарственных средств на результаты лабораторных исследований (приложение Д);
г) требованиях ГОСТ Р ИСО 15189 (раздел 5.4).
Правила предназначены для обеспечения такого качества ведения преаналитического этапа клинических лабораторных исследований, которое необходимо для получения их результатов, достоверно отражающих состояние внутренней среды обследуемых пациентов в момент обследования, путем:
— правильной подготовки пациентов к проведению лабораторных тестов;
— информирования пациентов о требуемых ограничениях в диете, физической активности, курении, о правилах сбора биологических материалов, которые обычно собирает сам пациент (моча, кал);
— инструктирования персонала, участвующего во взятии образцов биологических материалов у пациентов, об особенностях процедур взятия различных видов этих материалов;
— рациональной организации процесса взятия образцов биоматериалов;
— полноценного обеспечения процедур взятия образцов биоматериалов необходимыми инструментами, посудой, средствами первичной обработки и транспортировки.
Принимая во внимание потенциальную биоопасность образцов биологического материала, получаемого от пациентов, персонал, выполняющий эти функции, должен быть информирован и обучен правилам безопасного взятия образцов и должен располагать средствами защиты (перчатки, устройства для безопасного сбора использованных игл и т.п.) в соответствии с требованиями ГОСТ Р ИСО 15190.
Настоящие правила содержат общие положения, которые по отношению к отдельным биологическим материалам и отдельным изучаемым в них аналитам, биологическим объектам могут требовать особых условий и процедур, что должно быть отражено в нормативных документах по технологиям оказания соответствующих простых или комплексных медицинских услуг, применительно к функциям различных категорий клинического персонала.
На основании этих общих правил в каждой медицинской организации следует разрабатывать и вводить для обязательного исполнения внутренние правила ведения преаналитического этапа применительно к каждому виду исследований, выполняемых в лаборатории, учитывающие особенности медицинского профиля и организационной формы учреждения. В случае выполнения исследований в лаборатории другого учреждения правила ведения преаналитического этапа, включая условия транспортирования образцов, применительно к этим исследованиям следует согласовывать с руководителем лаборатории, выполняющей эти исследования. Наличие и исполнение персоналом правил ведения преаналитического этапа лабораторных исследований является одним из обязательных условий при сертификации процессов выполнения исследований в клинико-диагностической лаборатории.
3.2 Требования к условиям и процедурам взятия образца биологического материала
Для исследования аналитов в цельной крови, сыворотке или плазме образец крови берут чаще всего из локтевой вены. Показания для взятия крови из пальца на клиническое исследование крови:
— при ожогах, занимающих большую площадь поверхности тела пациента;
— при наличии у пациента очень мелких вен или когда они труднодоступны;
— при выраженном ожирении пациента;
— при установленной склонности к венозному тромбозу;
При взятии образца крови из венозного или артериального катетера, через который проводилось вливание инфузионного раствора, катетер следует предварительно промыть изотоническим солевым раствором в объеме, соответствующем объему катетера, и отбросить первые 5 мл (миллилитров) взятой из катетера крови. Недостаточное промывание катетера может привести к загрязнению образца крови препаратами, вводившимися через катетер. Из катетеров, обработанных гепарином, нельзя брать образцы крови для исследований системы свертывания крови.
Для исследования ряда нестабильных гормонов (остеокальцина, кальцитонина, адренокортикотропного гормона) используют ингибитор апротинин.
Для получения из образцов крови вариантов проб для различных видов исследований рекомендуется следующая последовательность наполнения пробирок:
Во избежание ятрогенной анемизации пациентов объем забираемой для исследований крови должен быть рационально рассчитан, исходя из того, что в конечном итоге непосредственно для анализа расходуется лишь половина от первоначально взятого объема (с учетом использования сыворотки или плазмы при гематокрите 0,5).
При использовании современных анализаторов достаточны следующие объемы образцов:
— для биохимических исследований: 4-5 мл; при использовании гепаринизированной плазмы: 3-4 мл;
— для гематологических исследований: 2-3 мл крови с ЭДТА;
— для исследований свертывающей системы: 2-3 мл цитратной крови;
— для иммуноисследований, включая исследования белков и др.: 1 мл цельной крови для 3-4 иммуноанализов;
— для исследования скорости оседания эритроцитов: 2-3 мл цитратной крови;
Рационально применение пробирок для взятия крови небольшого объема (4-5 мл) при соотношении диаметра и высоты пробирки 13 на 75 мм. Использование плазмы вместо сыворотки дает увеличение на 15%-20% выхода анализируемого материала при одном и том же объеме взятой у пациента крови. Взятие венозной крови облегчается применением вакуумных пробирок. Под влиянием вакуума кровь из вены быстро поступает в пробирку, что упрощает процедуру взятия и сокращает время наложения жгута.
Что такое преаналитический этап лабораторной диагностики
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Технологии лабораторные клинические
ОБЕСПЕЧЕНИЕ КАЧЕСТВА КЛИНИЧЕСКИХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ
Правила ведения преаналитического этапа
Clinical laboratory technologies. Quality assurance of clinical laboratory tests. Part 4. Rules for conducting of preanalytical stage
Дата введения 2010-01-01
Сведения о стандарте
1 РАЗРАБОТАН Лабораторией проблем клинико-лабораторной диагностики Московской медицинской академии им. И.М.Сеченова Росздрава, кафедрой биохимии Российской медицинской академии последипломного образования Росздрава
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 466 «Медицинские технологии»
1 Область применения
Настоящий стандарт устанавливает требования к условиям и процедурам ведения преаналитического этапа клинических лабораторных исследований с целью исключения или ограничения влияния эндогенных, экзогенных, ятрогенных и иных факторов, мешающих правильному отражению состояния внутренней среды обследуемых пациентов в результатах клинических лабораторных исследований.
Настоящий стандарт может использоваться всеми организациями, учреждениями и предприятиями, а также индивидуальными предпринимателями, деятельность которых связана с оказанием медицинской помощи.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие национальные стандарты:
ГОСТ Р ИСО 15189-2006 Лаборатории медицинские. Специальные требования к качеству и компетентности
ГОСТ Р ИСО 15190-2007* Лаборатории медицинские. Требования к безопасности
3 Правила ведения преаналитического этапа клинических лабораторных исследований
3.1 Общие положения
Достоверность отражения в результатах лабораторных исследований состояния внутренней среды пациента, содержания искомых компонентов биологических материалов в значительной степени зависит от условий, в которых пациент находился в период, предшествовавший взятию у него образца биоматериала, от условий и процедур взятия образца, его первичной обработки и транспортирования в лабораторию, то есть от факторов преаналитического этапа клинического лабораторного исследования.
С целью исключения или ограничения влияния внелабораторных факторов преаналитического этапа на результаты лабораторных исследований настоящий стандарт регламентирует:
а) условия периода, предшествующего взятию у пациента образца биологического материала (приложение А);
б) условия и процедуры взятия образца биологического материала у пациента;
в) процедуры первичной обработки образца биологического материала;
г) условия хранения и транспортирования образцов биоматериалов в клинико-диагностические лаборатории.
Требования стандарта основаны на:
а) научных данных о постоянных и переменных факторах физического, химического и биологического характера, способных оказать влияние на содержание веществ и клеток в биологических материалах пациентов;
б) обобщенных данных о стабильности компонентов в образцах биологических материалов после их взятия при различных условиях хранения (приложения Б, В, Г);
в) обобщенных данных о влиянии принимаемых пациентом лекарственных средств на результаты лабораторных исследований (приложение Д);
г) требованиях ГОСТ Р ИСО 15189 (раздел 5.4).
Правила предназначены для обеспечения такого качества ведения преаналитического этапа клинических лабораторных исследований, которое необходимо для получения их результатов, достоверно отражающих состояние внутренней среды обследуемых пациентов в момент обследования, путем:
— правильной подготовки пациентов к проведению лабораторных тестов;
— информирования пациентов о требуемых ограничениях в диете, физической активности, курении, о правилах сбора биологических материалов, которые обычно собирает сам пациент (моча, кал);
— инструктирования персонала, участвующего во взятии образцов биологических материалов у пациентов, об особенностях процедур взятия различных видов этих материалов;
— рациональной организации процесса взятия образцов биоматериалов;
— полноценного обеспечения процедур взятия образцов биоматериалов необходимыми инструментами, посудой, средствами первичной обработки и транспортировки.
Принимая во внимание потенциальную биоопасность образцов биологического материала, получаемого от пациентов, персонал, выполняющий эти функции, должен быть информирован и обучен правилам безопасного взятия образцов и должен располагать средствами защиты (перчатки, устройства для безопасного сбора использованных игл и т.п.) в соответствии с требованиями ГОСТ Р ИСО 15190.
Настоящие правила содержат общие положения, которые по отношению к отдельным биологическим материалам и отдельным изучаемым в них аналитам, биологическим объектам могут требовать особых условий и процедур, что должно быть отражено в нормативных документах по технологиям оказания соответствующих простых или комплексных медицинских услуг, применительно к функциям различных категорий клинического персонала.
На основании этих общих правил в каждой медицинской организации следует разрабатывать и вводить для обязательного исполнения внутренние правила ведения преаналитического этапа применительно к каждому виду исследований, выполняемых в лаборатории, учитывающие особенности медицинского профиля и организационной формы учреждения. В случае выполнения исследований в лаборатории другого учреждения правила ведения преаналитического этапа, включая условия транспортирования образцов, применительно к этим исследованиям следует согласовывать с руководителем лаборатории, выполняющей эти исследования. Наличие и исполнение персоналом правил ведения преаналитического этапа лабораторных исследований является одним из обязательных условий при сертификации процессов выполнения исследований в клинико-диагностической лаборатории.
3.2 Требования к условиям и процедурам взятия образца биологического материала
Для исследования аналитов в цельной крови, сыворотке или плазме образец крови берут чаще всего из локтевой вены. Показания для взятия крови из пальца на клиническое исследование крови:
— при ожогах, занимающих большую площадь поверхности тела пациента;
— при наличии у пациента очень мелких вен или когда они труднодоступны;
— при выраженном ожирении пациента;
— при установленной склонности к венозному тромбозу;
При взятии образца крови из венозного или артериального катетера, через который проводилось вливание инфузионного раствора, катетер следует предварительно промыть изотоническим солевым раствором в объеме, соответствующем объему катетера, и отбросить первые 5 мл (миллилитров) взятой из катетера крови. Недостаточное промывание катетера может привести к загрязнению образца крови препаратами, вводившимися через катетер. Из катетеров, обработанных гепарином, нельзя брать образцы крови для исследований системы свертывания крови.
Для исследования ряда нестабильных гормонов (остеокальцина, кальцитонина, адренокортикотропного гормона) используют ингибитор апротинин.
Для получения из образцов крови вариантов проб для различных видов исследований рекомендуется следующая последовательность наполнения пробирок:
Во избежание ятрогенной анемизации пациентов объем забираемой для исследований крови должен быть рационально рассчитан, исходя из того, что в конечном итоге непосредственно для анализа расходуется лишь половина от первоначально взятого объема (с учетом использования сыворотки или плазмы при гематокрите 0,5).
При использовании современных анализаторов достаточны следующие объемы образцов:
— для биохимических исследований: 4-5 мл; при использовании гепаринизированной плазмы: 3-4 мл;
— для гематологических исследований: 2-3 мл крови с ЭДТА;
— для исследований свертывающей системы: 2-3 мл цитратной крови;
— для иммуноисследований, включая исследования белков и др.: 1 мл цельной крови для 3-4 иммуноанализов;
— для исследования скорости оседания эритроцитов: 2-3 мл цитратной крови;
Рационально применение пробирок для взятия крови небольшого объема (4-5 мл) при соотношении диаметра и высоты пробирки 13 на 75 мм. Использование плазмы вместо сыворотки дает увеличение на 15%-20% выхода анализируемого материала при одном и том же объеме взятой у пациента крови. Взятие венозной крови облегчается применением вакуумных пробирок. Под влиянием вакуума кровь из вены быстро поступает в пробирку, что упрощает процедуру взятия и сокращает время наложения жгута.
Преаналитический этап лабораторных исследований в практике медицинских сестер. Венозная кровь
Преаналитический этап лабораторных исследований в практике медицинских сестер. Венозная кровь
М.О. Егорова
д-р мед. наук, проф. кафедры КЛД ГОУ ВО Российский национальный исследовательский медицинский университет имени Н.И. Пирогова Минздрава России, руководитель отдела развития технологий и обучения Компании «ОМБ»,
Т.П. Сапенко
канд. мед. наук, ведущий специалист отдела развития технологий и обучения Компании «ОМБ»,
Н.В. Патругина
специалист по продукции отдела развития технологий и обучения Компании «ОМБ»
В статье подробно рассмотрены факторы преаналитического этапа, оказывающие влияние на результат лабораторного исследования проб крови, о которых необходимо знать медицинским сестрам. К ним относятся: заполнение бланка-заявки, подготовка пациента к исследованиям, время суток и положение пациента при взятии проб, условия хранения и доставки пробы в лабораторию и многое другое. Представленный материал позволит учесть факторы преаналитического этапа и подготовить стандартные операционные процедуры взятия венозной крови, что повысит качество результатов лабораторных исследований.
Клиническая лабораторная диагностика – постоянно развивающаяся область медицины, основная задача которой – получение объективных данных о состоянии здоровья пациента.
Клинические решения основаны на результатах лабораторных исследований, что определяет ответственность лаборатории в соблюдении технологии аналитического этапа. Значительную часть преаналитического этапа выполняют вне лаборатории, однако ошибки, возникающие в этот период, ведут к искажению результатов лабораторного исследования. Выбор необходимых для обследования пациента лабораторных тестов, соблюдение процедуры взятия крови, идентификации пациента и образца зависит от врача-клинициста и процедурной медицинской сестры. Стандартизация процедур преаналитического этапа – задача, решаемая совместно врачом-клиницистом, медицинской сестрой процедурного кабинета, лабораторией и поставщиком медицинской продукции для обеспечения преаналитического и аналитического этапов лабораторного исследования.
На преаналитический этап приходится не менее 50% общего числа лабораторных ошибок [2], которые могут привести к неправильной постановке диагноза и последующему назначению неадекватной терапии. Ценой такой ошибки может стать жизнь пациента.
Одной из основных задач преаналитического этапа является адекватный отбор проб крови и обеспечение стабильности (сохранности) образца.
Практика показывает, что именно стандартизация преаналитического этапа позволяет сократить ошибки диагностики. Важным условием стандартизации преаналитического этапа служит не только соблюдение протокола, но и использование сертифицированных и одноразовых расходных материалов для взятия крови.
Правила заполнения бланка направления
Первый шаг при инициации лабораторного обследования пациента – формирование направления. Бланк-направление в лабораторию для проведения исследований должен содержать информацию о пациенте (Ф. И. О., пол, возраст, домашний адрес, номер страхового полиса), об источнике получения крови (тип образца: венозная, артериальная, капиллярная). Необходимо также указать дату и время взятия крови и, конечно, перечень необходимых исследований.
Источник получения крови (как и возраст) определяет соответствующие референтные значения. Например, существуют различия между концентрацией глюкозы капиллярной и венозной крови. Капиллярная кровь – среда, содержащая интерстициальную жидкость и артериальную кровь, поэтому концентрация глюкозы в капиллярной крови (в среднем 5,4 ммоль/л) выше, чем в венозной (в среднем 4,1 ммоль/л).
Маркировка времени взятия крови на бланке позволяет оценить сохранность компонентов пробы крови до исследования. Наряду с традиционным периодом доставки крови, в течение часа после получения пробы, есть ряд исследований, которые необходимо выполнить в течение 10 мин после взятия крови. Для подобных исследований бланк-направление в лабораторию может иметь специальную пометку и указание способа доставки (вакуумная почта, например) и условий сохранности содержимого пробы. Например, пробы для исследования гемостаза, наиболее чувствительные к условиям хранения,
должна доставлять в лабораторию медицинская сестра клинического отделения. Дополнительно можно предусмотреть предварительное центрифугирование пробы (в случае использования пробирок с разделительным гелем). Это обеспечит последующую сохранность содержимого сыворотки или плазмы до 48 ч при необходимости длительной транспортировки.
Последний момент – перечень необходимых исследований.
Врач, направивший больного на обследование с рукописным бланком, может упустить необходимые и желаемые исследования. Использование лабораторной информационной системы упрощает заполнение бланка, позволяя сделать выбор из списка. Кроме того, по результатам считывания штрихкода в направлении можно получить всю информацию, заключенную в бланке, как о пациенте, так и о направившем его враче.
Факторы, влияющие на результат анализа
В утреннее и вечернее время содержание многих компонентов крови отличается. Суточные биоритмы определяют концентрацию и активность биологических процессов и, например, максимальную экскрецию с мочой фосфатов, катехоламинов, кортизола, альдостерона отмечают в вечерние часы, а натрия – в утренние. Содержание в сыворотке крови гормонов АКТГ, кортизола, адреналина, норадреналина, ренина максимально в утренние часы, тогда как тиреотропного, соматотропного гормона, железа, калия – в вечерние часы [7].
Взятие крови для исследования в утренние часы в одно и тоже время важно и с точки зрения последующего сравнения результатов исследования в динамике. Оценить, что послужило причиной изменения содержания компонента в крови – суточные колебания или влияние терапии, – сложно, если нет развернутой информации о времени исследования, условиях взятия крови, лекарственной терапии, составе пи-
тания, предшествующей физической нагрузке и других факторах. Поэтому по умолчанию кровь берут у пациента утром натощак [7], до любых физиотерапевтических процедур, рентгенодиагностики и УЗИ. Необходимо исключить прием алкоголя и курение за 24 ч до времени сдачи анализа. Курение и прием кофе влияют на результаты исследования многих компонентов (например, С-реактивный белок, билирубин и многие др.). [7, 9]
Физические нагрузки изменяют значения некоторых лабораторных показателей в крови: в первую очередь концентрацию лактата, креатинина, белков и активность ферментов.
После прекращения физической нагрузки длительно, в течение 24 ч и более, сохраняется повышенная активность креатинкиназы и ЛДГ. [9]
Лабораторное обследование выполняют, как правило, неоднократно. Врачу-клиницисту важно получить и увидеть эффект терапии в динамике. Поэтому необходимо выполнять
исследование каждый раз в одно и то же время (учитывая суточные колебания) и получать кровь пациента в одной и той же позиции (в положении лежа или сидя).
От положения тела зависит интенсивность диффузии жидкости в тканевое пространство. В положении сидя концентрация белка, кальция, гормонов, количество клеток в образце будет выше. В некоторых случаях отличия при исследовании проб одного и того же пациента, взятых при разных положениях тела, будут значительными (табл. 1)[3]. Чаще всего горизонтальное положение тела при венепункции предпочтительнее, т. к. при вертикальной позиции происходит отток жидкости из сосудов, изменяя концентрацию аналитов на 5–9% и более.[8]
Изменение некоторых биохимических аналитов при смене положения пациента: из горизонтального в вертикальное
| Параметр | Увеличение, % |
| Гемоглобин | 5 |
| Лейкоциты | 7 |
| Гематокрит | 13 |
| Эритроциты | 15 |
| Кальций | 5 |
| АСТ активность | 6 |
| Tироксин | 7 |
| IgG | 7 |
| IgA | 8 |
| IgM | 6 |
| Белок | 9 |
| Tриглицериды | 9 |
| Холестерин ЛПВП | 10 |
| Aльдостерон | 15 |
| Эпинефрин | 48 |
| Ренин | 60 |
Фактором, существенно изменяющим или затрудняющим лабораторное исследование образца, служит липемия (хилез), возникающий физиологически в течение 12 ч после приема пищи. Липемия определяется как мутность, видимая невооруженным глазом, в жидкой надосадочной части исследуемых образцов; в крови возникает мутность за счет наличия хиломикронов, носителей экзогенных (пищевых) липидов. [5]
Традиционно используемое понятие «натощак» означает, что последний прием пищи был не позднее 12 ч до времени взятия крови. Отдельные пациенты, например страдающие сахарным диабетом, не могут выдержать столь длительный перерыв в еде. Минимально короткий возможный перерыв (при приеме нежирной пищи) составляет 4 ч. В таком случае можно полагать, что хиломикроны, поступающие из кишечника в кровь, будут уже метаболизированы.
Причин изменения состава образца крови, не связанных с патологическими состояниями пациента, может быть несколько. Нарушение времени последнего приема пищи, поглаживание руки пациента, наложение жгута на период более 1 мин, длительная «работа кулаком» для пациента с фиксированной жгутом веной приводят к гемолизу и гиперкалемии.
Спектральная интерференция (влияние на получаемый результат), вызываемая липемией, в корне отличается от интерференции, возникающей при гемолизе и иктеричности.
Липемия создает помехи за счет присутствия в образце жиросодержащих компонентов, которые, рассеивая свет, образуют молочный или мутный вид образца сыворотки/плазмы крови. Степень рассеяния света зависит от количества, размера и показателя преломления взвешенных частиц (хиломикроны и липопротеиды очень низкой плотности), которые образуют мутность и создают белую окраску сыворотки, называемую хилезом или липемией (рис. 1b).
Гемолиз
Одной из проблем, препятствующей исследованию образца, является гемолиз – нарушение целостности эритроцитов и последующее увеличение во внеклеточном пространстве концентрации внутриклеточных компонентов. Внутриклеточная концентрация некоторых клеточных компонентов в 10 раз выше их внеклеточной концентрации. Гемолиз, обнаруживаемый в плазме/сыворотке крови, служит причиной увеличения концентрации таких аналитов, как калий, лактатдегидрогеназа, аспартатаминотрансфераза, магний.
Спектральная интерференция гемолиза (рис. 1c) определяется выходом внутриэритроцитарного гемоглобина в сыворотку/плазму крови. Гемоглобин отличается высоким поглощением света при характерной для него длине волны.
Отмеченное увеличение или уменьшение результатов при гемолизе зависит от метода и концентрации аналита.
Наличие гемолиза распознают по появлению различной выраженности красноватого окрашивания плазмы или сыворотки крови после центрифугирования. Основные причины гемолиза указаны в табл. 2.
Кроме хилеза и гемолиза, наиболее частую интерференцию результатов исследования может повлечь повышенный уровень билирубина в крови пациента (гипербилирубинемия), обуславливающий иктеричность сыворотки (рис. 2).
Гемолиз в пробе (за исключением исследований, не чувствительных к гемолизу) служит критерием для отказа в принятии лабораторией биоматериала на исследования (ГОСТ Р 53079.4-2008. Технологии
лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть 4. Правила ведения преаналитического этапа). [6]
Процедура взятия крови зависит не только от опыта и навыка процедурной сестры, но и от используемого расходного материала для венепункции и получения образца. Пациенты в отделении химиотерапии, пожилые больные требуют специальных приспособлений для комфортной венепункции, таких как игла-бабочка и иглы большего диаметра.
Условия, в которых будет получен адекватный результат, следует оговорить и сообщить пациенту, указав в направлении.
Так, чтобы исключить возможность ложноположительных результатов при исследовании PSA и его растворимой фракции, взятие крови следует проводить не ранее чем через 5 сут после таких манипуляций, как пальцевое ректальное исследование, массаж простаты, трансректальное ультразвуковое исследование (когда датчик вводят в прямую кишку) и после любых других механических воздействий на предстательную железу (клизма, тепловые процедуры и т. п.). Рекомендуют также избегать эякуляции за 2–3 дня до исследования, езды на велосипеде или на лошади, а также употребления алкоголя. [1]
Нельзя забывать, что принимаемые лекарства могут существенно менять состав исследуемого образца. Например, прием единичной дозы железосодержащего препарата накануне исследования может повысить концентрацию железа в исследуемой сыворотке пациента на 300–500 мкг/100 мл, и этот эффект часто маскирует дефицит железа. [4]
В таблице 3 отражены ограничения для некоторых лабораторных исследований. Каждый раз, внедряя новый лабораторный тест, лаборатория изучает инструкцию и сообщает условия взятия биоматериала врачам-клиницистам, медицинским сестрам, в направлении или памятке для пациента.
(Продолжение материала в мартовском номере издания. Следите за новостями!)
Список литературы
1. Говоров А.В. ПСА в деталях // Урология сегодня. 2011. № 6. С. 2–4.
2. Гудер В.Г., Нарайанан С., Виссер Г., Цавта Б. Проба: от пациента до лаборатории / Пер. с англ. Меньшикова В.В. Мюнхен: GIT VERLAG GmbH. 2003. 105 с.
3. Егорова М.О. Биохимическое обследование в клинической практике. М.: Практическая медицина. 2008. 144 с.
4. Тиц Н. Клиническое руководство по лабораторным тестам / Пер. с англ. под редакцией Меньшикова В.В. М.: Юнимед-пресс. 2003. 570 с.
5. Tомас Л., Гиньска E., Митчел C.A., Мэй К. Сывороточные индексы: сокращение ошибок в лабораторной медицине. Результат, которому можно доверять. ООО «РОШ Диагностика Рус». 2013. 12 с.
6. ГОСТ Р 53079.4-2008. Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть 4. Правила ведения преаналитического этапа. 2009.
7. Справочное пособие. Обеспечение качества лабораторных исследований. Преаналитический этап / Под. ред. В.В. Меньшикова. М.: ЛАБИНФОРМ, 1999. 316 с.
8. Blick K.E., Liles S.M. Principles of Clinical Chemistry. NY.: Wiley and Sons. 1985. Р. 697.
9. McCall E., Tankersley M. Phlebotomy essentials. 3-rd edition. Lippincott Williams & Wilkins. 2003. Р. 306.
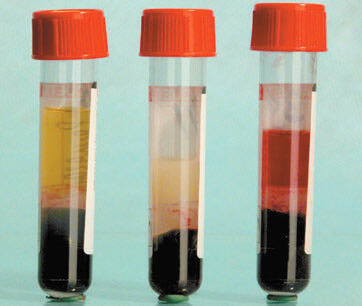
Рис. 1. Вид сыворотки крови после
центрифугирования:
а – сыворотка, пригодная для исследования;
b – образец хилезной сыворотки;
c – образец гемолизной сыворотки

Рис. 2. Вид пробы с различными компонентами
интерференции:
a – хилез;
b – лаковый гемолиз;
c – гипербилирубинемия 100 мкмоль/л;
d – билирубинемия 9 мкмоль/л;
e – билирубинемия 3 мкмоль/л
а b c а b c d e



