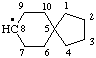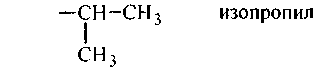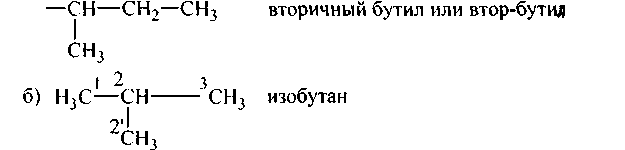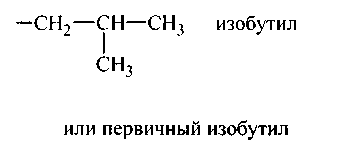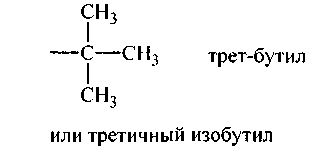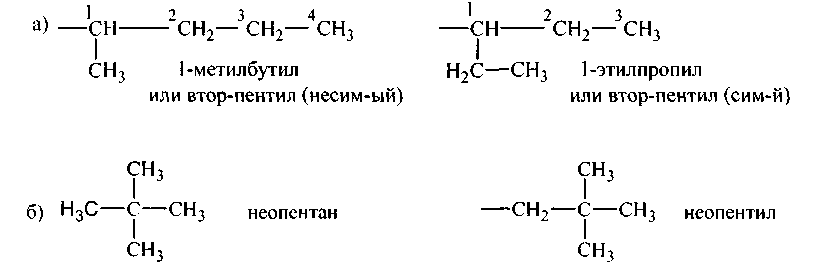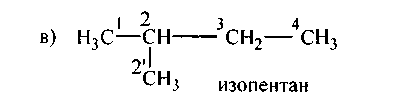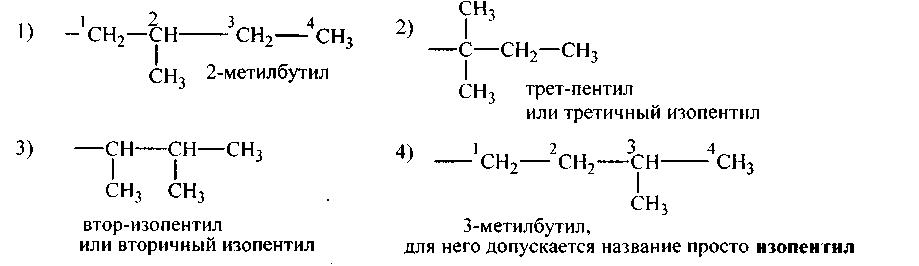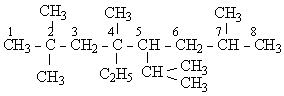Радикал (химия)
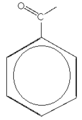
Углеводоро́дный радика́л (от лат. radix — корень; также — углеводородный остаток) в химии — группа атомов, соединённая с функциональной группой молекулы. Обычно при химических реакциях радикал переходит из одного соединения в другое без изменения. Но радикал и сам может содержать функциональные группы, поэтому с его «неизменностью» нужно быть осторожным; например, аминокислота аспарагиновая кислота содержит в той части молекулы, которая в общем виде рассматривается как остаток аминокислоты, ещё одну карбоксильную группу. Часто углеводородный радикал называют просто радикал, что может вызвать путаницу с таким понятием как свободный радикал. Некоторые углеводородные радикалы могут также являться функциональными группами, например фенил (−C6H5), винил (−C2H3) и пр. Углеводородными радикалами обычно являются остатки углеводородов, которые входят в состав многих органических соединений.
Содержание
Номенклатура
Моновалентные углеводородные радикалы
Поливалентные углеводородные радикалы
l-соглашение
Примеры
Обозначение в формулах
Если не принципиально, какой углеводородный радикал находится в молекуле, то часто его обозначают просто буквой R (например, общая формула гомологического ряда спиртов — R−OH). Иногда вместо R используют символ Org. Если соединение содержит несколько разных радикалов, их обозначают R, R’, R», R 4 и т. д.
Иногда необходимо разделить ароматические, гетероциклические и алкильные радикалы. Для этого вместо символа R используют:
В органической химии нередко применяют сокращенные обозначения:
Иногда между обозначением характера радикала (t, i и др.) и остальной частью названия ставят чёрточку: t-Bu.
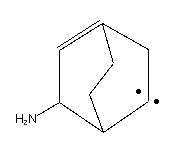
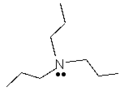
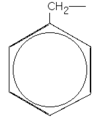
Структурные формулы некоторых примеров изображены здесь:
Применение
Тривиальные, не номенклатурные названия многих органических соединений состоят из названия углеводородного радикала и названия атомов или групп атомов, замещающих водород, например: СН3Сl — хлористый метил, C2H5Br — бромистый этил и т. д.
Первичные, вторичные, третичные и четверичные атомы углерода
Примечания
См. также
Полезное
Смотреть что такое «Радикал (химия)» в других словарях:
Химия — У этого термина существуют и другие значения, см. Химия (значения). Химия (от араб. کيمياء, произошедшего, предположительно, от египетского слова km.t (чёрный), откуда возникло также название Египта, чернозёма и свинца «черная… … Википедия
Радикал в химии — (химич. radical, radicale) слово, впервые введенное в научную химическую литературу, по видимому, Гитоном де Морво. В докладе французской Академии наук [ M émoire sur le Développement des Principes de la Nomenclature Mé thodique (18 апр. 1787).… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Радикал, в химии — (химич. radical, radicale) слово, впервые введенное в научную химическую литературу, по видимому, Гитоном де Морво. В докладе французской Академии наук [ Mémoire sur le Développement des Principes de la Nomenclature Méthodique (18 апр. 1787).… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ХИМИЯ ОРГАНИЧЕСКАЯ. НОМЕНКЛАТУРА СОЕДИНЕНИЙ — Для наименования органических соединений используется несколько систем, но ни одна из них не подходит для всех соединений. Сохранились многие тривиальные названия, которые либо применялись еще в начальный период органической химии и отражают… … Энциклопедия Кольера
ОРГАНИЧЕСНАЯ ХИМИЯ — первоначально составляла часть химии вообще и не имела особого названия; позже под О. х. стали разуметь химию веществ, встречающихся только в животном и растительном организме. Берцелиус (Berzelius) определил в 1827 г. О. х. как химию… … Большая медицинская энциклопедия
Углеводородный радикал — (от лат. radix «корень»; также углеводородный остаток) в химии группа атомов, соединённая с функциональной группой молекулы. Обычно при химических реакциях радикал переходит из одного соединения в другое без изменения. Но… … Википедия
Органическая химия — В Викисловаре есть статья «органическая химия» Органическая химия раздел химии, изучающий со … Википедия
ОРГАНИЧЕСКАЯ ХИМИЯ — наука, изучающая соединения углерода с др. элементами (органические соединения), а также законы их превращений. Назв. О. х. возникло на ранней стадии развития науки, когда предмет изучения ограничивался соед. углерода растит, и животного… … Химическая энциклопедия
Винил (радикал) — У этого термина существуют и другие значения, см. Винил (значения). Химическая структура винила Винил (от лат. vinum (vini) вино) одновалентный радикал этилена, СН=СН2. С … Википедия
Радиационная химия — область химии, охватывающая химические процессы, вызываемые действием ионизирующих излучений (См. Ионизирующие излучения) на вещество. Ионизирующей способностью обладают как электромагнитные излучения (рентгеновские лучи, γ лучи,… … Большая советская энциклопедия
Что такое радикал изобразите структурные формулы одновалентных радикалов состава
УРОК №2 ПО ТЕМЕ «НОМЕНКЛАТУРА АЛКАНОВ».
Изучив материал, нужно будет:
— Понятие – радикал, типы радикалов.
— Формулы и правила построения названий радикалов разного характера.
— Правила построения названий разветвлённых алканов.
— Называть алканы по имеющейся формуле.
— Строить формулы алканов разветвлённого строения по имеющемуся названию.
— Записывать формулы радикалов разного характера.
1.Радикал – это частица, обладающая не спаренным электроном, а, следовательно и неизрасходованной единицей валентности. На основе гомологического ряда алканов, можно построить и ряд радикалов, причем первичные радикалы отличаются от соответствующих им алканов, тем, что в их составе имеется на один атом водорода меньше. Очень важно выучить наизусть название первых 10 алканов и соответствующих им радикалов, так как названия представителей других классов органических соединений строятся на основе названий алканов.
Начиная с четвёртого представителя ряда алканов при построении названия углеводорода неразветвлённого строения перед основным названием добавляется буква – н, которая и говорит о том, что данный углеводород имеет неразветвлённое строение (например, н – бутан).
В приведенной ниже таблице даны формулы и соответствующие им названия для первых 10 представителей ряда алканов и соответствующих им радикалов.
Алкан
Чтобы построить название радикала, необходимо в название соответствующего алкана заменить суффикс – ан на суффикс – ил. Одновалентные углеводородные радикалы имеют общее название алкилы.
Однако помимо первичных радикалов очень часто в соединениях встречаются вторичные и третичные радикалы.
Первичный радикал – это радикал, содержащий первичный атом углерода, то есть такой атом углерода, который соединен в свою очередь лишь с одним другим атомом углерода (или тремя атомами водорода в случае радикала CH 3 –метил). Примерами первичных радикалов могут служить: C 2 H 5 – этил, C 3 H 7 – пропил и др.
Формулы некоторых вторичных, третичных радикалов, а также двух и трех валентных радикалов, наиболее часто употребляющихся приведены в таблице ниже.
Метилен
Изобутил (первичный изобутил)
двухвалентных радикалов (с двумя свободными валентностями у одного и того же атома углерода) производят заменой суффикса – ан на – илиден (исключение – радикал метилен CH 2 ). Трехвалентные радикалы имеют суффикс – илидин (исключение – радикал метин – СН).
Чтобы построить названия алканов разветвленного строения и их производных необходимо воспользоваться следующими правилами:
1. Выбирают главную цепь атомов углерода в веществе (самая длинная цепь) и нумеруют арабскими цифрами атомы углерода сверху с того конца, где ближе разветвление (к какому концу ближе в боковой цепи находятся радикалы).
2. Затем цифрами, их количеством, соответствующими приставками указывают все имеющиеся в веществе радикалы, их количество и местоположение.
3.Затем подсчитывают общее число атомов углерода в главной цепи и к уже имеющемуся названию дописывают название алкана, соответствующего числу атомов углерода в главной цепи.
Назвать алканы можно и по-другому, рассматривая их как производные метана, в молекуле которого один или несколько атомов водорода замещены на радикалы. А названия строят так: по старшинству называют все заместители, указывая их число, если они одинаковые, а за основу названия берётся слово «метан». Такая номенклатура называется рациональной.
Рассмотрим несколько приведённых ниже соединений и назовем их по систематической и рациональной (в скобках) номенклатурам.
Домашнее задание: осмыслить теоретический материал, составить формулы веществ по имеющимся названиям: 1,1,1 трихлорпентан, 2,2 диметил 3,3 дибром нонан, 1,1,6,6 тетрахлоргексан, н – декан, 2,3,5,триметил, 5 бром декан.
Одновалентные радикалы предельных углеводородов (алканов)
Алкилы изостроения
Равноценны между собой 1-й, 3-й и 2′ углероды, третичный углерод (2-й) с ними неравноценен.
Следовательно, возможны два алкила:
а) 1 СНз — СН2 — 3 СН2 — 4 СН2 — 5 СНз н-пентан. У пентана равноценные между собой попарно: 1-й и 5-й, 2-й и 4-й, а 3-й углерод с ними неравноценен. Возможны 3 алкила, один нормальный, два изомерного строения:
Возможен 1 алкил, ибо первичные углеродные атомы равноценны:
Равноценны между собой только 1-й и 2′. Следовательно, возможны четыре алкила:
Аналогично могут быть названы одновалентные радикалы других предельных углеводородов.
Дата добавления: 2017-05-02 ; просмотров: 6228 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Одновалентные радикалы предельных углеводородов жирного ряда
Конспект Углеводороды
Углеводороды –органические соединения, состоящие из углерода и водорода. В зависимости от строения углеродной цепи их разделяют на соединения с открытой цепью (ациклические, алифатические) и циклические.
В каждом ряду углеводороды делятся на классы. Схема классификации представлена на рис. 1.
Рис. 1. Классификация углеводородов
Каждый класс углеводородов образует гомологический ряд.
Гомологический ряд –это бесконечный ряд веществ, отличающихся друг от друга на любое число групп CH2 (гомологическая разность), имеющих сходное строение и, следовательно, сходные химические свойства.
Предельные (метановые) углеводороды (алканы, парафины)
Алканы –предельные (насыщенные) углеводороды состава CnH2n+2.
Строение
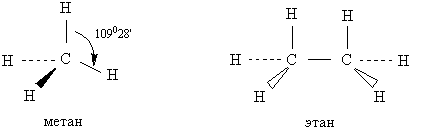
Гибридизация –это смешение валентных (внешних) орбиталей атома (в нашем случае атома углерода) и выравнивание их по формам и энергии.
Вокруг связи С-С в алканах существует свободное вращение. Число σ-связей, образованных данным атомом углерода равно числу гибридных орбиталей (в алканах – 4), которые имеют тетраэдрическую ориентацию.
Рис. 2. Тетраэдрическое строение алканов
Гомологи
Гомологи –это вещества, имеющие сходное химическое строение, сходные химические свойства, но отличаются на одну или несколько метиленовых групп (-СН2-) – гомологическую разность.
Гомологи, расположенные в порядке возрастания молярной массы, образуют гомологический ряд.
Радикал –это нейтральный атом или группа атомов, имеющих один или несколько неспаренных электронов.
Одновалентные радикалы предельных углеводородов жирного ряда
| Упрощенная структурная формула | Название |
| 1) СН3— | метил |
| 2) СН3-СН2— | этил |
3) СН3-СН2-СН2—  | пропил, н-пропил вторичный пропил, изо-пропил, i-пропил |
5) СН3-СН2-СН2-СН2— 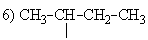 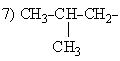 | первичный бутил, бутил, н-бутил вторичный бутил, втор-бутил первичный изобутил, изо-бутил |
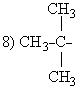 | третичный изобутил, третичный бутил, трет-бутил |
9) СН3-СН2-СН2-СН2-СН2— 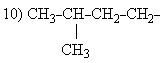 | первичный амил, амил первичный изоамил, изоамил |
Если в молекуле углеводорода атом углерода связан с одним заместителем, то его называют первичным, с двумя заместителями – вторичным, с тремя – третичным, с четырмя – четвертичным.
Номенклатура
Поэтому в настоящее время распространены две номенклатуры:
а) систематическая номенклатура, принятая международным союзом по общей и прикладной химии (ИЮПАК), которая постоянно совершенствуется;
б) рациональная номенклатура, которая пришла в помощь тривиальной номенклатуре.
Углеводородный радикал
Углеводоро́дный радика́л (от лат. radix — «корень»; также — углеводородный остаток) в химии — группа атомов, соединённая с функциональной группой молекулы. Обычно при химических реакциях радикал переходит из одного соединения в другое без изменения. Но радикал и сам может содержать функциональные группы, поэтому с его «неизменностью» нужно быть осторожным: например, аминокислота аспарагиновая кислота содержит в той части молекулы, которая в общем виде рассматривается как остаток аминокислоты, ещё одну карбоксильную группу. Часто углеводородный радикал называют просто радикал, что может вызвать путаницу с таким понятием как свободный радикал. Некоторые углеводородные радикалы могут также являться функциональными группами, например, фенил (−C6H5), винил (−C2H3) и пр. Углеводородными радикалами обычно являются остатки углеводородов, которые входят в состав многих органических соединений.
Содержание
Номенклатура
Моновалентные углеводородные радикалы
Поливалентные углеводородные радикалы
Если радикал способен присоединиться к атому углерода с образованием двойной или тройной связи или присоединиться сразу к нескольким атомам углерода (т. е., имеет несколько свободных валентностей), он называется поливалентным (в конкретном случае — би-, тривалентным, и т. д.). Названия таких радикалов строятся путём присоединения к корню названия углеводорода суффикса «-илиден» или «-илидин» соответственно. Ранее исключениями из этого правила были метилен и метин (но не теперь); впрочем, применяются и эти названия.
l-соглашение
Поливалентные углеводородные радикалы также могут быть поименованы согласно l-соглашению. В этом случае название строится по схеме: [заместитель при атоме со свободной валентностью] — [порядковый номер атома со свободной валентностью] l n — [название углеводорода, который получился бы при образовании на месте свободных валентностей связей с атомами водорода]. n здесь — количество свободных валентностей, которыми обладает атом.
Примеры
Обозначение в формулах
Если не принципиально, какой углеводородный радикал находится в молекуле, то часто его обозначают просто буквой R (например, общая формула гомологического ряда спиртов — R−OH). Иногда вместо R используют символ Org. Если соединение содержит несколько разных радикалов, их обозначают R, R’, R», R 4 и т. д.
Иногда необходимо разделить ароматические, гетероциклические и алкильные радикалы. Для этого вместо символа R используют:
В органической химии нередко применяют сокращенные обозначения:
Иногда между обозначением характера радикала (t, i и др.) и остальной частью названия ставят чёрточку: t-Bu.
Структурные формулы некоторых примеров изображены здесь: