Что такое рецептор в фармакологии
Рецепторы — макромолекулы, функция которых заключается в связывании веществ-посредников и в преобразовании этой связи в действие, т, е. изменение клеточной функции. Рецепторы отличаются по своей структуре и способу преобразования контакта с лигандом в клеточный ответ (преобразование сигнала).
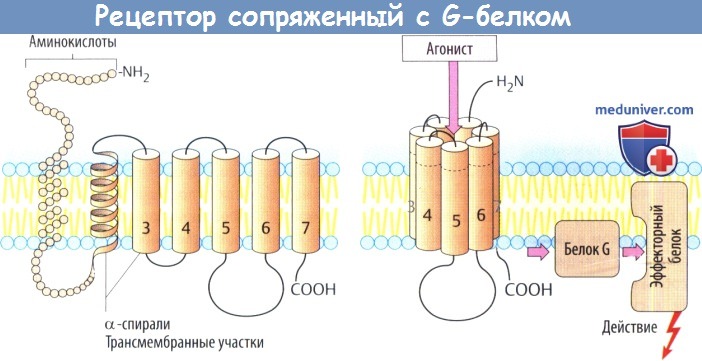
а) Рецепторы, сопряженные с белком G, состоят из цепи аминокислот, которая направлена в сторону мембраны и от нее в виде серпантина. С вне-мембранными петлевыми участками молекулы связаны углеводные остатки через различные точки N-гликозилирования.
Семь а-спиральных, охватывающих мембрану участков образуют окружность возле центральной ниши, которая несет участки для связывания медиаторных веществ. Связывание молекулы медиатора или структурно связанной молекулы агониста вызывает изменение конформации белка, в результате чего он вступает во взаимодействие с белком G (белок, связывающий нуклеотид гуанил).
Белки G располагаются в нижнем слое плазмолеммы и состоят из трех субъединиц, обозначаемых а, β и γ. Существует несколько белков G, которые отличаются в основном своей a-единицей. Контакте рецептором активирует белок G, что, в свою очередь, приводит к активации другого белка (фермента, ионного канала). Многие медиаторы действуют через рецепторы, сопряженные с белком G.
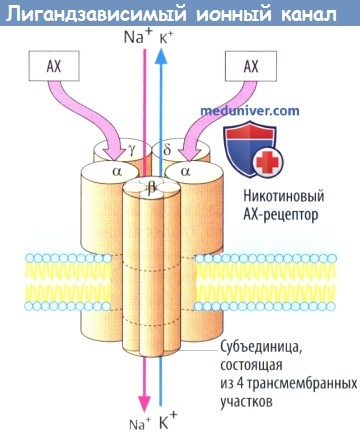
б) Примером лигандзависимого ионного канала является никотиновый холинорецептор на концевой пластинке двигательного нерва. Рецепторный комплекс образован пятью субъединицами, каждая из которых содержит четыре трансмембранных участка.
Одновременное связывание двух молекул АХ двумя а-субъединицами приводит к открытию ионного канала со входом Na + (и выходом некоторого количества К + ), деполяризации мембраны и активации потенциала действия. Нейронные N-холинорецепторы, очевидно, состоят лишь изо- и β-субъединиц.
Ряд рецепторов медиатора γ-аминомасляной кислоты (ГАМК) принадлежат к данной группе: подтип ГАМКA связан с хлорными каналами (и с участком связывания бензодиазепинов). Глутамат и глицин оба действуют через лигандзависимые ионные каналы.
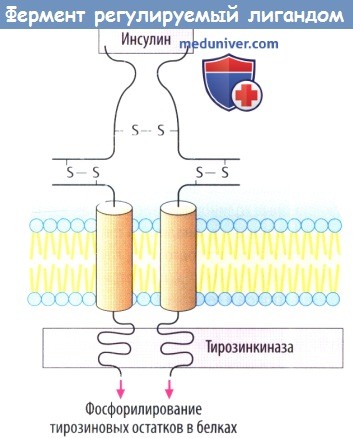
в) Белок инсулинового рецептора представляет собой управляемый лигандом фермент, каталитический рецептор. При связывании инсулина с внеклеточным участком «отключается» активность тирозинкиназы внутри клетки. Фосфорилирование белка приводит к изменению клеточной функции в результате образования других сигнальных белков. Рецепторы гормонов роста тоже принадлежат к классу каталитических рецепторов.
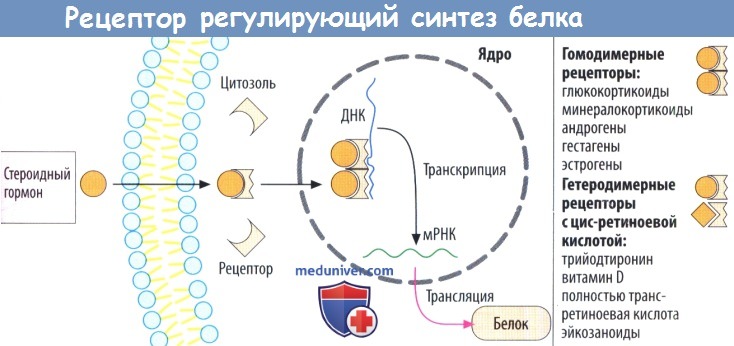
г) Рецепторы, регулирующие синтез белка, стероидов и гормонов щитовидной железы, находятся в цитозоле и в клеточном ядре соответственно. Белки рецепторов также расположены внутриклеточно, в зависимости от гормона — в цитозоле (глюкокортикоиды, минералокортикоиды, андрогены и гестагены) или в клеточном ядре (эстрогены, гормоны щитовидной железы).
При связывании гормона открывается скрытый в норме участок белка рецептора, что дает возможность последнему связаться с особой последовательностью нуклеотидов ДНК в гене и регулировать его транскрипцию. Из этого следует, что комплексы лиганд-рецептор работают как факторы, регулирующие транскрипцию. Обычно происходит активация или усиление и, редко, блокада транскрипции.
Комплексы гормон-рецептор взаимодействуют парно с ДНК. Эти пары (димеры) могут состоять из двух идентичных комплексов гормон-рецептор (гомодимерная форма, например, с гормонами надпочечников или половыми гормонами). Комплекс тиреоидный гормон-рецептор встречается в гетеродимерной форме и сочетается с комплексом цис-ретиноевая кислота-рецептор.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Виды фармакологического действия ЛС (часть 2)
Избирательное (селективное) действие лекарственных веществ обусловлено их сродством (аффинитетом) к отдельным подтипам рецепторов или селективным изменением транспорта ионов (Na+, K+, Ca2+, Cl-) в определенном органе, что зависит от химической структуры биологически активного вещества, наличием в его структуре определенных функциональных групп.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармфакультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Например, сердечные гликозиды избирательно влияют на сердечную мышцу; Окситоцин – на гладкую мускулатуру матки; Сальбутамол (Вентолин) избирательно стимулирует b2-адренорецепторы бронхов и матки; Метопролол (Беталок ЗОК) селективно блокирует b1-адренорецепторы сердца. Антидиарейное средство Лоперамид (Имодиум) – селективный агонист опиоидных рецепторов кишечника. Он на длительный период замедляет перистальтику ЖКТ, устраняет понос и нормализует нормальный стул пациента. Препарат не оказывает влияния на подтипы опиоидных рецепторов ЦНС, поэтому при повторном применении не вызывает привыкания и лекарственной зависимости.
Неизбирательным (неселективным) действием обладают ЛС, воздействующие на многие рецепторы одновременно. Например, такое действие оказывает гормон мозгового слоя надпочечников – адреналин, как ЛС является адреномиметиком, связывается с α, β-адренергическими рецепторами. Антихолинергические средства (атропин, платифиллин) блокируют неизбирательно все мускариночувствительные М1, М2, М3-холинорецепторы.
Преимущественное действие – когда один и тот же препарат, действуя на различные рецепторы, обладает более выраженным фармакологическим эффектом на один из рецепторов. Например, орципреналина сульфат (Алупент, Астмопент), воздействуя на β1β2 адренорецепторы, вызывает более выраженный эффект на β2-адренорецепторы бронхов, поэтому в клинической практике его используют как бронхорасширяющее средство.
Иногда трудно определить, на какой конкретно орган действует то или иное лекарственное средство, тогда говорят об общем действии на организм или о неспецифическом действии. Такие препараты вызывают широкий спектр фармакологических эффектов и влияют на различные биохимические процессы в организме. При воздействии ЛС на конкретные отделы головного, спинного мозга, обеспечивающим адекватную ответную реакцию организма, говорят о центральном действии. Влияние ЛС на функции внутренних органов рассматривают как периферическое действие.
Общее действие развивается при применении лекарств, оказывающих фармакологический эффект одновременно на весь организм (в целом). Общим действием обладают общетонизирующие ЛС, адаптогены, такие как женьшень, элеутерококк, заманиха. Действующие вещества этих растений приспосабливают организм к изменившейся внешней или внутренней среде. При применении этих препаратов в осенне-весенний период повышается общий тонус, работоспособность, снимается умственная и физическая усталость, переутомление, общая слабость организма. Таким же общим действием обладают поливитаминные препараты, содержащие комплекс витаминов, макро- и микроэлементов. Наркозные средства или общие анестетики – Ксенон, Кетамин – обладают общим обратимым угнетающим действием на большинство клеток в ЦНС и этот эффект распространяется и на периферические органы.
Центральное действие оказывают лекарственные средства, действие которых направлено на различные отделы центральной нервной системы (ЦНС). Действие на ЦНС развивается только после прохождения лекарств через гематоэнцефалический барьер. Это сложный липидный барьер между кровью, нейроглиальными клетками, эндотелиальными клетками капилляров сосудов мозга, оболочками базальной мембраны, интерстициальной жидкостью мозга. К ЛС, воздействующим на ЦНС, относятся следующие группы – «Противопаркинсонические ЛС», «Противосудорожные (противоэпилептические) ЛС», «Наркотические анальгетики», «Снотворные средства». Центральным действием обладают психотропные средства, оказывающие влияние на психическую деятельность человека, – «Антипсихотические», «Анксиолитические», «Психостимуляторы», «Антидепрессанты» и др.
Периферическое действие развивается при действии лекарств непосредственно на периферические органы и ткани: печень, почки, сердце, сосуды, органы дыхания или при влиянии на эфферентные нервные окончания, иннервирующие внутренние органы и скелетную мускулатуру. Периферическим действием обладают диуретики, маточные, кардиотонические, гепатопротекторы, холинергические, адренергические средства и др.
Местное нежелательное действие проявляется при прямом контакте ЛС с кожей, подкожной жировой клетчаткой, слизистыми оболочками. Такое действие могут оказать препараты, обладающие раздражающим действием. Так, многие противогистаминные средства (например, Диазолин) оказывают раздражающее действие при введении внутрь, для устранения которого их выпускают в драже или таблетках, покрытых оболочкой.
Ульцерогенное действие проявляется раздражением и эрозивными поражениями слизистой оболочки, уменьшением выработки защитного слоя (муцина, слизи), защитных факторов (бикарбонатов, ПГЕ1) и повышением проницаемости эпителиальных клеток для Н+-ионов. Эрозивно-язвенные поражения ЖКТ и кровотечения возникают при приеме лекарств из групп «Глюкокортикостероиды» (ГКС) и «Нестероидные противовоспалительные средства» (НПВС). Например, при длительном применении больших доз ацетилсалициловой кислоты, основным проявлением побочного действия является ульцерогенное, включающее раздражение, изъязвление ЖКТ, возможно с кровотечением, – это отрицательный нежелательный эффект. Другие виды его фармакологического действия – анальгезирующий, жаропонижающий – являются побочными положительными, проявляющимися на фоне его основного противовоспалительного эффекта действия.
Рефлекторное нежелательное действие является следствием выраженного местного эффекта (раздражающего влияния) и сводится к торможению функций органа или системы органов, на которые оказывается основное действие. Например, рефлекторная остановка сердца и дыхания возможна при вдыхании больших концентраций эфира для наркоза.
Дисбактериоз – нарушение подвижного равновесия состава естественной микрофлоры, в норме заселяющей слизистые оболочки ЖКТ или влагалища. Это клинико-лабораторный синдром, сопутствующий острым и хроническим заболеваниям органов пищеварения, возникающий на фоне длительной антибактериальной терапии, хронического употребления алкоголя, нарушения питания, проживания в неблагоприятных условиях. Наблюдаются качественные и количественные изменения состава микробных ассоциаций, нарушается антагонистическая активность микрофлоры, начинают активно развиваться условно-патогенные и патогенные микроорганизмы.
Средства, блокирующие ангиотензинные АТ1–рецепторы
В нашем организме ренин–ангиотензин–альдостероновая система (РААС) представляет собой сложный ферментативно–гормональный биологический процесс. Данная система принимает активное участие в поддержании нормальных показателей артериального давления, обеспечивает водно–солевое равновесие в организме и поддерживает кислотно–щелочной баланс крови.
Преферанская Нина Германовна
Доцент кафедры фармакологии института фармации им. А.П. Нелюбина Первого МГМУ им. И.М. Сеченова (Сеченовский университет), к.фарм.н.
В нашем организме ренин–ангиотензин–альдостероновая система (РААС) представляет собой сложный ферментативно–гормональный биологический процесс. Данная система принимает активное участие в поддержании нормальных показателей артериального давления, обеспечивает водно-солевое равновесие в организме и поддерживает кислотно–щелочной баланс крови. Именно этой системе отводится важнейшая роль не только в патогенезе артериальной гипертензии, но и других ССЗ.
Главная эффекторная задача в РААС отдана ангиотензину II (АТII). АТII (октапептид) образуется в результате нескольких последовательных биохимических реакций. В секреторных гранулах юкстагломерулярного аппарата почек вырабатывается протеолитический фермент ренин, высвобождающийся в кровь. В кровяном русле из неактивного белка ангиотензиногена (полипептида, альфа2–глобулиновой фракции сыворотки) под действием ренина образуется неактивный декапептид АТI. Ренин разрывает в молекуле ангиотензиногена пептидную связь, образованную двумя остатками лейцина с образованием АТI. Под действием ангиотензин–превращающего фермента (АПФ), также присутствующего в плазме крови, происходит конверсия АТI в АТII. АПФ отщепляет от биологически неактивного АТI две молекулы аминокислоты, превращая его в высокоактивный АТII, с периодом полураспада 12 мин. АПФ — это цинксодержащая дипептидиловая карбоксипептидаза (кининаза–II), которая локализуется на эндотелиальных клетках, капиллярах легких, в паренхиме почек, сердца и надпочечниках. Фермент АПФ не обладает избирательностью действия и параллельно осуществляет инактивацию физиологического вазодилататора брадикинина, расширяющего периферические артериолы.
АТII считается основным высокоактивным пептидом, циркулирующим в РААС. Это наиболее сильный вазоконстриктор прямого действия, способный суживать артерии и вены, провоцировать сокращение периферических кровеносных сосудов, что приводит к скачку вверх кровяного давления. АТII стимулирует выработку катехоламинов из мозгового слоя надпочечников, повышая симпатический тонус. Из коры надпочечников в кровь он усиливает секрецию минералокортикоидного гормона — альдостерона, вызывающего задержку натрия и потерю калия в организме, сужает сосуды в почках, поднимает давление в почках и увеличивает общий объем циркулирующей крови. АТII оказывает влияние на ЦНС, при этом нарастает выработка антидиуретического гормона — вазопрессина, последний повышает реабсорбцию воды и возникает чувство жажды, что, в свою очередь, приводит к обилию жидкости в организме и возникновению отеков.
При длительном процессе концентрации АТII в крови и тканях усиливается образование коллагеновых волокон и развивается гипертрофия гладкомышечных клеток кровеносных сосудов. В результате стенки кровеносных сосудов утолщаются, уменьшается их внутренний диаметр, что приводит к поднятию артериального давления. Помимо этого, происходит истощение и дистрофия клеток сердечной мышцы с их последующей гибелью и замещением на соединительную ткань, что является причиной развития сердечной недостаточности. Вот почему необходимо подавлять чрезмерную активность АТII в кровяном русле и тканях больных не только гипертонией, но и ряда других заболеваний.
Было установлено, что ЛС группы «Ингибиторы АПФ» (ИАПФ) полностью не устраняют влияние АТII, остаются альтернативные пути его образования, влияющих на АД. В тканях превращение АТI в АТII катализируют другие ферменты. В стенке артерий под действием АПФ образуется только 30% АТII, тогда как в тканях под действием химазы и катепсина G — около 70%. Поэтому терапевтическая эффективность при применении ИАПФ у пациентов с артериальной гипертензией (АГ) и сердечной недостаточностью часто бывает ограничена. При лечении ИАПФ образование АТII уменьшается, а содержание в крови и тканях БАВ, таких как брадикинин, гистамин, нейропептид Y, субстанция Р, простагландин Е2, — повышается, что связано с развитием побочных результатов.
Почти все эффекты активации РААС в крови и тканях объясняются действием АТII на специфические ангиотензиновые рецепторы (АТR). Наибольшее сродство АТII имеет к АТ1–рецепторам (I типа), которые локализуются преимущественно в гладкой мускулатуре кровеносных сосудов, сердце, отдельных областях мозга, печени, почках, коре надпочечников. Поэтому в 1990–х гг. были предложены блокаторы АТ1– рецепторов, и первый в этой группе был Лозартан (Козаар) — препарат, с которого началась эра «сартанов», на основе которых сегодня созданы уже несколько поколений ЛП.
Сартаны
Еще недавно у данной группы ЛС в рекомендациях ВОЗ/МОГ было единственное показание — развитие кашля на прием ИАПФ. В настоящее время «сартаны» стали наиболее применяемой группой для коррекции многих патологических состояний.
Группу «Сартаны» (далее — сартаны) также называют блокаторами АТ1–рецепторов (БРА) или антагонистами (ингибиторами) АТII. По химической структуре сартаны делятся на 3 основные подгруппы:
В зависимости от наличия активного метаболита среди сартанов выделяют пролекарства и активные ЛС. К пролекарствам относятся: Лозартан и его фармакологически активный метаболит (Е 3174), Кандесартан и его активный метаболит (CV-11974), Азилсартана медоксомил превращается в активную молекулу азилсартана, Олмесартан медоксомил и его активный метаболит (CS-866).
Активными ЛС являются Валсартан, Ирбесартан, Телмисартан, Эпросартан, Фимасартан.
В зависимости от типа антагонизма с АТII их делят на селективные конкурентные антагонисты — лозартан, эпросартан, олмесартан, азилсартан и неконкурентные — вальсартан, ирбесартан, кандесартан, телмисартан.
В основе механизма действия сартанов лежит воздействие на РААС, с уменьшением ее активности. Данные ЛС блокируют АТ1–рецепторы, ослабляют эффекты АТII и опосредованно повышают активность АТ2–рецепторов (II типа). Среди эффектов, которые опосредуются через рецепторы II типа, возникает: вазодилатация, высвобождение оксида азота, стимуляция апоптоза, антипролиферативное действие и др.
Блокаторы АТ1–рецепторов имеют ряд преимуществ перед ИАПФ. ЛП более специфично и значительно подавляют сердечно–сосудистые эффекты активации РААС, блокируют негативные действия АТII, стимулируют при этом защитные эффекты, нарушают деградацию брадикинина, способствуя синтезу простациклина и оксида азота.
Сартаны устраняют действие АТII на сосуды, которые «отказываются» сокращаться, отчего нет артериальной вазоконстрикции и повышения АД. Оттого не происходит задержки натрия и воды. Кроме того, антагонисты АТII взаимодействуют с пресинаптическими рецепторами норадренергических нейронов, что приводит к значительному уменьшению высвобождения норадреналина в синаптическую щель и предотвращению симпатической вазоконстрикции.
Применение сартанов вызывает ремоделирование сосудистой стенки и миокарда, улучшается внутрисердечная гемодинамика, возникает уменьшение полости сердца и регрессия гипертрофии левого желудочка. Препараты снижают симпатическое влияние, повышенную эктопическую активность миокарда и оказывают стабилизирующее воздействие на кардиомиоциты. Отмечается и наличие антиаритмических свойств. Таким образом, ингибирование активности РААС сводит к минимуму сосудистое воспаление, способствует замедлению развития атеросклероза и исключают возможность накопления БАВ и связанных с ними нежелательных реакций.
Степень специфического сродства — аффиннитет (лат. affinitas — родственность) средства с АТ1–рецепторами обеспечивает прочность биомолекулярного комплекса со специфическими рецепторами и скорость диссоциации этой связи, что коррелирует с длительностью действия ЛС. По степени аффинности к рецепторам препараты располагаются в убывающей последовательности: кандесартан > олмесартан > телмисартан > валсартан > ирбесартан > лозартан.
Сартаны помимо гипотензивного действия положительно влияют на работу внутренних органов, проявляют кардиопротективный, ренопротективный, вазопротективный церебропротективными эффекты.
Сартаны имеют малую роль в концентрации глюкозы, показателях холестерина и пуринов в крови, но повышают чувствительность ткани к инсулину, за счет чего уменьшается инсулинорезистентность.
В ходе КИ, у пациентов, принимающих сартаны, редко возникали отеки, эректильная дисфункция и андрогенный дефицит. Практически не наблюдается частота развития острых аллергических реакций, таких как анафилактический шок или приступы сухого кашля.
ЛП редко вызывают гипотензию и коллаптоидные реакции, крайне редко — гиперкалиемию и гипонатриемию. Наиболее часто возникали головная боль и головокружения, боль в спине и миалгии, нарушения функции почек. В целом при применении данной группы ЛП не было отмечено клинически значимых изменений лабораторных показателей.
Лозартан, табл. 12,5 мг, 25 мг, 50 мг, 100 мг (ТН «Козаар», «Лозап», «Вазортенз», «Презартан», «Лориста») — первый непептидный блокатор АТ1–рецепторов, основные фармакологические эффекты которого обусловлены его активным метаболитом, который в 10–40 раз сильнее исходного препарата лозартан. Антигипертензивный эффект при назначении его в суточной дозе 50 мг и 100 мг один раз в день сохраняется 24 часа. По антигипертензивной эффективности лозартан не уступает бета–блокаторам, антагонистам кальция и ИАПФ, но лучше переносится больными и меньше вызывает побочных явлений. В отличие от других сартанов ЛП обладает урикозурическим действием, уникальной способностью увеличивать почечную экскрецию мочевой кислоты; также тормозит транспорт уратов в проксимальных почечных канальцах. К благоприятным эффектам Лозартана можно отнести торможение активации тромбоцитов.
Кандесартан (ТН «Атаканд», «Кандекор», «Ангиаканд», «Ордисс», «Гипокарт», «Ксартен») — для ЛП характерна высокая селективность, сродство к АТ1–рецепторам, прочность связи в 80 раз выше, чем у лозартана. ЛП обладает высокой липофильностью, оказывает длительное дозозависимое снижение АД: одноразовый прием вне зависимости от приема пищи обеспечивает снижение АД на сутки. Нефропротективный эффект после приема связан с увеличением почечного кровотока и скорости клубочковой фильтрации, снижением почечного сосудистого сопротивления и фильтрационной фракции. Ни ингибиторы, ни индукторы микросомальных цитохромных ферментов не оказывают существенного влияния на фармакокинетику этого ЛП.
Ирбесартан, табл. 150 мг, 300 мг (ТН «Апровель», «Ирсар», «Ирбис») — высокоселективный неконкурентный блокатор АТ1–рецепторов, который в 10 раз сильнее связывается с рецепторами, чем лозартан. ЛП снижает концентрацию альдостерона в плазме крови и не подавляет фермент АПФ, уменьшает постнагрузку, системное артериальное давление и давление в «малом» круге кровообращения. Обладает высокой липофильностью и более длительным дозозависимым действием. Гипотензивное действие развивается в течение 1–2 недель и достигает максимума эффективности через 4–6 недель после начала терапии.
Важно! Противопоказан в период беременности и лактации.
Валсартан, табл. 40 мг, 80 мг, 160 мг (ТН «Диован») — относится к специфическим антагонистам АТII, избирательно блокирует АТ1–рецепторы. Сродство валсартана АТ1–рецепторам в тысячи раз выше, чем к рецепторам подтипа АТ2. После однократного приема ЛП гипотензивный эффект поддерживается в течение суток. В контролируемых КИ у пациентов с АГ частота нежелательных явлений была сравнима с плацебо. Отмена в терапии не вызывает развития рикошетной гипертензии, также отсутствует гипотония первой дозы. ЛП не вызывает повышение уровня гликемии (не изменяет липидный профиль), триглицеридов и мочевой кислоты.
Телмисартан, табл. 40 мг, 80 мг (ТН «Микардис», «Телзап», «Телмиста», «Телсартан») — считается самым мощным из сартанов, т.к. помимо блокады рецепторов AT1, значительно активирует противовоспалительные ядерные рецепторы PPARγ, уменьшает воспаление и метаболические изменения и играет важную роль в нейропротекции (подробнее о применении см. в инструкции).
Начало гипотензивного действия после первого приема 80 мг отмечается в течение 3 часов и может пролонгироваться до 48 час.
Эпросартан, табл. 600 мг (ТН «Теветен») — связывается с АТ1–рецепторами сосудов сердца, почек и коры надпочечников, образуя с ними прочную связь. ЛП оказывает вазодилатирующее, гипотензивное и опосредованно диуретическое действие; не оказывает отрицательного влияния на концентрацию в крови глюкозы, общего холестерина, триглицеридов, липопротеидов низкой плотности. Нефропротективное действие связано с увеличением почечного кровотока, скорости клубочковой фильтрации, уменьшением выведения альбуминов. Внезапное прекращение приема эпросартана после его применения в течение длительного периода не сопровождается синдромом отмены.
Олмесартана медоксомил, табл. 10 мг, 20 мг и 40 мг (ТН «Кардосал») — отличается наличием прочного продолжительного связывания с АТ1–рецепторами, что обеспечивает наибольшую его эффективность при наблюдении АД. Препарат практически не связывается с АТ2–рецепторами. При АГ вызывает дозозависимое продолжительное снижение АД и значительно снижает риск осложнений ССЗ. Гипотензивное действие ЛП зависит от дозы, развивается в течение первых 2 недель, максимальный эффект — приблизительно через 4–8 недель после начала терапии.
Азилсартана медоксомил, табл. 20 мг, 40 мг, 80 мг (ТН «Эдарби») — допущен к использованию в США в 2011 г. для лечения больных с АГ и показал благоприятные результаты в снижении и контроле за АД. В 2012 году данный лекарственный препарат был одобрен для лечения АГ и в Японии. Азилсартана медоксомил является более эффективным, чем кандесартан в способности уменьшать плазменные концентрации глюкозы и жирных кислот. Также было доказано, что это азилсартан медоксомил уменьшает инсулинорезистентность, независимо от характера питания, увеличения массы тела или активации жировой PPAR–γ (Peroxisome proliferatorт– activated receptor gamma) — главного регулятора адипогенеза и вовлеченного в патологию множества заболеваний, включая ожирение, диабет, атеросклероз. Азилсартан может с достаточной эффективностью использоваться у больных с АГ в сочетании с инсулинорезистентностью, метаболическим синдромом и внести потенциальный вклад в дело уменьшения риска сердечно-сосудистых осложнений у лиц с высоким коронарным риском. Он модулирует многие метаболические функции участвующие в развитии и прогрессировании атеросклеротического процесса.
Фимасартан калия тригидрат, табл. 60 мг, 120 мг (ТН «Канарб») — мощный блокатор АТ1–рецепторов, изученный в широком спектре доклинических и КИ в Республике Корея. Многоцентровые, рандомизированные КИ завершились в 2016 году. После однократного перорального приема фимасартана в дозе от 20 до 480 мг максимум терапевт. Воздействия достигается спустя 6-8 час. и в полной мере может пролонгироваться до 48 часов. Для пациентов с легкой степенью хронической почечной и печеночной недостаточности начальной коррекции дозы ЛП не требуется.
При средней и тяжелой печеночной недостаточности — не рекомендован.
Важно! Применение ЛП у беременных женщин, и только еще планирующих беременность, противопоказано.
Артериальная гипертензия является одним из наиболее значимых факторов риска возникновения ССЗ. Применение сартанов для снижения АД до рекомендованного нормального уровня взаимосвязано с максимальным снижением риска неблагоприятных сердечно–сосудистых осложнений, повышением качества и увеличением продолжительности жизни больных.