Низкий сердечный индекс связан с повышенным риском развития деменции
Системы в организме человека взаимосвязаны, и проблемы в одной из них отражаются на работе других. Один из примеров – влияние сердечно-сосудистого фактора на риск развития деменции. Этот вопрос изучен за последние годы довольно подробно. Вот результаты одного из последних наблюдений ученых.
Одним из показателей работы сердечно-сосудистой системы является так называемый сердечный индекс – отношение минутного объема кровообращения к площади поверхности тела. Сердечный индекс выступает важным индикатором функционального состояния организма, поэтому специалисты медицинского центра университета Вандербильт (США) проследили зависимость между сердечным индексом и риском развития деменции. Участники, средний возраст которых составлял приблизительно 70 лет, не имели на начало наблюдения клинически диагностированных инсультов, микроинсультов и нейродегенеративных расстройств. Наблюдение за ними продолжалось около 7 лет. В оценку включались такие данные, как пол испытуемых, возраст, верхнее артериальное давление, прием препаратов от давления, наличие диабета, история болезней по сердечно-сосудистым заболеваниям, мерцательная аритмия, курение и образование. По истечении периода наблюдения диагноз «деменция» был поставлен 32 пациентам, и все они относились к группе с низким сердечным индексом.
По словам руководителя исследования, Анджелы Джефферсон, нарушение функционирования сердца может в конечном итоге оказаться одним из основных факторов, повышающих риск развития деменции, поскольку головной мозг в этом случае не получает достаточного количества кислорода и питательных веществ. Однако в отличие от генетического фактора, не поддающегося корректировке, сердце можно укрепить путем правильного питания и физических нагрузок, причем на любом этапе жизни человека.
УЗИ сердца: норма и расшифровка результатов
В различных областях медицины ультразвуковое исследование внутренних органов является основным методом диагностики.
УЗИ сердца в кардиологии называется эхокардиография. Исследование позволяет выявить изменения, аномалии, нарушения и пороки развития в работе сердца. Процедура безболезненная, неинвазивная, может быть назначена людям всех возрастов и даже беременным женщинам. Исследование сердца ультразвуком проводится уже на стадии внутриутробного развития плода.
Для обследования используется специальное оборудование – УЗИ аппарат или сканер. На кожу пациента наносится особый гель, который способствует лучшему проникновению ультразвука в мышцы сердца и другие структуры, прикрепляется датчик. Данные отображаются на мониторе и автоматически фиксируются.
Процедура длится от 30 до 60 минут. Эхокардиография проводится кардиологом, а также по направлению пульмонолога, невролога, эндокринолога, гинеколога.
Врач назначает обследование в случаях, если пациент имеет жалобы на головокружение, отдышку, боли в груди, слабость, аритмию, тахикардию, повышенное артериальное давление, признаки сердечной недостаточности, обмороки. Людям, перенесшим кардиологические операции, инфаркт необходимо проходить процедуру один раз в год.
Эхокардиография применяется для:
— определения шумов,
— диагностики состояния клапанов,
— обнаружения изменений в структурах,
— оценки работы отделов сердца у людей с хроническими заболеваниями,
— обнаружения скопления жидкости,
— оценки и мониторинга врожденных дефектов, кровотока, состояния кровеносных сосудов,
— обнаружения тромбов в камерах
УЗИ сердца показывает состояние перикарда, миокарда, сосудов, митральный клапан, стенки желудочков.
Во время процедуры кардиолог фиксирует полученные показания. Расшифровка данных дает возможность выявить заболевания, отклонения, патологии, аномалии в работе сердца. На основе полученной информации врач ставит диагноз, назначает лечение. Зачастую дополнительно к эхокардиографии назначают допплерографию. Данная процедура позволяет увидеть направление движения, определить скорость, турбулентность потока крови в камерах сердца.
Врач делает заключение в протоколе результатов диагностики, где отображаются данные, полученные с УЗИ аппарата.
С помощью эхокардиографии диагностируют:
— предынфарктное состояние;
— сердечную недостаточность;
— ишемическую болезнь;
— инфаркт миокарда;
— гипертонию, гипотонию;
— пороки сердца;
— нарушения ритма;
— кардиомиопатию;
— миокардит, перикардит;
— вегето-сосудистую дистонию;
— ревматизм.
В целях получения данных о работе сердца с физической нагрузкой проводят Стресс- эхокардиографию. Пациенту дают определенную физическую нагрузку или вызывают усиленную работу сердечной мышцы с помощью препаратов, снимают показания.
Довольно редко в практике встречаются случаи, когда провести стандартную процедуру УЗИ сердца не возможно: деформация грудной клетки, наличие клапанов-протезов, слой подкожно-жировой клетчатки, обильное оволосенение. В таком случае, проводится чреспищеводная (трансэзофагеальная) эхокардиография.
Типы эхокардиографии:
Провести полный и точный анализ расшифровки кардиограммы и составить заключение может только врач-кардиолог.
Нормы УЗИ сердца:
Левый желудочек
— масса миокарда (мужчины: 135-182 г; женщины: 95-141 г)
— индекс массы миокарда (мужчины: 71-94 г/м2; женщины: 71-80 г/м2)
— объем в состоянии покоя (мужчины: 65-193 мл; женщины: 59-136 мл)
— размер в состоянии покоя (мужчины: 5,7 см; женщины: 4,6 см)
— размер во время сокращения (мужчины: 4,3 см; женщины: 3,1см)
— толщина стенки вне сокращений сердца при работе: 1,1 см. Показатель 1,6 см свидетельствует о гипертрофии
— фракция выброса не менее 55-60%. Показатель указывает на объем крови, который при каждом сокращении выбрасывает сердце. Меньшее значение говорит о сердечной недостаточности
— ударный объем: 60-100 мл (количество крови, выбрасываемой за одно сокращение)
Правый желудочек
— толщина стенки 5 мм
Клапаны
— Уменьшение диаметра отверстия клапана, затруднение прокачивания крови свидетельствует о стенозе
— Сердечную недостаточность диагностируют в случае, если створки клапана препятствуют обратному движению крови, не выполняют возложенную функцию
Перикард
— Норма жидкости 10-30 мл. При показателе свыше 500 нормальная работа сердца затруднена. Возможно начало воспалительного процесса – перекардита, скопление жидкости, образование спайки сердца и околосердечной сумки.
Проведение процедуры УЗИ сердца помогает обнаружить заболевания сердечнососудистой системы на ранней стадии и вовремя принять необходимые меры.
Что такое сердечный индекс
В клинической литературе чаще используют понятие «минутный объем кровообращения» (МОК).
В системе транспорта кислорода аппарат кровообращения является лимитирующим звеном, поэтому соотношение максимальной величины МОК, проявляющейся при максимально напряженной мышечной работе, с его значением в условиях основного обмена дает представление о функциональном резерве сердечно-сосудистой системы. Это же соотношение отражает и функциональный резерв сердца в его гемодинамической функции. Гемодинамический функциональный резерв сердца у здоровых людей составляет 300—400 %. Это означает, что МОК покоя может быть увеличен в 3—4 раза. У физически тренированных лиц функциональный резерв выше — он достигает 500—700 %.
Для условий физического покоя и горизонтального положения тела испытуемого нормальные величины минутного объема кровообращения ( МОК ) соответствуют диапазону 4—6 л/ мин (чаще приводятся величины 5—5,5 л/мин). Средние величины сердечного индекса колеблются от 2 до 4 л/(мин • м2) — чаще приводятся величины порядка 3—3,5 л/(мин • м2).
Поскольку объем крови у человека составляет только 5—6 л, полный кругооборот всего объема крови происходит примерно за 1 мин. В период тяжелой работы МОК у здорового человека может увеличиваться до 25— 30 л/мин, а у спортсменов — до 30—40 л/мин.
Факторами, определяющими величину величины минутного объема кровообращения ( МОК ), являются систолический объем крови, частота сердечных сокращений и венозный возврат крови к сердцу.
Систолический объем крови. Объем крови, нагнетаемый каждым желудочком в магистральный сосуд (аорту или легочную артерию) при одном сокращении сердца, обозначают как систолический, или ударный, объем крови.
В покое объем крови, выбрасываемый из желудочка, составляет в норме от трети до половины общего количества крови, содержащейся в этой камере сердца к концу диастолы. Оставшийся в сердце после систолы резервный объем крови является своеобразным депо, обеспечивающим увеличение сердечного выброса при ситуациях, в которых требуется быстрая интенсификация гемодинамики (например, при физической нагрузке, эмоциональном стрессе и др.).
Таблица 9.3. Некоторые параметры системной гемодинамики и насосной функции сердца у человека (в условиях основного обмена)
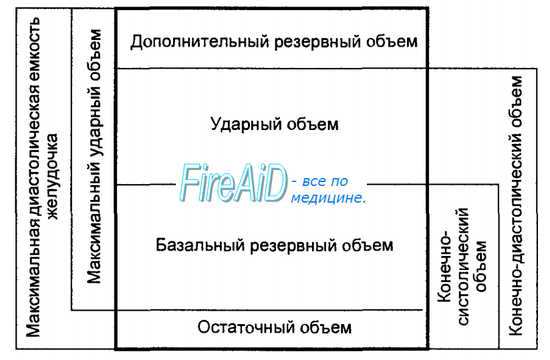
Величина систолического (ударного) объема крови во многом предопределена конечным диастолическим объемом желудочков. В условиях покоя диастолическая емкость желудочков сердца подразделяется на три фракции: ударного объема, базального резервного объема и остаточного объема. Все эти три фракции суммарно составляют конечно-диастолический объем крови, содержащийся в желудочках (рис. 9.4).
После выброса в аорту систолического объема крови оставшейся в желудочке объем крови — это конечно-систолический объем. Он подразделяется на базальный резервный объем и остаточный объем. Базальный резервный объем — это количество крови, которое может быть дополнительно выброшено из желудочка при увеличении силы сокращений миокарда (например, при физической нагрузке организма). Остаточный объем — это то количество крови, которое не может быть вытолкнуто из желудочка даже при самом мощном сердечном сокращении (см. рис. 9.4).
Величина резервного объема крови является одной из главных детерминант функционального резерва сердца по его специфической функции — перемещению крови в системе. При увеличении резервного объема, соответственно, увеличивается максимальный систолический объем, который может быть выброшен из сердца в условиях его интенсивной деятельности.
Регуляторные влияния на сердце реализуются в изменении систолического объема путем воздействия на сократительную силу миокарда. При уменьшении мощности сердечного сокращения систолический объем снижается.
У человека при горизонтальном положении тела в условиях покоя систолический объем составляет от 60 до 90 мл (табл. 9.3).
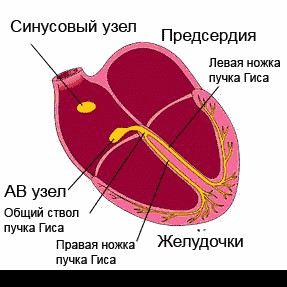
Нарушения сердечного ритма
Сердце человека в нормальных условиях бьется ровно и регулярно. Частота сердцебиения в минуту при этом составляет от 60 до 90 сокращений. Данный ритм задается синусовым узлом, который называется также водитель ритма. В нем имеются пейсмекерные клетки, от которых возбуждение передается далее на другие отделы сердца, а именно на атрио-вентрикулярный узел, и на пучок Гиса непосредственно в ткани желудочков.
Данное анатомо-функциональное разделение важно с позиции типа того или иного нарушения, потому что блок для проведения импульсов или ускорение проведения импульсов могут возникнуть на любом из этих участков.
Нарушения ритма сердца и его проводимости носят название аритмий и представляют собой состояния, когда сердечный ритм становится меньше нормы (менее 60 в минуту) или больше нормы (более 90 в минуту). Также аритмией является состояние, когда ритм является нерегулярным (неправильным, или несинусовым), то есть исходит из любого участка проводящей системы, но только не из синусового узла.
Классификация
Все нарушения ритма и проводимости классифицируются следующим образом:
В первом случае, как правило, происходит ускорение сердечного ритма и/или нерегулярное сокращение сердечной мышцы. Во втором же отмечается наличие блокад различной степени с урежением ритма или без него.
В целом к первой группе относятся нарушение образования и проведения импульсов:
Причины аритмии сердца
Причины аритмии (возникновения нарушений ритма сердца) настолько многообразны, что перечислить абсолютно все является очень трудной задачей. Тем не менее, во многих случаях именно от причины аритмии зависит ее безопасность для жизни больного, дальнейшая тактика лечения.
Предложено множество различных классификаций причин аритмии, однако ни одна из них в настоящее время не является общепринятой. Наиболее приемлемой для пациента мы считаем следующую классификацию. Она основывается на признаке наличия или отсутствия у больного первичного заболевания сердца. Если имеется заболевание сердца, аритмию называют органической, а если заболевания сердца нет — неорганической. Неорганические аритмии принято также называть функциональными.
Органические аритмии
К органическим аритмиям относятся:
Функциональные аритмии
Это также достаточно большая группа, включающая:
Одинаково ли проявляются нарушения ритма сердца?
Все нарушения ритма и проводимости клинически проявляют себя по разному у разных пациентов. Часть больных никаких симптомов не ощущает и узнает о патологии только после планового проведения ЭКГ. Эта часть больных незначительна, так как в большинстве случаев пациенты отмечают явную симптоматику.
Так, для нарушений ритма, сопровождающихся учащенным сердцебиением (от 100 до 200 ударов в мин), особенно для пароксизмальных форм, характерно резкое внезапное начало и перебои в сердце, нехватка воздуха, болевой синдром в области грудины.
Некоторые нарушения проводимости, например пучковые блокады, ничем не проявляются и распознаются только на ЭКГ. Синоатриальная и атрио-вентрикулярная блокады первой степени протекают с незначительным урежением пульса (50-55 в мин), из-за чего клинически могут проявляться лишь незначительной слабостью и повышенной утомляемостью.
Блокады 2 и 3 степени проявляются выраженной брадикардией (меньше 30-40 в мин) и характеризуются кратковременными приступами потери сознания.
Кроме этого, любое из перечисленных состояний может сопровождаться общим тяжелым состоянием с холодным потом, с интенсивными болями в левой половине грудной клетки, снижением артериального давления, общей слабостью и с потерей сознания. Эти симптомы обусловлены нарушением сердечной гемодинамики и требуют пристального внимания со стороны врача.
Разновидности аритмий
Большинство людей под аритмией подразумевает беспорядочные сокращения сердечной мышцы («сердце бьется, как захочет»). Однако это не совсем так. Врач этот термин использует при любом нарушении сердечной деятельности (урежение или учащение пульса), поэтому виды аритмий можно представить следующим образом:
По частоте сердечного ритма различают 3 формы мерцательной аритмии:
На ЭКГ при МА зубец Р не регистрируется, потому что нет возбуждения предсердий, а определяются только предсердные волны f (частота 350-700 в минуту), которые отличаются нерегулярностью, различием формы и амплитуды, что придает электрокардиограмме своеобразный вид.
Причиной МА могут быть:
Частота встречаемости трепетания предсердий (ТП) в 20-30 раз ниже, чем МА. Для него также характерны сокращения отдельных волокон, но меньшая частота предсердных волн (280-300 в минуту). На ЭКГ предсердные волны имеют большую амплитуду, чем при МА.
Интересно, что на одной ЭКГ можно видеть переход мерцания в трепетание и наоборот.
Причины возникновения трепетания предсердий аналогичны причинам формирования мерцания.
Симптомы мерцания и трепетания часто отсутствуют вообще, но иногда отмечаются некоторые клинические проявления, вызванные беспорядочной деятельностью сердца или симптомы основного заболевания, В общем, яркой клинической картины такая патология не дает.
Синдром слабости синусового узла
Эта патология возраст не выбирает, однако предпочитает определенные условия:
Заподозрить синдром слабости синусового узла можно по характерным для него признакам:
Последствием синдрома дисфункции синусового узла является внезапное возникновение приступа Адамса-Морганьи-Стокса и асистолия (остановка сердечной деятельности).
Медикаментозное лечение этого синдрома сводится к применению атропина, изадрина, препаратов белладонны. Однако, учитывая, что эффект от консервативного лечения, как правило, небольшой, больным показана имплантация постоянного кардиостимулятора.
Атриовентрикулярная (АВ) блокада — нарушение проведения возбуждения в желудочки из предсердий, с задержкой или прекращением проведения импульса. Она зачастую является спутницей воспалительных и дегенеративных процессов, происходящих в сердечной мышце, инфаркта миокарда или кардиосклероза. Повышенный тонус блуждающего нерва тоже играет определенную роль в формировании атриовентрикулярной блокады.
Атриовентрикулярная блокада, являясь последствием органических поражений сердца, сама дает еще худшие осложнения, в результате которых значительно возрастает опасность летального исхода. Если атриовентрикулярная блокада 1 ст. лечится путем воздействия на основное заболевание, то АВ блокада может переходить в полную, что нарушает кровоснабжение жизненно важных органов, которое приводит к развитию сердечной недостаточности. А это уже плохое последствие, поэтому лечение откладывать нельзя, больного госпитализируют и назначают препараты, стимулирующие сердечную деятельность в инъекционных растворах с постоянным наблюдением за состоянием пациента. Если брадикардия резко выраженная, отмечается тяжелая сердечная недостаточность, больному в экстренном порядке имплантируют искусственный водитель ритма.
Какие шкалы должен использовать кардиолог у пациентов с фибрилляцией предсердий? Что нового?
Частота фибрилляции предсердий (ФП) у взрослых людей в популяции составляет 2-4% [1]. Она увеличивается с возрастом, в том числе под действием различных сопутствующих заболеваний и факторов риска, таких как артериальная гипертония, сахарный диабет, коронарная болезнь сердца, хроническая болезнь почек, ожирение, употребление алкоголя, курение и т.д. В ближайшие годы можно ожидать дальнейшего роста распространенности ФП не только за счет увеличения продолжительности жизни и постарения населения, но и внедрения новых систем скрининга нарушений ритма с помощью мобильных технологий (смартфонов), позволяющих зарегистрировать малосимптомные или бессимптомные нарушения ритма [2]. Например, в исследовании REHEARSE-AF регистрация ЭКГ в одном отведении с помощью смартфона/ планшета два раза в неделю в течение 12 мес у пациентов в возрасте ≥65 лет привела к увеличению частоты диагностики ФП в 3,9 раза по сравнению с обычной тактикой ведения [3]. Использование подобных устройств для скрининга ФП наиболее обосновано у людей пожилого и старческого возраста, а также пациентов с высоким риском инсульта [4].
ФП ассоциируется более чем с 3-кратным увеличением риска смерти [5] и является одной из основных причин инсульта (20-30% и 10% случаев ишемического и криптогенного инсульта, соответственно), который характеризуется тяжелым и рецидивирующим течением и часто приводит к смерти или инвалидизации [1]. ФП сопровождается нарушением функции сердца и развитием сердечной недостаточности, как со сниженной, так и сохраненной фракцией выброса левого желудочка, которая наблюдается у 20-30% таких больных и вызывает дополнительное ухудшение прогноза для жизни [6]. Неблагоприятные последствия ФП включают в себя также снижение качества жизни, особенно у женщин [7], когнитивные расстройства вплоть до деменции [8] и частые госпитализации, ассоциирующиеся с увеличением затрат для системы здравоохранения [9]. По данным мета-анализа 35 исследований в целом более чем у 300000 больных с ФП частота госпитализаций составила в среднем 43,7 на 100 пациентов в год, а одним из основных факторов, ассоциировавшихся с увеличением вероятности поступления в стационар, был пожилой возраст [10].
Ведение больных с ФП

Антикоагулянтная терапия
Для оценки риска инсульта у больных с ФП и, соответственно, необходимости в применении антикоагулянтов используют шкалу CHA2DS2-VASc (табл. 1), которая включает в себя хроническую сердечную недостаточность (ХСН), артериальную гипертонию, возраст ≥75 лет, сахарный диабет, инсульт/транзиторную ишемическую атаку (ТИА)/системную эмболию в анамнезе, сердечно-сосудистое заболевание, в том числе стенозирующий коронарный атеросклероз, подтвержденный при ангиографии, перенесенный инфаркт миокарда, атеросклероз периферических артерий или бляшку в аорте, возраст 65-74 года и женский пол [18]. Необ ходимо отметить, что женский пол скорее модифицирует общий риск развития инсульта, чем является фактором риска сам по себе [19], так как при отсутствии дополнительных факторов риска у женщин вероятность развития инсульта такая же низкая как у мужчин с индексом по шкале CHA2DS2-VASc, равным 0. В то же время при наличии по крайней мере одного дополнительного фактора риска у женщин вероятность инсульта увеличивается в большей степени, чем у мужчин [20].
Склонность к падениям сама по себе не является независимым фактором риска кровотечения на фоне антикоагулянтной терапии, однако травма при падении у пожилого пациента, принимающего пероральные антикоагулянты, может привести к более тяжелому кровотечению, например, внутричерепному. Любопытные данные были получены в одном исследовании, в котором моделировались эффекты падений у пациентов, получающих пероральные антикоагулянты. Авторы показали, что пациенты, принимающие варфарин, должны падать примерно 295 раз в год, чтобы угроза серьезного кровотечений перевесила пользу снижения риска ишемического инсульта [26]. Тем не менее, приведенные данные не отменяют необходимость профилактики падений с помощью простых мер, таких как использование вспомогательных устройств при ходьбе, ношение соответствующей обуви, устранение препятствий для пожилого человека в квартире (ковры, лишняя мебель) и т.д.
Показания к назначению пероральных антикоагулянтов в новых рекомендациях Европейского общества кардиологов не изменились. Их применение необходимо, если значение индекса по шкале CHA2DS2-VASc составляет по крайней мере 2 у мужчин и 3 у женщин. Это означает, что пероральные антикоагулянты следует назначать всем больным с ФП (независимо от пола), достигшим возраста 75 лет, и пациентам в возрасте 6574 года при наличии по крайней мере одного дополнительного фактора риска инсульта, например, артериальной гипертонии или сахарного диабета, в то время как в более молодом возрасте основанием для антикоагуляции служит наличие по крайней мере двух факторов риска как у мужчин, так и у женщин (рис. 2). Если индекс по шкале CHA2DS2-VASc составляет 1 у мужчин или 2 у женщин, то антикоагулянтную терапию считают возможной, хотя четкие показания к ее назначению в таких случаях в рекомендациях не приводятся. ФП обычно развивается у людей пожилого и старческого возраста, страдающих различными заболеваниями, поэтому индекс по шкале CHA2DS2-VASc у большинства больных с этой аритмией превышает указанные значения, обосновывая применение антикоагулянтов. Кроме того, индекс CHA2DS2-VASc имеет тенденцию к увеличению как за счет возраста, так и присоединения новых заболеваний, повышающих риск инсульта. Необходимо еще раз подчеркнуть, что тип ФП (пароксизмальная/персистирующая или постоянная) не имеет значения для решения вопроса об антикоагулянтной терапии и не учитывается при расчете индекса по шкале CHA2DS2-VASc.
Для профилактики инсульта у пациентов с неклапанной ФП применяют антагонисты витамина К, прежде всего варфарин, или прямые оральные антикоагулянты (ПОАК), в том числе ривароксабан, апиксабан, дабигатрин и эдоксабан (последний не зарегистрирован в Российской Федерации). Комбинированная терапия ацетилсалициловой кислотой и клопидогрелом у таких пациентов по эффективности уступала варфарину и сопровождалась сопоставимым риском кровотечений [27], а монотерапия ацетилсалициловой кислотой оказалась неэффективной и ассоциировалась с более высоким риском ишемического инсульта у пожилых людей с ФП [28]. Таким образом, антитромбоцитарные препараты не следует рассматривать как более безопасную альтернативу пероральным антикоагулянтам у пациентов с ФП, нуждающихся в эффективной профилактике инсульта.
В настоящее время ПОАК считают препаратами первой линии в профилактике инсульта у пациентов с неклапанной ФП [11]. В регистрационных клинических исследованиях все препараты этой группы по эффективности по крайне мере не уступали варфарину. Однако при мета-анализе клинических исследований у больных, получавших ПОАК, было выявлено снижение риска инсульта и системных эмболий на 19% по сравнению с таковым при лечении варфарином, снижение риска геморрагического инсульта на 51% и риска смерти от любых причин на 10%. Кроме того, при применении ПОАК было отмечено недостоверное снижение риска больших кровотечений на 14% и статистически значимое снижение риска внутричерепного кровотечения на 52%, в то время как частота желудочно-кишечных кровотечений увеличилась на 25% [29]. Эти данные позволяют рассматривать ПОАК в целом как более эффективную и безопасную альтернативу непрямым антикоагулянтам.
В отличие от ПОАК, варфарин может взаимодействовать с различными лекарственными препаратами, которые могут усилить или, наоборот, ослабить его антикоагулянтное действие. При лечении непрямыми антикоагулянтами необходимо регулярно контролировать международное нормализованное отношение (МНО) и при необходимости корректировать их дозы. В целом антагонисты витамина К считают эффективными и относительно безопасными препаратами, если МНО удается поддерживать в терапевтическом диапазоне более 70% времени, хотя добиться этого удается не всегда. Предложена шкала SAMe-TT2R2 (женский пол, возраст менее 60 лет, наличие по крайней мере двух сопутствующих заболеваний, таких как артериальная гипертония, сахарный диабет, ИБС, атеросклероз периферических артерий, сердечная недостаточность, инсульт в анамнезе, заболевание легких и поражение печени или почек, лечение некоторыми препаратами, курение, неевропеоидная раса), которая позволяет выделить пациентов с ФП, у которых труднее обеспечить адекватный антикоагулянтный эффект варфарина [30]. Величина индекса по этой шкале >2 служит дополнительным доводом в пользу выбора ПОАК. Если больному все же приходится назначить варфарин или другой антагонист витамина К (обычно по экономическим причинам), то необходимо принимать дополнительные меры, чтобы повысить эффективность и безопасность терапии, например, более частое мониторирование МНО, повторные консультации и т.п.
Профиль эффективности ПОАК в профилактике инсульта у пациентов с неклапанной ФП подтвержден также в пострегистрационных исследованиях, результаты которых соответствовали таковым рандомизированных контролируемых исследований 31. P. Kirchhof и соавт. обобщили результаты применения ривароксабана у 11121 пациента с неклапанной ФП (средний возраст 70,5±10,5 лет; 42,9% женщин), включенных в исследования, которые проводились в обычной клинической практике в 47 странах в рамках программы XANTUS (Xarelto for Prevention of Stroke in Patients With Atrial Fibrillation) [34]. Проспективный дизайн исследований повышает клиническую ценность полученных данных. Пациентов с ФП, начавших прием ривароксабана, наблюдали в течение 1 года. Частота больших кровотечений составила в среднем 1,7 на 100-пациентолет, смерти от любых причин – 1,9 на 100 пациентолет, инсульта и системных эмболий – 1,0 на 100 пациенто-лет. Для сравнения, частота первичной конечной точки, включавшей в себя инсульт и системные эмболии, в рандомизированном исследовании ROCKET AF, подтвердившем эффективность ривароксабана в профилактике инсульта у пациентов с неклапанной ФП, составила 1,7 на 100 пациенто-лет [35]. Частота как кровотечений, так и инсульта была низкой во всех странах, принимавших участие в программе XANTUS, а доля пациентов, продолжавших прием ривароксабана в течение года, равнялась 77,4% (от 66,4% в странах Восточной Азии до 84,4% в Западной Европе). Высокая приверженность к приему антикоагулянтной терапии отражает удобство применения ривароксабана, в том числе отсутствие необходимости в титровании дозы и регулярном мониторировании МНО, низкий риск взаимодействия с другими лекарственными средствами, стабильность антикоагулянтного эффекта и возможность назначения один раз в день [36].
Все ПОАК частично выводятся почками – в большей степени дабигатран и в меньшей степени ривароксабан и апиксабан, поэтому при выборе препарата и его дозы следует учитывать функцию почек. Например, дозу ривароксабана у пациентов с клиренсом креатинина 1549 мл/мин следует снизить с 20 до 15 мг один раз в день. Чтобы обеспечить безопасность антикоагулянтной терапии у больных с ФП, необходимо регулярно контролировать функцию почек с помощью клиренса креатитина, рассчитанного по формуле Кокрофта-Гоулта, так как именно этот показатель использовался в регистрационных клинических исследованиях. Оценивать функцию почек следует по крайней мере один раз в год или чаще у пациентов, относящихся к группе риска, например, при наличии исходного снижения функции почек. У пациентов с нарушенной и/или ухудшающейся функцией почек целесообразно рассмотреть применение ПОАК, которые в меньшей степени выводятся почками (ривароксабан или апиксабан). В практическом руководстве Европейской ассоциации аритмологов клиренс креатинина рекомендовано измерять каждые 6 мес у больных в возрасте ≥75 лет (особенно при лечении дабигатраном) и «хрупких» пациентов [37]. Чтобы оценить минимальный интервал определения клиренса креатинина у пациентов с исходно сниженной функцией почек клиренс креатинина следует разделить на 10. Например, у пациентов с его значением 40 мл/мин, клиренс креатинина следует измерять по крайней мере каждые 4 мес. Необходимо учитывать, что функция почек может быстро ухудшиться под влиянием различных интеркуррентных заболеваний, например, инфекций или острой сердечной недостаточности. Соответственно, в таких случаях необходимо также измерить клиренс креатинина.
ФП примерно в трети случаев сочетается с хронической болезнью почек (ХБП) III-V стадии, т.е. снижением расчетной скорости клубочковой фильтрации (СКФ)
Улучшение контроля симптомов
Для оценки симптомов (сердцебиение, одышка, утомляемость, дискомфорт в груди и др.) ФП используют шкалу, предложенную Европейской ассоциацией аритмологов (EHRA) и отражающую влияние проявлений аритмии на обычную повседневную активность пациентов (табл. 3) [46,47]. Необходимо учитывать, что все указанные симптомы неспецифичны и могут быть следствием сопутствующих заболеваний, а подтвердить их связь с ФП иногда удается только ретроспективно. В рекомендациях Европейского общества кардиологов предлагается также оценивать тяжесть нагрузки ФП, которая отражает ее тип, общую длительность сохранения нарушения ритма при мониторировании ЭКГ, например, в течение 24 ч, число эпизодов аритмии, их максимальную длительность и т.п. [11]. Следует отметить, что в рекомендациях отсутствуют четкие критерии интепретации полученных данных. В некоторых исследованиях была выявлена ассоциация между параметрами нагрузки ФП и неблагоприятными клиническими исходами. A. Ganesan и соавт. при мета-анализе 12 исследований примерно у 100000 больных с непароксизмальной неклапанной ФП выявили увеличение риска тромбоэмболий и смерти (относительный риск 1,384; p ТАБЛИЦА 3. Шкала оценки выраженности симптомов ФП (EHRA)
Амиодарон остается самым эффективным антиаритмическим препаратом у больных с ФП, в том числе с сердечной недостаточностью и низкой фракцией выброса левого желудочка. В рекомендациях указано, что с учетом экстракардиальной токсичности амиодарона для длительного контроля синусового ритма у пациентов с ФП желательно по возможности применять другие антиаритмические препараты [11]. Тем не менее, как и в предыдущих версиях рекомендаций, другие антиаритмические средства, такие как пропафенон и соталол, рекомендовано использовать только при отсутствии признаков значительного структурного поражения сердца. Соталол может применяться у пациентов с ишемической болезнью сердца под тщательным контролем интервала QT, сывороточных уровней калия, клиренса креатинина и других факторов риска аритмогенного действия. К последним относят пожилой возраст, женский пол, нарушение функции почек и/или печени, коронарную болезнь сердца, гипокалиемию, случаи внезапной смерти у родственников. Анти арит мическую терапию не следует назначать пациентам с постоянной формой ФП, которые получают урежающие ритм препараты, а также больным с выраженными нарушениями проводимости, если им не установлен водитель ритма.
Лечение сердечно-сосудистых и других сопутствующих заболеваний
Сердечно-сосудистые заболевания и факторы риска, с одной стороны, способствуют развитию и рецидированию ФП, а, с другой стороны, сами могут быть причиной неблагоприятных исходов, в том числе инсульта, инфаркта и смерти. A. Gómez-Outes и соавт. провели мета-анализ 4 клинических исследований, в которых ПОАК сравнивали с варфарином в целом у 71683 больных с неклапанной ФП [55]. Во время периода наблюдения умерли 9% из них, а скорректированная смертность составила 4,72% в год. Доля сердечных причин в структуре общей смертности составила 46%. Основными факторами риска смерти от любых причин были сердечная недостаточность, постоянная/персистирующая ФП, сахарный диабет, мужской пол, пожилой возраст и сниженный клиренс креатинина. Сходные данные были получены в одном из исследований, включенных в мета-анализ, – ROCKET AF, в котором изучался ривароксабан [56]. Приведенные данные указывают на важность модификации сердечнососудистых факторов риска для улучшения прогноза у больных с неклапанной ФП.
Предложены шкалы, позволяющие стратифицировать больных с неклапанной ФП по риску основных сердечно-сосудистых событий, в том числе смертель ного и несмертельного инфаркта миокарда, реваску ляризации коронарных артерий и смерти от сердечно-сосудистых причин. Например, на основании проспективного когортного исследования у 1019 пациентов с ФП разработан индекс 2MACE, который рассчитывается с учетом возраста и наличия метаболического синдрома, застойной сердечной недоста точности и инфаркта миокарда/реваскуляризации коронарных артерий и тромбоэмболий в анамнезе (табл. 4) [57]. Величина индекса 2MACE варьируется от 0 до 7, а его значение ≥3 позволяло с высокой чувствительностью и специфичностью предсказать развитие неблагоприятных исходов у пациентов с неклапанной ФП (отношение рисков 3,92, 95% ДИ 2,41-6,40, p ТАБЛИЦА 4. Шкала 2MACE, предназначенная для оценки риска сердечно-сосудистых событий у пациентов с неклапанной ФП
Заключение
Современная стратегия лечения больных с неклапанной ФП, которая подробно рассматривается в рекомендациях Европейского общества кардиологов 2020 г., предполагает антикоагуляцию с целью профилактики инсульта и системных эмболий, улучшение контроля симптомов ФП путем урежения ЧСС или восстановления и удержания синусового ритма и оптимальное лечение сердечно-сосудистых и других сопутствующих заболеваний, которые в структуре смертности паци ентов с ФП занимают даже более важное место, чем ишемический инсульт. Накапливаются данные, демонстрирующие дополнительные преимущества ПОАК перед непрямыми антикоагулянтами. Например, в мета-анализах рандомизированных клинических исследованиях показано снижение риска развития инфаркта миокарда/ОКС при лечении ривароксабаном по срав нению с контролем. В ретроспективных исследованиях лечение ривароксабаном улучшало почечные исходы у пациентов с неклапанной ФП. Пациентам с ФП следует проводить структурированное обследование, включающее в себя оценку риска инсульта, выраженности симптомов, тяжести нагрузки ФП (тип аритмии, число и длительность эпизодов и т.п.) и предрасполагающего состояния. Важное значение имеет использование различных шкал, в том числе CHA2DS2-VASc (риск инсульта), HAS-BLED (риск кровотечения), EHRA (выраженность симптомов ФП) и 2MACE (риск сердечно-сосудистых исходов), которые помогают выбрать оптимальное лечение. Для более точной оценки риска инсульта и кровотечений у пациентов с ФП предложены новые шкалы на основе не только клинических показателей, но и лабораторных маркеров, однако их потенциальные преимущества перед существующими общепринятыми индексами нуждаются в подтверждении.